Иодид алюминия
| Иодид алюминия | |
|---|---|
  | |
| Систематическое название | Иодид алюминия |
| Химическая формула | AlI3 |
| Внешний вид | кристаллическое вещество белого цвета с желтоватым оттенком |
| Свойства | |
| Молярная масса | 407,69 г/моль |
| Температура плавления | 188.3 °C (461,45 К) |
| Температура кипения | 382.5 °C (655,65 К) |
| Плотность | 3,98 г/см³ |
| Константа диссоциации pKa |
1) 5,02 2) 5,33 3) 5,87 4) 7,50 |
| Давление пара |
1 мм рт. ст. (178 °C) 10 мм рт. ст. (225 °C) 100 мм рт. ст. (296 °C) |
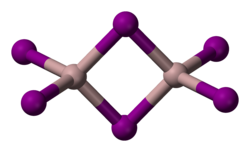
| Структура | |
| Кристаллическая решётка | гексагональная |
| Термодинамические свойства | |
| Стандартная энтальпия образования | −308 кДж/моль |
| Энтальпия плавления | +15,9 кДж/моль |
| Стандартная молярная энтропия | +190 Дж/(моль·К) |
| Стандартная энергия образования Гиббса | −304 кДж/моль |
| Классификация | |
| Регистрационный номер CAS | 7784-23-8 |
| Регистрационный номер EC | 232-054-8 |
| Безопасность | |
| R-фразы | R14; R34; R40; R42/43 |
| S-фразы | S22; S26; S36/37/39; S45 |
| H-фразы | H314; H317 |
| P-фразы | P280; P305 + P351 + P338; P310 |
| Пиктограммы опасности |
|
| Пиктограммы опасности СГС |
|
| NFPA 704 | |
| Где это не указано, данные приведены при стандартных условиях (25 °C, 100 кПа). | |
Иоди́д алюми́ния — неорганическое вещество с химической формулой . Относится к классу бинарных соединений, также может рассматриваться как соль алюминия и иодоводородной кислоты. Твердое вещество белого цвета с желтоватым оттенком.
Физические свойства[править | править код]
Безводный иодид алюминия при нормальных условиях — белое кристаллическое вещество с гексагональной сингонией кристаллической решётки. Плавится и кипит без разложения, гигроскопичен. Образует кристаллогидрат состава светло-жёлтого цвета. Кристаллогидрат хорошо растворим в воде, растворим в этаноле, эфире, сероуглероде[1][2].
Химические свойства[править | править код]
Иодид алюминия обладает следующими химическими свойствами[1].
- Реагирует с концентрированной серной кислотой:
- При поглощении влаги воздуха частично разлагается с образованием осно́вной соли, та же соль образуется при нагревании кристаллогидрата:
- При нагревании раствора иодида алюминия выпадает осадок гидроксида алюминия:
- В газовой фазе при температуре выше 250 °C происходит частичная димеризация:
- Кроме того, иодид алюминия обладает всеми свойствами, общими для растворимых солей алюминия:
- при растворении в воде происходит диссоциация, сопровождающаяся гидратацией и последующим многоступенчатым гидролизом катиона; при этом создаётся кислотная среда, в частности, для первой ступени гидролиза константа кислотности равна
- с разбавленными щелочами образует осадок гидроксида алюминия, с концентрированными разлагается с образованием тетрагидроксоалюмината
Получение[править | править код]
Иодид алюминия может быть получен непосредственно реакцией порошкообразного алюминия и иода (для реакции необходимо небольшое количество воды в качестве катализатора — образующиеся при реакции иода с водой кислоты растворяют покрывающую алюминий оксидную плёнку, ускоряя реакцию[3])[1]:
Применение[править | править код]
Иодид алюминия используется в органическом синтезе в качестве катализатора для разрыва определенных типов связей C - O и N - O. Он расщепляет ариловые эфиры и разлагает эпоксиды. Его также можно использовать для получения йодированных органических соединений.
Этот раздел не завершён. |
Токсичность[править | править код]
Иодид алюминия токсичен, способен вызывать ожоги кожи и слизистых оболочек (глаз, органов дыхания, ЖКТ). Может вызывать аллергические реакции.
Примечания[править | править код]
- ↑ 1 2 3 Лидин Р. А., Молочко В. А., Андреева Л. Л. Реакции неорганических веществ: справочник / Под ред. Р. А. Лидина. — 2-е изд., перераб. и доп. — М.: Дрофа, 2007. — С. 20. — 637 с. — ISBN 978-5-358-01303-2.
- ↑ Лидин Р.А., Андреева Л. Л., Молочко В. А. Константы неорганических веществ: справочник / Под ред. Р. А. Лидина. — 2-е изд., перераб. и доп. — М.: Дрофа, 2006. — С. 76, 442. — 685 с. — ISBN 5-7107-8085-5.
- ↑ Получение йодида алюминия Архивная копия от 29 апреля 2014 на Wayback Machine — видеоопыт в Единой коллекции цифровых образовательных ресурсов








![{\displaystyle K_{a1}={\frac {\mathsf {[Al(H_{2}O)_{5}(OH)^{2+}]\ \cdot \ [H_{3}O^{+}]}}{\mathsf {[Al(H_{2}O)_{6}^{3+}]}}}=9,55\cdot 10^{-6}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/730d5f8dea818a2043e82063227a19ca37bbc99a)

![{\displaystyle {\mathsf {AlI_{3}\ +\ 4OH^{-}\ \longrightarrow \ [Al(OH)_{4}]^{-}+\ 3I^{-}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/dd8d8202af719218632d6dbf01d6fe8037d4e666)
![{\displaystyle {\mathsf {2Al\ +\ 3I_{2}\ {\xrightarrow[{}]{H_{2}O}}2AlI_{3}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2545340fe6ffdae6857cc9a4f5d89865ca19db57)