Сульфат алюминия-натрия
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 16 января 2021 года; проверки требуют 2 правки.
| Сульфат алюминия-натрия | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
Сульфат алюминия-натрия |
| Традиционные названия | Сернокислый алюминий-натрий; алюмонатриевые квасцы; натрий-алюминиевые квасцы |
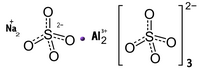
| Хим. формула | NaAl(SO4)2 |
| Физические свойства | |
| Молярная масса |
242,10; гидрат 458,28 г/моль |
| Плотность | гидрат 1,325 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | гидрат 61 °C |
| Химические свойства | |
| Растворимость | |
| • в воде | 37,440; 39,7220; 44,040 г/100 мл |
| Классификация | |
| Рег. номер CAS | 10102-71-3 |
| PubChem | 24939 |
| Рег. номер EINECS | 233-277-3 |
| SMILES | |
| InChI | |
| Кодекс Алиментариус | E521 |
| ChemSpider | 23313 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Сульфа́т алюми́ния-на́трия — неорганическое соединение, двойная соль алюминия, натрия и серной кислоты с формулой NaAl(SO4)2, белые гигроскопичные кристаллы, хорошо растворимые в воде, образует кристаллогидрат — алюмонатриевые квасцы.
Получение[править | править код]
- В природе встречается минерал сольфатерит — NaAl(SO4)2·12H2O.
- Совместная кристаллизация сульфатов натрия и алюминия:
Физические свойства[править | править код]
Сульфат алюминия-натрия — белые гигроскопичные кристаллы, хорошо растворимые в воде.
Из водных растворов выделяется в виде кристаллогидрата NaAl(SO4)2·12H2O — бесцветных кристаллов кубической сингонии, пространственная группа P a3, параметры ячейки a = 1,221 нм с температурой плавления 61 °C (в собственной кристаллизационной воде).
Химические свойства[править | править код]
- Разлагается при сильном нагревании:
- Водные растворы имеют кислую реакцию из-за гидролиза по катиону алюминия:
Применение[править | править код]
- Пищевая добавка E521.
- Применяется для осветления и обесцвечивания воды.
- Консервант для овощей, фруктов, а также мяса рыбы.
- Используется в качестве кровоостанавливающего и прижигающего средства в медицине.
- Протрава при крашении тканей, средства для проклеивания бумаги, дубления кож.
Литература[править | править код]
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1990. — Т. 2. — 671 с. — ISBN 5-82270-035-5.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 2-е изд., испр. — М.—Л.: Химия, 1966. — Т. 1. — 1072 с.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
Это заготовка статьи о неорганическом веществе. Помогите Википедии, дополнив её. |


![{\displaystyle {\mathsf {[Al(H_{2}O)_{6}]^{3+}+H_{2}O\ \rightleftarrows \ [Al(H_{2}O)_{5}(OH)]^{2+}+H_{3}O^{+}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ba16387d5a14a8416db87826e179db6f0ab8c79e)