Фотосинтез

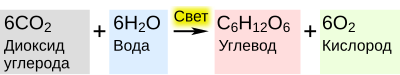
Фотоси́нтез (от др.-греч. φῶς — «свет» и σύνθεσις — «соединение», «складывание», «связывание», «синтез») — сложный химический процесс преобразования энергии видимого света (в некоторых случаях инфракрасного излучения) в энергию химических связей органических веществ при участии фотосинтетических пигментов (хлорофилл у растений, бактериохлорофилл у бактерий и бактериородопсин у архей).
В физиологии растений под фотосинтезом чаще понимается фотоавтотрофная функция — совокупность процессов поглощения, превращения и использования энергии квантов света в различных эндергонических реакциях, в том числе превращения углекислого газа в органические вещества.
Классификация[править | править код]
У живых организмов обнаружено два типа пигментов, способных выполнять функцию фотосинтетических приемников (антенн). Эти пигменты поглощают кванты видимого света и обеспечивают дальнейшее запасание энергии излучения в виде энергии электрохимического градиента ионов H+ (протонов) на биологических мембранах. У подавляющего большинства организмов роль антенн играют хлорофиллы; менее распространён случай, при котором в качестве антенны служит производное витамина А ретиналь. В соответствии с этим выделяют хлорофилльный и бесхлорофилльный фотосинтез.
Бесхлорофилльный фотосинтез[править | править код]
Система бесхлорофилльного фотосинтеза отличается значительной простотой организации, в связи с чем предполагается эволюционно первичным механизмом запасания энергии электромагнитного излучения. Эффективность бесхлорофилльного фотосинтеза как механизма преобразования энергии сравнительно низка (на один поглощённый квант переносится лишь один H+).
Открытие у галофильных архей[править | править код]
Дитер Остерхельт (Dieter Oesterhelt) и Уолтер Стокениус (Walther Stoeckenius) идентифицировали в «пурпурных мембранах» представителя галофильных архей Halobacterium salinarium (прежнее название Н. halobium) белок, который позже был назван бактериородопсином. Впоследствии были накоплены факты, указывающие на то, что бактериородопсин является светозависимым генератором протонного градиента. В частности, было продемонстрировано фотофосфорилирование на искусственных везикулах, содержащих бактериородопсин и митохондриальную АТФ-синтазу, фотофосфорилирование в интактных клетках H. salinarium, светоиндуцируемое падение pH среды и подавление дыхания, причём все эти эффекты коррелировали со спектром поглощения бактериородопсина. Таким образом, были получены неопровержимые доказательства существования бесхлорофилльного фотосинтеза.
Механизм[править | править код]

Фотосинтетический аппарат экстремальных галобактерий является наиболее примитивным из ныне известных; в нём отсутствует электронтранспортная цепь. Цитоплазматическая мембрана галобактерий является сопрягающей мембраной, содержащей два основных компонента: светозависимый протонный насос (бактериородопсин) и АТФ-синтазу. Работа такого фотосинтетического аппарата основана на следующих трансформациях энергии:
- Хромофор бактериородопсина ретиналь поглощает кванты света, что приводит к конформационным изменениям в структуре бактериородопсина и транспорту протона из цитоплазмы в периплазматическое пространство. Таким образом, в результате работы бактериородопсина энергия солнечного излучения трансформируется в энергию электрохимического градиента протонов на мембране.
- При работе АТФ-синтазы энергия трансмембранного градиента трансформируется в энергию химических связей АТФ. Таким образом осуществляется хемиосмотическое сопряжение.
При бесхлорофилльном типе фотосинтеза (как и при реализации циклических потоков в электрон-транспортных цепях) не происходит образования восстановительных эквивалентов (восстановленного ферредоксина или НАД(Ф)Н), необходимых для ассимиляции углекислого газа. Поэтому при бесхлорофилльном фотосинтезе не происходит ассимиляции углекислого газа, а осуществляется исключительно запасание солнечной энергии в форме АТФ (фотофосфорилирование).
Значение[править | править код]
Основной путь получения энергии для галобактерий — аэробное окисление органических соединений (при культивировании штаммов используют углеводы и аминокислоты). При дефиците кислорода помимо бесхлорофильного фотосинтеза источниками энергии для галобактерий может служить анаэробное нитратное дыхание или сбраживание аргинина и цитруллина. Однако в эксперименте было показано, что бесхлорофильный фотосинтез может служить и единственным источником энергии в анаэробных условиях при подавлении анаэробного дыхания и брожения при обязательном условии, что в среду вносят ретиналь, для синтеза которого необходим кислород.
Хлорофилльный фотосинтез[править | править код]
Хлорофилльный фотосинтез отличается от бактериородопсинового значительно большей эффективностью запасания энергии. На каждый эффективно поглощённый квант излучения против градиента переносится не менее одного H+, и в некоторых случаях энергия запасается в форме восстановленных соединений (ферредоксин, НАДФ).
Аноксигенный[править | править код]
Аноксигенный (или бескислородный) фотосинтез протекает без выделения кислорода. К аноксигенному фотосинтезу способны пурпурные и зелёные бактерии, а также гелиобактерии.
При аноксигенном фотосинтезе возможно осуществление:
- Светозависимого циклического транспорта электронов, не сопровождающегося образованием восстановительных эквивалентов и приводящего исключительно к запасанию энергии света в форме АТФ. При циклическом светозависимом электронном транспорте необходимости в экзогенных донорах электронов не возникает. Потребность в восстановительных эквивалентах обеспечивается нефотохимическим путём, как правило, за счёт экзогенных органических соединений.
- Светозависимого нециклического транспорта электронов, сопровождающегося и образованием восстановительных эквивалентов, и синтезом АДФ. При этом возникает потребность в экзогенных донорах электронов, которые необходимы для заполнения электронной вакансии в реакционном центре. В качестве экзогенных доноров электронов могут использоваться как органические, так и неорганические восстановители. Среди неорганических соединений наиболее часто используются различные восстановленные формы серы (сероводород, молекулярная сера, сульфиты, тиосульфаты, тетратионаты, тиогликоляты), также возможно использование молекулярного водорода.
Оксигенный[править | править код]
Оксигенный (или кислородный) фотосинтез сопровождается выделением кислорода в качестве побочного продукта. При оксигенном фотосинтезе осуществляется нециклический электронный транспорт, хотя при определённых физиологических условиях осуществляется исключительно циклический электронный транспорт. В качестве донора электронов при нециклическом потоке используется крайне слабый донор электронов — вода.
Оксигенный фотосинтез распространён гораздо шире. Характерен для высших растений, водорослей, многих протистов и цианобактерий.
Этапы[править | править код]
Фотосинтез — процесс с крайне сложной пространственно-временной организацией.
Разброс характерных времен различных этапов фотосинтеза составляет 19 порядков: скорость процессов поглощения квантов света и миграции энергии измеряется в фемтосекундном интервале (10−15 с), скорость электронного транспорта имеет характерные времена 10−10—10−2 с, а процессы, связанные с ростом растений, измеряются днями (105—107 с).
Также большой разброс размеров характерен для структур, обеспечивающих протекание фотосинтеза: от молекулярного уровня (10−27 м3) до уровня фитоценозов (105 м3).
В фотосинтезе можно выделить отдельные этапы, различающиеся по природе и характерным скоростям процессов:
- фотофизический;
- фотохимический;
- химический:
- реакции транспорта электронов;
- «темновые» реакции или циклы углерода при фотосинтезе.
На первом этапе происходит поглощение квантов света пигментами, их переход в возбуждённое состояние и передача энергии к другим молекулам фотосистемы (пластохинон)[1].
На втором этапе происходит разделение зарядов в реакционном центре. Молекула воды теряет электрон под воздействием катиона-радикала, образовавшегося из молекулы хлорофилла после потери ей своего электрона и передачи его пластохинону на первом этапе: . Затем образовавшиеся гидроксильные радикалы под воздействием положительно заряженных ионов марганца преобразуются в кислород и воду: [1]. Одновременно с этим процессом происходит перенос электронов по фотосинтетической электронотранспортной цепи, что заканчивается синтезом АТФ и НАДФН[1]. Первые два этапа вместе называют светозависимой стадией фотосинтеза.
Третий этап заключается в поглощении второй молекулой хлорофилла кванта света и передаче ею электрона ферредоксину. Затем хлорофилл получает электрон после цепи его перемещений на первом и втором этапах. Ферредоксин восстанавливает универсальный восстановитель НАДФ[1].
Четвёртый этап происходит уже без обязательного участия света и включает в себя биохимические реакции синтеза органических веществ с использованием энергии, накопленной на светозависимой стадии. Чаще всего в качестве таких реакций рассматривается цикл Кальвина и глюконеогенез, образование сахаров и крахмала из углекислого газа воздуха[1].
Пространственная локализация[править | править код]
Лист[править | править код]
Фотосинтез растений осуществляется в хлоропластах — полуавтономных двухмембранных органеллах, относящихся к классу пластид. Хлоропласты могут содержаться в клетках стеблей, плодов, чашелистиков, однако основным органом фотосинтеза является лист. Он анатомически приспособлен к поглощению энергии света и ассимиляции углекислоты. Плоская форма листа, обеспечивающая большое отношение поверхности к объёму, позволяет более полно использовать энергию солнечного света. Вода, необходимая для поддержания тургора и протекания фотосинтеза, доставляется к листьям из корневой системы по ксилеме — одной из проводящих тканей растения. Потеря воды в результате испарения через устьица и в меньшей степени через кутикулу (транспирация) служит движущей силой транспорта по сосудам. Однако избыточная транспирация является нежелательной, и у растений в ходе эволюции сформировались различные приспособления, направленные на снижение потерь воды. Отток ассимилятов, необходимый для функционирования цикла Кальвина, осуществляется по флоэме. При интенсивном фотосинтезе углеводы могут полимеризоваться, и при этом в хлоропластах формируются крахмальные зёрна. Газообмен (поступление углекислого газа и выделение кислорода) осуществляется путём диффузии через устьица (некоторая часть газов движется через кутикулу).
Поскольку дефицит углекислого газа значительно увеличивает потери ассимилятов при фотодыхании, необходимо поддерживать высокую концентрацию углекислоты в межклеточном пространстве, что возможно при открытых устьицах. Однако поддержание устьиц в открытом состоянии при высокой температуре приводит к усилению испарения воды, что приводит к водному дефициту и также снижает продуктивность фотосинтеза. Этот конфликт решается в соответствии с принципом адаптивного компромисса. Кроме того, первичное поглощение углекислого газа ночью, при низкой температуре, у растений с CAM-фотосинтезом позволяет избежать высоких транспирационных потерь воды.
У некоторых суккулентов с вырожденными листьями (например, у большинства видов кактусов) основная фотосинтетическая активность связана со стеблем.
Фотосинтез на тканевом уровне[править | править код]
На тканевом уровне фотосинтез у высших растений обеспечивается специализированной тканью — хлоренхимой. Она располагается близ поверхности тела растения, где получает достаточно световой энергии. Обычно хлоренхима находится непосредственно под эпидермой. У растений, растущих в условиях повышенной инсоляции, между эпидермой и хлоренхимой может располагаться один или два слоя прозрачных клеток (гиподерма), обеспечивающих рассеивание света. У некоторых тенелюбивых растений хлоропластами богата и эпидерма (например, кислица). Часто хлоренхима мезофилла листа дифференцирована на палисадную (столбчатую) и губчатую, но может состоять и из однородных клеток. В случае дифференцировки наиболее богата хлоропластами палисадная хлоренхима.

Хлоропласты[править | править код]
Хлоропласты отделены от цитоплазмы двойной мембраной, обладающей избирательной проницаемостью. Внутреннее пространство хлоропласта заполнено бесцветным содержимым (стромой) и пронизано мембранами (ламеллами), которые, соединяясь друг с другом, образуют тилакоиды, которые, в свою очередь, группируются в стопки, называемые гранами. На мембранах тилакоидов располагаются молекулы хлорофилла и других вспомогательных пигментов (каротиноиды). Поэтому их называют фотосинтезирующими мембранами. Внутритилакоидное пространство отделено и не сообщается с остальной стромой; предполагается также, что внутреннее пространство всех тилакоидов сообщается между собой. Световые стадии фотосинтеза приурочены к мембранам, автотрофная фиксация CO2 происходит в строме.
В хлоропластах имеются свои ДНК, РНК, рибосомы (с седиментацией типа 70 S), идёт синтез белка (хотя этот процесс и контролируется из ядра). Они не синтезируются вновь, а образуются путём деления предшествующих. Всё это позволило считать их потомками свободных цианобактерий, вошедших в состав эукариотической клетки в процессе симбиогенеза.
Фотосинтетические мембраны прокариот[править | править код]
Цианобактерии, таким образом, как бы сами являются хлоропластом, и в их клетке фотосинтетический аппарат не вынесен в особую органеллу. Их тилакоиды не образуют стопок, а формируют различные складчатые структуры (у единственной цианобактерии Gloeobacter violaceus тилакоиды отсутствуют вовсе, а весь фотосинтетический аппарат находится в цитоплазматической мембране, не образующей впячиваний). У них и растений также есть различия в светособирающем комплексе (см. ниже) и пигментном составе.
Световая (светозависимая) стадия[править | править код]
В ходе световой стадии фотосинтеза образуются высокоэнергетические продукты: АТФ, служащий в клетке источником энергии, и НАДФ, использующийся как восстановитель. В качестве побочного продукта выделяется кислород.
Фотохимическая суть процесса[править | править код]
Хлорофилл имеет два уровня возбуждения (с этим связано наличие двух максимумов на спектре его поглощения): первый связан с переходом на более высокий энергетический уровень электрона системы сопряжённых двойных связей, второй — с возбуждением неспаренных электронов азота и магния порфиринового ядра. При неизменном спине электрона формируются синглетные первое и второе возбуждённые состояния, при изменённом — триплетное первое и второе.
Второе возбуждённое состояние наиболее высокоэнергетично, нестабильно, и хлорофилл за 10−12 с переходит с него на первое с потерей 100 кДж/моль энергии только в виде теплоты. Из первого синглетного и триплетного состояний молекула может переходить в основное с выделением энергии в виде света (флуоресценция и фосфоресценция соответственно) или тепла с переносом энергии на другую молекулу, либо, поскольку электрон на высоком энергетическом уровне слабо связан с ядром, с переносом электрона на другое соединение.
Первая возможность реализуется в светособирающих комплексах, вторая — в реакционных центрах, где под воздействием кванта света переходящий в возбуждённое состояние хлорофилл становится донором электрона (восстановителем) и передаёт его первичным акцепторам. Чтобы предотвратить возвращение электрона на положительно заряженный хлорофилл, первичный акцептор передаёт его вторичному. Кроме того, время жизни полученных соединений выше, чем у возбуждённой молекулы хлорофилла. Происходит стабилизация энергии и разделение зарядов. Для дальнейшей стабилизации вторичный донор электронов восстанавливает положительно заряженный хлорофилл, первичным же донором в случае оксигенного фотосинтеза является вода.
Проблемой, с которой сталкиваются при этом проводящие оксигенный фотосинтез организмы, является различие окислительно-восстановительных потенциалов воды (для полуреакции H2O → O2 (E0 = +0,82 В) и НАДФ+ (E0 = −0,32 В). Хлорофилл при этом должен иметь в основном состоянии потенциал больше +0,82 В, чтобы окислять воду, но при этом иметь в возбуждённом состоянии потенциал меньше −0,32 В, чтобы восстанавливать НАДФ+. Одна молекула хлорофилла не может отвечать обоим требованиям. Поэтому сформировались две фотосистемы, и для полного проведения процесса необходимы два кванта света и два хлорофилла разных типов.
Светособирающие комплексы[править | править код]
Хлорофилл выполняет две функции: поглощения и передачи энергии. Более 90 % всего хлорофилла хлоропластов входит в состав светособирающих комплексов (ССК), выполняющих роль антенны, передающей энергию к реакционному центру фотосистем I или II. Помимо хлорофилла, в ССК имеются каротиноиды, а у некоторых водорослей и цианобактерий — фикобилины, роль которых заключается в поглощении света тех длин волн, которые хлорофилл поглощает сравнительно слабо.
Передача энергии идёт резонансным путём (механизм Фёрстера) и занимает для одной пары молекул 10−10—10−12 с, расстояние, на которое осуществляется перенос, составляет около 1 нм. Передача сопровождается некоторыми потерями энергии (10 % от хлорофилла a к хлорофиллу b, 60 % от каротиноидов к хлорофиллу), из-за чего возможна только от пигмента с максимумом поглощения при меньшей длине волны к пигменту с большей. Именно в таком порядке взаимно локализуются пигменты ССК, причём наиболее длинноволновые хлорофиллы находятся в реакционных центрах. Обратный переход энергии невозможен.
ССК растений расположен в мембранах тилакоидов, у цианобактерий основная его часть вынесена за пределы мембран в прикреплённые к ним фикобилисомы — палочковидные полипептидно-пигментные комплексы, в которых находятся различные фикобилины: на периферии фикоэритрины (с максимумом поглощения при 495—565 нм), за ними фикоцианины (550—615 нм) и аллофикоцианины (610—670 нм), последовательно передающие энергию на хлорофилл a (680—700 нм) реакционного центра.
Основные компоненты цепи переноса электронов[править | править код]
Фотосистема II[править | править код]
Фотосистема — совокупность ССК, фотохимического реакционного центра и переносчиков электрона. Светособирающий комплекс II содержит 200 молекул хлорофилла a, 100 молекул хлорофилла b, 50 молекул каротиноидов и 2 молекулы феофитина. Реакционный центр фотосистемы II представляет собой пигмент-белковый комплекс, расположенный в тилакоидных мембранах и окружённый ССК. В нём находится димер хлорофилла-a с максимумом поглощения при 680 нм (П680). На него в конечном счёте передаётся энергия кванта света из ССК, в результате чего один из электронов переходит на более высокое энергетическое состояние, связь его с ядром ослабляется, и возбуждённая молекула П680 становится сильным восстановителем (химический потенциал E0 = −0,7 В).
П680 восстанавливает феофитин, в дальнейшем электрон переносится на хиноны, входящие в состав ФС II и далее на пластохиноны, транспортируемые в восстановленной форме к комплексу b6f. Одна молекула пластохинона переносит 2 электрона и 2 протона, которые берутся из стромы.
Заполнение электронной вакансии в молекуле П680 происходит за счёт воды. В состав ФС II входит водоокисляющий комплекс, содержащий в активном центре 4 иона марганца. Для образования одной молекулы кислорода требуется две молекулы воды, дающие 4 электрона. Поэтому процесс проводится в 4 такта и для его полного осуществления требуется 4 кванта света. Комплекс находится со стороны внутритилакоидного пространства, и полученные 4 протона выбрасываются в него.
Таким образом, суммарный результат работы ФС II — это окисление 2 молекул воды с помощью 4 квантов света с образованием 4 протонов во внутритилакоидном пространстве и 2 восстановленных пластохинонов в мембране.
Цитохром-b6/f-комплекс[править | править код]
b6f-комплекс — это насос, перекачивающий протоны из стромы во внутритилакоидное пространство и создающий градиент их концентрации за счёт выделяющейся в окислительно-восстановительных реакциях электронтранспортной цепи энергии. 2 пластохинона дают перекачку 4 протонов. В дальнейшем трансмембранный протонный градиент (pH стромы около 8, внутритилакоидного пространства — 5) используется для синтеза АТФ трансмембранным ферментом АТФ-синтазой.
Фотосистема I[править | править код]
Светособирающий комплекс I содержит примерно 200 молекул хлорофилла.
В реакционном центре первой фотосистемы находится димер хлорофилла a с максимумом поглощения при 700 нм (П700). После возбуждения квантом света он восстанавливает первичный акцептор — хлорофилл a, тот — вторичный (витамин K1 или филлохинон), после чего электрон передаётся на ферредоксин, который и восстанавливает НАДФ с помощью фермента ферредоксин-НАДФ-редуктазы.
Белок пластоцианин, восстановленный в b6f-комплексе, транспортируется к реакционному центру первой фотосистемы со стороны внутритилакоидного пространства и передаёт электрон на окисленный П700.
Циклический и псевдоциклический транспорт электрона[править | править код]
Помимо полного нециклического пути электрона, описанного выше, обнаружены циклический и псевдоциклический.
Суть циклического пути заключается в том, что ферредоксин вместо НАДФ восстанавливает пластохинон, который переносит его назад на b6f-комплекс. В результате образуется больший протонный градиент и больше АТФ, но не возникает НАДФН.
При псевдоциклическом пути ферредоксин восстанавливает кислород, который в дальнейшем превращается в воду и может быть использован в фотосистеме II. При этом также не образуется НАДФН.
Темновая фаза[править | править код]
В темновой стадии с участием АТФ и НАДФ происходит восстановление CO2 до глюкозы (C6H12O6). Хотя свет не требуется для осуществления данного процесса, он участвует в его регуляции.
С3-фотосинтез, цикл Кальвина[править | править код]
Цикл Кальвина или восстановительный пентозофосфатный цикл состоит из трёх стадий:
- карбоксилирования;
- восстановления;
- регенерация акцептора CO2.
На первой стадии к рибулозо-1,5-бисфосфату присоединяется CO2 под действием фермента рибулозобисфосфат-карбоксилаза/оксигеназа. Этот белок составляет основную фракцию белков хлоропласта и предположительно наиболее распространённый фермент в природе. В результате образуется промежуточное неустойчивое соединение, распадающееся на две молекулы 3-фосфоглицериновой кислоты (ФГК).
Во второй стадии ФГК в два этапа восстанавливается. Сначала она фосфорилируется АТФ под действием фосфороглицерокиназы с образованием 1,3-бисфосфоглицериновой кислоты (ДФГК), затем при воздействии триозофосфатдегидрогеназы и НАДФН ацил-фосфатная группа ДФГК дефосфорилируется и восстанавливается до альдегидной и образуется глицеральдегид-3-фосфат — фосфорилированный углевод (ФГА).
В третьей стадии участвуют 5 молекул ФГА, которые через образование 4-, 5-, 6- и 7-углеродных соединений объединяются в 3 5-углеродных рибулозо-1,5-бифосфата, для чего необходимы 3 АТФ.
Наконец, две ФГА необходимы для синтеза глюкозы. Для образования одной её молекулы требуется 6 оборотов цикла, 6 CO2, 12 НАДФН и 18 АТФ.
С4-фотосинтез[править | править код]
Отличие этого механизма фотосинтеза от обычного заключается в том, что фиксация углекислого газа и его использование разделены в пространстве между различными клетками растения[2].
При низкой концентрации растворённого в строме CO2 рибулозобифосфаткарбоксилаза катализирует реакцию окисления рибулозо-1,5-бифосфата и его распад на 3-фосфоглицериновую кислоту и фосфогликолевую кислоту, которая вынужденно используется в процессе фотодыхания.
Для увеличения концентрации CO2 растения типа С4 изменили анатомию листа. Цикл Кальвина у них локализуется в клетках обкладки проводящего пучка, в клетках мезофилла же под действием ФЕП-карбоксилазы фосфоенолпируват карбоксилируется с образованием щавелеуксусной кислоты, которая превращается в малат или аспартат и транспортируется в клетки обкладки, где декарбоксилируется с образованием пирувата, возвращаемого в клетки мезофилла.
С4-фотосинтез практически не сопровождается потерями рибулозо-1,5-бифосфата из цикла Кальвина, поэтому более эффективен. Однако он требует не 18, а 30 АТФ на синтез 1 молекулы глюкозы. Это оправдывает себя в тропиках, где жаркий климат требует держать устьица закрытыми, что препятствует поступлению CO2 в лист, а также при рудеральной жизненной стратегии.
Фотосинтез по пути С4 проводят около 7600 видов растений. Все они относятся к цветковым: многие Злаковые (61 % видов, в том числе культурные — кукуруза, сахарный тростник, сорго и др.[3][4]), Гвоздичноцветные (наибольшая доля в семействах Маревые — 40 % видов, Амарантовые — 25 %), некоторые Осоковые, Астровые, Капустные, Молочайные[5][6].
CAM-фотосинтез[править | править код]
При фотосинтезе типа CAM (англ. Crassulaceae acid metabolism — кислотный метаболизм толстянковых) происходит разделение ассимиляции CO2 и цикла Кальвина не в пространстве, как у С4, а во времени[2]. Ночью в вакуолях клеток по аналогичному вышеописанному механизму при открытых устьицах накапливается малат, днём при закрытых устьицах идёт цикл Кальвина. Этот механизм позволяет максимально экономить воду, однако уступает в эффективности и С4, и С3. Он оправдан при стресстолерантной жизненной стратегии.
Значение[править | править код]
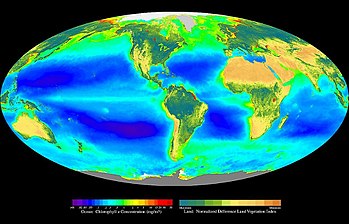
Фотосинтез составляет энергетическую основу всего живого на планете, кроме хемосинтезирующих бактерий.
Фотосинтез совершается в зеленых частях наземных растений и в водорослях. За один год зеленые водоросли выделяют в атмосферу Земли тонн кислорода, что составляет всего кислорода, вырабатываемого в процессе фотосинтеза на Земле. Фотосинтез — самый массовый биохимический процесс на Земле[7].
Возникновение на Земле более 3 млрд лет назад механизма расщепления молекулы воды квантами солнечного света с образованием O2 представляет собой важнейшее событие в биологической эволюции, сделавшее свет Солнца главным источником энергии биосферы.
Фототрофы обеспечивают конверсию и запасание энергии термоядерных реакций, протекающих на Солнце, в энергию органических молекул. Солнечная энергия при участии фототрофов конвертируется в энергию химических связей органических веществ. Существование гетеротрофных организмов возможно исключительно за счёт энергии, запасённой фототрофами в органических соединениях. При использовании энергии химических связей органических веществ гетеротрофы высвобождают её в процессах дыхания и брожения.
Фотосинтез является основой продуктивности как сельскохозяйственных растений, так и животной пищи.
Энергия, получаемая человечеством при сжигании биотоплива (дрова, пеллеты, биогаз, биодизель, этанол, метанол) и ископаемого топлива (уголь, нефть, природный газ, торф), также является запасённой в процессе фотосинтеза.
Фотосинтез служит главным входом неорганического углерода в биогеохимический цикл.
Большая часть свободного кислорода атмосферы — биогенного происхождения и является побочным продуктом фотосинтеза. Формирование окислительной атмосферы (кислородная катастрофа) полностью изменило состояние земной поверхности, сделало возможным появление дыхания, а в дальнейшем, после образования озонового слоя, позволило жизни существовать на суше.
История изучения[править | править код]
Первые опыты по изучению фотосинтеза были проведены Джозефом Пристли в 1770—1780-х годах, когда он обратил внимание на «порчу» воздуха в герметичном сосуде горящей свечой (воздух переставал поддерживать горение, а помещённые в него животные задыхались) и «исправление» его растениями. Пристли сделал вывод, что растения выделяют кислород, который необходим для дыхания и горения, однако не заметил, что для этого растениям нужен свет. Это показал вскоре Ян Ингенхауз.
Позже было установлено, что помимо выделения кислорода растения поглощают углекислый газ и при участии воды синтезируют на свету органическое вещество. В 1842 году Роберт Майер на основании закона сохранения энергии постулировал, что растения преобразуют энергию солнечного света в энергию химических связей. В 1877 году В. Пфеффер назвал этот процесс фотосинтезом.
Хлорофиллы были впервые выделены в 1818 году П. Ж. Пеллетье и Ж. Каванту. Разделить пигменты и изучить их по отдельности удалось М. С. Цвету с помощью созданного им метода хроматографии. Спектры поглощения хлорофилла были изучены К. А. Тимирязевым, он же, развивая положения Майера, показал, что именно поглощённые лучи позволяют повысить энергию системы, создав вместо слабых связей С−О и О−Н высокоэнергетические С−С (до этого считалось, что в фотосинтезе используются жёлтые лучи, не поглощаемые пигментами листа). Сделано это было благодаря созданному им методу учёта фотосинтеза по поглощённому CO2: в ходе экспериментов по освещению растения светом разных длин волн (разного цвета) оказалось, что интенсивность фотосинтеза совпадает со спектром поглощения хлорофилла.
Большой вклад в изучение фотосинтеза внёс А. С. Фаминцын.[8]. В 1868 году он впервые экспериментально доказал и научно обосновал применение искусственного освещения для выращивания растений, использовав керосиновые лампы вместо солнечного света[9]. Фамицын первым системно изучил процессы образования крахмала в тканях растений под воздействием света, а также влияния света на образование хлорофилла, его расположение в листьях растений различных таксонов[10][11].
Окислительно-восстановительную сущность фотосинтеза (как оксигенного, так и аноксигенного) постулировал Корнелис ван Ниль, он же в 1931 году доказал, что пурпурные бактерии и зелёные серобактерии осуществляют аноксигенный фотосинтез[12][13]. Окислительно-восстановительный характер фотосинтеза означал, что кислород в оксигенном фотосинтезе образуется полностью из воды, что экспериментально подтвердил в 1941 году А. П. Виноградов в опытах с изотопной меткой. В 1937 году Роберт Хилл установил, что процесс окисления воды (и выделения кислорода), а также ассимиляции CO2 можно разобщить. В 1954—1958 годах Д. Арнон установил механизм световых стадий фотосинтеза, а сущность процесса ассимиляции CO2 была раскрыта Мелвином Кальвином с использованием изотопов углерода в конце 1940-х годов, за эту работу в 1961 году ему была присуждена Нобелевская премия.
В 1955 году был выделен и очищен фермент рибулозобисфосфат-карбоксилаза/оксигеназа. С4-фотосинтез был описан Ю. С. Карпиловым в 1960 году и М. Д. Хэтчем и Ч. Р. Слэком в 1966 году.
Эволюция[править | править код]
Существующие данные указывают на то, что наиболее древними организмами, запасающими энергию света в форме химической энергии, были археи, осуществляющие бесхлорофилльный фотосинтез, при котором не происходит образования восстановителя (НАДФН) и фиксации углекислого газа, а энергия запасается лишь в форме АТФ.
Несколько позже (3,7—3,8 миллиарда лет назад) независимо от архей и многократно в ходе эволюции возникали организмы (зелёные, пурпурные бактерии и другие группы эубактерий) с одной из фотосистем, позволяющей осуществлять аноксигенный фотосинтез, при котором в качестве доноров электронов используются соединения с низким редокс-потенциалом (водород, сульфиды и сероводород, сера, соединения железа (II), нитриты) или осуществляется циклический поток электронов вокруг фотосистемы.
Система оксигенного фотосинтеза, при которой в электрон-транспортной цепи совместно функционируют две фотосистемы, характерная для цианобактерий и происшедших от них в ходе эндосимбиоза хлоропластов водорослей и высших растений, возникла в эволюции однократно, по разным оценкам, от 3,5 до 2,4 миллиардов лет назад. Появление фотосистемы II позволило использовать в качестве неограниченного донора электронов воду — соединение с высоким редокс-потенциалом, то есть не склонное выступать в окислительно-восстановительных процессах в роли восстановителя, однако крайне распространённое на Земле.
С момента появления оксигенных фотосинтезирующих организмов начинается увеличение содержания молекулярного кислорода (сильный окислитель) на Земле, что приводит к накоплению кислорода в водах мирового океана, к окислению горных пород, к формированию озонового экрана и в конечном счёте к накоплению кислорода в атмосфере планеты. Таким образом возникновение системы оксигенного фотосинтеза рассматривается как причина кислородной катастрофы и в частности перестройки древней восстановительной атмосферы Земли и формированию современной атмосферы окислительного типа. Формирование озонового слоя, защищающего поверхность Земли от опасного для живых организмов высокоэнергетического ультрафиолетового излучения, сделало возможным выход жизни на сушу. Одновременно с описанными перестройками гидро-, лито- и атмосферы происходили значительные изменения в биосфере: накопление кислорода привело к смене доминирующих анаэробных сообществ аэробными.
Прочие факты[править | править код]
- Некоторые брюхоногие моллюски ассимилируют хлоропласты съеденных водорослей в клетки пищеварительного тракта. Так, в организме морского слизня Elysia chlorotica хлоропласты водоросли Vaucheria litorea способны фотосинтезировать несколько месяцев, что позволяет ему жить за счёт глюкозы, полученной в результате фотосинтеза[14].
- Предполагается, что в естественной среде фотосинтезирующие бактерии могут использовать не только свет Солнца, но и другие источники света, а потому могут находиться в местах, не подвергающихся солнечному облучению[15]. В 2005 году Томас Битти из университета Британской Колумбии и Роберт Блейкеншип из университета Аризоны в глубоководных пробах, взятых в окрестностях глубоководного термального источника у побережья Коста Рики, обнаружили серобактерию GSB1, сходную с серобактериями родов Chlorobium и Prosthecochloris, содержащую бактериохлорофилл. Они предположили, что вероятность контаминации образца невелика и, следовательно, GSB1 использует для фотосинтеза не солнечный свет (который не проникает сквозь 2,4-километровую толщу моря), а тусклый длинноволновый (~750 нм) свет, испускаемый гидротермальными источниками[15].
- По состоянию на конец 1970-х годов мощность солнечной энергии, перерабатываемой земной растительностью при фотосинтезе, всего лишь на порядок превосходила мощность всех электростанций в мире[16]. По другим данным, первичная мощность фотосинтеза составляет 1014 Вт[17]. В 2015 году в мире произведено 24 × 1012 кВт·ч электроэнергии. Получаем среднюю мощность всех электростанций в мире в 2015 году: Вт. Это составляет около 3 % от первичной мощности фотосинтеза.
- Для оценки эффективности трансформации энергии излучения в энергию химических связей органических соединений используются различные расчётные коэффициенты эффективности фотосинтеза.
См. также[править | править код]
Примечания[править | править код]
- ↑ 1 2 3 4 5 Полищук В. Р. Как разглядеть молекулу. — М., Химия, 1979. — Тираж 70000 экз. — С. 301—305.
- ↑ 1 2 Стасевич К. Почему кактусы не высыхают. Архивировано 8 января 2017 года. // Наука и жизнь. — 2016. — № 12. — С. 70—73. — ISSN 0028-1263.
- ↑ Sage, Rowan; Russell Monson. 16 // C4 Plant Biology (англ.). — 1999. — P. 551—580. — ISBN 0-12-614440-0.
- ↑ Ботаники объяснили появление энергоэффективных растений. Архивировано 28 декабря 2012 года..
- ↑ Sage, Rowan; Russell Monson. 7 // C4 Plant Biology (англ.). — 1999. — P. 228—229. — ISBN 0-12-614440-0.
- ↑ Kadereit, G.; Borsch, T.; Weising, K.; Freitag, H. Phylogeny of Amaranthaceae and Chenopodiaceae and the Evolution of C4 Photosynthesis (англ.) // International Journal of Plant Sciences : journal. — 2003. — Vol. 164, no. 6. — P. 959—986. — doi:10.1086/378649.
- ↑ Николаев Л. А. Химия жизни. — М., Просвещение, 1977. — С. 214
- ↑ ФАМИ́НЦЫН : [арх. 16 февраля 2019] // Уланд — Хватцев. — М. : Большая российская энциклопедия, 2017. — С. 191. — (Большая российская энциклопедия : [в 35 т.] / гл. ред. Ю. С. Осипов ; 2004—2017, т. 33). — ISBN 978-5-85270-370-5.
- ↑ Кошель П. Фотосинтез. Газета «Биология» № 43/2004. bio.1september.ru. Дата обращения: 16 февраля 2019. Архивировано 17 февраля 2019 года.
- ↑ Сельскохозяйственная биология: 1-2010 Манойленко. www.agrobiology.ru. Дата обращения: 16 февраля 2019. Архивировано 8 августа 2018 года.
- ↑ Фаминцын. Справочник химика 21. chem21.info. Дата обращения: 16 февраля 2019. Архивировано 24 июня 2018 года.
- ↑ Кондратьева Е. Н. Фототрофные бактерии // Жизнь растений : в 6 т. / гл. ред. Ал. А. Фёдоров. — М. : Просвещение, 1974. — Т. 1 : Введение. Бактерии и актиномицеты / под ред. Н. А. Красильникова, А. А. Уранова. — С. 323. — 487 с. — 300 000 экз.
- ↑ van Niel C. B. On the morphology and physiology of the purple and green sulphur bacteria (англ.) // Archiv für Mikrobiologie[англ.] : journal. — 1932. — Vol. 3, no. 1. — P. 1—112. — doi:10.1007/BF00454965.
- ↑ Rumpho M. E., Worful J. M., Lee J., et al. Horizontal gene transfer of the algal nuclear gene psbO to the photosynthetic sea slug Elysia chlorotica (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 2008. — November (vol. 105, no. 46). — P. 17867—17871. — doi:10.1073/pnas.0804968105. — PMID 19004808. — PMC 2584685. Архивировано 24 сентября 2015 года.
- ↑ 1 2 Beatty, J. Thomas; Jörg Overmann, Michael T. Lince, Ann K. Manske, Andrew S. Lang, Robert E. Blankenship, Cindy L. Van Dover, Tracey A. Martinson, F. Gerald Plumley. An obligately photosynthetic bacterial anaerobe from a deep-sea hydrothermal vent (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 2005. — Vol. 102, no. 26. — P. 9306—9310. — doi:10.1073/pnas.0503674102. Архивировано 25 марта 2012 года.
- ↑ Б. М. Смирнов Углекислый газ в атмосфере земли. Архивировано 22 октября 2012 года. // Объединённый институт высоких температур РАН, 126 (11) (1978), Москва.
- ↑ Пономарёв Л. И. Под знаком кванта. — М., Наука, 1989. — Тираж 75 000 экз. — ISBN 5-02-014049-X. — С. 331—339.
Литература[править | править код]
- Холл Д., Рао К. Фотосинтез: Пер. с англ. — М.: Мир, 1983.
- Физиология растений / под ред. проф. Ермакова И. П. — М.: Академия, 2007.
- Молекулярная биология клетки / Альбертис Б., Брей Д. и др. В 3 т. — М.: Мир, 1994
- Рубин А. Б. Биофизика. В 2 т. — М.: Изд. Московского университета и Наука, 2004.
- Чернавская Н. М., Чернавский Д. С. Туннельный транспорт электронов в фотосинтезе. М., 1977.
- В. Любименко. Влияние света на усвоение органических веществ зелёными растениями // Известия Императорской Академии наук. VI серия. — 1907. — № 12. — С. 395—426, с 6 табл.
- Медведев С. С. Физиология растений — СПб.: СПбГУ, 2006.
- Gaffron H. «Research in photosynthesis». New York, Interscience Publ., 1957. OCLC 252395040
Ссылки[править | править код]
- Molecular Cell Biology (англ.) на сайте Google Книги
- Учебное пособие по фотосинтезу (начальный уровень) (англ.). Maricopa Community Colleges. Архивировано из оригинала 28 ноября 2009 года.
- Статья «Фотосинтез» в Физической энциклопедии
- Механизм фотосинтеза использует вибронную квантовую когерентность // Научно-популярная статья на Elementy.ru




