Сигнальные молекулы газообразных веществ
Сигнальные молекулы газообразных веществ — малые молекулы таких химических соединений, которые при температуре тела и нормальном атмосферном давлении находились бы в газообразном агрегатном состоянии, будучи выделены в свободном виде. Сигнальные молекулы газообразных веществ выполняют в организме, ткани или клетке сигнальные функции, вызывая своим воздействием физиологические или биохимические изменения и/или участвуя в регуляции и модуляции физиологических и биохимических процессов. Некоторые из сигнальных молекул газообразных веществ (СМГВ) образуются эндогенно, то есть в самом организме, некоторые другие, как, например, кислород, поступают извне.
В условиях организма СМГВ растворены во внутриклеточной и/или внеклеточной жидкости, в биологических жидкостях, таких, как плазма крови. Однако во внешнюю среду (например, с выдыхаемым воздухом, отрыжкой или кишечными газами) они выделяются именно в газообразном состоянии.
К сигнальным молекулам газообразных веществ относятся, в частности, окись азота, угарный газ, сероводород и, возможно, некоторые другие. Некоторые СМГВ, образующиеся эндогенно (в самом организме), в литературе иногда называют «эндогенными газами». Употребляются также термины газотрансмиттеры, газомодуляторы. В отношении некоторых сигнальных молекул газообразных веществ, а именно молекул оксида азота (II), угарного газа и сероводорода, в настоящее время (март 2015 года) сложился консенсус специалистов относительно правомерности их причисления как к «эндогенным газам», так и к газотрансмиттерам. Образование же молекул некоторых других газообразных веществ (таких, как, например, закись азота) в живом организме (а не в пробирке с культурой ткани или с белками-ферментами и их субстратами) в физиологических или патофизиологических условиях и притом в физиологически значимых, релевантных концентрациях, и/или их участие в регуляции тех или иных физиологических процессов (то есть их физиологическое значение и сигнальная функция) подвергается сомнению или точно не установлено, либо признаётся не всеми авторами, и молекулы этих веществ рассматриваются, скорее, как «потенциальные кандидаты в эндогенные газы» или «потенциальные кандидаты в газотрансмиттеры», «потенциальные кандидаты в сигнальные молекулы газообразных веществ». При этом у разных авторов списки «потенциальных кандидатов в эндогенные газы» или «потенциальных кандидатов в газотрансмиттеры/сигнальные молекулы газообразных веществ» различаются. Так, например, L. Li и P. K. Moore в своей статье от 2007 года называют среди потенциальных кандидатов в эндогенные газы аммиак, ацетальдегид, оксид серы (IV) и закись азота.[1] Другой учёный, Rui Wang, в статье от 2014 года называет среди потенциальных кандидатов в газотрансмиттеры метан и аммиак, но не упоминает сернистый газ или ацетальдегид.[2]
Некоторые сигнальные молекулы газообразных веществ являются общими для всех или нескольких царств, то есть играют сигнальную роль и у человека и животных, и у растений, и у ряда видов прокариот. Некоторые же, наоборот, имеют важное физиологическое сигнальное значение для, например, растений (как пример — этилен), но образуются в очень малых количествах и, по-видимому, не играют какой-либо существенной физиологической роли у человека и животных, и наоборот. Поэтому рассматривать передачу биологических сигналов с помощью сигнальных молекул газообразных веществ имеет смысл только раздельно по царствам.
Понятие о газотрансмиттерах[править | править код]
Газотрансмиттерами называют некоторые из сигнальных молекул газообразных веществ, синтезируемых в организме человека и животных. Традиционно к газотрансмиттерам причисляют окись азота, угарный газ и сероводород.[3][4]
Газотрансмиттерами принято называть подсемейство сигнальных молекул газообразных веществ, включающее в себя оксид азота (II), угарный газ, сероводород.[3][4]. Упомянутые NO, CO, H2S имеют много общего в эффекте, оказываемом на физиологию организма, однако выполняют свои функции уникальным образом, что отличает их от «классических» сигнальных молекул организма человека и животных, таких, как гормоны, цитокины или нейромедиаторы типа адреналина и ацетилхолина. Впервые идея о том, что растворённое в биологических жидкостях газообразное вещество может оказывать прямое действие на известные фармакологические рецепторные мишени и, таким образом, действовать как нейромедиатор, была выдвинута в 1981 году на основании клинических наблюдений за действием закиси азота.[5][6][7] Эксперименты in vitro подтвердили эти наблюдения,[8] которые позже были воспроизведены другой исследовательской группой на морских свинках.[9]
Концепция «газотрансмиттера» и соответствующая терминология, а также критерии, позволяющие причислить те или иные эндогенные газы или сигнальные молекулы газообразных веществ к «газотрансмиттерам», была впервые предложена в 2002 году[10]. Согласно предложенным критериям, для того, чтобы молекулы эндогенного газообразного вещества могли причисляться к «газотрансмиттерам», для них должны выполняться следующие условия:[11][10]
- Это малая молекула вещества, которое является газообразным при его выделении в свободном состоянии при температуре тела и нормальном атмосферном давлении;
- Молекулы этого вещества способны легко проникать сквозь биологические мембраны. Вследствие этого эффекты газотрансмиттеров не обязаны зависеть от воздействия на уже известные мембранные рецепторы.
- Газотрансмиттер может оказывать эндокринные, паракринные или аутокринные эффекты. В частности, в эндокринном режиме газотрансмиттеры могут выделяться в кровь в месте их производства, переноситься с током крови, захватываться транспортными белками (белками-переносчиками), такими, как гемоглобин, доставляться к удалённым органам и тканям-мишеням, и там высвобождаться, модулируя функции клеток органа или ткани-мишени, удалённой от места первоначального образования молекул газотрансмиттера;
- Это газообразное вещество образуется эндогенно, а не поступает извне, причём образуется ферментативным путём (то есть в результате строго определённых, хорошо известных ферментативных реакций), а образование этого вещества контролируется и регулируется организмом;
- Это газообразное вещество имеет чётко определённые специфические физиологические функции в физиологически релевантных (то есть встречающихся в норме в организме) концентрациях. Таким образом, изменение эндогенных уровней этого газа при помощи тех или иных внешних воздействий вызывает определённые специфические физиологические и биохимические изменения;
- Эндогенные физиологические функции, выполняемые газообразной сигнальной молекулой — предполагаемым «газотрансмиттером», и вызываемые им физиологические и биохимические изменения в функционировании организма могут быть имитированы введением его газообразного аналога в организм извне, в физиологически релевантных концентрациях;
- Его внутриклеточные физиологические и биохимические эффекты могут осуществляться как непосредственно, так и через те или иные системы вторичных посредников, однако должны иметь специфические клеточные, субклеточные и/или молекулярные мишени.
В 2011 году была основана Европейская сеть исследований в области газотрансмиттеров (ENOG)[12]. Целью этой организации является поощрение исследований в области биологической роли эндогенных окисида азота, эндогенного угарного газа, эндогенного сероводорода в качестве газотрансмиттеров с целью лучшего понимания этой роли и установления специфической роли каждого из них как в поддержании здоровья, так и в патологических состояниях. Кроме того, эта организация также ставит одной из своих целей преобразование базовых знаний в области биохимии и физиологии газотрансмиттеров в практически пригодные терапевтические и клинико-диагностические инструменты.
Не все из известных эндогенных газов являются газотрансмиттерами: не для всех образующихся в организме эндогенных газообразных соединений выполняются все вышеперечисленные условия. В частности, не для всех показана роль в передаче внутриклеточных или межклеточных сигналов и/или в регуляции тех или иных физиологических функций. Также не для всех показано образование в клетках организма человека или животного. Так, некоторые из них образуются преимущественно или исключительно микрофлорой кишечника, что, впрочем, не отменяет того, что они могут частично всасываться в кровь и могут оказывать те или иные физиологические эффекты, то есть могут не являться физиологически нейтральными. Для некоторых доказано образование в пробирке — в культуре ткани или при взаимодействии фермента с субстратом, но не доказано образование в живом организме и/или существенный физиологический эффект в результате воздействия образующихся концентраций. Таким образом, термин «эндогенные газы» значительно шире термина «газотрансмиттеры». Ниже рассматривается биологическая роль только тех газов, которые либо являются общепризнанными сигнальными молекулами газообразных веществ, либо предложены кем-либо из авторов в качестве потенциальных кандидатов в сигнальные молекулы газообразных веществ.
Общепризнанные сигнальные молекулы газообразных веществ[править | править код]
У человека и животных[править | править код]
Кислород[править | править код]
Оксид азота (II)[править | править код]
Окись азота является одним из немногих известных газотрансмиттеров и, кроме того, является также химически высокореактивным свободным радикалом, способным выступать как в роли окислителя, так и в роли восстановителя. Окись азота является ключевым вторичным посредником в организмах позвоночных и играет важную роль в межклеточной и внутриклеточной передаче сигнала и, как следствие, во множестве биологических процессов.[13] Известно, что окись азота производится практически всеми типами живых организмов, от бактерий, грибов и растений, до клеток животных.[14]
Окись азота, первоначально известная под именем эндотелиального сосудорасширяющего фактора (химическая природа которого тогда ещё была не известна) синтезируется в организме из аргинина при участии кислорода и НАДФ ферментом синтазой оксида азота. Восстановление неорганических нитратов также может быть использовано для производства организмом эндогенной окиси азота. Эндотелий кровеносных сосудов использует окись азота в качестве сигнала окружающим гладкомышечным клеткам расслабиться, что приводит к вазодилатации и увеличению кровотока. Окись азота является высокореактивным свободным радикалом со временем жизни порядка нескольких секунд, но при этом обладает высокой способностью к проникновению сквозь биологические мембраны. Это делает окись азота идеальной сигнальной молекулой для кратковременного аутокринного (внутри клетки) или паракринного (между близко расположенными или соседними клетками) обмена сигналами.[15]

Независимо от активности синтазы оксида азота, существует и другой путь биосинтеза окиси азота, так называемый нитрат-нитрит-оксидный путь, состоящий в последовательном восстановлении пищевых нитратов и нитритов, получаемых из растительной пищи.[16] Было показано, что богатые нитратами овощи, в особенности листовая зелень, такая, как шпинат и руккола, а также свёкла, способны повышать уровень эндогенной окиси азота и обеспечивать защиту миокарда от ишемии, а также снижать артериальное давление у лиц с предрасположенностью к артериальной гипертензии или начинающимся развитием АГ.[17][18] Для того, чтобы организм мог производить окись азота из нитратов пищи по нитрат-нитрит-оксидному пути, сначала обязательно должно произойти восстановление нитратов до нитритов с помощью сапрофитных бактерий (бактерий-комменсалов), которые обитают во рту.[19] Мониторинг содержания окиси азота в слюне позволяет обнаружить биотрансформацию растительных нитратов в нитриты и окись азота. Повышение уровня окиси азота в слюне наблюдается при диетах, богатых листовой зеленью. В свою очередь, листовая зелень — часто важнейший компонент многих антигипертензивных и «сердечных» диет, разработанных для лечения гипертонической болезни, ишемической болезни сердца, сердечной недостаточности.[20]
Выработка окиси азота повышена у людей, живущих в горах, особенно на больших высотах. Это способствует приспособлению организма к условиям пониженного парциального давления кислорода и уменьшению вероятности гипоксии за счёт увеличения кровотока как в лёгких, так и в периферических тканях. Известные эффекты окиси азота включают в себя не только вазодилатацию, но и участие в нейротрансмиссии в качестве газотрансмиттера, и активацию роста волос,[21] и образование реактивных промежуточных продуктов обмена, и участие в процессе эрекции пениса (благодаря способности окиси азота расширять сосуды полового члена). Фармакологически активные нитраты, такие, как нитроглицерин, амилнитрит, нитропруссид натрия, реализуют своё вазодилатирующее, антиангинальное (антиишемическое), гипотензивное и спазмолитическое действие благодаря тому, что из них в организме образуется окись азота. Вазодилатирующее гипотензивное лекарство миноксидил содержит остаток NO и может работать, кроме всего прочего, ещё и как агонист NO. Аналогично, силденафил и подобные ему препараты способствуют улучшению эрекции преимущественно за счёт того, что усиливают работу связанного с NO сигнального каскада в половом члене.


Окись азота способствует поддержанию гомеостаза сосудов, вызывая расслабление гладких мышц стенок сосудов и угнетая их рост и утолщение интимы сосудов (гипертензивное ремоделирование сосудов), а также угнетая адгезию и агрегацию тромбоцитов и адгезию лейкоцитов к эндотелию сосудов. У больных с атеросклерозом сосудов, сахарным диабетом или гипертензией часто имеются признаки нарушения обмена оксида азота или нарушения во внутриклеточных каскадах передачи сигнала от оксида азота.[22]
Было также показано, что высокое потребление соли снижает образование окиси азота у больных с гипертонической болезнью, хотя биодоступность окиси азота не меняется, остаётся прежней.[23]
Окись азота также образуется в процессе фагоцитоза такими способными к фагоцитозу клетками, как моноциты, макрофаги, нейтрофилы, как часть иммунного ответа на вторжение чужеродных микроорганизмов (бактерий, грибков и др.).[24] Клетки, способные к фагоцитозу, содержат индуцируемую синтазу оксида азота (iNOS), которая активируется γ-интерфероном или сочетанием фактора некроза опухоли со вторым сигналом воспаления.[25][26][27] С другой стороны, β-трансформирующий фактор роста (TGF-β) оказывает сильное угнетающее действие на активность iNOS и биосинтез оксида азота фагоцитами. Интерлейкины 4 и 10 оказывают слабое угнетающее действие на активность iNOS и биосинтез оксида азота соответствующими клетками. Таким образом, иммунная система организма обладает способностью регулировать активность iNOS и доступный фагоцитам арсенал средств иммунного ответа, что играет роль в регуляции процессов воспаления и силы иммунных реакций.[28] Оксид азота секретируется фагоцитами в процессе иммунного ответа в качестве одного из свободных радикалов и является высокотоксичным для бактерий и внутриклеточных паразитов, включая лейшманий[29] и малярийных плазмодиев.[30][31][32] Механизм бактерицидного, противогрибкового и антипротозойного действия оксида азота включает в себя повреждение ДНК бактерий, грибков и простейших[33][34][35] и повреждение железосодержащих белков с разрушением комплексов железа с серой и образованием нитрозилов железа.[36]
В ответ на это многие патогенные бактерии, грибки и простейшие эволюционно развили механизмы устойчивости к образующемуся в процессе фагоцитоза оксиду азота или механизмы его быстрого обезвреживания.[37]
Механизм бактерицидного (в отношении анаэробных микроорганизмов) и антипротозойного действия производных нитроимидазола (таких, как метронидазол) заключается, среди прочего, в образовании в бактериальной клетке или в клетке простейшего, такого, как амёба, в анаэробных условиях свободного оксида азота (II), что приводит к образованию токсичных свободных радикалов, повреждению белков и ДНК и в конечном счёте убивает микроорганизм. Одним из механизмов бактерицидного действия производных нитрофурана, таких, как фурацилин (хотя в этом случае не единственным и не главным) также является образование свободного NO в бактериальной клетке.
Поскольку повышение образования эндогенного оксида азота является одним из маркеров воспаления и поскольку эндогенный оксид азота может оказывать провоспалительное действие при таких состояниях, как бронхиальная астма и бронхообструктивные заболевания, в практической медицине наблюдается повышенный интерес к возможному использованию анализа на содержание оксида азота в выдыхаемом воздухе в качестве простого дыхательного теста при заболеваниях дыхательных путей, сопровождающихся их воспалением. Пониженные уровни эндогенного оксида азота в выдыхаемом воздухе были обнаружены у курильщиков и у велосипедистов, подвергающихся воздействию загрязнения воздуха. В то же время в других популяциях (то есть не среди велосипедистов) с воздействием загрязнения воздуха ассоциировалось повышение уровня эндогенного оксида азота в выдыхаемом воздухе.[38]
Эндогенный оксид азота может привносить свой вклад в повреждение тканей при ишемии и последующей реперфузии, поскольку в процессе реперфузии может образовываться избыточное количество оксида азота, который может реагировать с супероксидом или пероксидом водорода и образовывать сильный и токсичный окислитель, повреждающий ткани — пероксинитрит. Напротив, при отравлении паракватом вдыхание оксида азота способствует повышению выживаемости и лучшему восстановлению больных, поскольку паракват вызывает образование в лёгких больших количеств супероксида и пероксида водорода, снижение биодоступности NO вследствие его связывания с супероксидом и образования пероксинитрита и угнетение активности синтазы оксида азота.

Два важнейших механизма, при помощи которых эндогенный оксид азота проявляет своё биологическое действие на клетки, органы и ткани — это S-нитрозилирование тиоловых соединений (включая тиоловые группы серосодержащих аминокислот, таких, как цистеин) и нитрозилирование ионов переходных металлов. S-нитрозилирование означает обратимое преобразование тиоловых групп (например, цистеиновых остатков в составе молекул белков) в S-нитрозотиолы (RSNO). S-нитрозилирование является важным механизмом динамической, обратимой посттрансляционной модификации и регуляции функций многих, если не всех, основных классов белков.[39] Нитрозилирование ионов переходных металлов подразумевает связывание NO с ионом переходного металла, такого, как железо, медь, цинк, хром, кобальт, марганец, в том числе с ионами переходных металлов в составе простетических групп или активных каталитических центров металлоферментов. В этой роли NO является нитрозильным лигандом. Типичные случаи нитрозилирования ионов переходных металлов включают в себя нитрозилирование гем-содержащих белков, таких, как цитохром, гемоглобин, миоглобин, что приводит к нарушению функции белка (в частности, невозможности гемоглобина выполнять свою транспортную функцию, или инактивации фермента). Особенно важную роль играет нитрозилирование двухвалентного железа, поскольку связывание нитрозильного лиганда с ионом двухвалентного железа особенно сильное и приводит к образованию очень прочной связи. Гемоглобин является важным примером белка, функция которого может изменяться под влиянием NO обоими способами: NO может как непосредственно связываться с железом в составе гема в реакции нитрозилирования, так и образовывать S-нитрозотиолы при S-нитрозилировании серосодержащих аминокислот в составе гемоглобина.[40]
Таким образом, существует несколько механизмов, при помощи которых эндогенный оксид азота оказывает влияние на биологические процессы в живых организмах, клетках и тканях. Эти механизмы включают окислительное нитрозилирование железосодержащих и других металлосодержащих белков, таких, как рибонуклеотид-редуктаза, аконитаза, активацию растворимой гуанилатциклазы с повышением образования цГМФ, стимуляцию АДФ-зависимого рибозилирования белков, S-нитрозилирование сульфгидрильных (тиоловых) групп белков, приводящее к их посттрансляционной модификации (активации либо инактивации), активацию регулируемых факторов транспорта железа, меди и других переходных металлов.[41] Было также показано, что эндогенный оксид азота способен активировать ядерный фактор транскрипции каппа (NF-κB) в мононуклеарных клетках периферической крови. А известно, что NF-κB является важным фактором транскрипции в регуляции процессов апоптоза и воспаления, и в частности важным фактором транскрипции в процессе индукции экспрессии гена индуцируемой синтазы оксида азота. Таким образом, продукция эндогенного оксида азота саморегулируется — повышение уровня NO угнетает дальнейшую экспрессию индуцируемой синтазы оксида азота и предотвращает чрезмерное повышение её уровня и чрезмерное повреждение тканей организма хозяина в процессе воспаления и иммунного ответа.[42]
Известно также, что вазодилатирующее действие оксида азота опосредуется в основном через стимуляцию им активности растворимой гуанилатциклазы, являющейся гетеродимерным ферментом, активирующимся при нитрозилировании. Стимуляция активности гуанилатциклазы приводит к накоплению циклического ГМФ. Увеличение концентрации в клетке циклического ГМФ приводит к повышению активности протеинкиназы G. Протеинкиназа G, в свою очередь, фосфорилирует ряд важных внутриклеточных белков, что приводит к обратному захвату ионов кальция из цитоплазмы во внутриклеточные хранилища и к открытию активируемых кальцием калиевых каналов. Снижение концентрации ионов кальция в цитоплазме клетки приводит к тому, что киназа лёгкой цепи миозина, активируемая кальцием, теряет активность и не может фосфорилировать миозин, что приводит к нарушению образования в молекуле миозина «мостиков» и нарушению его свёртывания в более компактную структуру (сокращения), а следовательно и к расслаблению гладкомышечной клетки. А расслабление гладкомышечных клеток стенок сосудов ведёт к расширению сосудов (вазодилатации) и увеличению кровотока.[43]
Моноксид углерода[править | править код]
Эндогенный моноксид углерода (CO) вырабатывается в норме клетками организма человека и животных и играет роль сигнальной молекулы. Он может играть физиологическую роль в организме, в частности, являться нейротрансмиттером и вызывать вазодилатацию.[44] Ввиду роли эндогенного CO в организме, нарушения его метаболизма связывают с различными заболеваниями, такими, как нейродегенеративные заболевания, атеросклероз кровеносных сосудов, гипертоническая болезнь, сердечная недостаточность, различные воспалительные процессы.[44]
Моноксид углерода образуется в организме в процессе окислительного разрушения протогема IX ферментом гемоксигеназой (EC 1.14.99.3).[45] В свою очередь, протогем IX образуется в процессе разрушения гема из гемоглобина и миоглобина, а также других гемосодержащих белков, таких, как цитохром. Гемоксигеназа разрушает протогем IX с помощью окислительного разрушения его α-метенового мостика. При этом помимо моноксида углерода образуются также биливердин IXa и свободное двухвалентное ионизированное железо. Биливердин IXa затем превращается в билирубин IXa с помощью фермента биливердин-редуктазы. У млекопитающих известны минимум три изоформы гемоксигеназы, ответственных за окислительное разрушение гема — HO-1, HO-2 и HO-3.[46][47]При этом изоформа HO-1 является индуцируемой, и её экспрессия и активность повышаются в ответ на те или иные стрессорные воздействия, а изоформа HO-2 является конституционально активной. Изоформа HO-3, обнаруженная сравнительно недавно, ещё полностью не охарактеризована, и её сравнительная роль в окислительном разрушении гема в физиологических и патологических условиях окончательно не выяснена. Однако известно, что константа Михаэлиса по отношению к протогему IX для изоформы HO-3 выше, чем для двух других изоформ. Разнообразные стрессорные воздействия, такие, как действие провоспалительных цитокинов, гипоксия, образование свободных радикалов, повышенное содержание в крови или тканях свободного гема или ионов тяжёлых и переходных металлов являются индукторами гемоксигеназы-1. Регуляция транскрипции гена гемоксигеназы-1 довольно сложна.[48]
Все три продукта гемоксигеназной реакции являются биологически активными. Так, в частности, биливердин и билирубин являются мощными эндогенными антиоксидантами, способными связывать и обезвреживать свободные радикалы.[49][50]Свободное двухвалентное железо повышает токсичность супероксида и пероксида водорода, благодаря реакции Фентона. Однако, с другой стороны, свободное двухвалентное железо связывается с железосвязывающими белками, в частности, с белком, который является фактором транскрипции железотранспортирующего белка ферритина и стабилизирует мРНК ферритина. Таким образом, свободное железо повышает своё собственное связывание с белками и обезвреживание. В результате уровень свободного железа после кратковременного повышения, вызванного разрушением гема, снижается ниже исходного уровня (лишнее железо связывается с индуцированным его же избытком ферритином и с другими белками). Поскольку не один лишь угарный газ, но все три продукта гемоксигеназной реакции оказывают столь важное и многообразное физиологическое действие, получается, что индукция гемоксигеназы-1 в ответ на стресс (например, воспаление, гипоксию) и образование всех трёх продуктов — биливердина и затем билирубина, угарного газа и двухвалентного железа с последующей индукцией двухвалентным железом биосинтеза ферритина — является защитным механизмом от оксидативного стресса и повреждения тканей и от чрезмерной интенсивности воспаления.
Гемоксигеназа обильно экспрессируется в нормальных физиологических условиях в основном в четырёх органах: в мозгу, в печени, в селезёнке и в яичках. Роль угарного газа как нейромедиатора, газообразной сигнальной молекулы, была впервые обнаружена в мозгу.[51] Однако в опытах на мышах, лишённых функционирующей гемоксигеназы-1 или гемоксигеназы-2, не удалось показать важность угарного газа для нейротрансмиссии.[52] Зато была показана важная роль, которую играет эндогенный угарный газ в регуляции работы и тонуса сосудистой системы печени, её синусов.[53][54]Интересно отметить, что в печени разные изоформы гемоксигеназы по-разному экспрессируются в разных типах клеток печёночной ткани. Так, гемоксигеназа-2 конституционально активна в гепатоцитах, в то время как гемоксигеназа-1 (индуцируемая) обнаруживается в купферовских клетках печени. Накапливающиеся данные свидетельствуют о том, что эндогенный угарный газ, образующийся в печени, принимает участие не только в регуляции микрососудистого тонуса, но и в регуляции секреции желчи и метаболизма ксенобиотиков. Механизмы, при помощи которых эндогенный угарный газ модулирует активность метаболизма ксенобиотиков, включают в себя угнетение активности цитохромов P450 и цитохромоксидаз, а также повышение проницаемости межклеточных и околоклеточных пространств между гепатоцитами, которое приводит к облегчению пассивной диффузии ксенобиотиков в неизменённом виде в желчевыводящие пути. Физиологическое значение этого механизма заключается в «экономии» ненужного расхода цитохромов и цитохромоксидаз и связанного с ними гема, ограничении образования свободных радикалов в процессе метаболизма ксенобиотиков и в предотвращении повреждения печени в результате чрезмерной метаболической перегрузки печени ксенобиотиками. Последние данные показывают также, что повышение образования эндогенного угарного газа в печени за счёт индукции гемоксигеназы-1 в стрессовых условиях значительно изменяет отток желчи и её химический состав, причём это действие угарного газа осуществляется несколькими механизмами.
Помимо роли эндогенного угарного газа в регуляции физиологических функций нормально работающей печени, угарный газ, вырабатываемый в повышенных количествах в результате индукции активности гемоксигеназы-1 предотвращает или уменьшает гепатобилиарную недостаточность и улучшает желчевыделительную функцию печени в условиях эндотоксемии (например, бактериальной эндотоксемии). Улучшение экскреции желчи в результате действия угарного газа отчасти является результатом улучшения кровотока в дольках печени вследствие вызываемой угарным газом вазодилатации. В подобных случаях вазодилатирующее действие угарного газа осуществляется в основном благодаря угнетению монооксигеназ системы цитохромов, а не благодаря повышению активности растворимой гуанилатциклазы. Вызываемое активацией экспрессии гемоксигеназы-1 увеличение образования эндогенного угарного газа не приводит к значительному увеличению концентрации цГМФ в ткани, несмотря на выраженное вазодилатирующее действие угарного газа, что и заставляет предполагать другой, не гуанилатциклазный, основной механизм вазодилатации. Вызываемое угарным газом повышенное желчеотделение является не только результатом улучшения кровотока в дольках и синусах печени, но и результатом его прямого действия на гепатоциты. В микромолярных концентрациях угарный газ стимулирует межклеточный транспорт билирубина-IXa, биливердина-IXa и глютатиона в желчь. При этом усиливаются противовоспалительные, антиоксидантные, детоксицирующие и цитопротекторные свойства выделяемой в двенадцатиперстную кишку желчи. Интересно отметить, что кривая влияния угарного газа на желчевыделительную функцию печени имеет двухфазный характер. При низких концентрациях угарного газа выделение желчи повышается, в то время как в высоких (очевидно, токсических) выделение желчи блокируется. При этом вызываемое угарным газом повышение суммарного количества выделяемой желчи сопровождается также повышением концентрации билирубина, биливердина и глютатиона в желчи. В то же время угарный газ не изменяет содержание в желчи холестерина, фосфолипидов или желчных кислот. Точные механизмы, с помощью которых эндогенный угарный газ способствует экскреции с желчью органических анионов, таких, как билирубин и биливердин, ещё мало изучены, однако уже понятно, что эндогенный угарный газ является одним из факторов, гарантирующих надёжную экскрецию желчи и желчных пигментов (билирубина и биливердина) в условиях повышенного разрушения гема и стрессовой или токсической нагрузки на печень.
Вследствие своей высокой способности обратимо связываться с железосодержащими и в частности гем-содержащими белками, эндогенный угарный газ способен взаимодействовать с растворимой гуанилатциклазой, а также с цитохромами P450 и цитохромоксидазами, и реализует внутриклеточную передачу своего сигнала через них. Поскольку эндогенный оксид азота (II) также способен взаимодействовать с этими белками и использовать их в качестве передатчиков своего сигнала, то долгое время полагали, что эндогенный угарный газ является всего лишь «заместительным» газотрансмиттером вместо оксида азота (II), а их физиологическое действие полностью совпадает, то есть не отличается. Однако в последние годы было показано, что это не так. Поскольку способность угарного газа взаимодействовать с этими белками, изменяя их функцию, отличается от таковой способности у оксида азота (II), то отличается и их физиологическое действие в реальных условиях живого организма. Угарный газ является частичным агонистом активации гуанилатциклазы, в то время как оксид азота (II) — полным. Таким образом, при низких концентрациях оксида азота (II) или его полном отсутствии, угарный газ проявляет свойства агониста, стимулирует гуанилатциклазу, повышает уровень цГМФ, активность протеинкиназы G и в конечном счёте вызывает вазодилатацию. Однако при нормальном или повышенном уровне оксида азота (II) эндогенный угарный газ конкурирует с ним за связывание с гуанилатциклазой, сравнительно слабо индуцируя её активность сам, и, таким образом, приводит к снижению активности гуанилатциклазы, снижению уровня цГМФ и активности протеинкиназы G и к вазоконстрикции по сравнению с действием одного только оксида азота (II) в тех же концентрациях. Гуанилатциклаза является гемосодержащим гетеродимерным белком-ферментом, способным превращать гуанозин-5'-трифосфат в цГМФ. Для работы этого фермента критически важен железосодержащий протопорфирин. Связывание оксида азота с двухвалентным железом в простетической группе гема вызывает разрыв связи проксимально расположенной аминокислоты гистидина с железом и формирование 5-координированного нитрозил-гемового комплекса. Это, в свою очередь, приводит к конформационным изменениям структуры белка гуанилатциклазы и к повышению её каталитической ферментативной активности в сотни раз, и, соответственно, к повышению в сотни раз скорости образования цГМФ из ГТФ. Угарный газ также обладает высоким сродством к железу гема в составе гуанилатциклазы, однако он образует 6-координированный комплекс карбонил-гема. При этом связь проксимального гистидина с железом остаётся ненарушенной. Это приводит к образованию другой, менее сильно отличающейся от «неактивной», конфигурации белка гуанилатциклазы. Такая конфигурация обладает намного меньшей ферментативной активностью по сравнению с конфигурацией, образующейся при связывании NO с гемом и нитрозилировании гема. Таким образом, способность угарного газа активировать гуанилатциклазу намного меньше, чем аналогичная способность оксида азота (II). Имаи с соавторами вывели трансгенную мышку, у которой ген гемоксигеназы-1 экспрессировался преимущественно в гладкомышечных клетках стенок сосудов и, соответственно, в стенках сосудов было повышено образование эндогенного угарного газа. При этом наиболее интересно то, что эти мышки оказались гипертониками от рождения, а также проявляли устойчивость к сосудорасширяющему действию экзогенных нитратов, таких, как нитроглицерин, нитропруссид натрия. Поскольку функциональная активность гуанилатциклазы, равно как и активность синтазы оксида азота и способность синтезировать оксид азота (II), у этих мышек была не нарушена, то предполагаемый механизм развития у этих мышек артериальной гипертензии включает в себя конкурентный антагонизм за связывание с простетическим гемом гуанилатциклазы между повышенным уровнем эндогенного угарного газа — слабого частичного агониста гуанилатциклазы, и обычным (нормальным) уровнем оксида азота (II) — полного агониста гуанилатциклазы, приводящий к снижению сосудорасширяющего действия оксида азота. Таким образом, «тонкая настройка» сосудистого тонуса регулируется соотношением этих газов (NO и CO), которые связываются с одним и тем же белком — гуанилатциклазой, в одном и том же месте (в простетической группе гема), но вызывают разные конфигурации и по-разному модулируют функцию этого белка. Кроме того, было обнаружено, что избыточное образование NO (например, в результате назначения нитратов) приводит к индукции гемоксигеназы-1 и к повышению образования эндогенного угарного газа, который не только конкурирует с NO за связывание с гуанилатциклазой и уменьшает её активацию и сосудорасширяющее действие NO, но и — через карбонилирование ряда факторов транскрипции — понижает экспрессию синтазы оксида азота, тем самым понижая образование NO. Этот механизм служит не только защитой от избыточного образования NO, но и одной из причин развития устойчивости к сосудорасширяющему и антиангинальному воздействию нитратов у больных с ишемической болезнью сердца и другими сердечно-сосудистыми заболеваниями.
Угарный газ также является важным источником углерода для микроорганизмов. Они используют угарный газ для восстановления и преобразования в метан и ацетил-коэнзим А при помощи фермента CO-дегидрогеназы. Интересно, что CO-дегидрогеназа, в отличие от многих других ферментов, взаимодействующих с угарным газом, не содержит гема. Вместо этого в активном каталитическом центре CO-дегидрогеназы используется молибден или никель, которые образуют с CO менее прочные связи, чем железо гема. Кроме того, анаэробные бактерии, обладающие способностью производить гемолитические токсины, экспрессируют бактериальную гемоксигеназу и, таким образом, способны сами окислять гем, образующийся при разрушении гемоглобина крови под влиянием их гемолитических токсинов, и добывать из гема угарный газ и двухвалентное железо для собственных биохимических нужд. Бактериальная гемоксигеназа анаэробных гемолизирующих микробов выполняет те же функции, что и гемоксигеназа млекопитающих — окисляет и разрушает гем, добытый микробами из пищи (из повреждённых тканей с их гемосодержащими белками) или из гемоглобина гемолизированных эритроцитов, с образованием свободного двухвалентного железа и угарного газа.
У многих видов бактерий, в том числе сапрофитных бактерий кишечника, также обнаружен интересный гемосодержащий белок, названный CooA и являющийся высокочувствительным химическим детектором (сенсором) содержания угарного газа в окружающей среде. Комплекс CooA с угарным газом (CooA-CO) является фактором транскрипции, стимулирующим интенсивное размножение бактерий. В то же время известно, что гемоксигеназа-2, конституционально активная и всегда производящая угарный газ, обильно экспрессируется в нервных окончаниях желудочно-кишечного тракта. Предполагается, что бактерии, обитающие в ЖКТ, не только используют образуемый в нервных клетках кишечника хозяина угарный газ для собственных метаболических нужд, но и воспринимают его в качестве сигнала для интенсификации размножения, и что, регулируя выделение угарного газа в нервных окончаниях кишечника, нервная система хозяина способна регулировать интенсивность размножения в нём сапрофитных бактерий.
Образование эндогенного угарного газа закономерно вызывает образование в крови человека небольшого количества карбоксигемоглобина, даже если человек не курит и дышит не атмосферным воздухом (всегда содержащим небольшие количества экзогенного угарного газа), а чистым кислородом или смесью азота с кислородом.
Вслед за появившимися в 1993 году первыми данными о том, что эндогенный угарный газ является нормальным нейротрансмиттером в организме человека,[51][55] а также одним из трёх эндогенных газов, которые в норме модулируют течение воспалительных реакций в организме (два других — оксид азота (II) и сероводород), эндогенный угарный газ привлёк значительное внимание клиницистов и исследователей как важный биологический регулятор. Было показано, что во многих тканях все три вышеупомянутых газа являются противовоспалительными веществами, вазодилататорами, а также вызывают ангиогенез.[56] Однако не всё так просто и однозначно. Ангиогенез — не всегда полезный эффект, поскольку он, в частности, играет роль в росте злокачественных опухолей, а также является одной из причин повреждения сетчатки при макулярной дегенерации. В частности, важно отметить, что курение (основной источник угарного газа в крови, дающий в несколько раз большую концентрацию его, чем естественная продукция) повышает риск макулярной дегенерации сетчатки в 4-6 раз.
Существует теория о том, что в некоторых синапсах нервных клеток, где происходит долговременное запоминание информации, принимающая клетка в ответ на принятый сигнал вырабатывает эндогенный угарный газ, который передаёт сигнал обратно передающей клетке, чем сообщает ей о своей готовности и в дальнейшем принимать сигналы от неё и повышая активность клетки-передатчика сигнала. Некоторые из этих нервных клеток содержат гуанилатциклазу, фермент, который активируется при воздействии эндогенного угарного газа.[55]
Исследования, посвящённые роли эндогенного угарного газа как противовоспалительного вещества и цитопротектора, проводились во множестве лабораторий по всему миру. Эти свойства эндогенного угарного газа делают воздействие на его метаболизм интересной терапевтической мишенью для лечения таких разных патологических состояний, как повреждение тканей, вызванное ишемией и последующей реперфузией (а это, например, инфаркт миокарда, ишемический инсульт), отторжение трансплантата, атеросклероз сосудов, тяжёлый сепсис, тяжёлая малярия, аутоиммунные заболевания. Проводились в том числе и клинические испытания на человеке, однако результаты их пока ещё не опубликованы.[57]
Суммируя, то, что известно на 2015 год о роли эндогенного угарного газа в организме, можно изложить следующим образом:[58]
- Эндогенный угарный газ — одна из важных эндогенных сигнальных молекул;
- Эндогенный угарный газ модулирует функции ЦНС и сердечно-сосудистой системы;
- Эндогенный угарный газ ингибирует агрегацию тромбоцитов и их адгезию к стенкам сосудов;
- Влияние на обмен эндогенного угарного газа в будущем может быть одной из важных терапевтических стратегий при ряде заболеваний.
Сероводород[править | править код]
Эндогенный сероводород производится в небольших количествах клетками млекопитающих и выполняет ряд важных биологических функций, в том числе сигнальную. Это третий из открытых «газотрансмиттеров» (после окиси азота и угарного газа).
Эндогенный сероводород образуется в организме из цистеина при помощи ферментов цистатионин-β-синтетазы и цистатионин-γ-лиазы. Он является спазмолитиком (расслабляет гладкие мышцы) и вазодилататором, подобно окиси азота и угарному газу.[59] Он также проявляет активность в ЦНС, где он повышает NMDA-опосредованную нейротрансмиссию и способствует долговременному запоминанию информации.[60]
В дальнейшем сероводород окисляется до сульфита в митохондриях при помощи фермента тиосульфат-редуктазы. Сульфит в дальнейшем окисляется до тиосульфата и затем сульфата ферментом сульфит-оксидазой. Сульфаты, как конечный продукт метаболизма, экскретируются с мочой.[61]
Благодаря свойствам, сходным со свойствами окиси азота (но без её способности образовывать пероксиды, реагируя с супероксидом), эндогенный сероводород считается сейчас одним из важных факторов, защищающих организм от сердечно-сосудистых заболеваний.[59] Известные кардиопротективные свойства чеснока связаны с катаболизмом полисульфидных групп аллицина в сероводород, причём эта реакция катализируется восстановительными свойствами глютатиона.[62]
Хотя и окись азота, и сероводород способны расслаблять мышцы и вызывать вазодилатацию, их механизмы действия, судя по всему, различны. В то время как окись азота активирует фермент гуанилатциклазу, сероводород активирует АТФ-чувствительные калиевые каналы в гладкомышечных клетках. Исследователям до настоящего времени неясно, как распределяются физиологические роли в регулировании тонуса сосудов между окисью азота, угарным газом и сероводородом. Однако существуют некоторые данные, позволяющие предположить, что окись азота в физиологических условиях в основном расширяет крупные сосуды, в то время как сероводород ответственен за аналогичное расширение мелких кровеносных сосудов.[63]
Последние исследования заставляют предполагать значительное внутриклеточное кросс-общение между сигнальными путями окиси азота и сигнальными путями сероводорода,[64] демонстрирующие, что вазодилатирующие, спазмолитические, противовоспалительные и цитопротективные свойства этих газов взаимозависимы и взаимодополняющи. Кроме того, показано, что сероводород способен реагировать с внутриклеточными S-нитрозотиолами, в результате чего образуется наименьший возможный S-нитрозотиол — HSNO. Это заставляет предполагать, что сероводород играет роль в контроле за уровнем внутриклеточного содержания S-нитрозотиолов.[65]
Подобно окиси азота, сероводород играет роль в расширении сосудов полового члена, необходимом для осуществления эрекции, что создаёт новые возможности для терапии эректильной дисфункции при помощи тех или иных средств, повышающих продукцию эндогенного сероводорода.[66][67]
При инфаркте миокарда обнаруживается выраженный дефицит эндогенного сероводорода, что может иметь неблагоприятные последствия для сосудов.[68] Инфаркт миокарда приводит к некрозу сердечной мышцы в зоне инфаркта через два различных механизма: один — это повышенный оксидативный стресс и повышенное образование свободных радикалов, и другой — это сниженная биодоступность эндогенных вазодилататоров и «защитников» тканей от свободнорадикального повреждения — окиси азота и сероводорода.[69] Повышенное образование свободных радикалов происходит вследствие повышенного несвязанного электронного транспорта в активном сайте фермента эндотелиальной синтазы оксида азота — фермента, ответственного за превращение L-аргинина в окись азота.[68][69] Во время инфаркта, окислительная деградация тетрагидробиоптерина, кофактора в процессе производства окиси азота, ограничивает доступность тетрагидробиоптерина и соответственно ограничивает способность синтазы оксида азота к производству NO.[69] В результате синтаза оксида азота реагирует с кислородом, другим косубстратом, необходимым для производства окиси азота. Результатом этого является образование супероксидов, повышенное образование свободных радикалов и внутриклеточный оксидативный стресс.[68] Дефицит сероводорода ещё более ухудшает эту ситуацию, нарушая активность синтазы оксида азота за счёт ограничения активности Akt и угнетения фосфорилирования Akt синтазы оксида азота в сайте eNOSS1177, необходимом для её активации.[68][70] Вместо этого, при дефиците сероводорода, активность Akt изменяется таким образом, что Akt фосфорилирует ингибирующий сайт синтазы оксида азота — eNOST495 — что приводит к ещё большему угнетению биосинтеза окиси азота.[68][70]
«Сероводородная терапия» использует донор или прекурсор сероводорода, такой, как диаллил-трисульфид, для того, чтобы повысить содержание сероводорода в крови и тканях пациента с инфарктом миокарда. Доноры или прекурсоры сероводорода уменьшают повреждение миокарда после ишемии и реперфузии и риск осложнений инфаркта миокарда.[68] Повышенные уровни сероводорода в тканях и крови реагируют с кислородом, содержащимся в крови и тканях, в результате чего образуется сульфан-сера, промежуточный продукт, в составе которого сероводород «запасается», хранится и транспортируется в клетки.[68] Пулы сероводорода в тканях реагируют с кислородом, повышение содержания сероводорода в тканях активирует синтазу оксида азота и тем самым повышает продукцию окиси азота.[68] Вследствие повышения использования кислорода для производства окиси азота, меньше кислорода остаётся для реагирования с эндотелиальной синтазой оксида азота и производства супероксидов, повышенного при инфаркте, что в итоге приводит к уменьшению образования свободных радикалов.[68] Кроме того, меньшее образование свободных радикалов понижает оксидативный стресс в гладкомышечных клетках сосудов, понижая тем самым окислительную деградацию тетрагидробиоптерина.[69] Повышение доступности кофактора синтазы оксида азота — тетрагидробиоптерина — также способствует увеличению продукции окиси азота в организме.[69] Кроме того, более высокие концентрации сероводорода непосредственно повышают активность синтазы оксида азота через активацию Akt, что приводит к повышению фосфорилирования активирующего сайта eNOSS1177 и снижению фосфорилирования ингибирующего сайта eNOST495.[68][70] Это фосфорилирование приводит к повышению каталитической активности синтазы оксида азота, что приводит к более эффективному и более быстрому превращению L-аргинина в окись азота и повышению концентрации окиси азота.[68][70] Повышение концентрации окиси азота повышает активность растворимой гуанилатциклазы, что, в свою очередь, приводит к повышению образования циклического гуанозинмонофосфата цГМФ из ГТФ.[71] Повышение уровня циклического ГМФ приводит к повышению активности протеинкиназы G (PKG).[72] А протеинкиназа G приводит к снижению уровня внутриклеточного кальция в гладких мышцах стенок сосудов, что приводит к их расслаблению и усилению кровотока в сосудах.[72] Кроме того, протеинкиназа G также ограничивает пролиферацию гладкомышечных клеток стенок сосудов, уменьшая тем самым утолщение интимы сосудов. В конечном итоге, «сероводородная терапия» приводит к уменьшению размеров зоны инфаркта.[68][71]
При болезни Альцгеймера уровень сероводорода в мозгу резко понижен.[73] В модели на крысах болезни Паркинсона концентрация сероводорода в мозгу крыс также оказалась пониженной, причём введение крысам доноров или прекурсоров сероводорода улучшало состояние животных, вплоть до полного исчезновения симптомов.[74] При трисомии 21 (синдроме Дауна) организм, напротив, вырабатывает избыточное количество сероводорода.[61] Эндогенный сероводород также вовлечён в патогенез сахарного диабета 1-го типа. Бета-клетки поджелудочной железы больных сахарным диабетом 1-го типа вырабатывают чрезмерно повышенные количества сероводорода, что приводит к гибели этих клеток и к понижению секреции инсулина соседними, пока ещё живыми, клетками.[63]
В 2005 году было показано, что мышь можно погрузить в состояние почти анабиоза, искусственной гипотермии, подвергнув её воздействию низких концентраций сероводорода (81 ppm) во вдыхаемом воздухе. Дыхание животных замедлилось со 120 до 10 дыхательных движений в минуту, а их температура тела упала с 37 градусов Цельсия до уровня, всего на 2 градуса Цельсия превышающего температуру окружающей среды (то есть эффект был таков, как будто теплокровное животное внезапно стало холоднокровным). Мыши пережили эту процедуру в течение 6 часов, причём после этого у них не наблюдалось никаких негативных последствий для здоровья, нарушений поведения или каких-либо повреждений внутренних органов.[75] В 2006 году было показано, что артериальное давление у мыши, подвергнутой подобным образом воздействию сероводорода, существенно не снижается.[76]
Сходный процесс, известный как гибернация или «зимняя спячка», наблюдается в природе у многих видов млекопитающих, а также у жаб, но не у мыши (хотя мышь может впадать в ступор при долгом отсутствии еды). Было показано, что во время «зимней спячки» продукция эндогенного сероводорода у тех животных, которые впадают в зимнюю спячку, значительно повышается. Теоретически, если бы удалось заставить вызываемую сероводородом гибернацию столь же эффективно работать у людей, это могло бы быть очень полезным в клинической практике для спасения жизни тяжело травмированных или перенёсших тяжёлую гипоксию, инфаркты, инсульты больных, а также для консервации донорских органов. В 2008 году было показано, что гипотермия, вызванная сероводородом в течение 48 часов, у крыс способна уменьшать степень повреждения головного мозга, вызываемого экспериментальным инсультом или травмой мозга.[77]
Сероводород связывается с цитохромоксидазой C и тем самым предотвращает связывание с нею кислорода, что приводит к резкому замедлению метаболизма, но в больших количествах «парализует» клеточное дыхание и приводит к «удушью» на уровне клетки — к клеточной гипоксии. И у человека, и у животных все клетки организма в норме производят некоторое количество сероводорода. Ряд исследователей предположили, что, помимо других физиологических ролей, сероводород также используется организмом для естественной саморегуляции скорости метаболизма (метаболической активности), температуры тела и потребления кислорода, что может объяснить вышеописанное наступление гибернации у мышей и крыс при повышенных концентрациях сероводорода, а также повышение его концентрации при физиологической спячке у животных.[78]
Однако два последних исследования вызывают сомнения в том, что этого эффекта гибернации и индукции гипометаболизма при помощи сероводорода возможно достичь у более крупных животных. Так, исследование 2008 года не смогло воспроизвести этот же эффект на свиньях, что привело исследователей к заключению, что эффект, наблюдаемый у мышей, не наблюдается у более крупных животных.[79] Аналогично, другая статья отмечает, что эффекта индукции гипометаболизма и гибернации при помощи сероводорода, легко достижимого у мышей и крыс, не удаётся достичь у овец.[80]
В феврале 2010 года учёный Марк Рот заявил на конференции, что вызванная сероводородом гипотермия у человека прошла I фазу клинических испытаний.[81] Однако решение о проведении дальнейших клинических испытаний на больных с инфарктом было отозвано основанной им компанией Ikaria в августе 2011 года ещё до начала набора участников испытаний без объяснения причин, со ссылкой на «решение компании».[82][83]
У растений[править | править код]
Этилен[править | править код]
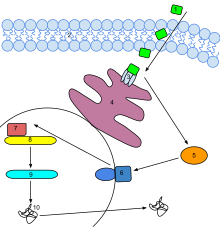
Этилен у растений является своеобразным растительным гормоном, обладающим очень широким спектром биологических эффектов.[84] Он действует в ничтожных, следовых количествах в течение всей жизни растения, стимулируя и регулируя процесс созревания плодов (в частности, фруктов), распускание бутонов (процесс цветения), опадание листьев, рост корневой системы растений.
В коммерческом сборе плодов и фруктов используют специальные комнаты или камеры для дозревания плодов, в атмосферу которых этилен впрыскивается из специальных каталитических генераторов, производящих газообразный этилен из жидкого этанола. Обычно для стимулирования дозревания плодов используется концентрация газообразного этилена в атмосфере камеры от 500 до 2000 ppm в течение 24-48 часов. При более высокой температуре воздуха и более высокой концентрации этилена в воздухе дозревание плодов идёт быстрее. Важно, однако, при этом обеспечивать контроль содержания углекислого газа в атмосфере камеры, поскольку высокотемпературное созревание (при температуре выше 20 градусов Цельсия) или созревание при высокой концентрации этилена в воздухе камеры приводит к резкому повышению выделения углекислого газа быстро созревающими плодами, порой до 10 % углекислоты в воздухе спустя 24 часа от начала дозревания, что может привести к углекислотному отравлению как работников, убирающих уже дозревшие плоды, так и самих фруктов.[85]
Этилен использовался для стимулирования созревания плодов ещё в Древнем Египте. Древние египтяне намеренно царапали или слегка мяли, отбивали финики, фиги и другие плоды с целью стимулировать их созревание (повреждение тканей стимулирует образование этилена тканями растений). Древние китайцы сжигали деревянные ароматические палочки или ароматические свечи в закрытых помещениях с целью стимулировать созревание персиков (при сгорании свеч или дерева выделяется не только углекислый газ, но и недоокисленные промежуточные продукты горения, в том числе и этилен). В 1864 году было обнаружено, что утечка природного газа из уличных фонарей вызывает торможение роста близлежащих растений в длину, их скручивание, аномальное утолщение стеблей и корней и ускоренное созревание плодов.[84] В 1901 году русский учёный Дмитрий Нелюбов показал, что активным компонентом природного газа, вызывающим эти изменения, является не основной его компонент, метан, а присутствующий в нём в малых количествах этилен.[86] Позднее в 1917 году Сара Дубт доказала, что этилен стимулирует преждевременное опадание листьев.[87] Однако только в 1934 году Гейн обнаружил, что сами растения синтезируют эндогенный этилен.[88] В 1935 году Крокер предположил, что этилен является растительным гормоном, ответственным за физиологическое регулирование созревания плодов, а также за старение вегетативных тканей растения, опадание листьев и торможение роста.[89]
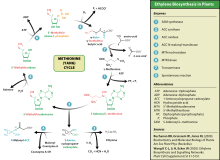
Этилен образуется практически во всех частях высших растений, включая листья, стебли, корни, цветки, мякоть и кожуру плодов и семена. Образование этилена регулируется множеством факторов, включая как внутренние факторы (например фазы развития растения), так и факторы внешней среды. В течение жизненного цикла растения, образование этилена стимулируется в ходе таких процессов, как оплодотворение (опыление), созревание плодов, опадание листьев и лепестков, старение и гибель растения. Образование этилена стимулируется также такими внешними факторами, как механическое повреждение или ранение, нападение паразитов (микроорганизмов, грибков, насекомых и др.), внешние стрессы и неблагоприятные условия развития, а также некоторыми эндогенными и экзогенными стимуляторами, такими, как ауксины и другие.[90]
Цикл биосинтеза этилена начинается с превращения аминокислоты метионина в S-аденозил-метионин (SAMe) при помощи фермента метионин-аденозилтрансферазы. Затем S-аденозил-метионин превращается в 1-аминоциклопропан-1-карбоксиловую кислоту (АЦК, ACC) при помощи фермента 1-аминоциклопропан-1-карбоксилат-синтетазы (АЦК-синтетазы). Активность АЦК-синтетазы лимитирует скорость всего цикла, поэтому регуляция активности этого фермента является ключевой в регуляции биосинтеза этилена у растений. Последняя стадия биосинтеза этилена требует наличия кислорода и происходит при действии фермента аминоциклопропанкарбоксилат-оксидазы (АЦК-оксидазы), ранее известной как этиленобразующий фермент. Биосинтез этилена у растений индуцируется как экзогенным, так и эндогенным этиленом (положительная обратная связь). Активность АЦК-синтетазы и, соответственно, образование этилена повышается также при высоких уровнях ауксинов, в особенности индолуксусной кислоты, и цитокининов.
Этиленовый сигнал у растений воспринимается минимум пятью различными семействами трансмембранных рецепторов, представляющих собой димеры белков. Известен, в частности, рецептор этилена ETR1 у арабидопсиса (Arabidopsis). Гены, кодирующие рецепторы для этилена, были клонированы у арабидопсиса и затем у томата. Этиленовые рецепторы кодируются множеством генов как в геноме арабидопсиса, так и в геноме томатов. Мутации в любом из семейства генов, которое состоит из пяти типов этиленовых рецепторов у арабидопсиса и минимум из шести типов рецепторов у томата, могут привести к нечувствительности растений к этилену и нарушениям процессов созревания, роста и увядания.[91] Последовательности ДНК, характерные для генов этиленовых рецепторов, были обнаружены также у многих других видов растений. Более того, этиленсвязывающий белок был найден даже у цианобактерий.[84]
Неблагоприятные внешние факторы, такие, как недостаточное содержание кислорода в атмосфере, наводнение, засуха, заморозки, механическое повреждение (ранение) растения, нападение патогенных микроорганизмов, грибков или насекомых, могут вызывать повышенное образование этилена в тканях растений. Так, например, при наводнении корни растения страдают от избытка воды и недостатка кислорода (гипоксии), что приводит к биосинтезу в них 1-аминоциклопропан-1-карбоксиловой кислоты. АЦК затем транспортируется по проводящим путям в стеблях вверх, до листьев, и в листьях окисляется до этилена. Образовавшийся этилен способствует эпинастическим движениям, приводящим к механическому стряхиванию воды с листьев, а также увяданию и опаданию листьев, лепестков цветков и плодов, что позволяет растению одновременно и избавиться от избытка воды в организме, и сократить потребность в кислороде за счёт сокращения общей массы тканей.[92]
Оксид азота (II)[править | править код]
У растений эндогенный оксид азота может производиться одним из четырёх способов:
- При помощи аргинин-зависимой синтазы оксида азота;[93][94][95] (хотя существование у растений прямых гомологов синтазы оксида азота животных всё ещё является предметом дискуссий и признаётся не всеми специалистами),[96]
- При помощи находящейся в плазматической мембране растительных клеток нитрат-редуктазы, восстанавливающей усваиваемые из почвы нитраты и нитриты;
- При помощи электронного транспорта, происходящего в митохондриях;
- При помощи неферментативного окисления аммиака или неферментативного восстановления нитратов и нитритов.
У растений эндогенный оксид азота также является сигнальной молекулой (газотрансмиттером), способствует снижению или предотвращению оксидативного стресса клеток, а также играет роль в защите растений от патогенных микроорганизмов и грибков. Было показано, что воздействие низких концентраций экзогенного оксида азота на срезанные цветы и другие растения увеличивает продолжительность времени до их увядания, пожелтения и осыпания листьев и лепестков.[97]
Синильная кислота (цианистый водород)[править | править код]
Потенциальные кандидаты в сигнальные молекулы газообразных веществ[править | править код]
У человека и животных[править | править код]
Закись азота[править | править код]
Закись азота образуется как при ферментативном, так и при неферментативном восстановлении из окиси азота.[98] В опытах in vitro было обнаружено, что закись азота образуется при реакции между окисью азота и тиолом или тиол-содержащими соединениями.[99] Сообщается, что образование N2O из окиси азота было обнаружено в цитозоле гепатоцитов, что заставляет предполагать возможное образование этого газа в клетках млекопитающих в физиологических условиях.[100] В организме бактерий закись азота образуется в ходе процесса, называемого денитрификацией, и катализируемого нитрооксид-редуктазой. Ранее этот процесс предполагался специфичным для некоторых видов бактерий и отсутствующим у млекопитающих, но новые данные заставляют предполагать, что это не так. Было показано, что физиологически релевантные концентрации закиси азота ингибируют как ионные токи, так и опосредуемые эксайтотоксичностью нейродегенеративные процессы, происходящие при чрезмерном возбуждении NMDA-рецепторов.[101] Также закись азота ингибирует биосинтез метионина, угнетая активность метионин-синтетазы и скорость превращения гомоцистеина в метионин и повышая концентрацию гомоцистеина в культурах лимфоцитов[102] и в биоптатах человеческой печени.[103] Хотя закись азота не является лигандом для гема, и не реагирует с тиоловыми группами, она обнаруживается во внутренних структурах гемосодержащих белков, таких, как гемоглобин, миоглобин, цитохромоксидаза.[104] Способность закиси азота нековалентно, обратимо изменять структуру и функции гемосодержащих белков была показана исследованием сдвига инфракрасных спектров тиоловых групп цистеинов гемоглобина[105] и тем, что закись азота способна частично и обратимо ингибировать функцию цитохромоксидазы C.[106] Точные механизмы этого нековалентного взаимодействия закиси азота с гемосодержащими белками и биологическое значение этого явления заслуживают дальнейших исследований. В настоящее время представляется возможным, что эндогенная закись азота участвует в регуляции активности NMDA[101] и опиоидной системы.[107][108]
Сернистый газ[править | править код]
Роль эндогенного сернистого газа в физиологии организма млекопитающих ещё окончательно не выяснена.[109] Сернистый газ блокирует нервные импульсы от рецепторов растяжения лёгких и устраняет рефлекс, возникающий в ответ на перерастяжение лёгких, стимулируя тем самым более глубокое дыхание.
Показано, что эндогенный сернистый газ играет роль в предотвращении повреждения лёгких, уменьшает образование свободных радикалов, оксидативный стресс и воспаление в лёгочной ткани, в то время как экспериментальное повреждение лёгких, вызываемое олеиновой кислотой, сопровождается, наоборот, снижением образования сернистого газа и активности опосредуемых им внутриклеточных путей и повышением образования свободных радикалов и уровня оксидативного стресса. Что ещё более важно, блокада фермента, способствующего образованию эндогенного сернистого газа, в эксперименте способствовала усилению повреждения лёгких, оксидативного стресса и воспаления и активации апоптоза клеток лёгочной ткани. И напротив, обогащение организма подопытных животных серосодержащими соединениями, такими, как глютатион и ацетилцистеин, служащими источниками эндогенного сернистого газа, приводило не только к повышению содержания эндогенного сернистого газа, но и к уменьшению образования свободных радикалов, оксидативного стресса, воспаления и апоптоза клеток лёгочной ткани.[110]
Считают, что эндогенный сернистый газ играет важную физиологическую роль в регуляции функций сердечно-сосудистой системы, а нарушения в его метаболизме могут играть важную роль в развитии таких патологических состояний, как лёгочная гипертензия, гипертоническая болезнь, атеросклероз сосудов, ИБС, ишемия-реперфузия и др.[111]
Показано, что у детей с врождёнными пороками сердца и лёгочной гипертензией повышен уровень гомоцистеина (вредного токсичного метаболита цистеина) и снижен уровень эндогенного сернистого газа, причём степень повышения уровня гомоцистеина и степень снижения выработки эндогенного сернистого газа коррелировала со степенью выраженности лёгочной гипертензии. Предложено использовать гомоцистеин как маркер степени тяжести состояния этих больных и указано, что метаболизм эндогенного сернистого газа может быть важной терапевтической мишенью у этих больных.[112]
Также показано, что эндогенный сернистый газ понижает пролиферативную активность клеток гладких мышц эндотелия сосудов, угнетая активность MAPK-сигнального пути и одновременно активируя аденилатциклазный путь и протеинкиназу A.[113] А пролиферация гладкомышечных клеток стенок сосудов считается одним из механизмов гипертензивного ремоделирования сосудов и важным звеном патогенеза артериальной гипертензии, а также играет роль в развитии стеноза (сужения просвета) сосудов, предрасполагающего к развитию в них атеросклеротических бляшек.
Эндогенный сернистый газ оказывает эндотелий-зависимое вазодилатирующее действие в низких концентрациях, а в более высоких концентрациях становится эндотелий-независимым вазодилататором, а также оказывает отрицательное инотропное действие на миокард (понижает сократительную функцию и сердечный выброс, способствуя снижению артериального давления). Этот вазодилатирующий эффект сернистого газа опосредуется через АТФ-чувствительные кальциевые каналы и кальциевые каналы L-типа («дигидропиридиновые»). В патофизиологических условиях эндогенный сернистый газ оказывает противовоспалительное действие и повышает антиоксидантный резерв крови и тканей, например при экспериментальной лёгочной гипертензии у крыс. Эндогенный сернистый газ также снижает повышенное артериальное давление и тормозит гипертензивное ремоделирование сосудов у крыс в экспериментальных моделях гипертонической болезни и лёгочной гипертензии. Последние (на 2015 год) исследования показывают также, что эндогенный сернистый газ вовлечён в регуляцию липидного метаболизма и в процессы ишемии-реперфузии.[114]
Эндогенный сернистый газ также уменьшает повреждение миокарда, вызванное экспериментальной гиперстимуляцией адренорецепторов изопротеренолом, и повышает антиоксидантный резерв миокарда.[115]
Аммиак[править | править код]

Аммиак является важным источником азота для живых организмов. Несмотря на высокое содержание свободного азота в атмосфере (более 75 %), очень мало живых существ способны использовать свободный, нейтральный двухатомный азот атмосферы, газ N2. Поэтому для включения азота атмосферы в биологический оборот, в частности в синтез аминокислот и нуклеотидов, необходим процесс, который называется «фиксацией азота». Некоторые растения зависят от доступности аммиака и других нитрогенных остатков, выделяющихся в почву разлагающимися органическими остатками других растений и животных. Некоторые другие, такие, как азотфиксирующие бобовые, используют преимущества симбиоза с азотфиксирующими бактериями (ризобиями), которые способны образовывать аммиак из атмосферного азота.[117]
У некоторых организмов аммиак образуется из атмосферного азота с помощью ферментов, называемых нитрогеназами. Этот процесс называется фиксацией азота. И хотя маловероятно, что когда-либо будут изобретены биомиметические методы, способные конкурировать по производительности с химическими методами производства аммиака из азота, тем не менее учёные прилагают большие усилия к тому, чтобы как можно лучше понять механизмы биологической фиксации азота. Научный интерес к этой проблеме отчасти мотивируется необычной структурой активного каталитического центра азотфиксирующего фермента (нитрогеназы), которая содержит необычный биметаллический молекулярный ансамбль Fe7MoS9.
Аммиак является также конечным побочным продуктом метаболизма аминокислот, а именно продуктом их дезаминирования, катализируемого такими ферментами, как глутамат-дегидрогеназа. Экскреция аммиака в неизменённом виде является обычным путём детоксикации аммиака у водных существ (рыбы, водные беспозвоночные, отчасти амфибии). У млекопитающих, включая человека, аммиак обычно быстро превращается в мочевину, которая гораздо менее токсична и, в частности, имеет менее щелочную реакцию и меньшую реакционную способность в качестве восстановителя. Мочевина является основным компонентом сухого остатка мочи. Большинство птиц, пресмыкающихся, насекомых, паукообразных, однако, выделяют в качестве основного нитрогенного остатка не мочевину, а мочевую кислоту.
Аммиак также играет важную роль как в нормальной, так и в патологической физиологии животных. Аммиак производится в процессе нормального метаболизма аминокислот, однако весьма токсичен в высоких концентрациях.[118] Печень животных преобразует аммиак в мочевину с помощью серии последовательных реакций, известных как цикл мочевины. Нарушение функции печени, такое, например, какое наблюдается при циррозе печени, может приводить к нарушению способности печени обезвреживать аммиак и образовывать из него мочевину, и, как следствие, к повышению уровня аммиака в крови, состоянию, называемому гипераммониемия. К аналогичному результату — повышению уровня свободного аммиака в крови и развитию гипераммониемии — приводит наличие врождённых генетических дефектов в ферментах цикла мочевины, таких, например, как орнитин-карбамилтрансфераза. К тому же результату может приводить нарушение выделительной функции почек при тяжёлой почечной недостаточности и уремии: вследствие задержки выделения мочевины её уровень в крови возрастает настолько, что «цикл мочевины» начинает работать «в обратную сторону» — избыток мочевины гидролизуется обратно почками в аммиак и углекислый газ, и, как следствие, уровень аммиака в крови возрастает. Гипераммониемия привносит свой вклад в нарушения сознания и развитие сопорозных и коматозных состояний при печёночной энцефалопатии и уремии, а также в развитие неврологических нарушений, часто наблюдаемых у больных со врождёнными дефектами ферментов цикла мочевины или с органическими ацидуриями.[119]
Менее выраженная, однако клинически существенная, гипераммониемия может наблюдаться при любых процессах, при которых наблюдается повышенный катаболизм белков, например, при обширных ожогах, синдроме сдавления или размозжения тканей, обширных гнойно-некротических процессах, гангрене конечностей, сепсисе и т. д., а также при некоторых эндокринных нарушениях, таких, как сахарный диабет, тяжёлый тиреотоксикоз. Особенно высока вероятность возникновения гипераммониемии при этих патологических состояниях в тех случаях, когда патологическое состояние, помимо повышенного катаболизма белков, вызывает также выраженное нарушение детоксицирующей функции печени или выделительной функции почек.
Аммиак важен для поддержания нормального кислотно-щелочного баланса крови. После образования аммиака из глютамина, альфа-кетоглутарат может быть далее расщеплен с образованием двух молекул гидрокарбоната, которые затем могут использоваться как буфер для нейтрализации кислот, поступающих с пищей. Полученный из глютамина аммиак затем выделяется с мочой (как непосредственно, так и в виде мочевины), что, с учётом образования двух молекул бикарбоната из кетоглутарата, приводит в сумме к потере кислот и сдвигу pH крови в щелочную сторону. Кроме того, аммиак может диффундировать через почечные канальцы, соединяться с ионом водорода и экскретироваться совместно с ним (NH3 + H+ => NH4+), и тем самым ещё больше способствовать выведению кислот из организма.[120]
Аммиак и ионы аммония являются токсическим побочным продуктом метаболизма у животных. У рыб и водных беспозвоночных аммиак выделяется непосредственно в воду. У млекопитающих (включая водных млекопитающих), земноводных и у акул аммиак в цикле мочевины преобразуется в мочевину, поскольку мочевина гораздо менее токсична, менее химически реакционноспособна и может более эффективно «храниться» в организме до момента возможности её выделения. У птиц и пресмыкающихся (рептилий) аммиак, образовавшийся в процессе метаболизма, преобразуется в мочевую кислоту, которая является твёрдым остатком и может быть выделена с минимальными потерями воды.[121]
Ацетальдегид[править | править код]
Эндогенный ацетальдегид в организме человека и животных образуется благодаря окислению эндогенного или экзогенного этанола ферментом алкогольдегидрогеназой. Он постоянно присутствует в низких концентрациях в крови и вызывает вазодилатацию (расслабление гладкомышечных клеток стенок сосудов), предположительно вследствие воздействия на кальциевые каналы. Клетки эндотелия сосудов способны окислять ацетальдегид до уксусной кислоты, ацетил-КоА и в конечном счёте углекислого газа и воды.
Метан[править | править код]
Показано, что эндогенный метан способен вырабатываться не только метаногенной микрофлорой кишечника, но и клетками эукариот, и что его образование значительно возрастает при экспериментальном вызывании клеточной гипоксии, например, при нарушении работы митохондрий при помощи отравления организма экспериментального животного азидом натрия, известным митохондриальным ядом. Высказывается предположение, что образование метана клетками эукариот, в частности животных, может быть внутриклеточным или межклеточным сигналом испытываемой клетками гипоксии.[122]
Также показано увеличение образования метана клетками животных и растений под влиянием различных стрессовых факторов, например, бактериальной эндотоксемии или её имитации введением бактериального липополисахарида, хотя, возможно, этот эффект наблюдается не у всех видов животных (в эксперименте исследователи получили его у мышей, но не получили у крыс).[123] Возможно, что образование метана клетками животных в подобных стрессовых условиях играет роль одного из стрессовых сигналов.
Предполагается также, что метан, выделяемый кишечной микрофлорой человека и не усваиваемый организмом человека (он не метаболизируется и частично удаляется вместе с кишечными газами, частично всасывается и удаляется при дыхании через лёгкие), не является «нейтральным» побочным продуктом метаболизма бактерий, а принимает участие в регуляции перистальтики кишечника, а его избыток может вызывать не только вздутие живота, отрыжку, повышенное газообразование и боли в животе, но и функциональные запоры.[124]
Углекислый газ[править | править код]
Организм человека выделяет приблизительно 2,3 кг углекислого газа в сутки[125], что эквивалентно содержанию 0.63 кг углерода.
Этот углекислый газ переносится от тканей, где он образуется в качестве одного из конечных продуктов метаболизма, по венозной системе и затем выделяется с выдыхаемым воздухом через лёгкие. Таким образом, содержание углекислого газа в крови велико в венозной системе, и уменьшается в капиллярной сети лёгких, и мало в артериальной крови. Содержание углекислого газа в пробе крови часто выражают в терминах парциального давления, то есть давления, которое бы имел содержащийся в пробе крови в данном количестве углекислый газ, если бы весь объём пробы крови занимал только он.[126]
Содержание углекислого газа в крови человека приблизительно таково:
| Единицы измерения | Газ венозной крови | Альвеолярный лёгочный газ | Газ артериальной крови |
|---|---|---|---|
| кПа | 5.5[127]-6.8[127] | 4.8 | 4.7[127]-6.0[127] |
| мм рт. ст. | 41-51 | 36 | 35[128]-45[128] |
Углекислый газ (CO2) транспортируется в крови тремя различными способами (точное соотношение каждого из этих трёх способов транспортировки зависит от того, является ли кровь артериальной или венозной).
- Большая часть углекислого газа (от 70 % до 80 %) преобразуется ферментом карбоангидразой эритроцитов в ионы гидрокарбоната при помощи реакции CO2 + H2O → H2CO3 → H+ + HCO3-[129].
- Около 5 % — 10 % углекислого газа растворено в плазме крови[129].
- Около 5 % — 10 % углекислого газа связано с гемоглобином в виде карбаминосоединений (карбогемоглобин)[129].
Гемоглобин, основной кислород-транспортирующий белок эритроцитов крови, способен транспортировать как кислород, так и углекислый газ. Однако углекислый газ связывается с гемоглобином в ином месте, чем кислород. Он связывается с N-терминальными концами цепей глобина, а не с гемом. Однако благодаря аллостерическим эффектам, которые приводят к изменению конфигурации молекулы гемоглобина при связывании, связывание углекислого газа понижает способность кислорода к связыванию с ним же, при данном парциальном давлении кислорода, и наоборот — связывание кислорода с гемоглобином понижает способность углекислого газа к связыванию с ним же, при данном парциальном давлении углекислого газа. Помимо этого, способность гемоглобина к преимущественному связыванию с кислородом или с углекислым газом зависит также и от pH среды. Эти особенности очень важны для успешного захвата и транспорта кислорода из лёгких в ткани и его успешного высвобождения в тканях, а также для успешного захвата и транспорта углекислого газа из тканей в лёгкие и его высвобождения там.
Углекислый газ является одним из важнейших медиаторов ауторегуляции кровотока. Он является мощным вазодилататором. Соответственно, если уровень углекислого газа в ткани или в крови повышается (например, вследствие интенсивного метаболизма — вызванного, скажем, физической нагрузкой, воспалением, повреждением тканей, или вследствие затруднения кровотока, ишемии ткани), то капилляры расширяются, что приводит к увеличению кровотока и соответственно к увеличению доставки к тканям кислорода и транспорта из тканей накопившейся углекислоты. Кроме того, углекислый газ в определённых концентрациях (повышенных, но ещё не достигающих токсических значений) оказывает положительное инотропное и хронотропное действие на миокард и повышает его чувствительность к адреналину, что приводит к увеличению силы и частоты сердечных сокращений, величины сердечного выброса и, как следствие, ударного и минутного объёма крови. Это также способствует коррекции тканевой гипоксии и гиперкапнии (повышенного уровня углекислоты).
Ионы гидрокарбоната очень важны для регуляции pH крови и поддержания нормального кислотно-щелочного равновесия. Частота дыхания влияет на содержание углекислого газа в крови. Слабое или замедленное дыхание вызывает респираторный ацидоз, в то время как учащённое и чрезмерно глубокое дыхание приводит к гипервентиляции и развитию респираторного алкалоза.
Кроме того, углекислый газ также важен в регуляции дыхания. Хотя наш организм требует кислорода для обеспечения метаболизма, низкое содержание кислорода в крови или в тканях обычно не стимулирует дыхание (вернее, стимулирующее влияние нехватки кислорода на дыхание слишком слабо и «включается» поздно, при очень низких уровнях кислорода в крови, при которых человек нередко уже теряет сознание). В норме дыхание стимулируется повышением уровня углекислого газа в крови. Дыхательный центр гораздо более чувствителен к повышению уровня углекислого газа, чем к нехватке кислорода. Как следствие этого, дыхание сильно разрежённым воздухом (с низким парциальным давлением кислорода) или газовой смесью, вообще не содержащей кислорода (например, 100 % азотом или 100 % закисью азота) может быстро привести к потере сознания без возникновения ощущения нехватки воздуха (поскольку уровень углекислоты в крови не повышается, ибо ничто не препятствует её выдыханию). Это особенно опасно для пилотов военных самолётов, летающих на больших высотах (в случае попадания вражеской ракеты в кабину самолёта и разгерметизации кабины, пилоты могут быстро потерять сознание). Эта особенность системы регуляции дыхания также является причиной того, почему в самолётах стюардессы инструктируют пассажиров в случае разгерметизации салона самолёта в первую очередь надевать кислородную маску самим, прежде чем пытаться помочь кому-либо ещё — делая это, помогающий рискует быстро потерять сознание сам, причём даже не ощущая до последнего момента какого-либо дискомфорта и потребности в кислороде.[129]
Дыхательный центр человека пытается поддерживать парциальное давление углекислого газа в артериальной крови не выше 40 мм рт. ст. При сознательной гипервентиляции содержание углекислого газа в артериальной крови может снизиться до 10-20 мм рт. ст., при этом содержание кислорода в крови практически не изменится или увеличится незначительно, а потребность сделать очередной вдох уменьшится как следствие уменьшения стимулирующего влияния углекислого газа на активность дыхательного центра. Это является причиной того, почему после некоторого периода сознательной гипервентиляции легче задержать дыхание надолго, чем без предшествующей гипервентиляции. Такая сознательная гипервентиляция с последующей задержкой дыхания может привести к потере сознания до того, как человек ощутит потребность сделать вдох. В безопасной обстановке такая потеря сознания ничем особенным не грозит (потеряв сознание, человек потеряет и контроль над собой, перестанет задерживать дыхание и сделает вдох, дыхание, а вместе с ним и снабжение мозга кислородом, восстановится, а затем восстановится и сознание). Однако в других ситуациях, например, перед нырянием, это может быть опасным (потеря сознания и потребность сделать вдох наступят на глубине, и в отсутствие сознательного контроля в дыхательные пути попадёт вода, что может привести к утоплению). Именно поэтому гипервентиляция перед нырянием опасна и не рекомендуется.
Недокись углерода[править | править код]

Недокись углерода, или диоксид триуглерода, C3O2, может образовываться в малых количествах как побочный продукт во всех биохимических процессах, в которых обычно образуется угарный газ (CO), в частности при окислении гема ферментом гемоксигеназой. Кроме того, недокись углерода в организме может также образовываться из малоновой кислоты, внутренним ангидридом которой она является. Показано, что в организме недокись углерода способна полимеризоваться в макроциклические структуры вида (C3O2)n (в основном (C3O2)6 и (C3O2)8), причём эти макроциклические соединения обладают дигоксин-подобной активностью, способностью угнетать активность Na+/K+-АТФ-азы и кальций-зависимой АТФ-азы и натрийуретической активностью и, очевидно, являются эндогенными аналогами дигоксина и уабаина в клетках животных и эндогенными регуляторами функции Na+/K+-АТФ-азы и натрийуреза, а также эндогенными антигипертензивными веществами.[130][131][132] Кроме того, этим макроциклическим соединениям недокиси углерода приписывают также способность защищать клетки от свободнорадикального повреждения и оксидативного стресса (что логично, учитывая «недоокисленность» углерода в них) и роль эндогенной противоопухолевой защиты, в частности, в подвергающихся высокой степени воздействия оксидативного стресса светочувствительных клетках сетчатки глаза.[133]
Синильная кислота[править | править код]
Показано, что нейроны способны вырабатывать эндогенную синильную кислоту (цианистый водород, HCN) после их активации эндогенными или экзогенными опиоидами и что образование нейронами эндогенной синильной кислоты повышает активность NMDA-рецепторов и, таким образом, может играть важную роль в передаче сигнала между нейронами (нейротрансмиссии). Более того, образование эндогенного цианида оказалось необходимым для проявления в полном объёме анальгетического действия эндогенных и экзогенных опиоидов, а вещества, снижающие образование свободной HCN, оказались способны уменьшать (но не полностью устранять) анальгетическое действие эндогенных и экзогенных опиоидов. Выдвинуто предположение, что эндогенная синильная кислота может являться нейромодулятором.[134]
Известно также, что стимуляция мускариновых холинорецепторов клеток феохромоцитомы в культуре повышает образование ими эндогенной синильной кислоты, однако стимуляция мускариновых холинорецепторов ЦНС в живом организме крысы приводит, наоборот, к снижению образования эндогенной синильной кислоты.[135]
Также показано, что синильная кислота выделяется лейкоцитами в процессе фагоцитоза и способна убивать патогенные микроорганизмы.[134]
Возможно, что вазодилатация, вызываемая нитропруссидом натрия, связана не только с образованием окиси азота (механизм, общий для действия всех сосудорасширяющих препаратов группы нитратов, таких, как нитроглицерин, нитросорбид), но и с образованием цианида. Возможно, что эндогенный цианид и образующийся при его обезвреживании в организме тиоцианат играют роль в регуляции функций сердечно-сосудистой системы, в обеспечении вазодилатации, и являются одними из эндогенных антигипертензивных веществ.[136]
Водород[править | править код]
Этилен и этиленоксид[править | править код]
Небольшие количества эндогенного этилена также образуются в клетках животных, включая человека, в процессе перекисного окисления липидов. Некоторое количество эндогенного этилена затем окисляется до этиленоксида, который обладает способностью алкилировать ДНК и белки, в том числе гемоглобин (формируя специфический аддукт с N-терминальным валином гемоглобина — N-гидроксиэтил-валин).[137] Эндогенный этиленоксид также может алкилировать гуаниновые основания ДНК, что приводит к образованию аддукта 7-(2-гидроксиэтил)-гуанина, и является одной из причин присущего всем живым существам риска эндогенного канцерогенеза.[138] Эндогенный этиленоксид также является мутагеном.[139][140] С другой стороны, существует гипотеза, что если бы не образование в организме небольших количеств эндогенного этилена и соответственно этиленоксида, то скорость возникновения спонтанных мутаций и соответственно скорость эволюции была бы значительно ниже.
Примечания[править | править код]
- ↑ L. Li, P.K. Moore. An overview of the biological significance of endogenous gases: new roles for old molecules (англ.) // Biochemical Society Transactions. — Great Britain, Nov 2007. — Vol. 35, iss. 35 (Pt 5), no. Pt 5. — P. 1138—1141. — doi:10.1042/BST0351138. — PMID 17956296.
- ↑ Rui Wang. Gasotransmitters: growing pains and joys // Trends Biochem Sci.. — May 2014. — Т. 39, вып. 39(5), № 5. — С. 227—232. — doi:10.1016/j.tibs.2014.03.003. — PMID 24767680. Архивировано 23 декабря 2017 года.
- ↑ 1 2 Rui Wang (editor). Signal Transduction and the Gasotransmitters: NO, CO, and H2S in Biology and Medicine. — 378 p. — ISBN 978-1617375125.
- ↑ 1 2 Anton Hermann (Editor), Guzel F. Sitdikova (Editor), Thomas M. Weiger (Editor). Gasotransmitters: Physiology and Pathophysiology / Anton Hermann (Editor), Guzel F. Sitdikova (Editor), Thomas M. Weiger (Editor). — 2012th Ed.. — Springer. — 206 с. — 206 p. — ISBN 978-3642446528.
- ↑ Gillman M. A., Lichtigfeld F. J. A comparison of the effects of morphine sulphate and nitrous oxide analgesia on chronic pain states in man (англ.) // J. Neurol. Sci.[англ.] : journal. — 1981. — January (vol. 49, no. 1). — P. 41—5. — doi:10.1016/0022-510X(81)90186-6. — PMID 7205318.
- ↑ Gillman M. A., Lichtigfeld F. J. The similarity of the action of nitrous oxide and morphine (англ.) // Pain : journal. — 1981. — February (vol. 10, no. 1). — P. 110. — doi:10.1016/0304-3959(81)90054-3. — PMID 7232008.
- ↑ Gillman M. A., Lichtigfeld F. J. Nitrous oxide interacts with opioid receptors: more evidence (англ.) // Anesthesiology[англ.] : journal. — Lippincott Williams & Wilkins[англ.], 1983. — May (vol. 58, no. 5). — P. 483—484. — doi:10.1097/00000542-198305000-00021. — PMID 6301312.
- ↑ Daras, C; Cantrill, R; Gillman, M. A. (3H)Naloxone displacement: evidence for nitrous oxide as opioid receptor agonist (англ.) // Eur J Pharmacol[англ.] : journal. — Vol. 89. — P. 177—178. — doi:10.1016/0014-2999(83)90626-x.
- ↑ Ori, C.; Ford-Rice, F; London, E.D. Effects of nitrous oxide and halothane on mu and kappa opioid receptors in guinea-pig brain (англ.) // Anesthesiology[англ.] : journal. — Lippincott Williams & Wilkins[англ.], 1989. — Vol. 70. — P. 541—544. — doi:10.1097/00000542-198903000-00027.
- ↑ 1 2 Wang, R. Two's company, three's a crowd - Can H2S be the third endogenous gaseous transmitter? (англ.) // The FASEB Journal[англ.] : journal. — Federation of American Societies for Experimental Biology[англ.], 2002. — Vol. 16. — P. 1792—1798. — doi:10.1096/fj.02-0211hyp.
- ↑ Wang R (ed) (2004) Signal Transduction and the Gasotransmitters: NO, CO and H2S in Biology and Medicine. Humana Press, New Jersey, USA.
- ↑ [Европейская сеть исследований в области газотрансмиттеров (англ.). Дата обращения: 2 марта 2015. Архивировано 2 апреля 2015 года. Европейская сеть исследований в области газотрансмиттеров (англ.)]
- ↑ Weller, Richard, Could the sun be good for your heart? Архивная копия от 16 февраля 2014 на Wayback Machine TedxGlasgow. Filmed March 2012, posted January 2013
- ↑ Roszer, T (2012) The Biology of Subcellular Nitric Oxide. ISBN 978-94-007-2818-9
- ↑ Stryer, Lubert. Biochemistry, 4th Edition. — W.H. Freeman and Company[англ.], 1995. — С. 732. — ISBN 0-7167-2009-4.
- ↑ Plant-based Diets | Plant-based Foods | Beetroot Juice | Nitric Oxide Vegetables (англ.). Berkeley Test. Дата обращения: 4 октября 2013. Архивировано 4 октября 2013 года.
- ↑ Ghosh, S. M.; Kapil, V.; Fuentes-Calvo, I.; Bubb, K. J.; Pearl, V.; Milsom, A. B.; Khambata, R.; Maleki-Toyserkani, S.; Yousuf, M.; Benjamin, N.; Webb, A. J.; Caulfield, M. J.; Hobbs, A. J.; Ahluwalia, A. Enhanced Vasodilator Activity of Nitrite in Hypertension: Critical Role for Erythrocytic Xanthine Oxidoreductase and Translational Potential (англ.) // Hypertension : journal. — 2013. — Vol. 61, no. 5. — P. 1091—1102. — doi:10.1161/HYPERTENSIONAHA.111.00933. — PMID 23589565.
- ↑ Webb, A. J.; Patel, N.; Loukogeorgakis, S.; Okorie, M.; Aboud, Z.; Misra, S.; Rashid, R.; Miall, P.; Deanfield, J.; Benjamin, N.; MacAllister, R.; Hobbs, A. J.; Ahluwalia, A. Acute Blood Pressure Lowering, Vasoprotective, and Antiplatelet Properties of Dietary Nitrate via Bioconversion to Nitrite (англ.) // Hypertension : journal. — 2008. — Vol. 51, no. 3. — P. 784—790. — doi:10.1161/HYPERTENSIONAHA.107.103523. — PMID 18250365. — PMC 2839282.
- ↑ Hezel, MP; Weitzberg, E. The oral microbiome and nitric oxide homoeostasis // Oral Diseases. — 2013. — С. n/a. — doi:10.1111/odi.12157.
- ↑ Green, Shawn J. Turning DASH Strategy into Reality for Improved Cardio Wellness Outcomes: Part II (англ.). Real World Health Care (25 июля 2013). Дата обращения: 4 октября 2013. Архивировано 17 февраля 2015 года.
- ↑ Proctor, P. H. Endothelium-Derived Relaxing Factor and Minoxidil: Active Mechanisms in Hair Growth (англ.) // Archives in Dermatology : journal. — 1989. — August (vol. 125, no. 8). — P. 1146. — doi:10.1001/archderm.1989.01670200122026. — PMID 2757417. Архивировано 10 марта 2016 года.
- ↑ Dessy, C.; Ferron, O. Pathophysiological Roles of Nitric Oxide: In the Heart and the Coronary Vasculature (англ.) // Current Medical Chemistry – Anti-Inflammatory & Anti-Allergy Agents in Medicinal Chemistry : journal. — 2004. — Vol. 3, no. 3. — P. 207—216. — doi:10.2174/1568014043355348.
- ↑ Osanai, T; Fujiwara, N; Saitoh, M; Sasaki, S; Tomita, H; Nakamura, M; Osawa, H; Yamabe, H; Okumura, K. Relationship between salt intake, nitric oxide, and asymmetric dimethylarginine and its relevance to patients with end-stage renal disease (англ.) // Blood purification : journal. — 2002. — Vol. 20, no. 5. — P. 466—468. — doi:10.1159/000063555. — PMID 12207094.
- ↑ Green, SJ; Mellouk, S; Hoffman, SL; Meltzer, MS; Nacy, C. A. Cellular mechanisms of nonspecific immunity to intracellular infection: Cytokine-induced synthesis of toxic nitrogen oxides from L-arginine by macrophages and hepatocytes (англ.) // Immunology letters : journal. — 1990. — Vol. 25, no. 1—3. — P. 15—9. — doi:10.1016/0165-2478(90)90083-3. — PMID 2126524.
- ↑ Gorczyniski and Stanely, Clinical Immunology. Landes Bioscience; Austin, TX. ISBN 1-57059-625-5
- ↑ Green, SJ; Nacy, CA; Schreiber, RD; Granger, DL; Crawford, RM; Meltzer, MS; Fortier, A. H. Neutralization of gamma interferon and tumor necrosis factor alpha blocks in vivo synthesis of nitrogen oxides from L-arginine and protection against Francisella tularensis infection in Mycobacterium bovis BCG-treated mice (англ.) // Infection and immunity[англ.] : journal. — 1993. — Vol. 61, no. 2. — P. 689—698. — PMID 8423095. — PMC 302781.
- ↑ Kamijo, R; Gerecitano, J; Shapiro, D; Green, SJ; Aguet, M; Le, J; Vilcek, J. Generation of nitric oxide and clearance of interferon-gamma after BCG infection are impaired in mice that lack the interferon-gamma receptor (англ.) // Journal of inflammation : journal. — 1995. — Vol. 46, no. 1. — P. 23—31. — PMID 8832969.
- ↑ Green, SJ; Scheller, LF; Marletta, MA; Seguin, MC; Klotz, FW; Slayter, M; Nelson, BJ; Nacy, C. A. Nitric oxide: Cytokine-regulation of nitric oxide in host resistance to intracellular pathogens (англ.) // Immunology letters : journal. — 1994. — Vol. 43, no. 1—2. — P. 87—94. — doi:10.1016/0165-2478(94)00158-8. — PMID 7537721.
- ↑ Green, SJ; Crawford, RM; Hockmeyer, JT; Meltzer, MS; Nacy, C. A. Leishmania major amastigotes initiate the L-arginine-dependent killing mechanism in IFN-gamma-stimulated macrophages by induction of tumor necrosis factor-alpha (англ.) // Journal of immunology[англ.] : journal. — 1990. — Vol. 145, no. 12. — P. 4290—4297. — PMID 2124240.
- ↑ Seguin, M. C.; Klotz, FW; Schneider, I; Weir, JP; Goodbary, M; Slayter, M; Raney, JJ; Aniagolu, JU; Green, S. J. Induction of nitric oxide synthase protects against malaria in mice exposed to irradiated Plasmodium berghei infected mosquitoes: Involvement of interferon gamma and CD8+ T cells (англ.) // Journal of Experimental Medicine[англ.] : journal. — Rockefeller University Press[англ.], 1994. — Vol. 180, no. 1. — P. 353—358. — doi:10.1084/jem.180.1.353. — PMID 7516412. — PMC 2191552.
- ↑ Mellouk, S; Green, SJ; Nacy, CA; Hoffman, S. L. IFN-gamma inhibits development of Plasmodium berghei exoerythrocytic stages in hepatocytes by an L-arginine-dependent effector mechanism (англ.) // Journal of immunology[англ.] : journal. — 1991. — Vol. 146, no. 11. — P. 3971—3976. — PMID 1903415.
- ↑ Klotz, FW; Scheller, LF; Seguin, MC; Kumar, N; Marletta, MA; Green, SJ; Azad, A. F. Co-localization of inducible-nitric oxide synthase and Plasmodium berghei in hepatocytes from rats immunized with irradiated sporozoites (англ.) // Journal of immunology[англ.] : journal. — 1995. — Vol. 154, no. 7. — P. 3391—3395. — PMID 7534796.
- ↑ Wink, D.; Kasprzak, K.; Maragos, C.; Elespuru, R.; Misra, M; Dunams, T.; Cebula, T.; Koch, W.; Andrews, A.; Allen, J.; Et, al. DNA deaminating ability and genotoxicity of nitric oxide and its progenitors (англ.) // Science : journal. — 1991. — Vol. 254, no. 5034. — P. 1001—1003. — doi:10.1126/science.1948068. — PMID 1948068.
- ↑ Nguyen, T.; Brunson, D.; Crespi, C. L.; Penman, B. W.; Wishnok, J. S.; Tannenbaum, S. R. DNA Damage and Mutation in Human Cells Exposed to Nitric Oxide in vitro (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 1992. — Vol. 89, no. 7. — P. 3030. — doi:10.1073/pnas.89.7.3030. Free text.
- ↑ Li, Chun-Qi; Pang, Bo; Kiziltepe, Tanyel; Trudel, Laura J.; Engelward, Bevin P.; Dedon, Peter C.; Wogan, Gerald N. Threshold Effects of Nitric Oxide-Induced Toxicity and Cellular Responses in Wild-Type and p53-Null Human Lymphoblastoid Cells (англ.) // Chemical Research in Toxicology[англ.] : journal. — 2006. — Vol. 19, no. 3. — P. 399—406. — doi:10.1021/tx050283e. — PMID 16544944. — PMC 2570754. free text
- ↑ Hibbs, John B.; Taintor, Read R.; Vavrin, Zdenek; Rachlin, Elliot M. Nitric oxide: A cytotoxic activated macrophage effector molecule (англ.) // Biochemical and Biophysical Research Communications[англ.] : journal. — 1988. — Vol. 157, no. 1. — P. 87—94. — doi:10.1016/S0006-291X(88)80015-9. — PMID 3196352.
- ↑ Janeway, C. A.; and others. Immunobiology: the immune system in health and disease (англ.). — 6th. — New York: Garland Science[англ.], 2005. — ISBN 0-8153-4101-6.
- ↑ Jacobs, Lotte; Nawrot, Tim S; De Geus, Bas; Meeusen, Romain; Degraeuwe, Bart; Bernard, Alfred; Sughis, Muhammad; Nemery, Benoit; Panis, Luc. Subclinical responses in healthy cyclists briefly exposed to traffic-related air pollution: An intervention study (англ.) // Environmental Health[англ.] : journal. — 2010. — Vol. 9. — P. 64. — doi:10.1186/1476-069X-9-64. — PMID 20973949. — PMC 2984475.
- ↑ van Faassen, E. and Vanin, A. (eds.) (2007) Radicals for life: The various forms of nitric oxide. Elsevier, Amsterdam, ISBN 978-0-444-52236-8
- ↑ van Faassen, E. and Vanin, A. (2004) «Nitric Oxide», in Encyclopedia of Analytical Science, 2nd ed., Elsevier, ISBN 0-12-764100-9.
- ↑ Shami, PJ; Moore, JO; Gockerman, JP; Hathorn, JW; Misukonis, MA; Weinberg, J. B. Nitric oxide modulation of the growth and differentiation of freshly isolated acute non-lymphocytic leukemia cells (англ.) // Leukemia research : journal. — 1995. — Vol. 19, no. 8. — P. 527—533. — doi:10.1016/0145-2126(95)00013-E. — PMID 7658698.
- ↑ Kaibori M., Sakitani K., Oda M., Kamiyama Y., Masu Y. and Okumura T. Immunosuppressant FK506 inhibits inducible nitric oxide synthase gene expression at a step of NF-κB activation in rat hepatocytes (англ.) // J. Hepatol. : journal. — 1999. — Vol. 30, no. 6. — P. 1138—1145. — doi:10.1016/S0168-8278(99)80270-0. — PMID 10406194.
- ↑ Rhoades, RA; Tanner, G. A. Medical physiology 2nd edition. — 2003.
- ↑ 1 2 Wu, L; Wang, R. Carbon Monoxide: Endogenous Production, Physiological Functions, and Pharmacological Applications (англ.) // Pharmacol Rev[англ.] : journal. — 2005. — December (vol. 57, no. 4). — P. 585—630. — doi:10.1124/pr.57.4.3. — PMID 16382109.
- ↑ Maines MD. Heme oxygenase: function, multiplicity, regulatory mechanisms, and clinical applications. — July 1988. — Т. 2, вып. 2(10), № 10. — С. 2557—2568. — PMID 3290025. Архивировано 24 сентября 2015 года.
- ↑ S Shibahara, R Müller, H Taguchi, and T Yoshida. Cloning and expression of cDNA for rat heme oxygenase // Proc Natl Acad Sci USA.. — Dec 1985. — Т. 82, вып. 82(23), № 23. — С. 7865—7869. — PMID 3865203. — PMC 390870.
- ↑ Mahin D. Maine, G. Michael Trakshel, R. Krishnan Kutty. Characterization of two constitutive forms of rat liver microsomal heme oxygenase. Only one molecular species of the enzyme is inducible // The Journal of Biological Chemistry. — January 5, 1986. — Т. 261, вып. 261(1), № 1. — С. 411—419. — PMID 3079757.
- ↑ Choi AM, Alam J. Heme oxygenase-1: function, regulation, and implication of a novel stress-inducible protein in oxidant-induced lung injury // Am J Respir Cell Mol Biol.. — Jul 1996. — Т. 15, вып. 15(1), № 1. — doi:10.1165/ajrcmb.15.1.8679227. — PMID 8679227. Архивировано 1 октября 2016 года.
- ↑ Stocker R, Yamamoto Y, McDonagh AF, Glazer AN, Ames BN. Bilirubin is an antioxidant of possible physiological importance // Science.. — Feb 27, 1987. — Т. 235, вып. 235(4792), № 4792. — С. 1043—1046. — PMID 3029864. Архивировано 26 января 2018 года.
- ↑ Shinobu Hayashi, Rina Takamiya, Tokio Yamaguchi, Kenji Matsumoto, Shinichiro J. Tojo, Takuya Tamatani, Masaki Kitajima, Nobuya Makino, Yuzuru Ishimura, Makoto Suematsu. Induction of Heme Oxygenase-1 Suppresses Venular Leukocyte Adhesion Elicited by Oxidative Stress: Role of Bilirubin Generated by the Enzyme // Circulation Research.. — Oct 15, 1999. — Т. 85, вып. 85(8), № 8. — С. 663—671. — doi:10.1161/01.RES.85.8.663. — PMID 10521239.
- ↑ 1 2 Verma, A; Hirsch, D.; Glatt, C.; Ronnett, G.; Snyder, S. Carbon monoxide: A putative neural messenger (англ.) // Science. — 1993. — Vol. 259, no. 5093. — P. 381—384. — doi:10.1126/science.7678352. — . — PMID 7678352.
- ↑ Kenneth D. Poss, Mark J. Thomas, Alexander K. Ebralidze, Thomas J. O'Dell, Susumu Tonegawa. Hippocampal long-term potentiation is normal in heme oxygenase-2 mutant mice // Neuron.. — October 1995. — Т. 15, вып. 15(4), № 4. — С. 867—873. — doi:10.1016/0896-6273(95)90177-9. — PMID 7576635. (недоступная ссылка)
- ↑ M Suematsu, N Goda, T Sano, S Kashiwagi, T Egawa, Y Shinoda, Y Ishimura. Carbon monoxide: an endogenous modulator of sinusoidal tone in the perfused rat liver // The Journal of Clinical Investigation. — Nov 1995. — Т. 96, вып. 96(5), № 5. — doi:10.1172/JCI118300. — PMID 7593631. — PMC 185895. Архивировано 4 марта 2016 года.
- ↑ Suematsu M, Kashiwagi S, Sano T, Goda N, Shinoda Y, Ishimura Y. Carbon monoxide as an endogenous modulator of hepatic vascular perfusion // Biochem Biophys Res Commun.. — 15 Dec 1994. — Т. 205, вып. 205(2), № 2. — С. 1333—1337. — doi:10.1006/bbrc.1994.2811. — PMID 7802666. Архивировано 3 апреля 2015 года.
- ↑ 1 2 Kolata, Gina (1993-01-26). "Carbon Monoxide Gas Is Used by Brain Cells As a Neurotransmitter". The New York Times. Архивировано 9 февраля 2013. Дата обращения: 2 мая 2010.
- ↑ Li, L; Hsu, A; Moore, P. K. Actions and interactions of nitric oxide, carbon monoxide and hydrogen sulphide in the cardiovascular system and in inflammation—a tale of three gases! (англ.) // Pharmacology & therapeutics : journal. — 2009. — Vol. 123, no. 3. — P. 386—400. — doi:10.1016/j.pharmthera.2009.05.005. — PMID 19486912.
- ↑ Johnson, Carolyn Y. (2009-10-16). "Poison gas may carry a medical benefit". The Boston Globe. Архивировано 20 октября 2009. Дата обращения: 16 октября 2009.
- ↑ Olas, Beata. Carbon monoxide is not always a poison gas for human organism: Physiological and pharmacological features of CO (англ.) // Chemico-Biological Interactions[англ.] : journal. — 2014. — 25 April (vol. 222, no. 5 October 2014). — P. 37—43. — doi:10.1016/j.cbi.2014.08.005. Архивировано 24 сентября 2015 года.
- ↑ 1 2 Lefer, David J. A new gaseous signaling molecule emerges: Cardioprotective role of hydrogen sulfide (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 2007. — November (vol. 104, no. 46). — P. 17907—17908. — doi:10.1073/pnas.0709010104. — . — PMID 17991773. — PMC 2084269. Архивировано 18 февраля 2015 года.
- ↑ Kimura, Hideo. Hydrogen sulfide as a neuromodulator // Molecular Neurobiology. — 2002. — Т. 26, № 1. — С. 13—19. — doi:10.1385/MN:26:1:013. — PMID 12392053.
- ↑ 1 2 Kamoun, Pierre. H2S, a new neuromodulator // Médecine/Sciences. — 2004. — Июль (т. 20, № 6—7). — С. 697—700. — doi:10.1051/medsci/2004206-7697. — PMID 15329822.
- ↑ Benavides, Gloria A; Squadrito, Giuseppe L; Mills, Robert W; Patel, Hetal D; Isbell, T Scott; Patel, Rakesh P; Darley-Usmar, Victor M; Doeller, Jeannette E; Kraus, David W. Hydrogen sulfide mediates the vasoactivity of garlic (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 2007. — 13 November (vol. 104, no. 46). — P. 17977—17982. — doi:10.1073/pnas.0705710104. — . — PMID 17951430. — PMC 2084282.
- ↑ 1 2 «Toxic Gas, Lifesaver Архивная копия от 27 октября 2013 на Wayback Machine», Scientific American, March 2010
- ↑ Coletta C., Papapetropoulos A., Erdelyi K., Olah G., Módis K., Panopoulos P., Asimakopoulou A., Gerö D., Sharina I., Martin E., Szabo C. Hydrogen sulfide and nitric oxide are mutually dependent in the regulation of angiogenesis and endothelium-dependent vasorelaxation. (англ.) // Proceedings of the National Academy of Sciences of the United States of America. — 2012. — Vol. 109, no. 23. — P. 9161—9166. — doi:10.1073/pnas.1202916109. — PMID 22570497.
- ↑ Filipovic M. R., Miljkovic J. Lj, Nauser T., Royzen M., Klos K., Shubina T., Koppenol W. H., Lippard S. J., Ivanović-Burmazović I. Chemical characterization of the smallest S-nitrosothiol, HSNO; cellular cross-talk of H2S and S-nitrosothiols. (англ.) // Journal of the American Chemical Society. — 2012. — Vol. 134, no. 29. — P. 12016—12027. — doi:10.1021/ja3009693. — PMID 22741609.
- ↑ Roberta d'Emmanuele di Villa Biancaa, Raffaella Sorrentinoa, Pasquale Maffiaa, Vincenzo Mironeb, Ciro Imbimbob, Ferdinando Fuscob, Raffaele De Palmad, Louis J. Ignarroe und Giuseppe Cirino. Hydrogen sulfide as a mediator of human corpus cavernosum smooth-muscle relaxation (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 2009. — Vol. 106, no. 11. — P. 4513—4518. — doi:10.1073/pnas.0807974105. — . — PMID 19255435. — PMC 2657379.
- ↑ Hydrogen Sulfide. Potential Help for ED (англ.). WebMD (2 марта 2009). Дата обращения: 2 марта 2015. Архивировано 2 апреля 2015 года.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 King, Adrienne; Polhemus, Bhushan, Otsuka, Kondo, Nicholson, Bradley, Islam, Calvert, Tao, Dugas, Kelley, Elrod, Huang, Wang, Lefer; Bhushan, S.; Otsuka, H.; Kondo, K.; Nicholson, C. K.; Bradley, J. M.; Islam, K. N.; Calvert, J. W.; Tao, Y.-X.; Dugas, T. R.; Kelley, E. E.; Elrod, J. W.; Huang, P. L.; Wang, R.; Lefer, D. J. Hydrogen sulfide cytoprotective signaling is endothelial nitric oxide synthase-nitric oxide dependent (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 2014. — January (vol. 111, no. Early Edition). — P. 1—6. — doi:10.1073/pnas.1321871111. — .
- ↑ 1 2 3 4 5 Alp, Nicholas; Channon. Regulation of endothelial nitric oxide synthase by tetrahydrobiopterin in vascular disease (англ.) // Journal of the American Heart Association[англ.] : journal. — 2003. — Vol. 24. — P. 413—420. — doi:10.1161/01.ATV0000110785.96039.f6.
- ↑ 1 2 3 4 Coletta, Ciro; Papapetropoulos, Erdelyi, Olah, Modis, Panopoulos, Asimakopoulou, Gero, Sharina, Martin, Szabo; Erdelyi, K.; Olah, G.; Modis, K.; Panopoulos, P.; Asimakopoulou, A.; Gero, D.; Sharina, I.; Martin, E.; Szabo, C. Hydrogen sulfide and nitric oxide are mutually dependent in the regulation of angiogenesis and endothelium-dependent vasorelaxation (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 2012. — April (vol. 109, no. 23). — P. 9161—9166. — doi:10.1073/pnas.1202916109. — . — PMID 22570497. — PMC 3384190.
- ↑ 1 2 Boerth, N. J.; Dey, Cornwell, Lincoln. Cyclic GMP-dependent protein kinase regulates vascular smooth muscle cell phenotype (англ.) // Journal of Vascular Research : journal. — 1997. — Vol. 34, no. 4. — P. 245—259. — doi:10.1159/000159231. — PMID 9256084.
- ↑ 1 2 Lincoln, T. M.; Cornwell, Taylor. cGMP-dependent protein kinase mediates the reduction of Ca2+ by cAMP in vascular smooth muscle cells (англ.) // American Physiological Society[англ.] : journal. — 1990. — March (vol. 258, no. 3). — P. C399—C407. — PMID 2156436. Архивировано 31 января 2016 года.
- ↑ Eto, Ko; Takashi Asada; Kunimasa Arima; Takao Makifuchi; Hideo Kimura. Brain hydrogen sulfide is severely decreased in Alzheimer's disease (англ.) // Biochemical and Biophysical Research Communications[англ.] : journal. — 2002. — 24 May (vol. 293, no. 5). — P. 1485—1488. — doi:10.1016/S0006-291X(02)00422-9. — PMID 12054683. Архивировано 26 октября 2016 года.
- ↑ Hu L. F., Lu M., Tiong C. X., Dawe G. S., Hu G., Bian J. S. Neuroprotective effects of hydrogen sulfide on Parkinson's disease rat models. (англ.) // Aging cell. — 2010. — Vol. 9, no. 2. — P. 135—146. — doi:10.1111/j.1474-9726.2009.00543.x. — PMID 20041858.
- ↑ Mice put in 'suspended animation', BBC News, 21 April 2005
- ↑ Gas induces 'suspended animation' Архивная копия от 21 марта 2015 на Wayback Machine, BBC News, 9 October 2006
- ↑ Florian B., Vintilescu R., Balseanu A. T., Buga A-M, Grisk O., Walker L. C., Kessler C., Popa-Wagner A; Vintilescu; Balseanu; Buga; Grisk; Walker; Kessler; Popa-Wagner. Long-term hypothermia reduces infarct volume in aged rats after focal ischemia (англ.) // Neuroscience Letters[англ.] : journal. — 2008. — Vol. 438, no. 2. — P. 180—185. — doi:10.1016/j.neulet.2008.04.020. — PMID 18456407.
- ↑ Mark B. Roth and Todd Nystul. Buying Time in Suspended Animation. Scientific American, 1 June 2005
- ↑ Li, Jia; Zhang, Gencheng; Cai, Sally; Redington, Andrew N. Effect of inhaled hydrogen sulfide on metabolic responses in anesthetized, paralyzed, and mechanically ventilated piglets (англ.) // Pediatric Critical Care Medicine[англ.] : journal. — 2008. — January (vol. 9, no. 1). — P. 110—112. — doi:10.1097/01.PCC.0000298639.08519.0C. — PMID 18477923.. — «H2S does not appear to have hypometabolic effects in ambiently cooled large mammals and conversely appears to act as a hemodynamic and metabolic stimulant.».
- ↑ Haouzi P., Notet V., Chenuel B., Chalon B., Sponne I., Ogier V; and others. H2S induced hypometabolism in mice is missing in sedated sheep (англ.) // Respir Physiol Neurobiol : journal. — 2008. — Vol. 160, no. 1. — P. 109—115. — doi:10.1016/j.resp.2007.09.001. — PMID 17980679.
- ↑ Mark Roth. Suspended animation is within our grasp (англ.). Дата обращения: 2 марта 2015. Архивировано 25 октября 2011 года.
- ↑ IK-1001 (Sodium Sulfide (Na2S) for Injection) in Subjects With Acute ST-Segment Elevation Myocardial Infarction (англ.). ClinicalTrials.gov. U. S. Library of Medicine (4 ноября 2010). — «This study has been withdrawn prior to enrollment. (Company decision. Non-safety related.)». Дата обращения: 2 марта 2015. Архивировано 7 марта 2012 года.
- ↑ Reduction of Ischemia-Reperfusion Mediated Cardiac Injury in Subjects Undergoing Coronary Artery Bypass Graft Surgery (англ.). ClinicalTrials.gov. U. S. Library of Medicine (3 августа 2011). — «This study has been terminated. (Study Terminated — Company decision.)». Дата обращения: 2 марта 2015. Архивировано 7 марта 2012 года.
- ↑ 1 2 3 Lin, Z.; Zhong, S.; Grierson, D. Recent advances in ethylene research (англ.) // Journal of Experimental Botany : journal. — Oxford University Press, 2009. — Vol. 60, no. 12. — P. 3311—3336. — doi:10.1093/jxb/erp204. — PMID 19567479.
- ↑ External Link to More on Ethylene Gassing and Carbon Dioxide Control Архивировано 14 сентября 2010 года.. ne-postharvest.com
- ↑ Neljubov D. Uber die horizontale Nutation der Stengel von Pisum sativum und einiger anderen Pflanzen (нем.) // Beih Bot Zentralbl : magazin. — 1901. — Bd. 10. — S. 128—139.
- ↑ Doubt, Sarah L. The Response of Plants to Illuminating Gas (англ.) // Botanical Gazette : journal. — 1917. — Vol. 63, no. 3. — P. 209—224. — doi:10.1086/332006. — .
- ↑ Gane R. Production of ethylene by some fruits (англ.) // Nature. — 1934. — Vol. 134, no. 3400. — P. 1008. — doi:10.1038/1341008a0. — .
- ↑ Crocker W, Hitchcock AE, Zimmerman PW. (1935) «Similarities in the effects of ethlyene and the plant auxins». Contrib. Boyce Thompson Inst. 7. 231-48. Auxins Cytokinins IAA Growth substances, Ethylene
- ↑ Yang, S. F., and Hoffman N. E. Ethylene biosynthesis and its regulation in higher plants (англ.) // Ann. Rev. Plant Physiol. : journal. — 1984. — Vol. 35. — P. 155—189. — doi:10.1146/annurev.pp.35.060184.001103.
- ↑ Bleecker A. B., Esch J. J., Hall A. E., Rodríguez F. I., Binder B. M. The ethylene-receptor family from Arabidopsis: structure and function. (англ.) // Philosophical transactions of the Royal Society of London. Series B, Biological sciences. — 1998. — Vol. 353, no. 1374. — P. 1405—1412. — doi:10.1098/rstb.1998.0295. — PMID 9800203.
- ↑ Explaining Epinasty Архивная копия от 22 февраля 2015 на Wayback Machine. planthormones.inf
- ↑ Corpas, F. J.; Barroso, JB; Carreras, A; Quirós, M; León, AM; Romero-Puertas, MC; Esteban, FJ; Valderrama, R; Palma, JM; Sandalio, LM; Gómez, M; Del Río, L. A. Cellular and subcellular localization of endogenous nitric oxide in young and senescent pea plants (англ.) // Plant Physiology : journal. — American Society of Plant Biologists, 2004. — Vol. 136, no. 1. — P. 2722—2733. — doi:10.1104/pp.104.042812. — PMID 15347796. — PMC 523336.
- ↑ Corpas, F. J.; Barroso, Juan B.; Carreras, Alfonso; Valderrama, Raquel; Palma, José M.; León, Ana M.; Sandalio, Luisa M.; Del Río, Luis A. Constitutive arginine-dependent nitric oxide synthase activity in different organs of pea seedlings during plant development (англ.) // Planta : journal. — 2006. — Vol. 224, no. 2. — P. 246—254. — doi:10.1007/s00425-005-0205-9. — PMID 16397797.
- ↑ Valderrama, R.; Corpas, Francisco J.; Carreras, Alfonso; Fernández-Ocaña, Ana; Chaki, Mounira; Luque, Francisco; Gómez-Rodríguez, María V.; Colmenero-Varea, Pilar; Del Río, Luis A.; Barroso, Juan B. Nitrosative stress in plants (англ.) // FEBS Lett[англ.] : journal. — 2007. — Vol. 581, no. 3. — P. 453—461. — doi:10.1016/j.febslet.2007.01.006. — PMID 17240373.
- ↑ Corpas, F. J.; Barroso, Juan B.; Del Rio, Luis A. Enzymatic sources of nitric oxide in plant cells – beyond one protein–one function (англ.) // New Phytologist[англ.] : journal. — 2004. — Vol. 162, no. 2. — P. 246—247. — doi:10.1111/j.1469-8137.2004.01058.x.
- ↑ Siegel-Itzkovich J. Viagra makes flowers stand up straight // BMJ. — 1999. — 31 июля (т. 319, № 7205). — С. 274—274. — ISSN 0959-8138. — doi:10.1136/bmj.319.7205.274a.
- ↑ Neil Hogg, Ravinder J. Singh, B. Kalyanaraman. The role of glutathione in the transport and catabolism of nitric oxide (англ.) // FEBS Letters[англ.] : journal. — 1996. — 18 March (vol. 382, no. 3). — P. 223—228. — doi:10.1016/0014-5793(96)00086-5. — PMID 8605974. Архивировано 24 сентября 2015 года.
- ↑ DeMaster E. G., Quast B. J., Redfern B., Nagasawa HT. Reaction of nitric oxide with the free sulfhydryl group of human serum albumin yields a sulfenic acid and nitrous oxide (англ.) // Biochemistry : journal. — 1995. — 12 September (vol. 34, no. 36). — P. 11494—11499. — PMID 7547878. Архивировано 17 ноября 2015 года.
- ↑ Jinjoo Hyun, Gautam Chaudhuri, Jon M. Fukuto. The Reductive Metabolism of Nitric Oxide in Hepatocytes: Possible Interaction with Thiols (англ.) // Drug Metabolism & Disposition[англ.] : journal. — 1999. — 1 September (vol. 27, no. 9). — P. 1005—1009. — PMID 10460799. Архивировано 4 декабря 2018 года.
- ↑ 1 2 Jevtović-Todorović V., Todorović S. M., Mennerick S., Powell S., Dikranian K., Benshoff N., Zorumski C. F., Olney JW. Nitrous oxide (laughing gas) is an NMDA antagonist, neuroprotectant and neurotoxin (англ.) // Nat Med : journal. — 1998. — April (vol. 4, no. 4). — P. 460—463. — PMID 9546794. Архивировано 16 декабря 2017 года.
- ↑ Christensen B., Refsum H., Garras A., Ueland PM. Homocysteine remethylation during nitrous oxide exposure of cells cultured in media containing various concentrations of folates (англ.) // J Pharmacol Exp Ther.[англ.] : journal. — 1992. — June (vol. 261, no. 3). — P. 1096—1105. — PMID 1602376. Архивировано 17 ноября 2015 года.
- ↑ Koblin D. D., Waskell L., Watson J. E., Stokstad E. L., Eger EI 2nd. Nitrous oxide inactivates methionine synthetase in human liver (англ.) // Anesth Analg[англ.] : journal. — 1982. — February (vol. 61, no. 2). — P. 75—78. — PMID 7198880.
- ↑ Vijaya Sampath, Xiao-Jian Zhao, and Winslow S. Caughey. Anesthetic-like interactions of nitric oxide with albumin and hemeproteins. A mechanism for control of protein function (англ.) // The Journal of Biological Chemistry : journal. — 2001. — 27 April (vol. 276, no. 17). — P. 13635—13643. — doi:10.1074/jbc.M006588200. — PMID 11278308.
- ↑ Aichun Dong, Ping Huang, Xiao-Jian Zhao, Vijaya Sampath, and Winslow S. Caughey. Characterization of sites occupied by the anesthetic nitrous oxide within proteins by infrared spectroscopy (англ.) // The Journal of Biological Chemistry : journal. — 1994. — 30 September (vol. 269, no. 39). — P. 23911—23917. — PMID 7929038.
- ↑ Olof Einarsdottir, Winslow S. Caughey. Interactions of the anesthetic nitrous oxide with bovine heart cytochrome c oxidase. Effects on protein structure, oxidase activity, and other properties (англ.) // The Journal of Biological Chemistry : journal. — 1988. — 5 July (vol. 263, no. 19). — P. 9199—9205. — PMID 2837481.
- ↑ Gillman M. A., Lichtigfeld FJ. Nitrous oxide acts directly at the mu opioid receptor (англ.) // Anesthesiology[англ.] : journal. — Lippincott Williams & Wilkins[англ.], 1985. — March (vol. 62, no. 3). — P. 375—376. — PMID 2983587.
- ↑ Gillman M. A., Lichtigfeld FJ. A comparison of the effects of morphine sulphate and nitrous oxide analgesia on chronic pain states in man (англ.) // J Neurol Sci[англ.] : journal. — 1981. — January (vol. 49, no. 1). — P. 41—45. — PMID 7205318. Архивировано 17 ноября 2015 года.
- ↑ Liu, D.; Jin, H; Tang, C; Du, J. Sulfur dioxide: a novel gaseous signal in the regulation of cardiovascular functions (англ.) // Mini-Reviews in Medicinal Chemistry[англ.] : journal. — 2010. — Vol. 10, no. 11. — P. 1039—1045. — PMID 20540708. Архивировано 26 апреля 2013 года.
- ↑ Chen S, Zheng S, Liu Z, Tang C, Zhao B, Du J, Jin H. Endogenous sulfur dioxide protects against oleic acid-induced acute lung injury in association with inhibition of oxidative stress in rats // Lab Invest.. — Feb 2015. — Т. 95, вып. 95(2), № 2. — С. 142—156. — doi:10.1038/labinvest.2014.147. — PMID 25581610. Архивировано 21 сентября 2016 года.
- ↑ Tian H. Advances in the study on endogenous sulfur dioxide in the cardiovascular system // Chin Med J. — Nov 2014. — Т. 127, вып. 127(21), № 21. — С. 3803—3807. — PMID 25382339. Архивировано 8 ноября 2016 года.
- ↑ Yang R, Yang Y, Dong X, Wu X, Wei Y. Correlation between endogenous sulfur dioxide and homocysteine in children with pulmonary arterial hypertension associated with congenital heart disease (кит.) // Zhonghua Er Ke Za Zhi. — Aug 2014. — 第52卷, 第52(8)期, 第8数. — 第625—629 页. — PMID 25224243.
- ↑ Liu D, Huang Y, Bu D, Liu AD, Holmberg L, Jia Y, Tang C, Du J, Jin H. Sulfur dioxide inhibits vascular smooth muscle cell proliferation via suppressing the Erk/MAP kinase pathway mediated by cAMP/PKA signaling // Cell Death Dis.. — May 2014. — Т. 5, вып. 5(5), № 5. — С. e1251. — doi:10.1038/cddis.2014.229.. — PMID 24853429.
- ↑ Wang XB, Jin HF, Tang CS, Du JB. The biological effect of endogenous sulfur dioxide in the cardiovascular system // Eur J Pharmacol.. — 16 Nov 2011. — Т. 670, вып. 670(1), № 1. — doi:10.1016/j.ejphar.2011.08.031. — PMID 21925165. Архивировано 9 мая 2017 года.
- ↑ Liang Y, Liu D, Ochs T, Tang C, Chen S, Zhang S, Geng B, Jin H, Du J. Endogenous sulfur dioxide protects against isoproterenol-induced myocardial injury and increases myocardial antioxidant capacity in rats // Lab Invest.. — Jan 2011. — Т. 91, вып. 91(1), № 1. — С. 12—23. — doi:10.1038/labinvest.2010.156. — PMID 20733562.
- ↑ Karl S. Roth, MD. "eMedicine Specialties > Metabolic Diseases > Hyperammonemia". Архивировано 2 июля 2009. Дата обращения: 7 июля 2009.
- ↑ Adjei, M. B. Nitrogen Fixation and Inoculation of Forage Legumes : [англ.] : [арх. 20 мая 2007] / M. B. Adjei, K. H. Quesenberry, C. G. Chamblis // University of Florida IFAS Extension. — 2002. — June.
- ↑ "PubChem Substance Summary". Архивировано 28 декабря 2011. Дата обращения: 7 июля 2009.
- ↑ Zschocke, Johannes, and Georg Hoffman. Vademecum Metabolism. — Friedrichsdorf, Germany: Milupa GmbH, 2004.
- ↑ Rose, Burton, and Helmut Rennke. Renal Pathophysiology. — Baltimore: Williams & Wilkins[англ.], 1994. — ISBN 0-683-07354-0.
- ↑ Campbell, Neil A.[англ.]; Jane B. Reece. 44 // Biology. — 6th. — San Francisco: Pearson Education, Inc[англ.], 2002. — С. 937—938. — ISBN 0-8053-6624-5.
- ↑ Eszter Tuboly , Andrea Szabó , Dénes Garab , Gábor Bartha , Ágnes Janovszky , Gábor Ero″s , Anna Szabó , Árpád Mohácsi , Gábor Szabó , József Kaszaki , Miklós Ghyczy , Mihály Boros. Methane biogenesis during sodium azide-induced chemical hypoxia in rats (англ.) // American Physiological Society[англ.]. — 15 January 2013. — Vol. 304, iss. 304(2), no. 2. — P. 207—214. — doi:10.1152/ajpcell.00300.2012. — PMID 23174561.
- ↑ Tuboly E, Szabó A, Erős G, Mohácsi A, Szabó G, Tengölics R, Rákhely G, Boros M. Determination of endogenous methane formation by photoacoustic spectroscopy // J Breath Res.. — Dec 2013. — Т. 7, вып. 7(4), № 4. — doi:10.1088/1752-7155/7/4/046004. — PMID 24185326. Архивировано 21 сентября 2016 года.
- ↑ Sahakian AB, Jee SR, Pimentel M. Methane and the gastrointestinal tract // Dig Dis Sci. — Aug 2010. — Т. 55, вып. 55(8), № 8. — С. 2135—2143. — doi:10.1007/s10620-009-1012-0. — PMID 19830557.
- ↑ How much carbon dioxide do humans contribute through breathing? (англ.). Дата обращения: 30 апреля 2009. Архивировано 2 февраля 2011 года.
- ↑ Charles Henrickson. Chemistry. — Cliffs Notes, 2005. — ISBN 0-7645-7419-1.
- ↑ 1 2 3 4 Пересчитано из значений в мм.рт.ст. с использованием коэффициента пересчёта 0.133322 кПа/мм.рт.ст.
- ↑ 1 2 Таблица референсных значений. Юго-Западный медицинский центр при Университете Далласа.
- ↑ Franz Kerek. The structure of the digitalislike and natriuretic factors identified as macrocyclic derivatives of the inorganic carbon suboxide // Hypertension Research. — Sep 2000. — Т. 23, вып. 23 Suppl S33, № Suppl S33. — С. S33—38.. — doi:10.1291/hypres.23.Supplement_S33. — PMID 11016817. Архивировано 2 апреля 2015 года.
- ↑ Robert Stimac, Franz Kerek, Hans-Jurgen Apell. Macrocyclic carbon suboxide oligomers as potent inhibitors of the Na,K-ATPase // Annals of the New York Academy of Sciences. — Apr 2003. — Т. 986. — С. 327—329. — doi:10.1111/j.1749-6632.2003.tb07204.x. — PMID 12763840. Архивировано 19 сентября 2016 года.
- ↑ Franz Kerek, Robert Stimac, Hans-Jürgen Apell, Frank Freudenmann, Luis Moroder. Characterization of the macrocyclic carbon suboxide factors as potent Na,K-ATPase and SR Ca-ATPase inhibitors // Biochimica et Biophysica Acta (BBA) - Biomembranes. — 23 December 2002. — Т. 1567, № 1—2. — С. 213—220. — doi:10.1016/S0005-2736(02)00609-0. — PMID 12488055. Архивировано 24 сентября 2015 года.
- ↑ Tubaro E. Carbon suboxide, the probable precursor of an antitumor cellular sustance: retina (итал.) // Boll Chim Farm. — Jun 1966. — V. 105, fasc. 105(6), n. 6. — P. 415—416. — PMID 6005012. Архивировано 23 сентября 2016 года.
- ↑ 1 2 Borowitz JL, Gunasekar PG, Isom GE. Hydrogen cyanide generation by mu-opiate receptor activation: possible neuromodulatory role of endogenous cyanide // Brain Res.. — 12 Sep 1997. — Т. 768, вып. 768(1—2), № 1—2. — С. 294—300. — doi:10.1016/S0006-8993(97)00659-8. — PMID 9369328. Архивировано 23 сентября 2016 года.
- ↑ Gunasekar PG, Prabhakaran K, Li L, Zhang L, Isom GE, Borowitz JL. Receptor mechanisms mediating cyanide generation in PC12 cells and rat brain // Neurosci Res.. — May 2004. — Т. 49, вып. 49(1), № 1. — С. 13—18. — doi:10.1016/j.neures.2004.01.006. — PMID 15099699. Архивировано 24 сентября 2015 года.
- ↑ Smith RP, Kruszyna H. Toxicology of some inorganic antihypertensive anions // Fed Proc.. — Jan 1976. — Т. 35, вып. 35(1), № 1. — С. 69—72. — PMID 1245233.
- ↑ Filser J. G., Denk B., Törnqvist M., Kessler W., Ehrenberg L. Pharmacokinetics of ethylene in man; body burden with ethylene oxide and hydroxyethylation of hemoglobin due to endogenous and environmental ethylene (англ.) // Arch Toxicol. : journal. — 1992. — Vol. 66, no. 3. — P. 157—163. — PMID 1303633. Архивировано 21 июня 2018 года.
- ↑ Bolt H. M., Leutbecher M., Golka K. A note on the physiological background of the ethylene oxide adduct 7-(2-hydroxyethyl)guanine in DNA from human blood (англ.) // Arch Toxicol. : journal. — 1997. — Vol. 71, no. 11. — P. 719—721. — PMID 9363847. Архивировано 19 августа 2018 года.
- ↑ Csanády G. A., Denk B., Pütz C., Kreuzer P. E., Kessler W., Baur C., Gargas M. L., Filser JG. A physiological toxicokinetic model for exogenous and endogenous ethylene and ethylene oxide in rat, mouse, and human: formation of 2-hydroxyethyl adducts with hemoglobin and DNA (англ.) // Toxicol Appl Pharmacol. : journal. — 2000. — 15 May (vol. 165, no. 1). — P. 1—26. — PMID 10814549. Архивировано 21 июня 2018 года.
- ↑ Thier R., Bolt HM. Carcinogenicity and genotoxicity of ethylene oxide: new aspects and recent advances (англ.) // Crit Rev Toxicol. : journal. — 2000. — September (vol. 30, no. 5). — P. 595—608. — PMID 11055837. Архивировано 19 августа 2018 года.
Ссылки[править | править код]
- European Network on Gasotransmitters (англ.). — [Европейская сеть исследований в области газотрансмиттеров.]. Дата обращения: 1 сентября 2019.