Карбонильные комплексы


Карбони́лы мета́ллов, карбони́льные ко́мплексы — координационные комплексы переходных металлов с монооксидом углерода, являющегося лигандом. Многие карбонилы металлов очень летучи.
Находят применение в органическом синтезе, в качестве катализаторов (или прекурсоров катализаторов) для гомогенного катализа, например, при гидроформилировании или реакции Реппе. Карбонилы многих металлов, например, карбонил никеля, используются в процессе Монда для получения высокочистых металлов. В металлоорганической химии карбонилы металлов используются как прекурсоры для получения других металлоорганических комплексов.
Карбонилы металлов ядовиты. При всасывании через неповреждённую кожу, вдыхании пыли паров или аэрозолей карбонилов, проглатывании, токсическое действие вызвано, в частности, способностью карбонилов карбонилировать гемоглобин с образованием карбоксигемоглобина, который неспособен связывать О2[1].
История[править | править код]

Первые эксперименты по взаимодействию монооксида углерода с металлами были проведены Юстусом фон Либихом в 1834 году. Пропуская угарный газ над расплавленным калием, он получил вещество, имеющее эмпирическую формулу KCO, которое он назвал Kohlenoxidkalium[2]. Позднее было показано, что соединение не является карбонилом металла, а калиевой солью гексагидроксибензола и калиевой солью дигидроксиацетилена[3].

Синтез первого истинного гетеролептического карбонильного комплекса металла был выполнен Полем Шутценбергером в 1868. Пропусканием хлора и окиси углерода над платиновой чернью он получил дикарбонилдихлорплатину Pt(CO)2Cl2[4][5].
Людвиг Монд, один из основателей крупной химической компании Imperial Chemical Industries (ICI), исследовал в 1890-х годах вместе с Карлом Лангером (Carl Langer) и Фридрихом Квинке (Friedrich Quincke) различные процессы регенерации хлора, который расходовался в Солвэй-процессе (англ. Solvay process), с помощью металлического никеля, его оксида и солей[3]. В своих экспериментах группа обрабатывала никель оксидом углерода, и было обнаружено, что образующееся летучее вещество окрашивало пламя бунзеновской горелки в зеленовато-желтый цвет, а при нагревании его в стеклянной трубке образовывалось никелевое зеркало. Этот газ конденсировался в бесцветную жидкость, с температурой кипения 43 °C. Таким образом, Монд и его коллеги обнаружили первый чистый, гомолептический карбонил металла — тетракарбонил никеля (Ni(CO)4)[6]. Необычайно высокая летучесть соединения металла (тетракарбонила никеля) была отмечена фразой лорда Кельвина о том, что Монд «дал металлам крылья»[7].
В следующем году Монд и Марселен Бертло независимо открыли пентакарбонил железа, который производится по аналогичной методике, что и тетракарбонил никеля. Монд оценил экономический потенциал нового класса соединений, которые он коммерчески применил в процессе, позднее названном процессом Монда, и финансировал дополнительные исследования родственных соединений. Генрих Гиртц (Heinrich Hirtz) и его коллега М. Дальтон Ковап (M. Dalton Cowap) синтезировали карбонилы кобальта, молибдена, рутения, и впервые получили нонакарбонилдижелезо[8][9].
В 1906 году Джеймс Дьюар и Г. О. Джонс смогли определить структуру нонакарбонилдижелеза, которое образуется из пентакарбонила железа под действием солнечного света[10]. После смерти Монда в 1909 году, химия карбонилов металлов в течение нескольких лет не имела интереса. В 1924 году компания BASF начала промышленное производство пентакарбонила железа по методу, который был разработан Алвином Митташем. Пентакарбонил железа использовался для производства железа высокой чистоты, так называемого карбонильного железа, и железнооксидного пигмента — охры[11]. В 1927 году А. Жоб и А. Кассаль получили гексакарбонил хрома и гексакарбонил вольфрама, новые гомолептические карбонилы металлов[12].
Уолтер Хибер несколько лет после 1928 интенсивно занимался развитием химии карбонилов металлов. Он проводил систематические исследования и открыл, в частности, основную реакцию, позднее названную реакцией Хибера (Hieber base reaction[13]):
А в 1931 году получил и первый нейтральный гидрид карбонила: Fe(CO)4H2[12]. Это был первый известный способ синтеза гидридов карбонилов металлов и новый синтетический путь к некоторым неизвестным в то время карбонилам, например, декакарбонилдирению[14]. Так же им были открыты некоторые важные синтетические реакции карбонилов[12]:
Хибер, который с 1934 года был директором Института неорганической химии Технического Университета Мюнхена, опубликовал за четыре десятилетия 249 статей на тему химии карбонилов металлов[3].

(Ныне Институт угля имени Макса Планка)
В 1935 году Л. Полинг предложил описание химической связи M-CO на основе метода валентных связей[12].
В 1938 году О. Рёлен (O. Roelen) открыл реакцию гидроформилирования (оксо-синтез), позволяющую получить альдегиды взаимодействием ненасыщенных соединений с СО и Н2 в присутствии катализатора — карбонила металла VIII группы, чаще Co или Rh, которые образуют в реакционной среде активные гидриды состава H[M(CO)4][12]. В 1930-е годы Вольтер Реппе, промышленный химик, а позже член правления компании BASF, открыл ряд гомогенных каталитических процессов, например, гидрокарбокислирование, в котором олефины или алкины вступают в реакцию с монооксидом углерода и водой с образованием ненасыщенных кислот и их производных[3]. В этих реакциях карбонилы, например никеля или кобальта, действуют как катализаторы[15]. Реппе также открыл циклотримеризацию и тетрамеризацию ацетилена и его производных в бензол и производные бензола, используя карбонилы металлов в качестве катализаторов. Компания BASF построила в 1960-е годы производственные мощности для получения акриловой кислоты по процессу Реппе, который только в 1996 году был заменен на более современный метод, основанный на каталитическом окислении пропилена.
В 1963 году Л. Васка открыл комплекс Васка (англ. Vaska’s complex): транс-IrCl(CO)(PPh3)2, способный обратимо связывать кислород[12].
Представители многих новых классов металлоорганических соединений были получены на основе карбонилов. В 1964 году на основе карбонила вольфрама Э. О. Фишером был получен первый карбеновый комплекс (OC)5W=C(OMe)Me, а в 1975 году им же был получен первый карбиновый комплекс I(OC)4Gr≡CR. В 1965 Р. Петтитом (R. Pettit) на основе пентакарбонила железа был получен первый комплекс антиароматического циклобутадиена (C4H4Fe(CO)3). В 1995 году А. Х. Зевайл (англ. Ahmed Zewail) исследовал разрыв связей M-M и M-CO в молекуле карбонила марганца в фемтосекундном масштабе времени (10−15 с) при помощи пульсирующего лазера, за что удостоен Нобелевской премии по химии 1999 года[16].


В 1981 году Роалд Хоффман был удостоен Нобелевской премии по химии за разработку полуэмпирической концепции изолобальной аналогии, основанной на теории молекулярных орбиталей. Она дала возможность исходя из общих представлений обсуждать геометрию и реакционную способность молекул и комплексов, возможность обдуманно подойти к разработке (дизайну) новых комплексов. Концепция описывает металл-карбонильные фрагменты M(CO)n как части октаэдрических «строительных блоков» по аналогии с тетраэдрическими CH3-, CH2- или CH- фрагментами в органической химии. Например, декакарбонилдимарганец, с точки зрения изолобальной аналогии, формируется из двух фрагментов d7Mn(CO)5, которые изолобальны метильному радикалу CH3•. Аналогично тому, как метильные радикалы объединяются формируя этан, карбонил-марганцевые фрагменты могут объединиться в декакарбонилдимарганец. Однако само существование изолобально-аналогичных фрагментов не означает, что желаемые структуры могут быть синтезированы. В своей Нобелевской лекции Хоффман подчеркнул, что изолобальная аналогия является полезной, но очень простой моделью, и в некоторых случаях не приводит к успеху[17][18].
Экономическая выгода использования металл-катализируемого карбонилирования, например, в Реппе химии и гидроформилировании, привела к расширению сферы применения карбонилов и стимулирует их дальнейшее изучение. Кроме того, карбонильные соединения металлов были обнаружены в активных центрах трёх природных ферментов[19].
Номенклатура и терминология[править | править код]
Номенклатура карбонилов металлов определяется зарядом комплекса, числом и типом центральных атомов, количеством и типом лигандов и видом их связывания (терминальный, мостиковый, тип мостикового связывания). Карбонилы встречаются в виде нейтральных комплексов, катионов или солеобразующих анионов карбонилметаллатов. Монооксид углерода в качестве лиганда может быть связан с одним атомом металла (терминальный тип связывания) или мостиковой связью с двумя или более атомами металла. Комплексы могут быть гомолептическим, то есть содержащими только CO лиганды (например, карбонил никеля (Ni(CO)4), но чаще карбонилы металлов являются гетеролептическим и содержат смесь лигандов. Моноядерные карбонилы содержат только один атом металла в качестве центрального атома. За исключением гексакарбонила ванадия, только металлы с четным координационным числом, такие как хром, железо, никель и их соседи по подгруппе, способны образовывать нейтральные одноядерные комплексы. Полиядерные карбонилы, которые содержат связь металл-металл, образуют металлы с нечетными координационным числом[20]. Комплексы, образованные несколькими различными металлами, но только с одним типом лигандов называются ‘’’изолептическими’’’[20].
Число СО-лигандов в комплексе записывается греческой цифрой за которой следует слово «карбонил». Монооксид углерода в карбонилах металлов может иметь различные моды связывания, которые отличаются гаптичностью и видом связывания. Гаптичность отражает число молекул монооксида углерода, непосредственно связанных с центральным атомом, и указывается буквенным префиксом вида ηn в названии комплекса. Верхний индекс n указывает число атомов лиганда, образующих связи с другими атомами комплекса. В случае моногапто координации, например, терминально связанного монооксида углерода, гаптичность равна 1 и, как правило, не отражается в названии. Если монооксид углерода в комплексе связан и через атом углерода и через атом кислорода, то комплекс будет называться дигаптокоординированным η2[21].
Карбонильный лиганд проявляет несколько мод связывания в димерах карбонилов металлов и кластерах. Наиболее распространённый тип связывания — мостиковый, когда СО-лиганд соединяет два атома металлов. Эта мода связывания наблюдается у многих общедоступных карбонилов: Co2(CO)8, Fe2(CO)9, Fe3(CO)12, и Co4(CO)12[1][22]. В некоторых высших кластерах CO-лиганд образует мостики между тремя или даже четырьмя атомами металлов, такие моды обозначаются μ3-CO и μ4-CO. Менее распространены моды связывания, в которых оба атома C и O связаны с атомами металла, например μ3-η2.
Структура карбонилов и механизм связывания[править | править код]


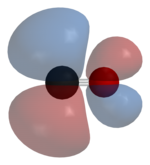
(разрыхляющая) молекулярная орбиталь


Монооксид углерода связывается с атомами переходных металлов по механизму обратного донирования (англ.: back-bonding, back-donation). Связывание состоит из трёх компонентов, что приводит к образованию частично тройной связи. Сигма связь возникает при перекрывании несвязывающей sp-гибридизированной орбитали (с парой электронов) на атоме углерода с d-, s- и р-орбиталями атома металла. Две π-связи образуются при перекрывании заполненных d-орбиталей атома металла с двумя π-разрыхляющими орбиталями атома углерода в молекуле СО. Последний вид связывания требует наличия у атома металла d-электронов и его относительно низкой степени окисления (<+2), в противном случае обратное донирование не является выгодным. Как только электроны металла заполняют π*-разрыхляющие орбитали СО, они ослабляют связь углерод-кислород по сравнению со свободной молекулой монооксида углерода, в то время как связь металл-углерод усиливается. Множественный характер связи М-СО приводит к укорочению расстояния металл-углерод, которое часто меньше 1,8 Â, что примерно на 0,2 Â короче, чем связь металл-алкил. Описать приблизительный механизм связывания молекулы CO с атомом металла можно с использованием резонансных структур канонических форм молекул.

Строение некоторых карбонилов металлов[править | править код]
| Карбонил металла | Симметрия | Структура |
|---|---|---|
| Ni(CO)4 | Тетраэдр | 
|
| Fe(CO)5 Ru(CO)5 Os(CO)5 |
Тригональная бипирамида | 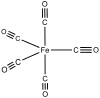
|
| V(CO)6 Cr(CO)6 Mo(CO)6 W(CO)6 |
Октаэдр | 
|
| Co2(CO)8 Rh2(CO)8 |
Незеркальная тригональная
бипирамида/мостиковый изомер |

|
| Mn2(CO)10 Tc2(CO)10 Re2(CO)10 |
Незеркальный диоктаэдр | 
|
| Fe2(CO)9 | Структура «Фонарь» | 
|
| Ru3(CO)12 Os3(CO)12 Fe3(CO)12 |
Треугольный кластер | 
|
| Ir4(CO)12 Co4(CO)12 |
Тетраэдрический кластер | 
|
| Rh4(CO)12 | Тетраэдрический кластер | 
|
Карбонилы Ti, Zr, Hf, Nb, Ta неизвестны, карбонилы Pd, Pt, Cu, Ag, Au в виде нейтральных бинарных комплексов зафиксированы только в низкотемпературной инертной матрице.(Ozin, 1976)[24]
Разделение циркония и гафния в виде карбонилов основывается на различии их температур кипения. В патентах не приводятся температуры кипения карбонилов, но отмечается, что карбонил циркония кипит при более низкой температуре, чем карбонил гафния, и отгоняется первым. Метод заключается в том, что тонко измельчённый порошок циркония, содержащий гафний, помещают в реакционную камеру, снабжённую мешалкой, вводят активированный уголь, а затем окись углерода в количестве, несколько превышающем стехиометрическое. При нагревании смеси под давлением 4—8 атм в интервале температур 300—800° С образуются жидкие карбонилы циркония и гафния, устойчивые при кипении и разрушающиеся при температурах на 50—100° С выше. [25]
Инфракрасная спектроскопия является чувствительным методом определения координированных карбонильных лигандов. Для соединений с мостиковыми СО лигандами, обозначается μ2-СО или просто μ-CO, полосы поглощения νCO обычно сдвинуты на 100—200 см-1 в сторону меньших энергий по сравнению с сигналами терминальных СО, приходящихся на область примерно 1800 см-1. Полосы «шапочных» (μ3) CO-лигандов проявляются при ещё более низких энергиях. Типичные значения νCO для родиевых карбонильных кластеров:[26] Кроме симметричных видов связывания CO встречаются несимметричные или образованные за счёт донирования с d-орбитали металла на π*-орбитали CO[27][28][29]. Усиление компонента π-связывания за счёт обратного донирования от нескольких ядер металлов приводит к дальнейшему ослаблению связи С-О.
Физические свойства карбонилов[править | править код]
Большинство моноядерных карбонильных комплексов представляют собой бесцветные или бледно-желтые летучие жидкости или твердые вещества, способные воспламеняться и крайне токсичные[30]. Гексакарбонил ванадия, стабильный 17-электронный карбонил, образует сине-чёрные кристаллы[1]. Ди- и полиядерные карбонилы, как правило, имеют более насыщенную окраску. Трикарбонил железа (Fe3(CO)12) образует темно-зелёные кристаллы. Большинство кристаллических карбонилов металлов способно сублимироваться в вакууме, хотя этот процесс обычно сопровождается деградацией (отщеплением CO и образованием полиядерных комплексов). При интенсивном нагревании карбонилы разлагаются с выделением CO и мелкодисперсного металла. Карбонилы металлов растворимы в неполярных и полярных органических растворителях, таких как бензол, диэтиловый эфир, ацетон, ледяная уксусная кислота и четыреххлористый углерод. Некоторые соли катионных и анионных карбонилов металлов растворимы в воде и низших спиртах.
Физические свойства некоторых карбонилов металлов[править | править код]
| Карбонил металла | Цвет | tпл, °C | tкип, °C | Плотность (при 20 °C), г/см³ |
|---|---|---|---|---|
| V(CO)6 | зелёно-голубой | разлагается | — | |
| Cr(CO)6 | бесцветный | 150 | разлагается | 1,77 |
| Mn2(CO)10 | жёлтый | 157 | возгоняется | 1,75 |
| Fe(CO)5 | жёлтый | −20 | 103 | 1,455 |
| Fe2(CO)9 | оранжевый | разлагается | 2,85 | |
| Fe3(CO)12 | тёмно-зелёный | 165 | разлагается | |
| Со2(СО)8 | оранжево-красный | 51 | разлагается | 1,87 |
| Со4(СО)12 | чёрный | разлагается | ||
| Ni(CO)4 | бесцветный | −19,3 | 43 | 1,31 |
| Mo(CO)6 | бесцветный | 150 | разлагается | 1,96 |
| Tc2(CO)10 | бесцветный | 160 | ||
| Ru(CO)5 | бесцветный | −22 | ||
| Ru3(CO)12 | оранжевый | 155 | ||
| Rh2(CO)8 | оранжевый | 76 | ||
| Rh4(CO)12 | красный | |||
| W(CO)6 | бесцветный | 150 | разлагается | 2,65 |
| Re2(CO)10 | бесцветный | 177 | разлагается | 2,87 |
| Os(CO)5 | бесцветный | −15 | ||
| Os3(CO)12 | жёлтый | 224 | разлагается | |
| Ir2(CO)8 | зелёно-жёлтый | разлагается | — | |
| Ir4(CO)12 | жёлтый |
Анализ и характеризация[править | править код]

Важными аналитическими методами исследования карбонилов металлов являются инфракрасная спектроскопия и C13ЯМР-спектроскопия. Эти методы позволяют получить структурную информацию на двух различных временных масштабах. Инфракрасно-активные колебательные моды, такие как валентные колебания СО, характеризуются более высокой частотой по сравнению с внутримолекулярными процессами, в то время как ЯМР-переходы происходят при более низких частотах, которые оказываются сравнимыми со скоростью внутримолекулярных процессов обмена лигандов. Таким образом, ЯМР-спектры содержат информацию о «усредненной по времени структуре», в то время как ИК-спектры, в своём роде, мгновенные «снимки»[31]. Примером различий во временных масштабах является то, что в инфракрасном спектре октакарбонила дикобальта (Co2(CO)8) наблюдается 13 полос поглощения νCO, что гораздо больше, чем ожидается для индивидуального соединения. Эта сложность спектра отражает наличие изомеров с мостиковыми CO-лигандами и без них. С13-ЯМР-спектр того же вещества содержит только один сигнал с химическим сдвигом 204 ppm. Это различие в спектрах означает, что изомеры карбонила быстро переходят друг в друга.
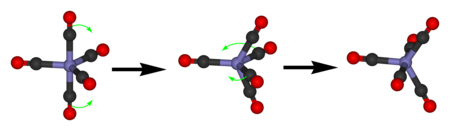
Пентакарбонил железа проявляет только один сигнал в С13-ЯМР спектре из-за быстрого обмена аксиального и экваториального СО-лигандов при псевдоротации Берри.
Инфракрасная спектроскопия карбонилов[править | править код]

Наиболее важным методом характеризации карбонилов металлов является инфракрасная спектроскопия[33]. Колебания C-O в газообразной свободной молекуле (обозначающиеся νCO) наблюдаются при 2143 см−1. Положение полос поглощения νCO карбонилов металлов связано с энергией ИК-активных колебательных мод, и коррелирует с прочностью связи углерод-кислород и обратно коррелирует с силой обратного донирования (англ. Backbonding) с d-орбиталей металла на π-орбитали углерода. π-основность металлического центра зависит от многих факторов: в изоэлектронном ряду от Ti к Fe (в нижней части этого раздела), гексакарбонилы проявляют уменьшение степени обратного донирования (π-backbonding) вслед за увеличением положительного заряда на металле. π-основные лиганды увеличивают плотность π-электронов на атоме металла, а также компенсируют снижение частоты, соответствующей νCO, вызванное обратным донированием. Электронный параметр Толмена использует фрагмент Ni(CO)3 для упорядочивания лигандов по их π-донирующей способности[34][35]. Число колебательных мод карбонильного комплекса металла может быть определено с помощью теории групп. Только те колебательные моды, которые преобразуются как оператор электрического дипольного момента, будут иметь ненулевое произведение групп и будут наблюдаются в ИК-спектре. Таким образом, можно предсказать число наблюдаемых ИК-переходов (но не их энергии)[36][37][38]. Например, CO-лиганды октаэдрических комплексов, например, Cr(CO)6, трансформируются как a1g[прояснить], eg[прояснить], и t1u, но только мода t1u (антисимметричное растяжение шапочных карбонильных лигандов) является ИК-активной. Таким образом, только одна полоса поглощения νCO наблюдается в ИК-спектрах октаэдрических гексакарбонилов металлов. Спектры комплексов более низкой симметрии являются более сложными. Например, в ИК-спектре Fe2(CO)9 проявляются полосы поглощения CO при 2082, 2019 и 1829 см−1. Перечень ИК-наблюдаемых колебательных мод для некоторых карбонилов металлов приведен в таблице, в литературных источниках доступны всеобъемлющие таблицы[33].
| Соединение | νCO (см−1) | Сдвиг C13-ЯМР |
|---|---|---|
| CO | 2143 | 181 |
| Ti(CO)6−2 | 1748 | |
| V(CO)6−1 | 1859 | |
| Cr(CO)6 | 2000 | 212 |
| Mn(CO)6+ | 2100 | |
| Fe(CO)62+ | 2204 | |
| Fe(CO)5 | 2022, 2000 | 209 |
| Карбонил | νCO, µ1[прояснить] (cm−1) | νCO, µ2[прояснить] (cm−1) | νCO, µ3[прояснить] (cm−1) |
|---|---|---|---|
| Rh2(CO)8 | 2060, 2084 | 1846, 1862 | |
| Rh4(CO)12 | 2044, 2070, 2074 | 1886 | |
| Rh6(CO)16 | 2045, 2075 | 1819 |
Спектроскопии ядерного магнитного резонанса[править | править код]
С13 ЯМР-спектроскопия является традиционным методом изучения карбонилов металлов. Для повышения чувствительности метода, комплексы нередко обогащают C13O. Типичный диапазон химических сдвигов для терминальных карбонильных лигандов составляет от 150 до 220 ppm, для мостиковых — от 230 до 280 ppm[1]. В спектрах C13 сигналы смещаются в сторону сильного поля с увеличением атомного номера центрального металла.
Спектроскопию ядерного магнитного резонанса можно использовать для экспериментального определения динамики комплекса[31]. Энергия активации процессов обменов лигандов может быть определена по температурной зависимости уширения линий в спектре[39].
Масс-спектрометрия[править | править код]
Масс-спектрометрия позволяет получить информацию о структуре и составе комплексов. Спектры поликарбонилов металлов обычно легко интерпретировать, поскольку доминирующим процессом фрагментации является потеря карбонильных лигандов (m/z = 28).
Ударная электронная ионизация является наиболее распространённым методом характеризации нейтральных карбонилов металлов. Нейтральный карбонил металла может быть преобразован в заряженный комплекс посредством химических превращений, что даёт возможность использовать ионизацию электрораспылением (электроспрей), оборудование для которой широко распространены и доступны. Например, обработка карбонила металла алкоксидом (алкоголятом ЩМ) даёт анионные металлкарбоксилаты (также называемые металлформиатами или карбонилметаллатами), которые можно анализировать с помощью ESI-MS:
Некоторые карбонилы металлов реагируют с азидами, что даёт изоцианатные комплексы с выделением азота[40]. Степень фрагментации можно контролировать регулируя напряжение на конусе и/или температуру. ESI-MS позволяет определить молекулярную массу исходного комплекса, а также информацию о структурных перестройках, связанных с потерей карбонильных лигандов[41].
Распространенность в природе[править | править код]

Для свободного гема гемоглобина человека в растворе сродство к CO превышает сродство к O2 в 20000 раз, что ставит под угрозу существование сложной жизни на Земле, однако белки гема — миоглобин и гемоглобин снижают селективность связывания, и отношение показателей селективности связывания CO к O2 составляет 25 к 200. Длительное время не удавалось установить причину этого эффекта. Например, для фрагмента Fe-C-O ранние рентгеноструктурные исследования показали неизвестное у карбонилов уголковое строение с углом 40-60˚. Лишь к концу XX века было установлено, что фрагмент практически линеен (с углом не более 7-9˚), причем линейная координация оказывается невыгодной из-за стерических затруднений, создаваемых белками окружения. Координированный O2, напротив, имеет уголковое строение, в котором терминальный атом кислорода образует стабилизирующую водородную связь с дальним гистидиновым остатком гемоглобина[43].
В исследованиях инфракрасного спектра Галактического Ядра в межзвездных пылевых облаках были обнаружены колебания CO, характерные для карбонилов железа[44]. Кластеры карбонилов железа также наблюдались посредством ИК-спектроскопии в хондритах Jiange H5. Были найдены четыре ИК-частоты растяжения, характерные для терминальных и мостиковых карбонильных лигандов[45].
В богатой кислородом атмосфере Земли карбонилы металлов окисляются до оксидов. Но возможность образования таких комплексов в восстановительной гидротермальной среде в пре-биотическом периоде истории и возможность их участия в качестве катализаторов в синтезе критических биохимических соединений, например, пировиноградной кислоты, является предметом дискуссий[46]. Следы карбонилов железа, никеля, вольфрама были найдены в газообразных эманациях осадков сточных вод муниципальных очистных сооружений[47].
Ферменты-гидрогеназы содержат молекулу СО, связанную с атомом железа. По-видимому, СО стабилизирует низкие степени окисления металла, что облегчает связывание водорода. Ферменты CO-дегидрогеназы и ацетил-КоА-синтазы также участвуют в биопревращениях СО[48]. Некоторые CO-содержащие комплексы задействуются при отравлении угарным газом и выполняют сигнальную роль[49].
Синтез карбонилов[править | править код]
Синтез карбонилов металлов является предметом интенсивных исследований металлорганической химии. С момента опубликования работ Монда (Mond), а затем Хибера (Hieber), было разработано множество методов синтеза как моноядерных карбонилов металлов, так и гомо- и гетерометаллических карбонильных кластеров[3].
Прямое взаимодействие металла с оксидом углерода[править | править код]
Тетракарбонил никеля и пентакарбонил железа могут быть получены согласно следующим уравнениям реакций при взаимодействии тонкодисперсного металла с монооксидом углерода:[50]
- , (1 bar, 55 °C)
- , (100 bar, 175 °C)
Никель реагирует с монооксидом углерода уже при 80 °C при атмосферном давлении, а тонко измельчённое железо реагирует при температурах 150—200 °C и давлении монооксида углерода от 50 до 200 Бар[11]. Карбонилы других металлов получают более сложным путём.
Восстановление солей металлов и их оксидов[править | править код]
Карбонилы некоторых металлов получают путём восстановления галогенидов металлов в присутствии моноокисида углерода под высоким давлением. Могут использоваться разнообразные восстановители, в том числе медь, алюминий, водород, а также алкилы металлов, например, триэтилалюминий. Показательным является образование гексакарбонила хрома из безводного хлорида хрома (III) в бензоле с алюминием в качестве восстанавливающего агента и хлоридом алюминия в качестве катализатора:[50]
Использование алкилов металлов, например триэтилалюминия и диэтилцинка в качестве восстановителей приводит к окислительному сочетанию алкильных радикалов в димеры:
Соли вольфрама, молибдена, марганца и родия могут быть восстановлены с помощью литийалюминийгидрида. Гексакарбонилванадий получают используя натрий в качестве восстанавливающего агента в хелатирующих растворителях, например — диглиме[30].
В водной среде соли никеля или кобальта могут быть восстановлены, например, с помощью дитионита натрия. В присутствии CO соли кобальта количественно превращаются в тетракарбонилкобальт-анион:[30]
Некоторые карбонилы металлов получают используя CO в качестве восстановителя. Именно таким путём Хибер (англ. Hieber) и Фукс (англ. Fuchs) впервые получили декакарбонилдирений из оксида рения:[51]
Если используются оксиды металлов, то, в качестве продукта реакции, образуется диоксид углерода. При восстановлении хлоридов металлов монооксидом углерода образуется фосген, как, например, при получении хлорида карбонил-осмия из хлорида осмия[3]. CO также подходит для восстановления сульфидов металлов, тогда побочным продуктом является карбонилсульфид.
Фотолиз и термолиз[править | править код]
Фотолиз или термолиз моноядерных карбонилов приводит к образованию двух- и полядерных карбонилов, как, например, нонакарбонилдижелезо (Fe2(CO)9)[52][53]. При дальнейшем нагревании карбонил разлагается в конечном счёте на свободный металл и монооксид углерода.
Термическое разложение додекакарбонила триосмия (Os3(CO)12) приводит к образованию многоядерных осмий-карбонильных кластеров, как, например, Os4(CO)13, Os6(CO)18 и даже Os8(CO)23[30].
Смешанно-лигандные карбонилы рутения, осмия, родия и иридия часто образуются в результате поглощения СО из растворителей, например диметилформамида (ДМФ) и 2-метоксиэтанола. Характерным является синтез комплекса Л. Васка (Vaska’s Complex)) транс-IrCl(CO)(PPh3)2 в результате реакции хлорида иридия (III) с трифенилфосфином в кипящем ДМФ.
Метатезис солей[править | править код]
Реакция метатезиса солей, например, KCo(CO)4 с [Ru(CO)3Cl2]2, приводит к избирательному образованию смешанного карбонильного комплекса, в данном случае: RuCo2(CO)11[54].
Катионы карбонилов металлов и карбонилметаллаты[править | править код]
Синтез ионных карбонильных комплексов возможен посредством окисления или восстановления нейтральных комплексов. Анионные карбонилметаллаты металлов могут быть получены, например, путём восстановления биядерных комплексов натрием. Известным примером является натриевая соль тетракарбонилата железа (Na2Fe(CO)4, реагент Коллмана), который используется в органическом синтезе[55].
Катионные соли гексакарбонила марганца, технеция и рения могут быть получены из галогенидов соответствующих карбонилов под давлением монооксида углерода по реакции с кислотой Льюиса.
Использованием сильных кислот удалось получить катионы карбонила золота, например [Au(CO)2]+, который используется в качестве катализатора для карбонилирования олефинов[56]. Катионные комплексы карбонила платины [Pt(CO)4]+ могут быть получены обработкой суперкислотами, например пентафторидом сурьмы.
Химические свойства карбонилов[править | править код]
Карбонилы металлов — важные прекурсоры в синтезе других металлоорганических комплексов и соединений. Основные реакции это реакции замещения карбонильного лиганда другими лигандами, реакции окисления и восстановления металлического центра и реакции карбонильного лиганда
Замещение CO[править | править код]
Замещение СО-лигандов другими донорными лигандами может быть индуцировано термически или фотохимически. Перечень лигандов-заместителей велик и включает в себя фосфины, цианиды (CN-), азот-содержащие донорные лиганды, и даже простые эфиры, особенно хелатирующие (диоксан, ТГФ). Эффективными лигандами также являются олефины и, особенно, диолефины, которые образуют синтетически значимые производные. Замещение в 18-электронных комплексах в целом соответствует диссоциативному механизму с образованием 16-электронного интермедиата.
Замещение идет по диссоциативному механизму:
Энергия диссоциации составляет 105 кДж моль −1 для карбонила никеля и 155 кДж −1 для гексакарбонила хрома[1].
Редко встречающееся замещение в 17-электронных комплексах протекает по ассоциативному механизму с 19-электронным интермедиатом:
Процесс замещения в 18-электронных комплексах иногда катализируется небольшим количеством окислителя посредством передачи электрона[57].
Восстановление[править | править код]
Карбонилы металлов вступают в реакцию с восстановителями, такими как металлический натрий или амальгама натрия, образуя карбонилметаллат-анионы:
Пентакарбонил железа образует тетракарбонилферрат с потерей CO:
Ртуть может встраиваться по связи металл-металл в некоторых полиядерных карбонилах металлов:
Нуклеофильная атака по CO[править | править код]
Обычно CO-лиганд легко подвергается нуклеофильной атаке. Например, триметиламин оксид и калия бис-(триметилсилил)амид преобразуют СО-лиганд в CO2 и CN-, соответственно. В основной реакции Хибера (англ. Walter Hieber), гидроксид-ион атакует СО-лиганд с образованием металлокарбоксилата, с последующим выделением диоксида углерода и образованием гидрида металла или карбонилметаллата. Хорошо известным примером такого нуклеофильного присоединения является превращение пентакарбонила железа в H2Fe(CO)4:
Протонирование гидридоаниона даёт нейтральный тетракарбонил гидрид железа:
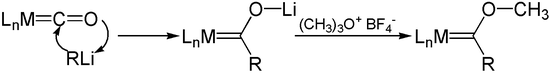
Добавление литийорганических реагентов к карбонилам металлов даёт ацилметаллические карбонильные анионы (комплексы Фишера). О — алкилирование этих анионов, например, солями Меервейна, даёт карбеновые комплексы переходных металлов (карбены Фишера).
С электрофилами[править | править код]
Несмотря на низкую формальную степень окисления, карбонилы металлов относительно инертны к действию многих электрофилов. Например, они устойчивы к действию алкилирующих агентов, слабых кислот, мягких окислителей. Большинство карбонилов металлов подвергается галогенированию. Пентакарбонил железа, например, образует карбонильные галогениды:
Галогены способны расщеплять связь металл-металл:
Разнообразие карбонилов и их химические формы[править | править код]
Большинство металл-карбонильных комплексов содержит смесь лигандов. Например исторически значимый комплекс Васка (транс-IrCl(CO)(PPh3)2) и антидетонационный агент метилциклопентадиенилтрикарбонил марганца (CH3C5H4)Mn(CO)3). Исходными соединениями для многих смешанных комплексов служат бинарные карбонилы, то есть отвечающие формуле [Mx(CO)n]z, многие из которых коммерчески доступны. Молекулярная формула многих карбонилов металлов может быть выведена исходя из 18-электронного правила.
Электронейтральные бинарные карбонилы металлов[править | править код]
- Карбонилы элементов 4 группы с 4 валентными электронами редки, но замещённые производные Ti(CO)7 известны.
- Карбонилы элементов 5 группы с 5 валентными электронами подвержены стерическим эффектам, которые препятствуют образованию М-М связей, как, например, в V2(CO)12, который неизвестен, хотя 17-электронный V(CO)6 известен и устойчив.
- Карбонилы элементов 6 группы с 6 валентными электронами образуют 18-электронные карбонильные комплексы Cr(CO)6, Mo(CO)6, W(CO)6. В металлорганическом синтезе для элементов 6 группы (как и для 7 группы) известен «цис эффект», заключающийся в лабилизации СО в цис-положении.
- Карбонилы элементов 7 группы с 7 валентными электронами образуют димеры карбонилов: Mn2(CO)10, Tc2(CO)10, и Re2(CO)10 (7 + 1 + 5 × 2 = 18 электронов).
- Карбонилы элементов 8 группы с 8 валентными электронами образуют карбонилы металлов
Fe(CO)5, Ru(CO)5 и Os(CO)5 (8 + 5 × 2 = 18 электронов). Последние два неустойчивы и склонны к декарбонилированию с образованием Ru3(CO)12, и Os3(CO)12. Так же известны два других карбонила железа: Fe2(CO)9 и Fe3(CO)12.
- Карбонилы элементов 9 группы с 9 валентными электронами, как и ожидается, образуют димеры карбонилов вида M2(CO)8. На практике устойчивыми оказываются только производные октакарбониладикобальта, но для всех трёх элементов 9 группы хорошо известны тетрамеры карбонилов: Co4(CO)12, додекакарбонил родия Rh4(CO)12, гексадекакарбонил родия Rh6(CO)16, и додекакарбонил иридия Ir4(CO)12 (9 + 3 + 3 × 2 = 18 электронов). В отличие от большинства 18-электронных карбонильных комплексов переходных металлов октакарбонилдикобальт Co2(CO)8 чувствителен к кислороду.
- Карбонилы элементов 10 группы с 10 валентными электронами образуют карбонилы вида Ni(CO)4 (10 + 4 × 2 = 18 электронов). Карбонилы Pd(CO)4 и Pt(CO)4 не являются стабильными.
Анионные биядерные карбонильные комплексы металлов[править | править код]
- Элементы 4 группы: дианионы карбонилов сходны с нейтральными производными карбонилов элементов 6 группы: [Ti(CO)6]2-[58].
- Элементы 5 группы: анионы сходны с нейтральными производными карбонилов элементов 6 группы: [Ti(CO)6]2-.
- Элементы 7 группы: моноанионы сходны с нейтральными производными карбонилов элементов 8 группы: [M(CO)5]- (M = Mn, Tc, Re).
- Элементы 8 группы: дианионы карбонилов сходны с нейтральными производными карбонилов элементов 10 группы: [M(CO)4]2- (M = Fe, Ru, Os). Конденсированные производные также известны.
- Элементы 9 группы: моноанионы карбонилов сходны с нейтральными производными карбонилов элементов 10 группы. Наиболее изученным является карбонил кобальта [Co(CO)4]-.
Также хорошо известны крупные анионные кластеры Ni, Pd и Pt.
Катионные карбонильные комплексы металлов[править | править код]
- Элементы 7 группы: монокатионы сходны с нейтральными производными карбонилов элементов 6 группы: [M(CO)6]+ (M = Mn, Tc, Re).
- Элементы 8 группы: бикатионы так же сходны с нейтральными производными карбонилов элементов 6 группы: [M(CO)6]2+ (M = Fe, Ru, Os)[59].
Гидриды карбонилов металлов[править | править код]
| Гидрид карбонила металла | pKa |
|---|---|
| HCo(CO)4 | «сильная» |
| HCo(CO)3(P(OPh)3) | 5.0 |
| HCo(CO)3(PPh3) | 7.0 |
| HMn(CO)5 | 7.1 |
| H2Fe(CO)4 | 4.4, 14 |
| [HCo(dmgH)2PBu3] | 10.5 |
Карбонилы металлов способны образовывать комплексы с отрицательными степенями окисления, как, например, анионы, описанные выше. Эти анионы могут быть протонированы с образованием соответствующих гидридов карбонильных комплексов металлов. Нейтральные гидриды карбонилов металлов обычно летучи и могут проявлять кислые свойства (псевдогалогены)[60].
Практическое применение[править | править код]

Карбонилы металлов используются в нескольких промышленных процессах. Возможно самым первым применением стало выделение и очистка никеля перегонкой его тетракарбонила (процесс Монда). Аналогично очень чистое порошковое железо получают термическим разложением пентакарбонила железа. Карбонил железа используется в частности для изготовления сердечников высокочастотных катушек индуктивности, красителей, диетических добавок[61], при производстве радиопоглощающих материалов для стелс-технологий[62] и для создания металлопокрытий термораспылением.
Карбонилы металлов — хорошие антидетонаторы моторного топлива, однако при их сгорании образуются трудноудаляемые оксиды. Некоторые карбонилы используются для получения очень чистого монооксида углерода.
Катализ[править | править код]
Карбонилы металлов используются в ряде промышленно важных реакций карбонилирования. В оксо (анг. oxo) процессе олефин, водород и монооксид углерода совместно взаимодействуют с катализатором (например, октакарбонилом дикобальта), образуя альдегиды. Например, в производстве масляного альдегида (бутираля):
Бутиральдегид преобразуется в промышленном масштабе в 2-этилгексанол, предшественник пластификаторов ПВХ, с помощью альдольной конденсации, с последующим гидрированием полученного гидроксиальдегида. Оксоальдегиды, полученные гидроформилированием, используются для крупномасштабного синтеза жирных спиртов, которые являются предшественниками моющих средств. Гидроформилирование является высокоэкономной реакцией, особенно если процесс протекает с высокой региоселективностью.
Другой важной реакцией, катализируемой карбонилами металлов, является гидрокарбоксилирование (реакция Реппе). Ниже приведен пример синтеза акриловой кислоты и сложных эфиров акриловой кислоты:
Также реакция циклизации ацетилена в циклооктатетраен осуществляется с использованием металл-карбонильных катализаторов:[63]
В процессах Монсанто (англ. Monsanto) и Кативы (англ. Cativa process), уксусную кислоту получают из метанола, моноокида углерода и воды с помощью родиевого и иридиевого карбонильного катализатора в присутствии йодоводорода. Родственные реакции карбонилирования дают уксусный ангидрид.
Медицина и лекарственные средства[править | править код]
CO-выделяющие молекулы (СО-ВМ; англ. CO-releasing molecules, CO-RMs) представляют собой карбонильные комплексы металлов, которые разрабатываются в качестве потенциальных CO-выделяющих препаратов. При низких концентрациях угарный газ функционирует как сосудорасширяющее и противовоспалительное средство. CO-ВМ задуманы как стратегический фармакологический метод транспорта и доставки контролируемых количеств CO к тканям и органам[64].
Гетеролигандные комплексы карбонилов[править | править код]
Многие карбонилы, как известно, образуют гомолептические и смешанные комплексы, которые являются производными или аналогичны карбонилам металлов.
Нитрозильные комплексы[править | править код]
Нитрозильные комплексы металлов, включающие молекулу NO в качестве лиганда, многочисленны, хотя гомолептические производные неизвестны. По сравнению с CO, NO является сильным акцептором, а изоцианиды лучшими донорами. Известные нитрозильные карбонилы включают CoNO(CO)3 и Fe(NO)2(CO)2[65]. Для нитрозильных комплексов так же известно два типа координации молекулы NO, в одном случае молекула линейна (резонансная структура NO+) и является донором трёх электронов, в другом имеет уголковое строение (резонансная структура NO-) и является донором одного электрона, тогда как молекула CO всегда является двухэлектронным донором. Как и CO, молекулы NO могут быть как терминальными, так и мостиковыми лигандами[66]. Некоторые водорастворимые нитрозильные комплексы могут использоваться в качестве NO-содержащих лекарственных препаратов, например, при терапии солидных раковых опухолей[67].
Тиокарбонильные комплексы[править | править код]
Комплексы, содержащие CS (моносероуглерод), известны, но редки[68][69]. Редкость таких комплексов отчасти обусловлена очевидной нестабильностью исходного соединения — моносульфида углерода. По этой причине синтез тиокарбонильных комплексов требует более сложных путей, как, например, взаимодействие тетракарбонилферрата натрия с тиофосгеном:
Комплексы, включающие CSe и CTe очень редки.
Фосфиновые комплексы[править | править код]
Все карбонилы металлов вступают в реакцию замещения карбонильных лигандов фосфорорганическими лигандами. Например, комплексы состава Fe(CO)5-x(PR3)x известны для х = 1, 2 и 3. PF3 ведёт себя аналогично, но примечателен способностью легко образовывать гомолептические аналоги биядерных карбонилов металлов. Например, летучие, устойчивые комплексы Fe(PF3)5 и Co2(PF3)8 представляют собой не содержащие CO аналоги Fe(CO)5 и Co2(CO)8 (не мостиковый изомер).
Изоцианидные комплексы[править | править код]
Изоцианиды также образуют обширные семейства смешанных комплексов с карбонилами металлов. Типичными изоцианидными лигандами являются метил- и трет-бутил изоцианид (Me3CNC). Особый случай представляет трифторметилизоцианид, нестабильные молекулы которого образуют устойчивые комплексы, физические и химические свойства которых весьма близко к поведению карбонилов металлов.
Токсикология[править | править код]
Все карбонилы являются ядовитыми веществами. Токсичность карбонилов металлов связана с токсичностью монооксида углерода и металла, и определяется летучестью и неустойчивостью комплексов. Попадание в организм происходит при вдыхании пыли или аэрозолей карбонилов, проглатывании жидких и твердых карбонилов, или при всасывании через кожу (ввиду хорошей растворимости карбонилов в жирах). Наибольший клинический опыт охватывает отравления карбонилом никеля и пентакарбонилом железа. Карбонил никеля считается одним из сильнейших ингаляционных ядов[70].
Вдыхание карбонила никеля вызывает острые неспецифические симптомы, сходные с отравлением угарным газом, в их числе тошнота, кашель, головные боли, лихорадка и головокружение. Через некоторое время появляются более тяжелые легочные симптомы — кашель, тахикардия, цианоз, или симптомы, связанные с желудочно-кишечным трактом. Кроме патологических изменений в легких, например, металлизации альвеол, наблюдаются повреждения мозга, печени, почек, надпочечников и селезёнки. Отравление карбонилами металлов обычно требует длительного периода восстановления организма[71]. Хроническое воздействие при вдыхании низких концентраций карбонила никеля может вызвать неврологические симптомы, такие как бессонница, головные боли, головокружение и потеря памяти[71]. Карбонил никеля считается канцерогеном, но может пройти от 20 до 30 лет от начала воздействия до клинических проявлений рака[72].
Литература[править | править код]
- Эльшенбройх К. Металлоорганическая химия. — М.: БИНОМ. Лаборатория знаний. — 2011. С. 324 — ISBN 978-5-9963-0203-1.
Примечания[править | править код]
- ↑ 1 2 3 4 5 Elschenbroich, C. Organometallics (неопр.). — Weinheim: Wiley-VCH, 2006. — ISBN 3-527-29390-6.
- ↑ Trout, W. E. Jr. The Metal Carbonyls. I. History; II. Preparation (англ.) // Journal of Chemical Education : journal. — 1937. — Vol. 14, no. 10. — P. 453. — doi:10.1021/ed014p453. — .
- ↑ 1 2 3 4 5 6 Herrmann, W. A. 100 Jahre Metallcarbonyle. Eine Zufallsentdeckung macht Geschichte (нем.) // Chemie in unserer Zeit : magazin. — 1988. — Bd. 22, Nr. 4. — S. 113—122. — doi:10.1002/ciuz.19880220402.
- ↑ Schützenberger, P. Mémoires sur quelques réactions domnant lieu à la production de l'oxychlorure de carbone, et sur nouveau composé volatil de platine (фр.) // Bulletin de la Société Chimique de Paris : magazine. — 1868. — Vol. 10. — P. 188—192. Архивировано 13 января 2016 года.
- ↑ Эльшенбройх К. Металлоорганическая химия. — М.: БИНОМ. Лаборатория знаний. — 2011. С. 11 — ISBN 978-5-9963-0203-1.
- ↑ Mond, L.; Langer, C.; Quincke, F. Action of Carbon Monoxide on Nickel (англ.) // Journal of the Chemical Society : journal. — Chemical Society, 1890. — Vol. 57. — P. 749—753. — doi:10.1039/CT8905700749.
- ↑ Gratzer, W. Eureka and Euphorias: The Oxford Book of Scientific Anecdotes (англ.) : journal. — Oxford University Press, 2002. — ISBN 0-19-280403-0.
- ↑ Mond, L.; Hirtz, H.; Cowap, M. D. Note on a Volatile Compound of Cobalt with Carbon Monoxide (англ.) // Chemical News : journal. — 1908. — Vol. 98. — P. 165—166.
- ↑ {{{заглавие}}} (неопр.) // Chemical Abstracts. — 1908. — Т. 2. — С. 3315.
- ↑ Dewar, J.; Jones, H. O. The Physical and Chemical Properties of Iron Carbonyl (англ.) // Proceedings of the Royal Society A: Mathematical, Physical and Engineering Sciences : journal. — 1905. — Vol. 76, no. 513. — P. 558—577. — doi:10.1098/rspa.1905.0063. — .
- ↑ 1 2 Mittasch, A. Über Eisencarbonyl und Carbonyleisen (нем.) // Angewandte Chemie : magazin. — 1928. — Bd. 41, Nr. 30. — S. 827—833. — doi:10.1002/ange.19280413002.
- ↑ 1 2 3 4 5 6 Эльшенбройх К. Металлоорганическая химия. — М.: БИНОМ. Лаборатория знаний. — 2011. С. 12 — ISBN 978-5-9963-0203-1.
- ↑ Highly-Reduced Metal Carbonyls — Beck — 2003 — Angewandte Chemie International Edition in English — Wiley Online Library. Дата обращения: 9 ноября 2014. Архивировано 29 ноября 2014 года.
- ↑ Basolo, F. From Coello to Inorganic Chemistry: A Lifetime of Reactions (англ.). — Springer, 2002. — P. 101. — ISBN 978-030-646774-5.
- ↑ Chemicals from Synthesis Gas: Catalytic Reactions of CO and H2 (англ.) / Sheldon, R. A.. — Kluwer, 1983. — Vol. 2. — P. 106. — ISBN 978-9027714893.
- ↑ Эльшенбройх К. Металлоорганическая химия. — М.: БИНОМ. Лаборатория знаний. — 2011. С. 13 — ISBN 978-5-9963-0203-1.
- ↑ Hoffmann, R. Building Bridges between Inorganic and Organic Chemistry. Nobelprize.org (8 декабря 1981). Дата обращения: 9 ноября 2014. Архивировано 9 ноября 2014 года.
- ↑ Эльшенбройх К. Металлоорганическая химия. — М.: БИНОМ. Лаборатория знаний. — 2011. С. 14 — ISBN 978-5-9963-0203-1.
- ↑ Tard, C; Pickett, C. J. Structural and Functional Analogues of the Active Sites of the [Fe]-, [NiFe]-, and [FeFe]-Hydrogenases (англ.) // Chemical Reviews : journal. — 2009. — Vol. 109, no. 6. — P. 2245—2274. — doi:10.1021/cr800542q. — PMID 19438209.
- ↑ 1 2 Arnold F. Holleman, Nils Wiberg: Lehrbuch der Anorganischen Chemie. 102., stark umgearb. u. verb. Auflage. de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, p. 1780.
- ↑ F. Albert Cotton: Proposed nomenclature for olefin-metal and other organometallic complexes. In: Journal of the American Chemical Society. 90, 1968, S. 6230-6232, doi:10.1021/ja01024a059.
- ↑ Dyson, P. J.; McIndoe, J. S. Transition Metal Carbonyl Cluster Chemistry (англ.). — Amsterdam: Gordon & Breach, 2000. — ISBN 90-5699-289-9.
- ↑ Эльшенбройх К. Металлоорганическая химия. — М.: БИНОМ. Лаборатория знаний. — 2011. С. 331 — ISBN 978-5-9963-0203-1.
- ↑ Эльшенбройх К. Металлоорганическая химия. — М.: БИНОМ. Лаборатория знаний. — 2011. С. 324 — ISBN 978-5-9963-0203-1.
- ↑ И.А.Шека, К. Ф. Карлышева. Разделение циркония и гафния в виде карбонилов 2г (СО), и ... - Справочник химика 21. Химия гафния. chem21.info (1972). Дата обращения: 16 июля 2018.
- ↑ Allian, A. D.; Wang, Y.; Saeys, M.; Kuramshina, G. M.; Garland, M. The Combination of Deconvolution and Density Functional Theory for the Mid-Infrared Vibrational Spectra of Stable and Unstable Rhodium Carbonyl Clusters (англ.) // Vibrational Spectroscopy : journal. — 2006. — Vol. 41, no. 1. — P. 101—111. — doi:10.1016/j.vibspec.2006.01.013.
- ↑ Spessard, G. O.; Miessler, G. L. Organometallic Chemistry (англ.). — 2nd. — New York: Oxford University Press, 2010. — P. 79—82. — ISBN 978-0-19-533099-1.
- ↑ Sargent, A. L.; Hall, M. B. Linear Semibridging Carbonyls. 2. Heterobimetallic Complexes Containing a Coordinatively Unsaturated Late Transition Metal Center (англ.) // Journal of the American Chemical Society : journal. — 1989. — Vol. 111, no. 5. — P. 1563—1569. — doi:10.1021/ja00187a005.
- ↑ Li, P.; Curtis, M. D. A New Coordination Mode for Carbon Monoxide. Synthesis and Structure of Cp4Mo2Ni2S2(η1, μ4-CO) (англ.) // Journal of the American Chemical Society : journal. — 1989. — Vol. 111, no. 21. — P. 8279—8280. — doi:10.1021/ja00203a040.
- ↑ 1 2 3 4 Holleman, A. F.; Wiberg, E.; Wiberg, N. Lehrbuch der Anorganischen Chemie (неопр.). — 102nd. — Berlin: de Gruyter, 2007. — С. 1780—1822. — ISBN 978-3-11-017770-1.
- ↑ 1 2 Londergan, C. H.; Kubiak, C. P. Electron Transfer and Dynamic Infrared-Band Coalescence: It Looks like Dynamic NMR spectroscopy, but a Billion Times Faster (англ.) // Chemistry - A European Journal : journal. — 2003. — Vol. 9, no. 24. — P. 5962—5969. — doi:10.1002/chem.200305028.
- ↑ Miessler, G. L.; Tarr, D. A. Inorganic Chemistry (неопр.). — Upper Saddle River, NJ: Pearson Prentice Hall, 2011. — С. 109—119; 534—538.
- ↑ 1 2 Braterman, P. S. Metal Carbonyl Spectra (неопр.). — Academic Press, 1975.
- ↑ Crabtree, R. H. 4. Carbonyls, Phosphine Complexes, and Ligand Substitution Reactions // The Organometallic Chemistry of the Transition Metals (англ.). — 4th. — 2005. — P. 87—124. — doi:10.1002/0471718769.ch4.
- ↑ Tolman, C. A. Steric effects of Phosphorus Ligands in Organometallic Chemistry and Homogeneous Catalysis (англ.) // Chemical Reviews : journal. — 1977. — Vol. 77, no. 3. — P. 313—348. — doi:10.1021/cr60307a002.
- ↑ Cotton, F. A. Chemical Applications of Group Theory (неопр.). — 3rd. — Wiley Interscience, 1990. — ISBN 978-0-471-51094-9.
- ↑ Carter, R. L. Molecular Symmetry and Group Theory (неопр.). — Wiley, 1997. — ISBN 978-0-471-14955-2.
- ↑ Harris, D. C.; Bertolucci, M. D. Symmetry and Spectroscopy: Introduction to Vibrational and Electronic Spectroscopy (англ.). — Oxford University Press, 1980. — ISBN 978-0-19-855152-2.
- ↑ Riedel, E.; Alsfasser, R.; Janiak, C.; Klapötke, T. M. Moderne Anorganische Chemie (неопр.). — de Gruyter, 2007. — ISBN 3-11-019060-5.
- ↑ Henderson, W.; McIndoe, J. S. Mass Spectrometry of Inorganic, Coordination and Organometallic Compounds: Tools – Techniques – Tips (англ.). — John Wiley & Sons. — ISBN 0-470-85015-9.
- ↑ Butcher, C. P. G.; Dyson, P. J.; Johnson, B. F. G.; Khimyak, T.; McIndoe, J. S. Fragmentation of Transition Metal Carbonyl Cluster Anions: Structural Insights from Mass Spectrometry (англ.) // Chemistry - A European Journal : journal. — 2003. — Vol. 9, no. 4. — P. 944—950. — doi:10.1002/chem.200390116. — PMID 12584710.
- ↑ Vásquez, G. B.; Ji, X.; Fronticelli, C.; Gilliland, G. L. Human Carboxyhemoglobin at 2.2 Å Resolution: Structure and Solvent Comparisons of R-State, R2-State and T-State Hemoglobins (англ.) // Acta Crystallographica D : journal. — International Union of Crystallography, 1998. — Vol. 54, no. 3. — P. 355—366. — doi:10.1107/S0907444997012250.
- ↑ Эльшенбройх К. Металлоорганическая химия. — М.: БИНОМ. Лаборатория знаний. — 2011. С. 330—331 — ISBN 978-5-9963-0203-1.
- ↑ Tielens, A. G.; Wooden, D. H.; Allamandola, L. J.; Bregman, J.; Witteborn, F. C. The Infrared Spectrum of the Galactic Center and the Composition of Interstellar Dust (англ.) // The Astrophysical Journal : journal. — IOP Publishing, 1996. — Vol. 461, no. 1. — P. 210—222. — doi:10.1086/177049. — . — PMID 11539170. Архивировано 21 января 2022 года.
- ↑ Xu, Y.; Xiao, X.; Sun, S.; Ouyang, Z. IR Spectroscopic Evidence of Metal Carbonyl Clusters in the Jiange H5 Chondrite (англ.) // Lunar and Planetary Science : journal. — 1996. — Vol. 26. — P. 1457—1458. — . Архивировано 14 июля 2014 года.
- ↑ Cody, G. D.; Boctor, N. Z.; Filley, T. R.; Hazen, R. M.; Scott, J. H.; Sharma, A.; Yoder, H. S. Jr. Primordial Carbonylated Iron-Sulfur Compounds and the Synthesis of Pyruvate (англ.) // Science : journal. — 2000. — Vol. 289, no. 5483. — P. 1337—1340. — doi:10.1126/science.289.5483.1337. — . — PMID 10958777.
- ↑ Feldmann, J. Determination of Ni(CO)4, Fe(CO)5, Mo(CO)6, and W(CO)6 in Sewage Gas by using Cryotrapping Gas Chromatography Inductively Coupled Plasma Mass Spectrometry (англ.) // Journal of Environmental Monitoring : journal. — 1999. — Vol. 1, no. 1. — P. 33—37. — doi:10.1039/A807277I. — PMID 11529076.
- ↑ Bioorganometallics: Biomolecules, Labeling, Medicine (англ.) / Jaouen, G.. — Weinheim: Wiley-VCH, 2006. — ISBN 3-527-30990-X.
- ↑ Boczkowski, J.; Poderoso, J. J.; Motterlini, R. CO–Metal Interaction: Vital Signaling from a Lethal Gas (англ.) // Trends in Biochemical Sciences : journal. — Cell Press, 2006. — Vol. 31, no. 11. — P. 614—621. — doi:10.1016/j.tibs.2006.09.001. — PMID 16996273.
- ↑ 1 2 Huheey, J.; Keiter, E.; Keiter, R. Metallcarbonyle // Anorganische Chemie (неопр.). — 2nd. — Berlin / New York: de Gruyter, 1995.
- ↑ Hieber, W.; Fuchs, H. Über Metallcarbonyle. XXXVIII. Über Rheniumpentacarbonyl (англ.) // Zeitschrift für Anorganische und Allgemeine Chemie : journal. — 1941. — Vol. 248, no. 3. — P. 256—268. — doi:10.1002/zaac.19412480304.
- ↑ King, R. B. Organometallic Syntheses (неопр.). — New York: Academic Press, 1965. — Т. 1: Transition-Metal Compounds. — ISBN 0-444-42607-8.
- ↑ Braye, E. H.; Hübel, W.; Rausch, M. D.; Wallace, T. M. Diiron Enneacarbonyl (англ.) // Inorganic Syntheses : journal. — 1966. — Vol. 8. — P. 178—181. — ISBN 978-0-470-13239-5. — doi:10.1002/9780470132395.ch46.
- ↑ Roland, E.; Vahrenkamp, H. Zwei neue Metallcarbonyle: Darstellung und Struktur von RuCo2(CO)11 und Ru2Co2(CO)13 (эст.) // Chemische Berichte. — 1985. — K. 118, nr. 3. — L. 1133—1142. — doi:10.1002/cber.19851180330.
- ↑ Pike, R. D. (2001). "Disodium Tetracarbonylferrate(-II)". Encyclopedia of Reagents for Organic Synthesis. doi:10.1002/047084289X.rd465.
- ↑ Xu, Q.; Imamura, Y.; Fujiwara, M.; Souma, Y. A New Gold Catalyst: Formation of Gold(I) Carbonyl, [Au(CO)n]+ (n = 1, 2), in Sulfuric Acid and Its Application to Carbonylation of Olefins (англ.) // Journal of Organic Chemistry : journal. — 1997. — Vol. 62, no. 6. — P. 1594—1598. — doi:10.1021/jo9620122.
- ↑ Ohst, H. H.; Kochi, J. K. Electron-Transfer Catalysis of Ligand Substitution in Triiron Clusters (англ.) // Journal of the American Chemical Society : journal. — 1986. — Vol. 108, no. 11. — P. 2897—2908. — doi:10.1021/ja00271a019.
- ↑ Ellis, J. E. Metal Carbonyl Anions: from [Fe(CO)4]2- to [Hf(CO)6]2- and Beyond (англ.) // Organometallics : journal. — 2003. — Vol. 22, no. 17. — P. 3322—3338. — doi:10.1021/om030105l.
- ↑ Finze, M.; Bernhardt, E.; Willner, H.; Lehmann, C. W.; Aubke, F. Homoleptic, σ-Bonded Octahedral Superelectrophilic Metal Carbonyl Cations of Iron(II), Ruthenium(II), and Osmium(II). Part 2: Syntheses and Characterizations of [M(CO)6][BF4]2 (M = Fe, Ru, Os) (англ.) // Inorganic chemistry : journal. — 2005. — Vol. 44, no. 12. — P. 4206—4214. — doi:10.1021/ic0482483. — PMID 15934749.
- ↑ Pearson, R. G. The Transition-Metal-Hydrogen Bond (англ.) // Chemical Reviews : journal. — 1995. — Vol. 85, no. 1. — P. 41—49. — doi:10.1021/cr00065a002.
- ↑ Fairweather-Tait, S. J.; Teucher, B. Iron and Calcium Bioavailability of Fortified Foods and Dietary Supplements (англ.) // Nutrition Reviews : journal. — 2002. — Vol. 60, no. 11. — P. 360—367. — doi:10.1301/00296640260385801.
- ↑ Richardson, D. Stealth-Kampfflugzeuge: Täuschen und Tarnen in der Luft (нем.). — Zürich: Dietikon, 2002. — ISBN 3-7276-7096-7.
- ↑ Wilke, G. Organo Transition Metal Compounds as Intermediates in Homogeneous Catalytic Reactions (англ.) // Pure and Applied Chemistry : journal. — 1978. — Vol. 50, no. 8. — P. 677—690. — doi:10.1351/pac197850080677. Архивировано 4 марта 2016 года.
- ↑ Roberto Motterlini and Leo Otterbein «The therapeutic potential of carbon monoxide» Nature Review Drug Discovery 2010, vol. 9, pp. 728-43. {{doi: 10.1038/nrd3228}}.
- ↑ Hayton, T. W.; Legzdins, P.; Sharp, W. B. Coordination and Organometallic Chemistry of Metal−NO Complexes (англ.) // Chemical Reviews : journal. — 2002. — Vol. 102, no. 4. — P. 935—992. — doi:10.1021/cr000074t. — PMID 11942784.
- ↑ Эльшенбройх К. Металлоорганическая химия. — М.: БИНОМ. Лаборатория знаний. — 2011. — ISBN 978-5-9963-0203-1
- ↑ Архивированная копия. Дата обращения: 9 ноября 2014. Архивировано 9 ноября 2014 года.
- ↑ Petz, W. 40 Years of Transition-Metal Thiocarbonyl Chemistry and the Related CSe and CTe Compounds (англ.) // Coordination Chemistry Reviews : journal. — 2008. — Vol. 252, no. 15—17. — P. 1689—1733. — doi:10.1016/j.ccr.2007.12.011.
- ↑ Hill, A. F.; Wilton-Ely, J. D. E. T. Chlorothiocarbonyl-bis(triphenylphosphine) iridium(I) [IrCl(CS)(PPh3)2] (англ.) // Inorganic Syntheses : journal. — 2002. — Vol. 33. — P. 244—245. — ISBN 0-471-20825-6. — doi:10.1002/0471224502.ch4.
- ↑ Madea, B. Rechtsmedizin. Befunderhebung - Rekonstruktion – Begutachtung (нем.). — Springer-Verlag, 2003. — ISBN 3-540-43885-8.
- ↑ 1 2 Stellman, J. M. Encyclopaedia of Occupational Health and Safety (англ.). — International Labour Org, 1998. — ISBN 91-630-5495-7.
- ↑ Mehrtens, G.; Reichenbach, M.; Höffler, D.; Mollowitz, G. G. Der Unfallmann: Begutachtung der Folgen von Arbeitsunfällen, privaten Unfällen und Berufskrankheiten (нем.). — Berlin / Heidelberg: Springer, 1998. — ISBN 3-540-63538-6.
![{\displaystyle {\mathsf {Fe(CO)_{5}+OH^{-}\rightarrow H[Fe(CO)_{4}]^{-}+CO_{3}^{2-}+H_{2}O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/cf7e6fd7f4df051ff7168f9c3dd7a74c30a6b5c5)







![{\displaystyle {\mathsf {L_{n}M(CO)+RO^{-}\rightarrow [L_{n}M{\text{-}}C({\text{=}}O)OR]^{-}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b7b4d9c0572c70cc80a377a985ffcfe21aff7cf6)




![{\displaystyle {\mathsf {VCl_{3}+4Na+6CO+2diglyme\rightarrow Na(diglyme)_{2}[V(CO)_{6}]+3NaCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7efe640c13eeece770bafce777286a3f6c90f882)
![{\displaystyle {\mathsf {[V(CO)_{6}]^{-}+H^{+}\rightarrow H[V(CO)_{6}]\rightarrow {\frac {1}{2}}H_{2}+V(CO)_{6}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1ef52e48f53b800b1f34ec8f74c28c5fb94795d5)
![{\displaystyle {\mathsf {Co^{2+}+1,5S_{2}O_{4}^{2-}+6OH^{-}+4CO\rightarrow [Co(CO)_{4}]^{-}+3SO_{3}^{2-}+3H_{2}O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c800f563a97f42647c9692e9d17a06472d43c31f)


![{\displaystyle {\mathsf {KCo(CO)_{4}+[Ru(CO)_{3}Cl_{2}]_{2}\rightarrow 2RuCo_{2}(CO)_{11}+4KCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/cae051d8a4b7a9655fb72ae5da51872b4e03f06c)
![{\displaystyle {\mathsf {Mn(CO)_{5}Cl+AlCl_{3}+CO\rightarrow [Mn(CO)_{6}]^{+}[AlCl_{4}^{-}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1a393d080cb14986b24ac6e44019d20b6687250b)




![{\displaystyle {\mathsf {Mn_{2}(CO)_{10}+2Na\rightarrow 2Na[Mn(CO)_{5}]^{-}+D}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/21502ce91218d4b348521fbdd7807e77f92d98d8)


![{\displaystyle {\mathsf {Fe(CO)_{5}+NaOH\rightarrow Na[Fe(CO)_{4}COOH]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7506a44d7ad796808a4f3d7211b882d57c2a20ff)
![{\displaystyle {\mathsf {Na[Fe(CO)_{4}COOH]+NaOH\rightarrow Na[HFe(CO)_{4}]+NaHCO_{3}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c2073f8c2e0c95139c1b51cb570c5987075131fb)
![{\displaystyle {\mathsf {Na[HFe(CO)_{4}]+H^{+}\rightarrow H_{2}Fe(CO)_{4}+Na^{+}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a61006986f977adee34b1ca0e3ee6be74ccf7044)







