Реакция Дильса — Альдера

Реакция Ди́льса — А́льдера (диеновый синтез) — реакция [4+2]-циклоприсоединения диенофилов и сопряжённых диенов с образованием шестичленного цикла.
В реакцию вступают циклические и ациклические сопряжённые диены, енины −C=C−C≡C− или их гетероаналоги — соединения с фрагментами −С=С−С=О, −С=С−С≡N. Диенофилами обычно являются алкены и алкины с кратной связью, активированной электроноакцепторными заместителями. В роли диенофилов также могут выступать соединения, содержащие двойные связи с гетероатомом, например >С=О, >С=N−, −СN, −N=О, −S=O, −N=N−[1].
История[править | править код]
В 1902 году в лаборатории И. Тиле аспирантом В. Альбрехтом была проведена реакция между циклопентадиеном и бензохиноном с целью получения сопряжённого полиена, однако вместо ожидаемого продукта конденсации было получено два дикетона — продукты присоединения одной или двух молекул циклопентадиена по двойным связям хинона. Строение полученных веществ не было установлено, а реакция не получила дальнейшего развития в этой лаборатории[2].
Также протекание реакции Дильса — Альдера наблюдали в 1910 году С. В. Лебедев (при димеризации изопрена), а в 1920 году — Г. фон Эйлер и К. Джозефсон (при взаимодействии изопрена с бензохиноном)[2].
Систематическое изучение реакции между 1,3-диенами и сопряжёнными кетонами было представлено Отто Дильсом и Куртом Альдером в 1928 году в журнале Justus Liebigs Annalen der Chemie. Авторы статьи привели свидетельства общего характера реакции, а также с уверенностью указали на возможность её использования в синтезе природных соединений, при этом заявив[2]:
Мы со всей определённостью оставляем за собой права на использование открытой нами реакции для решения этих синтетических проблем.
В следующие за открытием годы были изучены основные закономерности протекания реакции и показана широкая область её применимости, а авторы открытия в 1950 году были удостоены Нобелевской премии по химии[2].
Механизм[править | править код]
Реакция Дильса — Альдера представляет собой согласованное [4+2]-циклоприсоединение, протекающее между 1,3-диеном и ненасыщенным соединением — диенофилом. Обычно диен содержит электронодонорный заместитель, а диенофил — электроноакцепторную группу. Менее распространён обращённый вариант, когда электронообогащённым соединением является диенофил[3].
С точки зрения теории граничных орбиталей, реакцию можно представить как взаимодействие высшей занятой молекулярной орбитали (ВЗМО) электронодонорного диена и низшей свободной молекулярной орбитали (НСМО) диенофила. В случае обращённого варианта взаимодействуют НСМО диена и ВЗМО диенофила. По этой причине изменение заместителей в реагентах противоположным образом влияет на протекание классического и обращённого вариантов реакции. Например, классическая реакция Дильса — Альдера ускоряется при увеличении донорной способности диена, а обращённая, напротив, замедляется[3].
Активность реагентов[править | править код]
Диены[править | править код]

Для участия в реакции [4+2]-циклоприсоединения диен принимает плоскую s-цис-конформацию, в которой обе двойные связи находятся по одну сторону от одинарной C–C-связи[4].
Одним из наиболее активных диенов является циклопентадиен-1,3, в котором s-цис конформация закреплена. В случае бутадиена-1,3 скорость реакции заметно ниже, поскольку он существует в виде двух ротамеров (s-цис и s-транс). Однако энергия перехода между этими конформациями невелика, поэтому бутадиен может быть использован как диенофил в реакции Дильса — Альдера. 1-Алкилзамещённые диены вступают в реакцию с различной скоростью в зависимости от конфигурации двойной связи. Так, E-пиперилен достаточно активно реагирует с малеиновым ангидридом, тогда как для Z-изомера выход составляет лишь 4 % (через 24 часа при 100 °C). Подобное поведение объясняется невыгодностью s-цис-конформации для Z-пиперилена. В случае диенов, которые существуют в закреплённой s-транс-конформации, реакция Дильса — Альдера становится невозможной. Например, в отличие от активного α-фелландрена, β-фелландрен вовсе не вступает в циклоприсоединение с малеиновым ангидридом[4].

Диенофилы[править | править код]
Наиболее активными диенофилами являются алкены и алкины с электроноакцепторными заместителями (α,β-непредельные альдегиды, кетоны, карбоновые кислоты и их производные, винилсульфоны, нитроалкены). С увеличением числа акцепторных групп происходит увеличение активности диенофила. Так, в реакции с циклопентадиеном 1,1-дицианэтилен в 4,5·104 раз более активен, чем акрилонитрил (моноцианэтилен). Тетрацианэтилен ещё более активен и поэтому часто используется на практике в качестве «ловушки» генерируемых in situ молекул с 1,3-диеновым фрагментом[4].
Часто в качестве диенофилов используются дизамещённые алкены и алкины, например, малеиновая кислота, её эфиры, ацетилендикарбоновая кислота, п-бензохинон и другие соединения. В реакцию Дильса — Альдера вводят также непредельные углеводороды, хоть они и гораздо менее активны и реагируют только при нагревании. В частности, реакции этилена и ацетилена с циклопентадиеном могут применяться для синтеза норборнена и норборнадиена[4].

Для синтеза бензаннелированных соединений в качестве диенофила применяется дегидробензол, получаемый in situ из о-бромфторбензола под действием магния или диазотированием антраниловой кислоты[4].
Региоселективность реакции[править | править код]
При введении в реакцию Дильса — Альдера несимметричных реагентов наблюдается региоселективное образование продуктов циклоприсоединения. Так, при реакции 1-замещённых диенов с несимметричными алкенами преимущественно образуются продукты, в которых заместители расположены у соседних атомов углерода (так называемые «орто»-продукты), а продукты с 1,3-замещением («мета»-продукты) получаются в меньшем количестве. Эта закономерность наблюдается для ряда заместителей в молекуле диена, а также различных диенофилов. Для её объяснения можно рассматривать возникающее под действием заместителей распределение зарядов в молекулах реагентов. Согласно такой модели, избирательность реакции должна возрастать с увеличением донорной способности заместителя в диене и акцепторной способности заместителя в диенофиле[5].

В реакциях 2-замещённых диенов общей закономерностью является образование «пара»-продуктов, которое также может быть объяснено на основании поляризации реагентов[5].
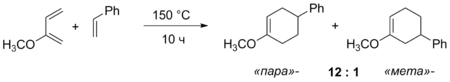
В случае дизамещённых и полизамещённых диенов ситуация усложняется и реакции протекают менее селективно и предсказуемо[5].
Стереохимия реакции[править | править код]
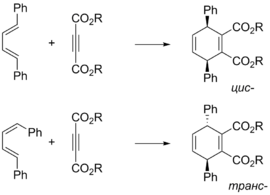
Поскольку реакция Дильса — Альдера протекает как согласованный процесс через циклическое переходное состояние, конфигурация продукта реакции определяется конфигурацией исходных реагентов. Так, из (Z)-алкенов образуются цис-продукты, а из (E)-алкенов — транс-продукты[5]. Подобный принцип применим и для заместителей в 1 и 4 положениях диена: если конфигурации двух двойных связей диена совпадают, то в продукте эти заместители находятся в цис-расположении[6].

|
|
Было замечено, что при реакции циклических диенов с различными диенофилами образуется, в основном, один из двух возможных диастереомеров с эндо-расположением заместителей диенофила. Соотношение эндо- и экзо-изомеров может принимать различные значения (от 3:2 до 20:1). Данная закономерность называется эндо-правилом Альдера. Эндо-правило выполняется и для реакций с участием ациклических 1,4-дизамещённых диенов. Наблюдаемые результаты объясняются вторичными орбитальными взаимодействиями, которые возникают при сближении акцепторной группы диенофила с С2- и С3-атомами диена. Данные взаимодействия стабилизируют переходное состояние и способствуют образованию эндо-продукта[5].

Катализ кислотами Льюиса[править | править код]
Долгое время считалось, что на реакцию не действуют какие-либо катализаторы, однако в 1960 году было показано, что реакция между антраценом и малеиновым ангидридом значительно ускоряется в присутствии хлорида алюминия AlCl3. В присутствии катализатора она протекает мгновенно при комнатной температуре, тогда как в некаталитическом варианте требуется кипячение в ксилоле (140 °C) в течение 72 часов. Кроме того, применение катализатора повышает региоселективность реакции и соотношение эндо- и экзо-изомеров[7].

Действие кислот Льюиса как катализаторов объясняется их способностью образовывать комплексы с диенофилами, за счёт чего происходит понижение энергии НСМО диенофила и уменьшение разницы энергий взаимодействующих НСМО диенофила и ВЗМО диена. Данный факт приводит к резкому увеличению скорости реакции. Влияние катализатора на селективность реакции наблюдается из-за изменения величин орбитальных коэффициентов в диенофиле и возрастающего различия в силе орбитальных взаимодействий при реализации альтернативных переходных состояний, приводящих к изомерным продуктам[7].
Благодаря своим преимуществам, каталитическая реакция Дильса — Альдера широко используется в лабораторном синтезе различных органических соединений[7].
Стереоселективная реакция Дильса — Альдера[править | править код]
Первые исследования стереоселективных вариантов реакции Дильса — Альдера были основаны на использовании хиральных диенофилов, в частности, сложных эфиров непредельных карбоновых кислот с хиральными спиртами. При этом было обнаружено, что на стереоселективность реакции сильно влияют условия её проведения. Например, реакция между бутадиеном и (–)-диметилфумаратом при нагревании протекала с низкой стереоселективностью, а использование катализатора AlCl3 приводило к получению продукта с оптической чистотой 72—76 %[8].
Продуктивным подходом в данной области оказалось использование оксазолидиновой методологии Эванса, в рамках которой в качестве диенофилов выступали α,β-ненасыщенные N-ацилоксазолидиноны. Согласно предложенной модели, данные реагенты образуют хелаты с кислотой Льюиса ((C2H5)2AlCl), в которых одна из сторон пространственно блокируется заместителем в оксазолидиноне, что и определяет стереоселективность реакции. Кроме того, получаемые продукты можно разлагать с регенерацией оксазолидиноновых фрагментов. Этот и подобные подходы, в которых диены и диенофилы содержали удаляемые вспомогательные хиральные группы, были использованы в синтезе многих природных соединений[8].

Позже была показана эффективность использования хиральных кислот Льюиса в качестве асимметрических индукторов. Одним из эффективных катализаторов оказался (R,R)-дихлор-2-нафтилциклогексилборан. Его применение в реакции циклопентадиена и метиловых эфиров акриловой, кротоновой или фумаровой кислот приводит к продукту с энантиомерным избытком 86—97 %. Широкое исследование было посвящено использованию хиральных оксазоборолидинов, синтезируемых из природных аминокислот[8].
В биохимии[править | править код]
Реакции [4+2]-циклоприсоединения встречаются во вторичном метаболизме разнообразных организмов. Протекающие в живой природе реакции Дильса — Альдера относятся к процессам биосинтеза поликетидов, изопреноидов, фенилпропаноидов, а также алкалоидов и других продуктов смешанного биосинтеза. Катализирующие эти реакции ферменты — дильсальдеразы — представляют собой белки или РНК. Возможность ферментативного катализа для реакций этого типа представляется весьма интригующим аспектом, так как высокое сходство структуры переходного состояния и продукта реакции (аддукта) предполагает конкурентное ингибирование последним специфического фермента, катализирующего реакцию. И действительно, полученные моноклональные антитела, проявляющие высокоспецифичную дильсальдеразную активность, как и ожидалось, ингибируются продуктом реакции. Катализ же рибозимами низкоспецифичен, необходимой частью активного рибозима является координированный ион переходного металла, поэтому считается, что катализ рибонуклеиновой кислотой подобен катализу кислотой Льюиса. Предполагается, что изучение биосинтетических реакций Дильса — Альдера может привести к открытию новых механизмов ферментативного катализа. Возможно, вступающие в реакцию диеновый компонент и диенофил дестабилизируются деформациями кручения, что способствует понижению энергии активации и эффективному протеканию реакции в физиологических условиях[9].
В настоящее время дильсальдеразы представляют большой интерес и активно изучаются.
Применение[править | править код]
Реакция используется для получения полициклических соединений, в том числе стероидов. С помощью реакции, также возможно получение многих хлорорганических пестицидов циклодиенового ряда: альдрина и его производных, гептахлора, нонахлора, хлордана, мирекса и т.д. [10].
См.также[править | править код]
Примечания[править | править код]
- ↑ Химическая энциклопедия. В пяти томах / Гл. ред. И. Л. Кнунянц. — Советская энциклопедия, 1990. — Т. 2. — С. 54—55. — ISBN 5-85270-035-5.
- ↑ 1 2 3 4 Смит, Дильман, часть 1, 2009, с. 605—607.
- ↑ 1 2 Смит, Дильман, часть 1, 2009, с. 607—609.
- ↑ 1 2 3 4 5 Смит, Дильман, часть 1, 2009, с. 609—612.
- ↑ 1 2 3 4 5 Смит, Дильман, часть 1, 2009, с. 612—618.
- ↑ Зауэр Е. Механизм реакции Дильса — Альдера // Успехи химии. — 1969. — Т. 38, № 4. — С. 624—661.
- ↑ 1 2 3 Смит, Дильман, часть 1, 2009, с. 618—621.
- ↑ 1 2 3 Смит, Дильман, часть 1, 2009, с. 621—631.
- ↑ Emily M. Stocking and Robert M. Williams. Chemistry and biology of biosynthetic Diels–Alder reactions. (Review) (англ.) // Angewandte Chemie International Edition : Научный журнал. — 2003. — Vol. 42, no. 27. — P. 3078—3115. — doi:10.1002/anie.200200534. — PMID 12866094.
- ↑ Вредные вещества в промышленности. Справочник для химиков, инженеров и врачей. Изд. 7-е, пер. и доп. В трех томах. Том I. Органические вещества. Под ред. засл. деят. науки проф. Н. В. Лазарева и докт. мед. наук Э. Н. Левиной. Л., «Химия», 1976. 592 стр., 27 табл., библиография —1850 названий.
Литература[править | править код]
- Оригинальные работы
- Diels O, Alder K. Synthesen in der hydroaromatischen Reihe (нем.) // Justus Liebigs Annalen der Chemie. — 1928. — Bd. 460, Nr. 1. — S. 98—122. — doi:10.1002/jlac.19284600106.
- Русскоязычные источники
- Смит В. А., Дильман А. Д. Глава 22. Реакция Дильса — Альдера. Часть I // Основы современного органического синтеза. — М.: Бином. Лаборатория знаний, 2009. — С. 605—642. — ISBN 978-5-94774-941-0.
- Смит В. А., Дильман А. Д. Глава 23. Реакция Дильса — Альдера. Часть II // Основы современного органического синтеза. — М.: Бином. Лаборатория знаний, 2009. — С. 643—681. — ISBN 978-5-94774-941-0.