Целекоксиб
Стиль этой статьи неэнциклопедичен или нарушает нормы литературного русского языка. |
| Целекоксиб | |
|---|---|
| Celecoxib | |
 | |
 | |
| Химическое соединение | |
| ИЮПАК |
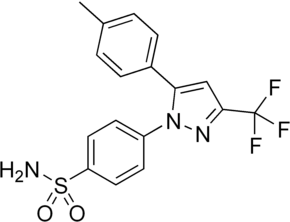
4-[5-(4-метилфенил)-3-(трифторметил)- пиразол-1-ил]бензолсульфонамид |
| Брутто-формула | C17H14F3N3O2S |
| CAS | 169590-42-5 |
| PubChem | 2662 |
| DrugBank | 00482 |
| Состав | |
| Классификация | |
| Фармакол. группа |
Ненаркотические анальгетики, включая нестероидные и другие противовоспалительные средства[1] |
| АТХ | L01XX33, M01AH01 |
| МКБ-10 | M06.9, M15—19[1] |
| Лекарственные формы | |
| капсулы 100 мг, 200 мг[2] | |
| Другие названия | |
| «Целебрекс»[2], «Флогоксиб» | |
Целекокси́б — лекарственное средство, нестероидный противовоспалительный препарат из группы коксибов. Используется для лечения остеоартрита, ревматоидного артрита, при острых болях, болезненных менструациях и менструальных симптомах, а также для уменьшения количества полипов толстой и прямой кишки у пациентов с семейным аденоматозным полипозом. Первоначально был разработан и выведен на рынок фирмой Pfizer (США) под торговой маркой «Целебрекс» (англ. Celebrex).
Представитель нового поколения нестероидных противовоспалительных препаратов — селективных ингибиторов циклооксигеназы-2[англ.] (ЦОГ-2; латиницей — COX-2). Избирательно нарушает образование простагландинов, участвующих в формировании воспалительной реакции, и не влияет на продукцию простагландинов, регулирующих почечный кровоток и целостность слизистой оболочки желудочно-кишечного тракта. Обладает выраженным противовоспалительным и анальгезирующим действием[3].
Побочные эффекты включают 37%-е увеличение числа основных сосудистых событий, которые включают нефатальный инфаркт миокарда, нефатальный инсульт или смерть от причины, связанной с кровеносным сосудом[4]. Кроме того, происходит 81%-е увеличение распространённости верхних желудочно-кишечных осложнений, которые включают перфорации, препятствия или желудочно-кишечные кровотечения, как и у всех нестероидных противовоспалительных препаратов (НПВП)[4]. В июле 2015 года FDA укрепило предупреждение о том, что неаспириновые НПВП могут вызывать сердечные приступы или инсульты[5].
В конце 2000-х годов Американская ассоциация сердца предупредила, что люди с высоким риском сердечных заболеваний должны использовать целекоксиб, только если нет других возможных методов лечения из-за более высокого риска сердечных побочных эффектов[6][7]. Однако последующее крупномасштабное исследование показало, что он не представляет большого риска для сердечных приступов и инсультов, чем другие часто используемые НПВП[8].
Применение в лечебной практике[править | править код]
Целекоксиб используется для остеоартрита, ревматоидного артрита, острой боли, мышечно-скелетной боли, болезненных менструаций, анкилозирующего спондилита и уменьшения количества полипов толстой кишки и прямой кишки у людей с семейным аденоматозным полипозом[9]. Он также может использоваться у детей с ревматоидным артритом среди несовершеннолетних, возраст которых превышает два года и весят более 10 кг (22 фунта)[9].
Для послеоперационной боли он более или менее равен ибупрофену[10][11]. Для облегчения боли он похож на парацетамол (ацетаминофен)[12]. А при остеоартрите ацетаминофен является первой линии лечения[13][14]. При остеоартрите коленного и тазобедренного суставов ацетаминофен может быть неэффективным[15].
Доказательства последствий не ясны, поскольку ряд исследований, проведённых производителем, не были выпущены для независимого анализа[16][17].
Психическое заболевание[править | править код]
Предварительные доказательства подтверждают его использование при лечении ряда психических расстройств, включая основную депрессию, биполярное расстройство и шизофрению[18][19][20][21][22].
Семейный аденоматозный полипоз[править | править код]
Он использовался для уменьшения полипов толстой кишки и прямой кишки у людей с семейным аденоматозным полипозом, но неизвестно, снижает ли он уровень рака[23], поэтому по этой причине это не является хорошим выбором[23].
Лечение ревматоидного артрита[править | править код]
Была оценена польза (уменьшение боли, скованности, улучшение физической функции) и вред (проблемы с сердцем и кишечником) целекоксиба в сравнении с другими аналогичными лекарствами или имитацией лекарства (плацебо) у взрослых с ревматоидным артритом.
При сравнении с плацебо, из каждых 100 человек, которые получали целекоксиб, у 15 наблюдалось уменьшение симптомов после 4‐12 недель. Люди, которые принимали целекоксиб, оценили уровень боли на 11 баллов ниже (по шкале от 0 до 100) после 12 недель.
Был сравнён целекоксиб и плацебо, результаты об улучшении физической функции и о числе людей, у которых развилась язвенная болезнь двенадцатипёрстной кишки свыше 3 мм в диаметре, были неубедительны. Также неубедительны были доказательства о вреде, который проявляется вскоре после применения лекарств. Ни в одном из исследований, которые сравнивали целекоксиб и плацебо, не сообщали о случаях инфаркта или инсульта.
При сравнении целекоксиба с традиционными НПВС, результаты об уменьшении боли и улучшении физической функции были неубедительны. Небольшое улучшение было обнаружено по шкале, используемой врачами для оценки состояния людей с ревматоидным артритом (ACR20, Критерии Американской коллегии ревматологии). На каждые 100 человек, которые принимали целекоксиб: было на 13 случаев меньше развития язвенной болезни двенадцатипёрстной кишки свыше 3 мм в диаметре; и на 7 случаев меньше выбывания из исследований, по сравнению с людьми, получающими традиционные НПВС.
Целекоксиб может уменьшить симптомы ревматоидного артрита и облегчить боль в большей степени, чем плацебо, но, вероятно, незначительно улучшает или совсем не улучшает физическую функцию[24][25].
Побочные эффекты[править | править код]
- Сердечно-сосудистые расстройства: НПВС связаны с повышенным риском серьёзных (и потенциально смертельных) неблагоприятных сердечно-сосудистых тромботических событий, включая инфаркт миокарда и инсульт. Риск может быть увеличен с продолжительностью использования или ранее существовавшими сердечно-сосудистыми факторами риска или заболеванием. Индивидуальные профили риска сердечно-сосудистых заболеваний следует оценивать до назначения. Может возникнуть гипертоническая болезнь нового возраста или обострение гипертонии (НПВП могут нарушать реакцию на тиазидные или петлевые диуретики) и могут способствовать сердечно-сосудистым событиям; контролировать кровяное давление и использовать с осторожностью у пациентов с гипертонией. Может вызвать удержание натрия и жидкости, следует использовать с осторожностью у пациентов с отёком или сердечной недостаточностью. Долгосрочный сердечно-сосудистый риск у детей не оценивался. Следует использовать самую низкую эффективную дозу в течение кратчайшего времени, в соответствии с индивидуальными целями пациента, для снижения риска сердечно-сосудистых событий; альтернативные методы лечения следует рассматривать для пациентов с высоким риском[26].
- Желудочно-кишечные расстройства: НПВС могут увеличить риск серьёзных язв желудочно-кишечного тракта, кровотечения и перфорации (может быть фатальным). Эти события могут возникать в любое время во время терапии и без предупреждения. Будьте осторожны с историей болезни ЖКТ (кровотечения или язвы), одновременной терапии аспирином, антикоагулянтами и / или кортикостероидами, курением, употреблением алкоголя, пожилых или ослабленных пациентов. Используйте самую низкую эффективную дозу в течение кратчайшего времени, в соответствии с индивидуальными целями пациента, для снижения риска нежелательных явлений GI; альтернативные методы лечения следует рассматривать для пациентов с высоким риском. При одновременном использовании с ≤325 мг аспирина происходит значительное увеличение риска развития желудочно-кишечных осложнений (например, язвы); рекомендуется сопутствующая гастропротекторная терапия (например, ингибиторы протонной помпы)[27].
- Гематологические эффекты: может возникнуть анемия; нужно контролировать гемоглобин или гематокрит у людей, находящихся на длительном лечении. Целекоксиб обычно не влияет на время протромбина, частичное время тромбопластина или количество тромбоцитов; он не ингибирует агрегацию тромбоцитов в одобренных дозах.
Люди с предшествующей историей язвенной болезни или кровотечения ЖКТ требуют особой меры предосторожности. Умеренная или тяжёлая печёночная недостаточность или токсичность для ЖКТ могут возникать с симптомами или без симптомов у людей, получающих НПВС.
Аллергия[править | править код]
Целекоксиб содержит сульфонамидный фрагмент и может вызывать аллергические реакции у аллергиков на другие препараты, содержащие сульфонамид. Это в дополнение к противопоказанию людям с тяжёлой аллергией к другим НПВС. Однако у него низкий (по сообщениям, 4 %) шанс вызвать кожные реакции у людей, у которых есть история таких реакций на аспирин или неселективные НПВП. НПВС могут вызывать серьёзные побочные эффекты кожи, включая эксфолиативный дерматит, синдром Стивенса-Джонсона и токсический эпидермальный некролиз; события могут происходить без предупреждения и у пациентов без предшествующей известной сульфаловой аллергии. Использование должно быть прекращено при первых признаках сыпи (или любой другой гиперчувствительности).
Сердечный приступ и инсульт[править | править код]
Коксибы (который включает целекоксиб) увеличивают риски серьёзных сердечно-сосудистых проблем примерно на 37 %[4]. Напроксен значительно не увеличивает скорость основных сосудистых событий[4].
В 2004 году из рынка был удалён ингибитор ЦОГ-2 рофекоксиб (Vioxx) из-за его риска. Как и все НПВС на рынке США, целекоксиб несёт в себе FDA -предупреждение о «чёрном ящике» для сердечно-сосудистого и желудочно-кишечного риска. В феврале 2007 года Американская кардиологическая ассоциация предупредила, что в отношении «пациентов с предшествующей историей или с высоким риском сердечно-сосудистых заболеваний … использование ингибиторов ЦОГ-2 для облегчения боли должно быть ограничено пациентами, для которых нет соответствующих альтернативы, а затем, только в самой низкой дозе и для кратчайшего срока»[6].
В 2005 году исследование, опубликованное в Annals of Internal Medicine, показало, что сердечно-сосудистые эффекты ингибиторов ЦОГ-2 различаются в зависимости от препарата[28]. Другие ингибиторы, индуцирующие ЦОГ-2, такие как рофекоксиб, имеют значительно более высокий уровень инфаркта миокарда, чем целекоксиб[29]. В апреле 2005 года, после обширного обзора данных, FDA заключила, что, вероятно, «существует „эффект класса“ для увеличения риска ССЗ для всех НПВС»[30]. В метаанализе рандомизированных контрольных исследований 2006 года были проанализированы цереброваскулярные события, связанные с ингибиторами ЦОГ-2, но не было обнаружено существенных рисков по сравнению с неселективными НПВП или плацебо[31].
В 2016 году рандомизированное исследование с участием более 24 000 участников показало, что целекоксиб обладает «неинфекционной» сердечно-сосудистой безопасностью по сравнению с ибупрофеном или напроксеном[32]. В результате в 2018 году консультативная группа FDA пришла к выводу, что целекоксиб не представляет большого риска для сердечных приступов и инсультов, чем обычно используемые ибупрофен или напроксен НПВС, и рекомендовал FDA рассмотреть возможность изменения своих рекомендаций врачам в отношении безопасности целекоксиба[8].
Взаимодействия лекарств[править | править код]
Целекоксиб преимущественно метаболизируется цитохромом Р450 2С9. Следует проявлять осторожность при одновременном применении ингибиторов 2С9, таких как флуконазол, которые могут значительно повышать уровень целекоксиба в сыворотке. При одновременном использовании лития целекоксиб увеличивает уровни лития в плазме. Если используется одновременно с варфарином, целекоксиб может привести к увеличению риска осложнений кровотечения. Препарат может увеличить риск почечной недостаточности с ингибиторами ангиотензинпревращающего фермента, такими как лизиноприл и диуретиками, такие как гидрохлоротиазид.
Беременность[править | править код]
В категориях беременности FDA США препарат относится к категории C до 30 недель беременности, а категория D начинается с 30 недель беременности.
Фармакологическое действие[править | править код]
Нестероидный противовоспалительный препарат (НПВП), избирательно блокирует вторую форму фермента циклооксигеназы (ЦОГ-2). Оказывает противовоспалительное, жаропонижающее и анальгезирующее действие, не оказывая влияния на агрегацию тромбоцитов[3]. Угнетая ЦОГ-2, уменьшает количество простагландинов (Pg), преимущественно в очаге воспаления, подавляет экссудативную и пролиферативную фазы воспаления. При назначении в высоких дозах, длительном применении или индивидуальных особенностях организма селективность снижается. По последним данным, полученным во время проведения исследований в рамках Присижн, было выяснено, что целекоксиб оказывает агрегацию крови, в связи с чем он противопоказан людям с проблемой агрегации.[2].
Общество и культура[править | править код]
Сфабрикованные исследования эффективности[править | править код]
Pfizer и его партнёр Pharmacia представили результаты своего исследования, что Celebrex «лучше защищает желудок от серьёзных осложнений, чем другие лекарства»[33]. Это стало главной точкой продаж Celebrex. Однако после федеральных исследований выяснилось, что Pfizer и Pharmacia «представили результаты только за первые шесть месяцев годового исследования, а не за весь период исследований». Эти частичные результаты были затем опубликованы в «Журнале Американской медицинской ассоциации»[33]. В 2001 году Управление по контролю за продуктами и лекарствами выпустило полные результаты исследования Pfizer и Pharmacia, в котором показано, что они оставили важные данные[33]. К 2012 году федеральный судья вскрыл «тысячи страниц внутренних документов и показаний» в «долговременном случае мошенничества с ценными бумагами против Pfizer»[33].
11 марта 2009 года Скотт С. Рубен, бывший руководитель острой боли в Медицинском центре Baystate, Спрингфилд, штат Массачусетс, признался, что данные за 21 исследование, которое он разработал для эффективности препарата (наряду с другими, такими как Vioxx), были сфабрикованы. Обезболивающие эффекты препаратов были преувеличены. Рубен был также бывшим платиновым представителем Pfizer. Хотя с 2002 по 2007 год Pfizer полностью посвятил исследования доктора Рубена, и «многие из его исследований показали, что препараты Celebrex и Lyrica, Pfizer эффективны против послеоперационной боли», Pfizer не знал о мошеннических данных[34]. Ни одно из отведённых исследований не было представлено ни Управлению по контролю за продуктами и лекарствами США, ни регулирующим органам Европейского союза до утверждения препарата. Хотя Pfizer опубликовал публичное заявление, заявив: «Очень жаль, что вы узнаете о предполагаемых действиях доктора Скотта Рубена. Когда мы решили поддержать исследования доктора Рубена, он работал в надёжном академическом медицинском центре и, по-видимому, был авторитетным исследователем»[35][36], документы, вскрытые в 2012 году, показали, что к февралю 2000 года сотрудники Pharmacia разработали стратегию для представления результатов[33].
Исследования[править | править код]
Профилактика рака[править | править код]
Роль целекоксиба, возможно, в снижении частоты некоторых видов рака была предметом многих исследований. Тем не менее, никакой текущей медицинской рекомендации не существует, чтобы использовать этот препарат для лечения рака.
Было исследовано использование целекоксиба для снижения риска колоректального рака, но для этого использования не назначают ни целекоксиб, ни какой-либо другой препарат[37]. Маломасштабные клинические испытания у людей с высоким уровнем риска (принадлежащих к семействам FAP) показали, что целекоксиб может предотвратить рост полипов. Следовательно, были проведены крупномасштабные рандомизированные клинические испытания[38]. Результаты показывают снижение рецидива полипа от 33 до 45 % у людей, получавших целекоксиб каждый день. Однако серьёзные сердечно-сосудистые события были значительно более частыми в группах, получавших целекоксиб. Аспирин проявляет аналогичный (и, возможно, более высокий) защитный эффект[39][40][41], продемонстрировал кардиозащитные эффекты и значительно дешевле, но никакие клинические испытания «голова к голове» не сравнили эти два препарата.
Лечение рака[править | править код]
В отличие от профилактики рака, лечение рака ориентировано на терапию уже сформированных опухолей и установили себя внутри пациента. Многие исследования продолжаются, чтобы определить, может ли целекоксиб быть полезным для этого последнего состояния[42]. Однако во время молекулярных исследований в лаборатории стало очевидно, что целекоксиб может взаимодействовать с другими внутриклеточными компонентами, кроме его самой известной цели, ЦОГ-2. Открытие этих дополнительных целей вызвало много споров, и первоначальное предположение о том, что целекоксиб уменьшает рост опухоли, в первую очередь за счёт ингибирования ЦОГ-2, становится спорным[43].
Конечно, ингибирование ЦОГ-2 имеет первостепенное значение для противовоспалительной и обезболивающей функции целекоксиба. Однако неясно, является ли ингибирование ЦОГ-2 доминирующей ролью в противораковых эффектах этого препарата. Например, недавнее исследование со злокачественными опухолевыми клетками показало, что целекоксиб может ингибировать рост этих клеток in vitro, но ЦОГ-2 не играет никакой роли в этом исходе; ещё более поразительно, противораковые эффекты целекоксиба были также получены с использованием типов раковых клеток, которые даже не содержат ЦОГ-2[44].
Дополнительная поддержка идеи о том, что другие цели, помимо ЦОГ-2, важны для противораковых эффектов целекоксиба, исходит из исследований с химически модифицированными версиями целекоксиба. Несколько десятков аналогов целекоксиба были получены с небольшими изменениями в их химических структурах[45]. Некоторые из этих аналогов сохранили ингибирующую активность ЦОГ-2, тогда как многие другие этого не сделали. Однако, когда исследовали способность всех этих соединений убивать опухолевые клетки в клеточной культуре, противоопухолевая активность вовсе не зависела от того, не может ли соответствующее соединение ингибировать ЦОГ-2, показывая ингибирование ЦОГ-2, не требуется для противораковых эффектов[45][46]. Одно из этих соединений, 2,5-диметилцелекоксиб, которое полностью лишено способности ингибировать ЦОГ-2, фактически проявляло более сильную противоопухолевую активность, чем целекоксиб[47].
Примечания[править | править код]
- ↑ 1 2 Целекоксиб. Реестр лекарственных средств. РеЛеС.ру (15 июля 2002). Дата обращения: 13 июня 2008. Архивировано 14 марта 2012 года.
- ↑ 1 2 3 Поиск по базе данных ЛС, опции поиска: МНН — Целекоксиб, флаги «Искать в реестре зарегистрированных ЛС», «Искать ТКФС», «Показывать лекформы». Обращение лекарственных средств. ФГУ «Научный центр экспертизы средств медицинского применения» Росздравнадзора РФ (27 марта 2008). — Типовая клинико-фармакологическая статья является подзаконным актом и не охраняется авторским правом согласно части четвёртой Гражданского кодекса Российской Федерации № 230-ФЗ от 18 декабря 2006 года. Дата обращения: 13 июня 2008. Архивировано из оригинала 3 сентября 2011 года.
- ↑ 1 2 Страчунский Л. С., Козлов С. Н. Целекоксиб (Целебрекс) // Нестероидные противовоспалительные средства. Методическое пособие. — Смоленская государственная медицинская академия. Кафедра клинической фармакологии. Архивировано 23 сентября 2015 года.
- ↑ 1 2 3 4 Bhala N., Emberson J., Merhi A., Abramson S., Arber N., Baron J.A., Bombardier C., Cannon C., Farkouh M.E., FitzGerald G.A., Goss P., Halls H., Hawk E., Hawkey C., Hennekens C., Hochberg M., Holland L.E., Kearney P.M., Laine L., Lanas A., Lance P., Laupacis A., Oates J., Patrono C., Schnitzer T.J., Solomon S., Tugwell P., Wilson K., Wittes J., Baigent C. Vascular and upper gastrointestinal effects of non-steroidal anti-inflammatory drugs: meta-analyses of individual participant data from randomised trials (англ.) // The Lancet : journal. — Elsevier, 2013. — August (vol. 382, no. 9894). — P. 769—779. — doi:10.1016/S0140-6736(13)60900-9. — PMID 23726390. — PMC 3778977.
- ↑ FDA Drug Safety Communication: FDA strengthens warning that non-aspirin nonsteroidal anti-inflammatory drugs (NSAIDs) can cause heart attacks or strokes. Food and Drug Administration (9 июля 2015). Дата обращения: 27 декабря 2015. Архивировано 3 января 2016 года.
- ↑ 1 2 Antman E.M., Bennett J.S., Daugherty A., Furberg C., Roberts H., Taubert K.A. Use of nonsteroidal antiinflammatory drugs: an update for clinicians: a scientific statement from the American Heart Association (англ.) // Circulation[англ.] : journal. — Lippincott Williams & Wilkins[англ.], 2007. — March (vol. 115, no. 12). — P. 1634—1642. — doi:10.1161/circulationaha.106.181424. — PMID 17325246. Архивировано 30 октября 2013 года.
- ↑ Should you still take Celebrex? Consumer Reports (август 2009). Дата обращения: 27 декабря 2015. Архивировано 18 декабря 2015 года.
- ↑ 1 2 Stein, Rob (2018-04-25). "FDA Panel Affirms Safety Of Painkiller Celebrex". NPR. Архивировано 20 мая 2018. Дата обращения: 19 мая 2018.
- ↑ 1 2 Celexoxib. The American Society of Health-System Pharmacists. Дата обращения: 2 января 2015. Архивировано 20 мая 2019 года.
- ↑ Derry S, Moore R. Single dose oral celecoxib for acute postoperative pain in adults. Cochrane Database of Systematic Reviews 2013, Issue 10. Art. No.: CD004233. DOI: 10.1002/14651858.CD004233.pub4. — Однократная доза перорального целекоксиба при послеоперационной боли. Дата обращения: 20 февраля 2019. Архивировано 10 декабря 2017 года.
- ↑ Derry S., Moore R.A. Single dose oral celecoxib for acute postoperative pain in adults (рум.) // Cochrane Database of Systematic Reviews. — 2013. — Octombrie (т. 10, nr. 10). — P. CD004233. — doi:10.1002/14651858.CD004233.pub4. — PMID 24150982. — PMC 4161494.
- ↑ Yelland M.J., Nikles C.J., McNairn N., Del Mar C.B., Schluter P.J., Brown R.M. Celecoxib compared with sustained-release paracetamol for osteoarthritis: a series of n-of-1 trials (англ.) // Rheumatology : journal. — 2007. — January (vol. 46, no. 1). — P. 135—140. — doi:10.1093/rheumatology/kel195. — PMID 16777855.
- ↑ Zhang W., Moskowitz R.W., Nuki G., Abramson S., Altman R.D., Arden N., Bierma-Zeinstra S., Brandt K.D., Croft P., Doherty M., Dougados M., Hochberg M., Hunter D.J., Kwoh K., Lohmander L.S., Tugwell P. OARSI recommendations for the management of hip and knee osteoarthritis, part I: critical appraisal of existing treatment guidelines and systematic review of current research evidence (англ.) // Osteoarthritis and Cartilage[англ.] : journal. — 2007. — September (vol. 15, no. 9). — P. 981—1000. — doi:10.1016/j.joca.2007.06.014. — PMID 17719803.
- ↑ Flood J. The role of acetaminophen in the treatment of osteoarthritis (англ.) // The American Journal of Managed Care[англ.] : journal. — 2010. — March (vol. 16 Suppl Management). — P. S48—54. — PMID 20297877.
- ↑ da Costa B.R., Reichenbach S., Keller N., Nartey L., Wandel S., Jüni P., Trelle S. RETRACTED: Effectiveness of non-steroidal anti-inflammatory drugs for the treatment of pain in knee and hip osteoarthritis: a network meta-analysis (англ.) // The Lancet : journal. — Elsevier, 2016. — May (vol. 387, no. 10033). — P. 2093—2105. — doi:10.1016/s0140-6736(16)30002-2. — PMID 26997557.
- ↑ Puljak L, Marin A, Vrdoljak D, Markotic F, Utrobicic A, Tugwell P. Celecoxib for osteoarthritis. Cochrane Database of Systematic Reviews 2017, Issue 5. Art. No.: CD009865. DOI: 10.1002/14651858.CD009865.pub2. — Польза и вред целекоксиба при лечении людей с остеоартритом. Дата обращения: 20 февраля 2019. Архивировано 25 июня 2018 года.
- ↑ Puljak L., Marin A., Vrdoljak D., Markotic F., Utrobicic A., Tugwell P. Celecoxib for osteoarthritis (англ.) // Cochrane Database of Systematic Reviews. — 2017. — May (vol. 5). — P. CD009865. — doi:10.1002/14651858.CD009865.pub2. — PMID 28530031.
- ↑ Fan X., Song X. Review: non-steroidal anti-inflammatory drugs may reduce schizophrenia symptom severity in the short term when added to antipsychotics (англ.) // Evidence-Based Mental Health[англ.] : journal. — 2013. — February (vol. 16, no. 1). — P. 10. — doi:10.1136/eb-2012-100865. — PMID 23093694. Архивировано 4 марта 2016 года.
- ↑ Müller N., Myint A.M., Krause D., Weidinger E., Schwarz M.J. Anti-inflammatory treatment in schizophrenia (англ.) // Progress in Neuro-Psychopharmacology & Biological Psychiatry[англ.] : journal. — 2013. — April (vol. 42). — P. 146—153. — doi:10.1016/j.pnpbp.2012.11.008. — PMID 23178230.
- ↑ Na K.S., Lee K.J., Lee J.S., Cho Y.S., Jung H.Y. Efficacy of adjunctive celecoxib treatment for patients with major depressive disorder: a meta-analysis (англ.) // Progress in Neuro-Psychopharmacology & Biological Psychiatry[англ.] : journal. — 2014. — January (vol. 48). — P. 79—85. — doi:10.1016/j.pnpbp.2013.09.006. — PMID 24056287.
- ↑ Rosenblat J.D., Cha D.S., Mansur R.B., McIntyre R.S. Inflamed moods: a review of the interactions between inflammation and mood disorders (англ.) // Progress in Neuro-Psychopharmacology & Biological Psychiatry[англ.] : journal. — 2014. — August (vol. 53). — P. 23—34. — doi:10.1016/j.pnpbp.2014.01.013. — PMID 24468642.
- ↑ Fond G., Hamdani N., Kapczinski F., Boukouaci W., Drancourt N., Dargel A., Oliveira J., Le Guen E., Marlinge E., Tamouza R., Leboyer M. Effectiveness and tolerance of anti-inflammatory drugs' add-on therapy in major mental disorders: a systematic qualitative review (англ.) // Acta Psychiatrica Scandinavica : journal. — 2014. — March (vol. 129, no. 3). — P. 163—179. — doi:10.1111/acps.12211. — PMID 24215721.
- ↑ 1 2 Celecoxib. The American Society of Health-System Pharmacists. Дата обращения: 21 апреля 2014. Архивировано 20 мая 2019 года.
- ↑ Fidahic M, Jelicic Kadic A, Radic M, Puljak L. Celecoxib for rheumatoid arthritis. Cochrane Database of Systematic Reviews 2017, Issue 6. Art. No.: CD012095. DOI: 10.1002/14651858.CD012095.pub2. — Польза и вред целекоксиба при лечении людей с ревматоидным артритом. Дата обращения: 20 февраля 2019. Архивировано 3 июля 2018 года.
- ↑ Mahir Fidahic; Antonia Jelicic Kadic; Mislav Radic; Livia Puljak. Celecoxib for rheumatoid arthritis // Cochrane Systematic Review - Intervention. — 2017. — 9 июня. — doi:10.1002/14651858.CD012095.pub2.
- ↑ Solomon S.D., McMurray J.J., Pfeffer M.A., Wittes J., Fowler R., Finn P., Anderson W.F., Zauber A, Hawk E., Bertagnolli M. Cardiovascular risk associated with celecoxib in a clinical trial for colorectal adenoma prevention (англ.) // The New England Journal of Medicine : journal. — 2005. — March (vol. 352, no. 11). — P. 1071—1080. — doi:10.1056/NEJMoa050405. — PMID 15713944.
- ↑ CELEBREX - celecoxib capsule (англ.). DailyMed. U. S. National Library of Medicine.
- ↑ Kimmel S.E., Berlin J.A., Reilly M., Jaskowiak J., Kishel L., Chittams J., Strom B.L. Patients exposed to rofecoxib and celecoxib have different odds of nonfatal myocardial infarction (англ.) // Annals of Internal Medicine[англ.] : journal. — 2005. — February (vol. 142, no. 3). — P. 157—164. — doi:10.7326/0003-4819-142-3-200502010-00005. — PMID 15684203.
- ↑ Mukherjee D., Nissen S.E., Topol E.J. Risk of cardiovascular events associated with selective COX-2 inhibitors (англ.) // JAMA : journal. — 2001. — Vol. 286, no. 8. — P. 954—959. — doi:10.1001/jama.286.8.954. — PMID 11509060.
- ↑ Analysis and recommendations for Agency action regarding nonsteroidal anti-inflammatory drugs and cardiovascular risk [decision memorandum] (PDF). FDA Center for Drug Evaluation and Research (6 апреля 2005). Архивировано 9 сентября 2005 года.
- ↑ Chen L.C., Ashcroft D.M. Do selective COX-2 inhibitors increase the risk of cerebrovascular events? A meta-analysis of randomized controlled trials (англ.) // Journal of Clinical Pharmacy and Therapeutics[англ.] : journal. — 2006. — December (vol. 31, no. 6). — P. 565—576. — doi:10.1111/j.1365-2710.2006.00774.x. — PMID 17176361.
- ↑ Nissen S.E., Yeomans N.D., Solomon D.H., Lüscher T.F., Libby P., Husni M.E., Graham D.Y., Borer J.S., Wisniewski L.M., Wolski K.E., Wang Q., Menon V., Ruschitzka F., Gaffney M., Beckerman B., Berger M.F., Bao W., Lincoff A.M. Cardiovascular Safety of Celecoxib, Naproxen, or Ibuprofen for Arthritis (англ.) // The New England Journal of Medicine : journal. — 2016. — December (vol. 375, no. 26). — P. 2519—2529. — doi:10.1056/NEJMoa1611593. — PMID 27959716.
- ↑ 1 2 3 4 5 Thomas, Katie (2012-06-24). "In Documents on Pain Drug, Signs of Doubt and Deception". New York Times. Архивировано 3 января 2016. Дата обращения: 27 декабря 2015.
- ↑ Harris, Gardiner (March 11, 2009), "Doctor Admits Pain Studies Were Frauds, Hospital Says", The New York Times, Архивировано 7 февраля 2019, Дата обращения: 27 декабря 2015
- ↑ Winstein, Keith J. (2009-03-11). "Top Pain Scientist Fabricated Data in Studies, Hospital Says". The Wall Street Journal. Архивировано 30 августа 2017. Дата обращения: 9 ноября 2018.
{{cite news}}: Неизвестный параметр|name-list-format=игнорируется (|name-list-style=предлагается) (справка) - ↑ Associated Press, Mar 11, 2009, Mass. doctor accused of faking pain pill data. Архивировано 16 марта 2009 года.
- ↑ Rial N.S., Zell J.A., Cohen A.M., Gerner E.W. Clinical end points for developing pharmaceuticals to manage patients with a sporadic or genetic risk of colorectal cancer (англ.) // Expert Review of Gastroenterology & Hepatology[англ.] : journal. — 2012. — August (vol. 6, no. 4). — P. 507—517. — doi:10.1586/egh.12.23. — PMID 22928902. — PMC 3587976.
- ↑ Bertagnolli M.M., Eagle C.J., Zauber A.G., Redston M., Solomon S.D., Kim K., Tang J., Rosenstein R.B., Wittes J., Corle D., Hess T.M., Woloj G.M., Boisserie F., Anderson W.F., Viner J.L., Bagheri D., Burn J., Chung D.C., Dewar T., Foley T.R., Hoffman N., Macrae F., Pruitt R.E., Saltzman J.R., Salzberg B., Sylwestrowicz T., Gordon G.B., Hawk E.T. Celecoxib for the prevention of sporadic colorectal adenomas (англ.) // The New England Journal of Medicine : journal. — 2006. — August (vol. 355, no. 9). — P. 873—884. — doi:10.1056/NEJMoa061355. — PMID 16943400.
- ↑ Baron J.A., Cole B.F., Sandler R.S., Haile R.W., Ahnen D., Bresalier R., McKeown-Eyssen G., Summers R.W., Rothstein R., Burke C.A., Snover D.C., Church T.R., Allen J.I., Beach M., Beck G.J., Bond J.H., Byers T., Greenberg E.R., Mandel J.S., Marcon N., Mott L.A., Pearson L., Saibil F., van Stolk R.U. A randomized trial of aspirin to prevent colorectal adenomas (англ.) // The New England Journal of Medicine : journal. — 2003. — March (vol. 348, no. 10). — P. 891—899. — doi:10.1056/NEJMoa021735. — PMID 12621133.
- ↑ Sandler R.S., Halabi S., Baron J.A., Budinger S., Paskett E., Keresztes R., Petrelli N., Pipas J.M., Karp D.D., Loprinzi C.L., Steinbach G., Schilsky R. A randomized trial of aspirin to prevent colorectal adenomas in patients with previous colorectal cancer (англ.) // The New England Journal of Medicine : journal. — 2003. — March (vol. 348, no. 10). — P. 883—890. — doi:10.1056/NEJMoa021633. — PMID 12621132.
- ↑ Bosetti C., Talamini R., Franceschi S., Negri E., Garavello W., La Vecchia C. Aspirin use and cancers of the upper aerodigestive tract (англ.) // British Journal of Cancer[англ.] : journal. — 2003. — March (vol. 88, no. 5). — P. 672—674. — doi:10.1038/sj.bjc.6600820. — PMID 12618872. — PMC 2376339.
- ↑ Dannenberg A.J., Subbaramaiah K. Targeting cyclooxygenase-2 in human neoplasia: rationale and promise (англ.) // Cancer Cell : journal. — 2003. — December (vol. 4, no. 6). — P. 431—436. — doi:10.1016/S1535-6108(03)00310-6. — PMID 14706335. Архивировано 17 марта 2018 года.
- ↑ Schönthal A.H. Direct non-cyclooxygenase-2 targets of celecoxib and their potential relevance for cancer therapy (англ.) // British Journal of Cancer[англ.] : journal. — 2007. — December (vol. 97, no. 11). — P. 1465—1468. — doi:10.1038/sj.bjc.6604049. — PMID 17955049. — PMC 2360267.
- ↑ Chuang H.C., Kardosh A., Gaffney K.J., Petasis N.A., Schönthal A.H. COX-2 inhibition is neither necessary nor sufficient for celecoxib to suppress tumor cell proliferation and focus formation in vitro (англ.) // Molecular Cancer : journal. — 2008. — May (vol. 7, no. 1). — P. 38. — doi:10.1186/1476-4598-7-38. — PMID 18485224. — PMC 2396175. Архивировано 5 сентября 2015 года.
- ↑ 1 2 Zhu J., Song X., Lin H.P., Young D.C., Yan S., Marquez V.E., Chen C.S. Using cyclooxygenase-2 inhibitors as molecular platforms to develop a new class of apoptosis-inducing agents (англ.) // Journal of the National Cancer Institute[англ.] : journal. — 2002. — December (vol. 94, no. 23). — P. 1745—1757. — doi:10.1093/jnci/94.23.1745. — PMID 12464646. Архивировано 7 января 2016 года.
- ↑ Schönthal A.H., Chen T.C., Hofman F.M., Louie S.G., Petasis N.A. Celecoxib analogs that lack COX-2 inhibitory function: preclinical development of novel anticancer drugs (англ.) // Expert Opinion on Investigational Drugs[англ.] : journal. — 2008. — February (vol. 17, no. 2). — P. 197—208. — doi:10.1517/13543784.17.2.197. — PMID 18230053.
- ↑ Schönthal A.H. Antitumor properties of dimethyl-celecoxib, a derivative of celecoxib that does not inhibit cyclooxygenase-2: implications for glioma therapy (англ.) // Neurosurgical Focus[англ.] : journal. — 2006. — April (vol. 20, no. 4). — P. E21. — doi:10.3171/foc.2006.20.4.14. — PMID 16709027.