Глиоксаль
| Глиоксаль | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование |
этандиаль | ||
| Традиционные названия | щавелевый альдегид | ||
| Хим. формула | OCHCHO | ||
| Рац. формула | C2H2O2 | ||
| Физические свойства | |||
| Состояние | жидкость | ||
| Молярная масса | 58,04 г/моль | ||
| Плотность | 1,27 г/см³ | ||
| Энергия ионизации | 10,1 эВ[1] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 15 °C | ||
| • кипения | 51 °C | ||
| Химические свойства | |||
| Растворимость | |||
| • в воде | 600 г/100 мл | ||
| Оптические свойства | |||
| Показатель преломления | 1,3826 | ||
| Классификация | |||
| Рег. номер CAS | 107-22-2 | ||
| PubChem | 7860 | ||
| Рег. номер EINECS | 203-474-9 | ||
| SMILES | |||
| InChI | |||
| ChEBI | 34779 | ||
| ChemSpider | 7572 | ||
| Безопасность | |||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
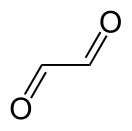
Глиокса́ль — органическое соединение, диальдегид щавелевой кислоты, жёлтая жидкость с запахом формалина. Является простейшим диальдегидом.
Производство[править | править код]
В лаборатории глиоксаль получают окислением ацетальдегида селенистой кислотой[2].
В промышленности глиоксаль получают двумя путями. Либо окислением в газовой фазе этиленгликоля в присутствии серебряного или медного катализатора, либо окислением в жидкой фазе ацетальдегида азотной кислотой. Более распространённым является окисление в газовой фазе.
Объём ежегодного производства составляет 220 000 тонн.
Первое коммерческое производство началось в Lamotte, Франция, в 1960 и сейчас принадлежит Clariant. Единый большой производитель — BASF в Людвигсхафен-на-Рейне, Германия, с производительностью 60 000 тонн/год. Только два производства глиоксаля есть в Америке (Geismer, LA and Charlotte, NC). Значительное производство недавно началось в Китае. Коммерческий глиоксаль поставляется в виде 40 % раствора.
В России глиоксаль производит единственная компания[3] - ООО "Новохим" в г. Томск с производительностью 1500 тонн/год, и с сентября 2012 года в Бийске[4].
Получение безводного глиоксаля включает нагревание твёрдых глиоксаль гидратов с пентаоксидом фосфора и конденсация паров в охлаждаемой ловушке.
Химические свойства[править | править код]


Карбонильные группы глиоксаля обладают ярко выраженными электрофильными свойствами. С водой глиоксаль образует дигидрат, становясь из жёлтого бесцветным.
Под действием щёлочи глиоксаль претерпевает внутримолекулярную реакцию Канниццаро, превращаясь в соответствующую соль гликолевой кислоты.
В присутствии поташа на воздухе окисляется до родизоновой кислоты
Кислым раствором перманганата калия или перекисью водорода окисляется до муравьиной кислоты.
Щелочным раствором перманганата калия до щавелевой кислоты.
Гидрирование на палладии (Pd/C) даёт этиленгликоль.
Со спиртами в присутствии кислоты получается моно- или диацетали.
С мочевиной образует 4,5-дигидроксиимидазолидин-2-он (1) и глиоксальуреид (2).
Применение[править | править код]
Он используется для придания нерастворимости и как агент кросс-сочетания в химии полимеров:
- белков (процесс дубления кожи)
- коллаген
- производные целлюлозы (текстиль)
- гидроколлоиды
- крахмал (мелование бумаги)
Глиоксаль — текстильно-вспомогательное вещество, придающее несминаемость хлопчатобумажным и вискозным материалам; гидрофобизирующий компонент составов для пропитки бумаги и кожи. Глиоксаль и глиоксальсульфат используются для получения кубовых красителей[5].
Глиоксаль ценный строительный блок в органическом синтезе, особенно в синтезе гетероциклов таких как имидазол. Обычная форма этого реагента используемого в лабораториях — бис-полуацеталь с этиленгликолем 1,4-диоксан-2,3-диол. Он доступен коммерчески.
Поведение в растворе[править | править код]
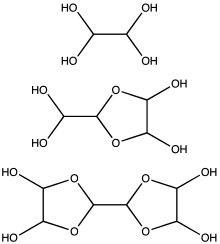
Глиоксаль типично поставляется в виде 40 % водного раствора. Как и другие низшие альдегиды, глиоксаль образует гидраты. Более того, гидраты конденсируются, образуя серии олигомеров, структуры которых остаются неизвестными. Для большинства применений точное знание структуры этих олигомеров не имеет значения.
По крайней мере два типа гидратов доступны коммерчески и являются твёрдыми веществами:
- глиоксаль димер, дигидрат: , 1,4-диоксан-транс-2,3-диол (CAS# 4845-50-5, температура плавления 91—95 °C);
- глиоксаль тример, дигидрат: (CAS# 4405-13-4), не гигроскопичен.
Установлено, что при концентрации меньшей 1 М глиоксаль существует в основном как мономер или его гидраты, , или .
При концентрации большей 1 М димер доминирует. Эти димеры скорее всего представляют собой диоксоланы с формулой . Димер и тример могут выпасть в осадок из-за низкой растворимости при температуре ниже 15 °C.
Безопасность[править | править код]
Вещество относительно малотоксично, ЛД50 для крыс, перорально, составляет 3300 мг/кг[6], для сравнения, токсичность поваренной соли — 3000 мг/кг[7].
Беречь от прямых солнечных лучей. Раздражает кожу. Работы с веществом проводить в вытяжном шкафу.
Примечания[править | править код]
- ↑ David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ Методика в Organic Syntheses. Дата обращения: 25 июня 2009. Архивировано из оригинала 23 мая 2009 года.
- ↑ Томский "Новохим" в 2011г планирует увеличить производство глиоксаля в 2,7 раза - Сибирь || Интерфакс Россия. www.interfax-russia.ru (2 марта 2011). Дата обращения: 18 апреля 2024.
- ↑ Запуск производства глиоксаля в Бийске. www.akvobr.ru. Дата обращения: 18 апреля 2024.
- ↑ Химическая энциклопедия, т. 1, 1988, «Сов. энциклопедия», стр. 583
- ↑ Mattioda, Georges; Blanc, Alain. "Glyoxal". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a12_491.pub2
- ↑ Safety (MSDS) data for sodium chloride. ox.ac.uk. Архивировано из оригинала 7 июня 2011 года.
Ссылки[править | править код]
- Колотов С. С., Менделеев Д. И. Глиоксаль // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.


![{\displaystyle {\ce {[(CHO)2]2(H2O)2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b8205e8d39a865b3e169d9de5589dd01f79dbdf0)
![{\displaystyle {\ce {[(CHO)2]3(H2O)2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/bcda04d4ad1b4e8be56de67c3f84217ab60e0037)



![{\displaystyle {\ce {[(HO)CH]2O2CHCHO}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d76f8bbd40a65db8b61813afc88286aa404d1237)