Зидовудин
| Зидовудин | |
|---|---|
| Zidovudine[1] | |
 | |
 | |
| Химическое соединение | |
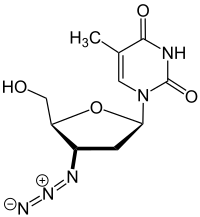
| ИЮПАК | 3'-Азидо-3'-дезокситимидин |
| Брутто-формула | C10H13N5O4 |
| Молярная масса | 267.242 |
| CAS | 30516-87-1 |
| PubChem | 35370 |
| DrugBank | DB00495 |
| Состав | |
| Классификация | |
| Фармакол. группа | Противовирусное (ВИЧ) средство |
| АТХ | J05AF01 |
| МКБ-10 | B20, B21, B22, B23, B24 |
| Фармакокинетика | |
| Биодоступн. | При пероральном приеме: 54 - 74% (у взрослых), по другим данным - 60 - 70% |
| Связывание с белками плазмы | 34 - 38 % |
| Метаболизм | Печень |
| Период полувывед. | 3.3 ч (из клеток), 0.8 - 1.2 ч (из крови у взрослых) |
| Экскреция | Почки |
| Лекарственные формы | |
| таблетки, покрытые оболочкой (100 мг, 300 мг); капсулы (100 мг, 200 мг, 300 мг); раствор для приема внутрь; раствор для инфузий | |
| Способы введения | |
| Перорально, внутривенно (капельно) | |
| Другие названия | |
| Зидовудин, Ретровир, Азидотимидин, Виро-Зет, Зидо-Эйч | |
Зидовудин (Zidovudine, ZDV), также известный как азидотимидин (AZT), — 3'-азидо-3'-дезокситимидин, противовирусный препарат, нуклеозидный ингибитор обратной транскриптазы вируса иммунодефицита человека. Первый антиретровирусный препарат: допущен к применению в марте 1987 года[2]. Применяется как самостоятельно, так и в составе комбинированных препаратов. Один из ключевых компонентов Антиретровирусной терапии.
История
[править | править код]3'-Азидо-3'-дезокситимидин был впервые синтезирован в 1964 году Джеромом Хорвицем[англ.] (1919—2012) с сотрудниками в качестве потенциального противоопухолевого препарата[3][4]. Вследствие неактивности AZT в животных моделях исследования не получили дальнейшего развития[4].
Разработка противовирусных препаратов в Исследовательских лабораториях Веллкама[англ.] (ныне принадлежат GlaxoSmithKline) проводилась под руководством Гертруды Элайон[4] (1918—1999). Азидопроизводные тимидина были синтезированы в 1981 году по опубликованным ранее методикам[5] и использованы в качестве синтетических предшественников некоторых соединений, а также включены в скрининговые библиотеки[4]. При скрининге антибактериальной активности AZT была обнаружена эффективность в отношении некоторых грамотрицательных, но не грамположительных бактерий: AZT эффективно фосфорилируется тимидинкиназами эшерихий до соответствующего трифосфата, эффективно терминирующего полимеризацию ДНК[4]. В испытаниях in vivo была продемонстрирована эффективность и безопасность AZT в качестве ингибитора бактериальных инфекций[4].
При скрининге противовирусной активности AZT не проявил активности против вирусов простого герпеса типов 1 и 2, вируса ветряной оспы, аденовируса типа 5, вируса гриппа A[англ.], респираторно-синцитиального вируса, риновируса B, вируса жёлтой лихорадки, вируса кори, коронавируса[уточнить], ротавируса крупного рогатого скота, вируса осповакцины[англ.], вируса везикулярного стоматита[англ.], вируса лейкоза мышей L1210[англ.], цитомегаловируса человека. Незначительная активность наблюдалась в отношении вируса Эпштейна — Барр[4].
В связи с открытием в 1983 году вируса иммунодефицита человека в начале 1984 года в лабораториях Веллкама были запущены исследования по поиску препаратов для лечения вызываемого ВИЧ заболевания. Был адаптирован метод бляшек[англ.], первоначально разработанный для других ретровирусов, и в процессе скрининга ранее исследованных противовирусных препаратов и других аналогов нуклеозидов AZT оказался единственным соединением, полностью подавлявшим репродукцию вируса[4]. Публикация противовирусной активности AZT[6] послужила толчком к дальнейшему исследованию аналогов нуклеозидов[англ.] в качестве ингибиторов обратной транскриптазы, в то время как для самого зидовудина был разработан метод масштабирования синтеза и начаты клинические исследования[4].
Зидовудин — первый антиретровирусный препарат, допущенный к применению в 1987 году. Патент на производство зидовудина в США истек в 2005 г. Вскоре этот препарат, возможно, будет продаваться значительно дешевле[7].
Благодаря коммерческому успеху зидовудина последовал всплеск интереса к нуклеозидным ингибиторам обратной транскриптазы: были разработаны диданозин[англ.], залцитабин[англ.], ставудин, ламивудин, абакавир и эмтрицитабин[2].
-
Диданозин
-
Залцитабин
-
Ставудин
-
Ламивудин
-
Абакавир
-
Эмтрицитабин
Синтез
[править | править код]Ключевая стадия первого синтеза 3'-азидо-3'-дезокситимидина, осуществлённого Хорвицем с соавторами, состояла в нуклеофильном замещении мезилатной группы при 3'-атоме углерода сахарного остатка действием азида лития в диметилформамиде[3]. После удаления тритильной защиты было получено целевое соединение в виде бесцветных игольчатых кристаллов[3].
Аналогичная последовательность реакций лежит в основе синтеза AZT, разработанного Лином и Прусоффом[5], однако методики отдельных стадий были ими оптимизированы.
Механизм действия
[править | править код]Аналогично другим нуклеозидным ингибиторам обратной транскриптазы, после троекратного фосфорилирования зидовудинтрифосфат выступает в качестве терминатора цепи ДНК, синтезируемой по матрице РНК[2]. Таким образом, зидовудин является пролекарством, поскольку сам по себе зидовудин обратную транскрипцию не ингибирует[6].
В экспериментах по ингибированию цитопатического действия ВИЧ был обнаружен выраженный протективный эффект зидовудина в концентрациях 5-10 мкМ, не подавляющих нормальное функционирование T-клеток и B-клеток[6]. При этом полное ингибирование обратной транскриптазы наблюдалось в концентрациях 0,5 мкМ и выше[6].
Фармакокинетика
[править | править код]Метаболизм
[править | править код]Клинические исследования
[править | править код]Зидовудин изучался в многочисленных клинических исследованиях, и по его применению накоплен наиболее обширный опыт по сравнению со всеми остальными препаратами (более 20 лет).
Физические свойства
[править | править код]
Бесцветные кристаллы. Растворимость в воде при 25 °C составляет 20,1 мг/мл. Температура плавления 119−121 °C[3]. рН водного 10 % раствора — 6,5 — 6,6.
Дозировка
[править | править код]Дозировки и формы выпуска: капсулы 100 мг, 300 мг; раствор для приема внутрь (50 мг в 5 мл, флаконы по 200 мл.); раствор для инфузий (200 мг, флаконы по 20мл).
Стандартные дозы и режим приема: 600 мг/сутки, разделенные на два или три приема: три раза в день по две капсулы 100 мг, или два раза в день по 300 мг.
Лекарственные взаимодействия и побочные эффекты
[править | править код]Можно применять вне зависимости от приема пищи, но жирная пища может замедлять всасывание. Не совместим со ставудином, комбинация с рибавирином может быть неэффективной. Усиление токсичности в отношении костного мозга в комбинациях с ганцикловиром, винкристином, амфотерицином «B», цитостатиками и другими препаратами, угнетающими костный мозг. Парацетамол увеличивает риск развития нейтропении. Метадон значимо повышает концентрацию в плазме (30—40 %), что может увеличивать риск развития побочных эффектов азидотимидина.
В высоких дозах предположительно является мутагеном, канцерогеном.
Острая токсичность — LD50 (крыса, перорально) — 3500 мг/кг.
Наиболее значимые побочные эффекты: в начале терапии (6—8 недель) — головокружение, слабость, сниженный аппетит, тошнота, рвота. При длительном применении — анемия, кожный зуд, боли в мышцах.
Уже в очень ранних исследованиях, посвященных монотерапии зидовудином, было установлено, что зидовудин существенно повышает выживаемость, по крайней мере, при тяжёлом иммунодефиците. Тем не менее в ходе очень крупных ранних исследований (ACTG 016 и ACTG 019) не удалось доказать статистически значимое влияние зидовудина на выживаемость у пациентов с бессимптомным течением ВИЧ-инфекции, хотя в обоих случаях отмечалось существенное уменьшение риска прогрессирования ВИЧ-инфекции. Уже тогда стало ясно, что эффективность монотерапии зидовудином, скорее всего, не очень высока. Вскоре репутация зидовудина пострадала ещё больше: в исследовании Concorde было установлено, что лечение зидовудином не даёт отдалённого положительного эффекта. Кроме того, в первые годы зидовудин назначали в очень высоких дозах (1500 мг/сут), которые вызывали выраженное угнетение кроветворения. Но и сейчас, когда зидовудин применяется в более низких дозах (500—600 мг/сут), не следует недооценивать его токсическое действие на костный мозг; поэтому у пациентов, получающих зидовудин, следует в обязательном порядке следить за показателями клинического анализа крови. Длительный приём зидовудина почти всегда приводит к макроцитозу (увеличению среднего объёма эритроцита, по наличию которого можно в некоторой степени судить о соблюдении режима лечения[7].
В 2011 году Зидовудин подвергся критике после проведения исследования Gilead 934, в котором было установлено, что зидовудин существенно уступает по эффективности тенофовиру. В этом крупном рандомизированном исследовании пациентам, ранее не получавшим АРТ, назначали эфавиренз в комбинации либо с зидовудином и ламивудином, либо с тенофовиром и эмтрицитабином. В частности, у пациентов, получавших зидовудин, чаще развивалась тяжёлая анемия, которая служила основанием для отмены терапии в 5,5 % случаев. Через 144 недели доля пациентов с вирусной нагрузкой меньше 400 копий/мл в группе, получавшей зидовудин, была меньше, чем в группе, получавшей тенофовир (58 % по сравнению с 71 %). Такая разница была обусловлена в значительной степени тем, что в группе, получавшей зидовудин, больше пациентов досрочно выбыло из исследования из-за побочных эффектов (11 % по сравнению с 5 %). Помимо симптомов угнетения кроветворения (анемии и нейтропении), побочные эффекты, приводившие к отмене терапии, включали главным образом нарушения работы ЖКТ (например, тошноту), которые обычно развивались в первые недели после начала лечения. Кроме того, у пациентов, получавших зидовудин, наблюдалось значимое уменьшение толщины подкожной жировой клетчатки на конечностях[7].
По вышеперечисленным причинам во многих рекомендациях и стандартах зидовудин был исключен из списка предпочтительных препаратов первого ряда для лечения пациентов, ранее не получавших АРТ. Другой важный недостаток этого препарата состоит в необходимости приема два раза в сутки, в то время как многие антиретровирусные препараты достаточно принимать один раз в сутки. Это исключает возможность включения зидовудина в схемы АРТ с однократным приемом препаратов в сутки. Однако зидовудин продолжает входить в некоторые схемы АРТ, схемы профилактики передачи ВИЧ от матери ребенку и схемы постконтактной профилактики, поскольку польза от его применения была доказана, особенно с учетом мутаций резистентности вируса. Например, штаммы с мутациями K65R или M184V гиперчувствительны к зидовудину. Дополнительными преимуществами зидовудина служат отсутствие токсического действия на ЦНС и хорошее проникновение через гематоэнцефалический барьер.
Показания к применению
[править | править код]Ранние (с числом клеток T4 менее 500/мм3) и поздние стадии ВИЧ-инфекции, профилактика трансплацентарного ВИЧ-инфицирования плода.
Противопоказания
[править | править код]Гиперчувствительность, лейкопения (число нейтрофилов менее 0,75×109/л)[8], анемия (гемоглобин ниже 70 г/л)[9].
Комбинированные препараты
[править | править код]Зидовудин очень эффективен при применении в комбинации с другими антиретровирусными препаратами. В 1990-е годы комбинация зидовудина и ламивудина была одной из наиболее широко применяемых базовых комбинаций НИОТ в схемах АРТ. В сентябре 1997 года был допущен к применению комбинированный препарат ламивудина и зидовудина, получивший торговое наименование Комбивир[2].
В ноябре 2000 года была допущена к применению комбинация абакавира, ламивудина и зидовудина, распространяемая под торговым наименованием Тризивир[2].
Источники
[править | править код]- ↑ Зидовудин. Энциклопедия лекарств и товаров аптечного ассортимента. РЛС Патент. — Инструкция, применение и формула.
- ↑ 1 2 3 4 5 De Clercq, Erik. Approved Antiviral Drugs over the Past 50 Years : [англ.] : [арх. 12 мая 2017] / Erik De Clercq, Guangdi Li // Clin. Microbiol. Rev. — 2016. — Vol. 29, no. 3 (1 July). — P. 695—747. — ISSN 1098-6618. — doi:10.1128/CMR.00102-15. — PMID 27281742.
- ↑ 1 2 3 4 Horwitz, Jerome P. Nucleosides. V. The Monomesylates of 1-(2'-Deoxy-β-D-lyxofuranosyl)thymine : [англ.] / Jerome P. Horwitz, Jonathan Chua, Michael Noel // J. Org. Chem. — 1964. — Vol. 29, no. 7 (July). — P. 2076—2078. — ISSN 0022-3263. — doi:10.1021/jo01030a546.
- ↑ 1 2 3 4 5 6 7 8 9 Pattishall, Katryn H. Discovery and Development of Zidovudine as the Cornerstone of Therapy to Control Human Immunodeficiency Virus Infection // The Search for Antiviral Drugs : Case Histories from Concept to Clinic : [англ.] : [арх. 3 января 2018] / Julian Adams ; Vincent J. Merluzzi. — Boston, MA : Birkhäuser, 1993. — 2. — P. 23—43. — XIII, 240 p. — ISBN 978-1-4899-6720-6. — doi:10.1007/978-1-4899-6718-3_2.
- ↑ 1 2 Lin, Tai-Shun. Synthesis and Biological Activity of Several Amino Analogues of Thymidine : [англ.] / Tai-Shun Lin, William H. Prusoff // J. Med. Chem. — 1978. — Vol. 21, no. 1 (January). — P. 109—112. — ISSN 0022-2623. — doi:10.1021/jm00199a020.
- ↑ 1 2 3 4 Mitsuya, Hiroaki. 3'-Azido-3'-deoxythymidine (BW A509U): an antiviral agent that inhibits the infectivity and cytopathic effect of human T-lymphotropic virus type III/lymphadenopathy-associated virus in vitro : [англ.] : [арх. 23 мая 2015] / Hiroaki Mitsuya, Kent J. Weinhold, Phillip A. Furman, Marty H. St. Clair, Sandra Nusinoff Lehrman, Robert C. Gallo, Dani Bolognesi, David W. Barry, Samuel Broder. // PNAS. — 1985. — Vol. 82, no. 20 (1 October). — P. 7096–7100. — PMID 2413459.
- ↑ 1 2 3 Кристиан Хоффман, Юрген К. Рокштро. Лечение ВИЧ-инфекции 2011 С. 89—90. Антиретровирусная терапия онлайн (2012). Дата обращения: 17 июня 2013. Архивировано 18 июня 2013 года.
- ↑ Инструкция по применению. Дата обращения: 2 октября 2022. Архивировано 2 октября 2022 года.
- ↑ Зидовудин. Антиретровирусная терапия онлайн (31 июля 2012). Дата обращения: 17 июня 2013. Архивировано 18 июня 2013 года.
Ссылки
[править | править код]Federally approved HIV/AIDS medical practice guidelines. (англ.). A service of the U.S. Department of Health and Human Services (HHS). Дата обращения: 30 января 2016.





