Тринитрофенол
| Тринитрофенол | |
|---|---|
  | |
 | |
| Общие | |
| Систематическое наименование |
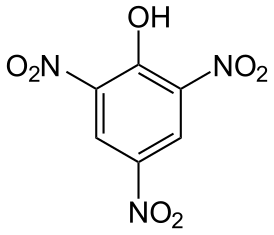
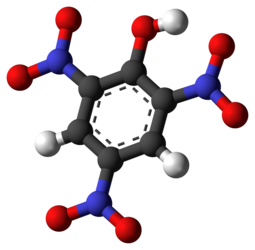
2,4,6-тринитрофенол |
| Традиционные названия | Пикриновая кислота |
| Хим. формула | C6H3N3O7 |
| Физические свойства | |
| Молярная масса | 229,10 г/моль |
| Плотность | 1,763 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 122 °C |
| • кипения | > 300 °C |
| • разложения | 300 °C |
| • вспышки | 302 ± 1 ℉[1] |
| Давление пара | 1 ± 1 мм рт.ст.[1] |
| Химические свойства | |
| Константа диссоциации кислоты | 0,25[2] и 0,38[3] |
| Растворимость | |
| • в воде | 1,27 г/100 мл |
| • в этаноле | 8,33 г/100 мл |
| • в бензоле | 10 г/100 мл |
| • в хлороформе | 2,86 г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1,76 |
| Классификация | |
| Рег. номер CAS | 88-89-1 |
| PubChem | 6954 |
| Рег. номер EINECS | 201-865-9 |
| SMILES | |
| InChI | |
| RTECS | TJ7875000 |
| ChEBI | 46149 |
| ChemSpider | 6688 |
| Безопасность | |
| Предельная концентрация | 0,1 мг/м³ |
| ЛД50 | 98—120 мг/кг |
| Токсичность | токсичен, весьма едкий, является ирритантом |
| Фразы риска (R) | R1, R4, R11, R23, R24, R25 |
| Фразы безопасности (S) | S28, S35, S37, S45 |
| Сигнальное слово | Опасно |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
2,4,6-Тринитрофенол (пикриновая кислота) — химическое соединение с химической формулой C6H2(NO2)3OH, нитропроизводное фенола. Молекулярная масса 229,11 а. е. м. При нормальных условиях — жёлтое кристаллическое ядовитое вещество. Пикриновую кислоту и её соли (пикраты) используют как взрывчатые вещества, а также в аналитической химии для определения калия, натрия.
Другие названия:
- мелинит (Melinite) во Франции
- мелинит (Melinit) в Российской империи
- лиддит (Lyddite) в Великобритании
- пертит (Pertit) в Италии
- пикриновая кислота (Picric acid, PA) в США
- пикринит, пикринита (Picrinit, Picrinita) в Испании
- Экразит (Ekrasit) в Австрии[уточнить]
- TNF в Польше, США и др.
- шимозе, шимоза (яп. 下瀬火薬 симосэ каяку) в Японии
История[править | править код]
Предположительно, соли пикриновой кислоты (пикраты свинца и калия) обнаружил в 1642 году Глаубер, воздействуя азотной кислотой (методы изготовления которой он разработал) на шерсть и рог.
В 1771 году Питер Вулф (en:Peter Woulfe) получил тринитрофенол действием азотной кислоты на природный краситель индиго[4]. Кислотные свойства соединения обнаружены в 1783 году Гаусманом[фр.][5]. При дальнейших исследованиях тринитрофенол получили при действии азотной кислотой на различные органические вещества: шёлк, природные смолы и прочие.
В 1841 Марчанд (Marchand) предложил формулу C12H6N6O14 (удвоенная формула тринитрофенола), а правильную формулу в 1842 году установил Лоран (Laurent), определив, что пикриновая кислота представляет собой тринитрофенол и может быть получена нитрованием фенола. Им же был выделен динитрофенол как продукт промежуточной стадии нитрования.
В 1869 году метод нитрования был усовершенствован Шмидтом и Глутцем (Schmidt, Glutz), предложившими сульфирование с последующим нитрованием. Взрывчатые свойства пикратов были обнаружены ещё в 1799 году Велтером (Welter), однако до 1830-х годов это свойство не находило применения. Во второй половине XIX века пикраты (в основном калия и аммония) стали широко использоваться в военном деле. Длительное время сам тринитрофенол использовался как жёлтый краситель для шерсти и шёлка и не считался взрывоопасным веществом, в 1871 году такой авторитетный специалист, как Абель, утверждал, что только пикраты обладают взрывчатыми свойствами, а тринитрофенол нет. Однако уже в 1873 году Шпренгель (Sprengel) показал способность тринитрофенола к детонации, а в 1885 году французский инженер Тюрпен обнаружил, что в сплавленном или сильно спрессованном состояниях тринитрофенол детонирует, и предложил его для снаряжения боеприпасов. Это дало начало широкому применению тринитрофенола в качестве мощного бризантного взрывчатого вещества.
Первое производство бризантных артиллерийских снарядов с плавленным тринитрофенолом было налажено во Франции, а затем во многих других странах. В Российской империи производство тринитрофенола началось в 1894 году. В Российской империи в военном деле было принято французское название этого вещества «мелинит». Артиллерийский офицер С. В. Панпушко разработал боеприпасы для тяжёлых и полевых орудий. Во время испытательных стрельб произошло два разрыва лёгких 87-мм полевых пушек с человеческими жертвами. 28 ноября 1891 года при взрыве опытной бомбы, снаряженной мелинитом, погиб и сам С. Панпушко и два его помощника, вместе с ним заряжавших роковой заряд, что затормозило разработки новых вооружений в России.
Во время русско-японской войны 1904—1905 годов японская армия применяла в широких масштабах снаряды «шимозе» к 75-мм полевым и горным пушкам, в которых заряд примерно 0,8 кг тринитрофенола был особым образом из расплава отлит в виде мелкозернистой массы. В этой же войне Японией были впервые применены крупнокалиберные (до 12 дюймов) снаряды корабельной артиллерии с массой заряда тринитрофенола до 41 кг, которые не могли пробить броневую защиту, но наносили значительные разрушения на палубах, вызывали обширные пожары и показали хорошую эффективность. Русско-японская война стала апофеозом применения тринитрофенола.
Высокая активность ВВ, большое количество несчастных случаев (большое количество разрывов снарядов в стволах, да и взрыв броненосца «Микаса» многие приписывают капризу «шимозе») заставили химиков многих стран искать альтернативу. Таковым стал тринитротолуол.
Военное значение тринитрофенола сохранялось вплоть до Второй мировой войны, однако использовался он всё меньше и меньше. Уже в Первую мировой войну его использование было ограничено. В настоящее время привлекательность его из-за повышенной коррозионной активности и чувствительности по сравнению с тротилом невысока. В то же время относительная простота кустарного изготовления и высокая взрывная эффективность тринитрофенола привлекали и продолжают привлекать внимание террористов.
С осени 1944 года промышленность Германии в виду тяжёлого положения на фронтах отказывается от промышленного производства тринитротолуола в пользу тринитрофенола (А. Б. Широкорад, Бог войны Третьего рейха). По этой причине складированные и неразорвавшиеся германские боеприпасы представляют для поисковиков повышенную опасность.
Физические свойства[править | править код]
Чистый тринитрофенол — твёрдое вещество в виде пластинчатых или призматических кристаллов[6][7], цвет от бесцветного до жёлтого, плотность 1813 кг/м³, температура плавления 122,5 °C.
Кристаллическая система орторомбическая бипирамидальная.
Давление паров при 195 °C — 2 мм рт. ст., при 255 °C — 50 мм рт. ст. Плотность расплава при 124 °C 1589 кг/м³, при 170 °C — 1513 кг/м³. Гравиметрическая (насыпная) плотность порошка 900—1000 кг/м³.
Порошок хорошо прессуется, особенно при подогревании. При давлении прессования 4500 кг/см² плотность 1740 кг/м³, однако практически из соображений безопасности порошок прессуют при давлениях до 2000 кг/см², при этом получается плотность не выше 1630 кг/м³. При медленном охлаждении расплава можно получить твёрдое вещество с плотностью 1580—1610 кг/м³. Чем меньше примесей, тем выше плотность плавлёного тринитрофенола.
Химические свойства[править | править код]
Растворимость[править | править код]
В холодной воде растворяется слабо, около 1,1 % при +15 °C. В горячей воде растворимость значительно увеличивается до 6,5 % при 100 °C. По другим данным, при +20 °C растворяется 1,14 %, при +60 °C — 2,94 % и при 100 °C — 9,14 %. Водный раствор тринитрофенола окрашен в интенсивный желтый цвет благодаря присутствию аниона. Неионизированная молекула в безводных растворах цвета не имеет (например, в петролейном эфире). В присутствии сильных кислот раствор также не имеет окраски, это свойство позволяет использовать тринитрофенол в качестве кислотно-основного индикатора.
В этиловом спирте и диэтиловом эфире растворимость относительно высока. В 100 г спирта при +20 °C растворяется 6,23 г пикриновой кислоты, а при температуре кипения — 66,2 г. При +13 °C в 1 л безводного эфира растворяется 10,8 г пикриновой кислоты; при содержании в эфире 0,8 % воды растворяется 36,8 г, а присодержании 1 % воды — 40 г.
Растворяется в метиловом спирте, глицерине, хлороформе, сероуглероде, ацетоне и особенно хорошо в бензоле. В 100 г бензола растворяется 3,7 г при +5 °C, 7,29 г — при +15 °C, 9,55 г — при +20 °C и 96,77 г — при +75 °C.
В смесях серной кислоты и воды растворимость заметно возрастает при концентрации кислоты выше 70 % и при увеличении температуры. При температуре +18 °C растворимость в безводной серной кислоте 10,1 г/100 мл кислоты, а при +80 °C — 25,8 г/100 мл кислоты. При разбавлении раствора в серной кислоте тринитрофенол выпадает в осадок.
Эвтектические смеси[править | править код]
Тринитрофенол образует со многими веществами эвтектические смеси, что широко использовалось при снаряжении боеприпасов, поскольку температура плавления чистого тринитрофенола 122,5 °C создаёт значительные технологические сложности. Наиболее привлекательными с практической точки зрения являются смеси с другими нитросоединениями:
- смесь с нитронафталином 1:1, температура плавления +49 °C
- смесь с тринитротолуолом 1:1, +47 °C
- смесь с тринитрокрезолом 1:1, +70 °C
Взаимодействие с металлами[править | править код]
Тринитрофенол достаточно сильная кислота, способная к обменным реакциям с образованием солей металлов (пикратов). Наиболее часто встречаются:
- пикрат натрия C6H2(NO2)3ONa
- пикрат кальция (C6H2(NO2)3O)2Ca
- пикрат железа (C6H2(NO2)3O)3Fe2
- пикрат свинца (C6H2(NO2)3O)2Pb
Все пикраты — твёрдые кристаллические вещества, обладающие значительно более высокой чувствительностью, чем тринитрофенол. Это требует особого внимания к применению металлов и металлическим загрязнениям при его производстве. Прямое образование пикратов в среде серной кислоты не происходит, основную опасность представляют примеси в промывочной воде и материалы, с которыми контактирует очищенный тринитрофенол. Из-за повышенной чувствительности пикратов, при изготовлении боеприпасов требуются специальные меры по изоляции заряда от металлической оболочки.
Другие свойства[править | править код]
- Характерная качественная реакция — с цианидом калия, в которой образуется ярко-красная изопурпуровая кислота.
- Тринитрофенол со многими ароматическими химическими веществами образует нестойкие соединения, в которых не образуются полноценные ковалентные или ионные химические связи.
- Окисляется сильными окислителями. В кипящей азотной кислоте окисляется до щавелевой кислоты. В кипящем растворе персульфата аммония полностью окисляется:
- Восстанавливается сульфидом или гидросульфитом натрия, сульфатом железа до пикрамовой (picramic) кислоты, применяемой как сырьё в производстве красок и диазодинитрофенола. Дальнейшее восстановление приводит к образованию триаминофенола.
- Кипячение в концентрированном растворе гидроксида натрия приводит к разложению:
- Взаимодействие с гипохлоритами приводит к разложению с образованием хлорпикрина, это один из промышленных способов его получения:
- Взаимодействие с хлором, царской водкой, хлоратом калия в присутствии HCl приводит к образованию хлоранила (chloranil) и хлорпикрина.
Взрывчатые свойства[править | править код]
Основные характеристики[править | править код]
- Реакция разложения
- Продукты взрыва в замкнутой бомбе: 71,05 % CO, 3,42 % CO2, 0,34 % O2, 1,02 % CH4, 13,8 % H2, 21,1 % N2
- Кислородный баланс при окислении до CO2 : −45 %
- Расчётные характеристики для разных плотностей:
| Показатель | При плотности 1,76 г/см³ | При плотности 1,00 г/см³ |
|---|---|---|
| Состав продуктов взрыва | ||
| CO2 | 2,661 | 1,310 |
| CO | 0,179 | 2,970 |
| H2O (г) | 1,499 | 1,409 |
| N2 | 1,500 | 1,496 |
| C (тв) | 3,160 | 1,713 |
| H2 | - | 0,065 |
| NH3 | - | 0,008 |
| CH4 | - | 0,006 |
| Скорость детонации, м/с | 7680 | 5545 |
| Давление детонации, кбар | 265 | 88 |
| Теплота взрыва, ккал/г | 1,27 | 1,02 |
| Объём продуктов взрыва, см³/г | 0,423 | 0,714 |
- Скорость детонации зависит от плотности:
| Плотность, г/см³ | Скорость детонации, м/с |
|---|---|
| 0,97 | 4965 |
| 1,32 | 6190 |
| 1,41 | 6510 |
| 1,62 | 7200 |
| 1,70 | 7480 |
Зависимость скорости детонации D от плотности ρ довольно точно описывается уравнением Кука (Cook):
D[м/с] = 5255 + 3045 (ρ[г/см³] — 1).
- Критический диаметр зависит от размера зёрен порошка и плотности заряда:
| Размер зёрен, мм | Плотность, г/см³ | Критический диаметр, мм |
|---|---|---|
| 0,1—0,75 | 0,95 | 9,0 |
| менее 0,1 | 0,95 | 5,5 |
| 0,01—0,05 | 0,8 | 2,1—2,3 |
| 0,05—0,07 | 0,7 | 3,6—3,7 |
- Фугасность в свинцовом блоке 310 мл (тротил 285 мл, гексоген 470)
- Бризантность по обжатию свинцового столбика 17 мм (тротил 16 мм, гексоген — 24)
- Чувствительность в сплавленном состоянии ниже, чем в порошке. В присутствии пикратов чувствительность значительно возрастает.
- Чувствительность к удару по сравнению с тротилом по одним данным ниже, а по другим — выше, в зависимости от условий испытаний. При испытании грузом 10 кг и высотой падения 25 см частость взрывов 24—32 % (тротил 4—8 %, гексоген 79—80 %, тэн 100 %)
- При трении между твёрдыми материалами (сталь, чугун) порошок детонирует, между цветными металлами детонация не возникает.
- При простреле свободно насыпанного порошка винтовочной пулей воспламеняется.
- При простреле замкнутых оболочек с плавленным тринитрофенолом может быть выгорание, частичная или полная детонация в зависимости от характера оболочки и заряда. Чем прочнее оболочка, тем вероятнее детонация.
- Чувствительность к нагреву:
| Температура, °C | Задержка до взрыва, сек. |
|---|---|
| 350 | 1,5 |
| 315 | 5,5 |
| 277 | 26,3 |
| 267 | 50,3 |
| 260 | не детонирует |
Инициирование взрыва[править | править код]
Детонирует от капсюля-детонатора. Восприимчивость снижается с возрастанием плотности прессованного и ещё ниже у плавленного тринитрофенола:
- при плотности 1580 кг/м³ (давление прессования 1500 кг/см²) детонирует от капсюля с 0,4 г гремучей ртути
- при плотности 1680 кг/м³ (давление прессования 2900 кг/см²) необходим капсюль с 0,65 г гремучей ртути
- для плавленного необходим капсюль с 3 г гремучей ртути, но на практике такими не пользуются и применяется промежуточный детонатор.
- для различных условий масса азида свинца для инициирования 0,03-0,24 г
Свойства при нагревании[править | править код]
При нагревании в различных условиях:
- при 122,5 °C плавится без разложения, в жидком состоянии жёлто-бурого цвета;
- при медленном нагревании слабо возгоняется;
- в свободном состоянии при 183 °C большой индукционный период до начала разложения, при уменьшении объёма для паров индукционный период уменьшается;
- при 230 °C индукционный период до начала разложения отсутствует;
- температура воспламенения 300—310 °C, в свободном состоянии сгорает без вспышки. Горит спокойно, сильно коптящим пламенем, с плавлением. Даже большие массы (порядка 100 кг) могут спокойно гореть, если при этом расплав свободно растекается;
- при быстром нагревании в замкнутой оболочке до 300 °C взрывается.
Опасность в производстве и применении[править | править код]
Этот раздел представляет собой неупорядоченный список разнообразных фактов о предмете статьи. |
- Взрыв пикриновой кислоты в 1887 году на фабрике в Манчестере был вызван образованием пикратов во время пожара. Расплавленная от пламени пикриновая кислота попала на литопон, в результате чего образовался пикрат свинца. Он послужил детонатором, от которого взорвалась пикриновая кислота.
- Пожар и взрыв в 1900 году на фабрике в Хаддерсфилде (Hudders-field) был вызван образованием пикрата железа на паровых трубах. При ремонте от удара пикрат железа загорелся, и пламя распространилось на сушилку пикриновой кислоты.
- 6 декабря 1917 года в гавани канадского города Галифакс произошёл мощнейший взрыв корабля "Монблан", который среди всего прочего перевозил 2300 тонн сухой и жидкой пикриновой кислоты. В результате взрыва Галифакс был практически полностью разрушен. 1963 человека погибли, 9 тысяч получили ранения, 2 тысячи человек пропали без вести, а общий ущерб от взрыва оценивается в 35 миллионов канадских долларов.
- На одной из фабрик во Франции вдоль железнодорожных путей образовались полосы пыли пикриновой кислоты. Значительное содержание кальция во влажной почве повлекло образование пикрата кальция. В жаркую сухую погоду он высох и вызвал пожар вдоль всех путей, по которым перемещали пикриновую кислоту.
Получение[править | править код]
Прямое нитрование фенола[править | править код]
Тринитрофенол может быть получен прямым нитрованием фенола в концентрированной азотной кислоте:
При этом идёт сильный разогрев, который приводит к разрушению и осмолению фенола, образованию различных побочных продуктов. Выход тринитрофенола низкий, в процессе происходит значительное разбавление кислоты. Тем не менее, этот способ был основным в период до и во время Первой мировой войны. Процесс осуществлялся в керамических горшках и обычно без перемешивания, поскольку растворы кислот корродировали металлы и загрязняли готовый продукт пикратами. Регулирование температуры также было затруднительно. Для преодоления недостатков этого способа были разработаны и нашли применение в производстве другие способы.
Синтез из фенола через фенолсульфокислоты[править | править код]
Из анисовой кислоты, содержащейся в анисовом, фенхелевом и ряде других эфирных масел, перегонкой выделяется анизол (масла Gaultheria procumbens, т. е. салицилово-метилового эфира[8]). Далее,
Фенол сильно окисляется (нитрирующей смесью), поэтому вначале его сульфируют, а потом нитруют азотной кислотой при нагревании. Следом за этим осуществляется электрофильное ипсо-замещение сульфогруппы на нитрогруппу.
Этим способом тринитрофенол получается из фенола последовательной обработкой серной и азотной кислотами. На первой стадии происходит сульфирование фенола до моно- и дисульфокислот, на второй стадии идёт нитрование сфенолсульфокислот с отщеплением сульфогрупп и образованием тринитрофенола:
Процесс также проводился в керамических горшках, стадии проводились последовательно. По сравнению с прямым нитрованием этот способ имеет как преимущества (меньшая опасность, отсутствие продуктов разложения фенола, более высокий выход), так и недостатки (значительно больший расход кислот). У этого способа много технологических разновидностей, которые можно объединить в две группы:
- нитрование в относительно слабых растворах кислот с применением избытка серной кислоты на первой стадии, последующего разбавления и обработкой 65%-ной азотной кислотой (обычный способ) или натриевой селитрой («французский способ»).
- нитрование в относительно крепких растворах кислот (метод Каста и его вариации). Крепкие кислоты позволяли использовать металлические аппараты с регулированием температуры и перемешиванием. По методу Каста сульфирование фенола проводилось в 20%-ном олеуме при соотношении 1:4 при температуре 90—100 °C в течение 5 часов, при этом образовывался дисульфофенол. Реакционная масса разбавлялась серной кислотой с плотностью 1,84 г/см³ (95,6 %), а затем проводилась нитрация азотной кислотой с плотностью 1,46 г/см³ (80 %) либо серно-азотной смесью.
Получение из бензола через хлорбензол[править | править код]
Процесс проводится в несколько стадий, некоторые оказались достаточно сложны в производстве и метод долго отрабатывался и получил распространение в период и после Первой мировой войны.
1. Хлорирование бензола до монохлорбензола:
- .
2. Нитрования монохлорбензола до динитрохлорбензола смесью серной и азотной кислот:
- .
3. Обработка динитрохлорбензола каустической содой (гидроокисью натрия) с получением динитрофенолята натрия:
- .
4. Омыление динитрофенолята натрия серной кислотой с получением динитрофенола:
- .
5. Получение тринитрофенола обработкой динитрофенола смесью серной и азотной кислот:
- .
Практический выход тринитрофенола 1,6 тонны на 1 тонну бензола (54 % от теоретического). Недостаток способа — большие отходы растворов соляной кислоты.
Применение[править | править код]
- Промежуточный продукт в производстве красителей. Им красили кожу, поскольку способен реагировать с белками в коже, давая темно-коричневый цвет.
- Катализатор реакций полимеризации (например, полибутадиена).
- компонент окрашивающего раствора Ван Гизона (Van Gieson) в гистологии.
- Травитель в металловедении (ГОСТ 2567-54). Например, для выявления субструктуры феррита применяется травитель (4 г пикриновой кислоты; 96 мл этилового спирта)[9]. В металлургии, 4% пикриновая кислота в этаноле называется «picral» и широко использовалась в оптической металлографии, чтобы выявить границы зерен в ферритных сталях. Из-за опасности была заменена другими химическими травителями. Тем не менее, она все еще используется для травления магниевых сплавов, таких как AZ31.
- Антисептическое средство.
- общеалкалоидный осадительный реактив.
- Пигмент для пометки лабораторных животных.
Хранение[править | править код]
Рекомендуется хранить в воде, поскольку тринитрофенол чувствителен к ударам и трению. Пикриновая кислота является особенно опасной, поскольку она является летучей и медленно сублимируется даже при комнатной температуре. Со временем накопление пикратов на открытых металлических поверхностях может представлять опасность взрыва.
Физиологическое воздействие[править | править код]
Тринитрофенол имеет очень горький вкус. Пыль раздражает дыхательные пути. Продолжительное вдыхание и контакт со слизистыми и кожей ведут к поражению почек, кожным болезням. Слизистые оболочки глаз приобретают характерный жёлтый цвет.
Дополнительно[править | править код]
Примечания[править | править код]
- ↑ 1 2 http://www.cdc.gov/niosh/npg/npgd0515.html
- ↑ https://www.lachimie.org/docs/org/ch8_alcools_phenols_thiols.pdf — С. 11.
- ↑ http://sciences-physiques.ac-montpellier.fr/ABCDORGA/Famille/Produit/ACIDEPICRIQUE.html
- ↑ Peter Woulfe (1771) Experiments to shew the nature of aurum mosaicum Архивная копия от 22 декабря 2016 на Wayback Machine. Philosophical Transactions of the Royal Society of London 61: 114—130. See pages 127—130: «A method of dying wool and silk, of a yellow colour, with indigo; and also with several other blue and red colouring substances.» and «Receipt for making the yellow dye.» — where Woulfe treats indigo with nitric acid («acid of nitre»).
- ↑ MÉMOIRE SUR L'INDIGO ET SES DISSOLVANS; Par M. Jean-Michel Haussmann, à Colmar. Дата обращения: 4 января 2018. Архивировано 5 января 2018 года.
- ↑ D`Ans, Ellen Lax. Taschenbuch für Chemiker und Physiker, Band II, Springer-Verlag 1964.
- ↑ A. Bernthsen: Kurzes Lehrbuch der organischen Chemie. Friedr. Vieweg & Sohn, Braunschweig 1914.
- ↑ Брокгауз и Ефрон. Брокгауз и Евфрон. Энциклопедический словарь, 2012..
- ↑ М.Беккерт, Х.Клемм. Справочник по металлографическому травлению..
Литература[править | править код]
- Шимозе // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- Справочник по производству взрывчатых веществ./ Под ред. И. В. Лебедева. — ОНТИ, Госхимтехиздат. — М., Л. — 1934. — с. 146—170.
- Fedoroff, Basil T. et al Enciclopedia of Explosives and Related Items, vol.1—7. — Dover, New Jersey: Picatinny Arsenal. — 1960—1975. — P285-P295.
- Волков И. Подрывные средства при устройстве заграждений. — М.: Государственное военное издательство, 1933.













