Кофермент Q: различия между версиями
| [отпатрулированная версия] | [отпатрулированная версия] |
A5b (обсуждение | вклад) (МНН: Ubidecarenone, Убидекаренон; также известен как ...==не был одобрен американским регулятором FDA |
A5b (обсуждение | вклад) →Кардиология: кокрейн из https://en.wikipedia.org/w/index.php?title=Coenzyme_Q10&action=history cc-by-sa 3 |
||
| Строка 146: | Строка 146: | ||
=== Кардиология === |
=== Кардиология === |
||
По данным независимого метаанализа 2014 года, проведенного коллаборацией Cochrane, не было обнаружено убедительных доказательств в пользу использования Кофермента Q10 при лечении [[Сердечная недостаточность|сердечной недостаточности]].<ref>{{cite journal |title= Coenzyme Q10 for heart failure |url= http://onlinelibrary.wiley.com/doi/10.1002/14651858.CD008684.pub2/full |journal= [[Cochrane Library|Cochrane Database of Systematic Reviews]] |issue= 6 |page= Art. no. CD008684 |nopp= yes |last1= Madmani |first1= M.E. |last2= Yusuf Solaiman |first2= A. |last3= Tamr Agha |first3= K. |last4= Madmani |first4= Y. |last5= Shahrour |first5= Y. |last6= Essali |first6= A. |last7= Kadro |first7= W. |displayauthors= 4 |department= Heart Group |publisher= [[John Wiley & Sons]] |date= 2 June 2014 |subscription= yes |via= [[Cochrane Library|The Cochrane Library]] |doi=10.1002/14651858.CD008684.pub2}} "no convincing evidence to support or refute"</ref> Также недостаточны доказательства того, что кофермент Q10 способствует снижению риска сердечных заболеваний.<ref>{{cite journal| last1=Flowers |first1=N| last2=Hartley |first2=L| last3=Todkill |first3=D |last4=Stranges |first4=S|last5=Rees|first5=K|title=Co-enzyme Q10 supplementation for the primary prevention of cardiovascular disease.|journal=The Cochrane database of systematic reviews|date=4 December 2014|volume=12|pages=CD010405|pmid=25474484|doi=10.1002/14651858.CD010405.pub2}}</ref> |
|||
| ⚫ | |||
| ⚫ | |||
* [[сердечная недостаточность|сердечной недостаточности]];<!-- |
* [[сердечная недостаточность|сердечной недостаточности]];<!-- |
||
Версия от 06:58, 4 октября 2015
| Кофермент Q | |
|---|---|
| Coenzyme Q10, Ubidecarenone | |
 | |
| Химическое соединение | |
| ИЮПАК | 2-[(2E,6E,10E,14E,18E,22E,26E,30E,34E)-3,7,11,15,19,23,27,31,35,39-декаметилтетраконта-2,6,10,14,18,22,26,30,34,38-декаенил]-5, 6-диметокси-3-метилциклогекса-2,5-диен-1,4-дион |
| Брутто-формула | C59H90O4 |
| Молярная масса | 863.34 |
| CAS | 303-98-0 |
| PubChem | 5281915 |
| DrugBank | 09270 |
| Состав | |
| Классификация | |
| АТХ | C01EB09 |
| Лекарственные формы | |
| БАД (в отдельных странах) | |
| Другие названия | |
| Убихиноны, Коэнзим Q, Ubiquinone, Убихинон, Кофермент Q10, Коэнзим Q10 | |
Кофермент Q (МНН: Ubidecarenone, Убидекаренон; также известен как кофермент Q10, убихинон, ubiquinone, coenzyme Q10, coenzyme Q) — это группа коферментов — бензохинонов, содержащих хиноидную группу (отсюда обозначение Q) и содержащих несколько изопрениловых групп (например, 10 в случае кофермента Q10).
Общие сведения
Убихиноны — это жирорастворимые коферменты, представленные преимущественно в митохондриях эукариотических клеток. Убихинон является компонентом цепи переноса электронов и принимает участие в окислительном фосфорилировании. Максимальное содержание убихинона в органах с наибольшими энергетическими потребностями, например, в сердце и печени.
История
В 1955 году был впервые употреблен термин кофермент Q для обозначения вещества, содержащегося практически во всех живых клетках. В 1957-58 годах учеными Фредериком Крейном и Карлом Фолкерсом были получены препараты убихинона и была установлена его химическая структура. В 1965 году Ямамура с сотрудниками впервые применили кофермент Q для лечения сердечно-сосудистых заболеваний. В 1978 году за описание процессов хемиосмотического фосфорилирования Питер Митчелл удостоен Нобелевской премии в области химии. В 1997 году основан Международный центр по изучению убихинона[уточнить].
Физико-химические свойства
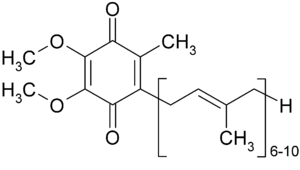
По химической природе кофермент Q имеет сходство в строении молекулы с витаминами Е и К и представляет собой 2,3-диметокси-5-метил-1,4-бензохинон с изопреновой цепью в 6-м положении. Число остатков изопрена в боковой цепи убихинон в разных организмах варьируется от 6 до 10. Такие варианты кофермента Q обозначают как Сo Q6, Сo Q7 и т. д.
В клетках Saccharomyces cerevisiae содержится Co Q6, Escherichia coli — Co Q8, грызунов — Co Q9. В митохондриях клеток большинства млекопитающих, включая человека, встречается убихинон только с 10 изопреновыми звеньями.[1]
Кофермент Q представляет собой желто-оранжевые кристаллы без вкуса и запаха. Температура плавления 49-51° С. Растворим в диэтиловом эфире, очень слабо растворим в этаноле, практически нерастворим в воде. На свету постепенно разлагается и окрашивается. С водой образует эмульсию с концентрацией 10 %, 20 % и 40 %.
Биосинтез убихинона
В организме человека кофермент Q синтезируется из мевалоновой кислоты и производных тирозина и фенилаланина.[1]
Биохимическая роль
Кофермент Q принимает участие в реакциях окислительного фосфорилирования, является компонентом цепи переноса электронов в митохондриях. Ингибиторы работы убихинона останавливают реакции окислительного фосфорилирования.
Кофермент Q является компонентом цепи переноса электронов, принимает участие в переносе электронов с NADH-дегидрогеназного комплекса (комплекс I) и сукцинатдегидрогеназного комплекса (II) на комплекс III, и участвует таким образом в синтезе АТФ.
Также кофермент Q является антиоксидантом и, в отличие от других антиоксидантов, регенерируется организмом. Кроме того, кофермент Q восстанавливает антиоксидантную активность витамина Е — α-токоферола.
Антиоксидантное действие кофермента Q обусловлено главным образом его восстановленной формой (Co QH2). Активность восстановленной формы кофермента Q на три порядка выше невосстановленной. Реакцию нейтрализации свободных радикалов восстановленным коферментом Q можно записать следующим образом 2LOO• + Co QH2 → 2LООН + Co Q.
Содержание в различных тканях организма
Кофермент Q необходим для нормальной жизнедеятельности живых организмов и, прежде всего, для функционирования тканей с высоким уровнем энергетического обмена. Наибольшая концентрация кофермента Q — в тканях сердечной мышцы. Естественный уровень кофермента Q в плазме крови человека составляет около 0.8-1.2 мкг/мл.[2][3]
Дефицит
Основными причинами, которые могут вести к дефициту CoQ10 у людей: уменьшение биосинтеза и повышенный расход организмом. Основным источником кофермента является биосинтез, для него требуется корректная работа по крайней мере 12 генов, и мутация в них может приводить к дефициту. Также дефицит Q10 может развиваться из-за других генетических дефектов, в частности из-за мутации митохондриальной ДНК, генов ETFDH, APTX, FXN, и BRAF[4]
Существует мнение, что старение (снижение функциональных возможностей сердца и других органов) связано со снижением концентрации кофермента Q[источник не указан 3128 дней]. Например, миокард людей старше 60 лет содержит на 40-60 % меньше кофермента Q, чем миокард молодых людей. Показано, что к двадцати годам концентрация кофермента Q в миокарде достигает максимума, к сорока годам содержание падает на 30 %, а к 60 годам — на 50 % от максимального значения.[источник не указан 3128 дней]
Снижение концентрации кофермента Q в организме может происходить и при различных заболеваниях. Некоторые исследователи[кто?] связывают дегенеративные заболевания (атеросклероз, болезнь Паркинсона, болезнь Альцгеймера) с недостатком естественного синтеза кофермента Q[источник не указан 3128 дней]. Дефицит кофермента Q может также возникать при гипертиреозе, гепатитах, бронхиальной астме.[источник не указан 3128 дней]
Содержание кофермента Q в различных продуктах
В разделе не хватает ссылок на источники (см. рекомендации по поиску). |
| Продукт | Содержание кофермента Q, мг (на 100 г продукта) |
|---|---|
| Красное пальмовое масло | 5,4 |
| Говядина жареная | 3,1 |
| Сельдь маринованная | 2,7 |
| Цыпленок жареный | 1,6 |
| Соевое масло | 8.7 |
| Радужная форель, на пару | 1,1 |
| Арахис | 2,8 |
| Кунжут | 1,8-2,3 |
| Фисташки | 2,1 |
| Брокколи варёная | 0,5 |
| Цветная капуста варёная | 0,4 |
| Апельсин | 0,2 |
| Клубника | 0,1 |
| Яйцо варёное | 0,1 |
В развитых странах ежедневное поступление Q10 с пищей оценивается отдельным исследованиями в 3-6 мг, большей частью из мяса[5].
Пищевые добавки с коферментом Q10
Кофермент Q10 не был одобрен американским регулятором FDA в качестве лекарственного средства для применения при каких-либо заболеваниях.[6]
Этот раздел статьи ещё не написан. |
Способы улучшения биодоступности кофермента Q10
Кофермент Q10 является жирорастворимым соединением с большим размером молекулы. Усвоение кофермента Q10 организмом происходит так же, как всех жирорастворимых веществ. Его всасывание, как и всех жирорастворимых веществ, происходит в тонком кишечнике с обязательным этапом предварительного эмульгирования желчью и образованием мицелл. В составе мицелл он проникает в клетки кишечника. Эффективность всасывания зависит от:
- Степени эмульгирования желчью кофермента Q10;
- Размеров образующихся после эмульгирования мицелл (не более 0,5 мкм);
- Площади поверхности активного всасывания в кишечнике;
- Присутствия других жиров в пище.
Производители[какие?] прибегают к использованию различных методов для улучшения биодоступности в выпускаемых препаратах кофермента Q10.
Уменьшение размеров частиц
Очевидным путем повышения биодоступности является уменьшение частиц кофермента Q10 до микро- и наноразмеров. На примере многих лекарственных веществ было показано, что уменьшение размеров частиц приводит к изменению биодоступности и эффективности [7]. Однако в целом, применительно к коферменту Q10[8], уменьшение размеров частиц не приводит к большому успеху в повышении биодоступности [9].
Заключение в капсулы с маслом
Хорошо известен тот факт, что всасывание жирорастворимых веществ улучшается, если в пище присутствуют липиды. Поэтому некоторые производители[какие?] для повышения биодоступности кофермента Q10 в препарате заключают его в капсулы с маслом.
Повышение растворимости в воде
Повышение биодоступности лекарственных веществ путем улучшения его растворимости в воде является часто используемым и применим также и к коэнзиму Q10. Примером такого подхода является получение водно-масляной микроэмульсии. Жирорастворимая форма Q10 с помощью пищевого эмульгатора переводится в водорастворимую форму, при этом образуются микроэмульсия, состоящая из водной фазы и ассоциатов Q10-эмульгатор. Технология молекулярного капсулирования позволяет переводить жирорастворимые вещества в водорастворимую форму; избежать в процессе всасывания этапа эмульгирования желчью жирорастворимого вещества; уменьшить размер частиц жирорастворимого вещества до всасываемых размеров. Это обеспечивает максимальное усваивание препарата, увеличивает биодоступность по сравнению с жирорастворимой формой Q10 в 2,6 раза[10] и делает препарат более эффективным.
Применение в медицине
Кардиология
По данным независимого метаанализа 2014 года, проведенного коллаборацией Cochrane, не было обнаружено убедительных доказательств в пользу использования Кофермента Q10 при лечении сердечной недостаточности.[11] Также недостаточны доказательства того, что кофермент Q10 способствует снижению риска сердечных заболеваний.[12]
Препараты на основе кофермента Q позиционируются отдельными авторами для применения при профилактики и терапии заболеваний сердечно-сосудистой системы. Было показано, что кофермент Q эффективен в комплексной терапии:
- сердечной недостаточности;[13]
- ишемической болезни сердца (стенокардия, инфаркт миокарда, постинфарктный кардиосклероз);[14][15]
- атеросклероза;[16][15]
- артериальной гипертонии;[17][18]
- кардиомиопатии;[19]
- диастолической дисфункции миокарда;[20]
- миокардиодистрофий различного происхождения;[20]
- нарушениях сердечного ритма и проводимости.[21]
За 20 лет (1989-2009) проведены десятки клинических исследований с участием тысяч больных с различными формами сердечно-сосудистых заболеваний. Большинство больных принимали кофермент Q в составе комплексной терапии сразу после выявления диагноза. У некоторых больных улучшение состояния было поразительным[уточнить]: сердце восстанавливало нормальные размеры и сократительную функцию. В более развитых формах заболевания полного восстановления не происходило, однако наблюдалось явное улучшение состояния.[22][13][17]
Сердечная недостаточность
Большинство исследований по клиническому применению кофермента Q10 было проведено именно при сердечной недостаточности. Также было показано, что тяжесть сердечной недостаточности коррелирует с низким уровнем кофермента Q.[23]
Наиболее масштабное исследование было проведено в 1994 году в Италии: в исследовании приняли участие 2 664 человека с сердечной недостаточностью.[24] За три месяца лечения у значительной части больных наблюдалось заметное улучшение состояния. При этом нормализовались следующие показатели: цианоз (у 78,1 %), отеки (у 78,6 %), субъективное ощущение больными аритмии (у 63,4 %), бессонница (у 66,28 %), головокружение (у 73,1 %). Побочные явления наблюдались у 36 больных (1,5 %), из которых только у двадцати человек они были связаны с применением кофермента Q.
Ишемическая болезнь сердца
Эффективность применения препаратов кофермента Q при ишемической болезни сердца подтверждена клиническими исследованиями. В одном из исследований 73 пациента после острого инфаркта миокарда наряду со стандартной терапией получали кофермент Q, участники контрольной группы (71 пациент) продолжали стандартную терапию. Через двенадцать месяцев применения было выявлено, что в группе, принимавшей препараты кофермента Q в 2 раза реже случались сердечно-сосудистые события (24 % против 45 %), нефатальные инфаркты миокарда (13,7 % против 25 %) и кардиальная смерть. При этом тошнота намного чаще отмечалась у больных контрольной группы (40,8 % против 6,8 %), что свидетельствует об отсутствии побочных эффектов.[15]
Выявлен возможный механизм положительного действия кофермента Q — предотвращение развития синдрома удлиненного QT. Как известно, данный синдром связан с более частой кардиальной смертью, особенно у больных инфарктом миокарда. Исследователи в течение 1 года наблюдали больных с острым инфарктом миокарда. Через 6 часов после начала острого инфаркта миокарда больные на фоне одинакового лечения, применяемого в постинфарктном периоде, получали либо плацебо, либо комплекс антиоксидантов, состоящий из кофермента Q и селена. У 40 % больных контрольной группы наблюдалось удлинение интервала QT > 440 мсек., в группе, получавшей антиоксиданты, удлинения интервала не наблюдалось. В течение года умерло от повторных инфарктов шесть больных контрольной группы и ни одного пациента из основной группы (за исключением одной смерти от некардиальной причины).[14]
В двойном слепом рандомизированном исследовании[каком?], включавшем 30 пациентов с миокардиопатией (со средним значением фракции выброса левого желудочка 26%), назначался кофермент Q или плацебо (каждый в течение 3 месяцев). Кофермент Q не влиял на объем выброса левого желудочка, гемодинамику и качество жизни.[источник не указан 3128 дней]
Атеросклероз
При атеросклерозе важную роль в патологии заболеваний играет перекисное окисление липидов. В норме данное состояние предотвращается за счет работы антиоксидантной системы (помимо кофермента Q в нее входят: витамин С, бета-каротин, альфа-токоферол и другие). С возрастом концентрация кофермента Q в тканях падает, в связи с чем возрастает риск возникновения и прогрессирования атеросклероза[источник не указан 3128 дней]. К настоящему моменту показано[кем?] положительное влияние приема кофермента Q на жировые отложения в дуге аорты у животных с моделированным атеросклерозом.[источник не указан 3128 дней]
Другой причиной атеросклероза является нарушение целостности эндотелия сосудов. Было показано[кем?], что кофермент Q улучшает эндотелиальную дисфункцию плечевой артерии у больных сахарным диабетом второго типа.[источник не указан 3128 дней]
Артериальная гипертензия
Было показано[кем?] гипотензивное действие кофермента Q. Были проанализированы 12 клинических исследований применения кофермента Q при артериальной гипертензии. Прием кофермента Q при артериальной гипертензии приводил к снижению систолического артериального давления в среднем на 16 мм рт. ст., а диастолического — на 10 мм рт. ст. Таким образом, кофермент Q может быть альтернативой лекарственным средствам, снижающим давление, либо усиливать эффект таких средств.[17]
Совместный прием кофермента Q и препаратов статинов
Статины представляют собой вещества, ингибиторующие 3-гидрокси-3-метилглутарил-коэнзим-А-редуктазу и снижающие синтез мевалоната - основного метаболического компонента на пути синтеза холестерина. Применение этих препаратов может вызывать жалобы пациентов на мышечную боль или миопатию. Так как путь к синтезу мевалоната также ведет к синтезу изопреноидной цепи кофермента Q10, различные исследования были посвящены изучению CoQ10 как возможного этиологического фактора статиновой миопатии. Данный вопрос широко изучался и хорошо описан в двух обзорных статьях [25][26]. Было подчеркнуто, что, помимо снижения концентраций CoQ10 в плазме, лечение статинами также приводит к снижению концентраций CoQ10 в лимфоцитах.
Несмотря на то, что не существует однозначных данных по эффекту статинов на концентрацию CoQ10 в скелетной мышце,[27][28] в 2005 году было показано, что высокие дозы статинов действительно приводят к снижению концентрации CoQ10 и уменьшению активности дыхательной цепи митохондрий в мышцах, что возможно связано со снижением числа или объема мышечных митохондрий [29].
В исследовании 2008 года была выявлена обратная зависимость между изменениями концентрации CoQ10, вызванными аторвастатином, и мозговым натрийуретическим пропептидом (МНПП). Был сделан вывод, что длительное лечение аторвастатином может увеличить уровни МНПП в плазме крови у пациентов с ишемической болезнью сердца при сопутствующем значительном снижении концентраций CoQ10.[30]
Что касается эффективости, в одном исследовании не было выявлено улучшения переносимости статинов или снижения миалгии[31], тогда как Касо и др.[32] сообщили о положительном эффекте CoQ10 на выраженность боли и влияние боли на повседневную активность в группе пациентов, получавших статины, с симптомами миопатии.
Педиатрия
В педиатрии кофермент Q применяют как для улучшения энергообмена в клетках, так и в качестве антиоксиданта.
Комплексная терапия кардиомиопатии
В 2003 году были опубликованы результаты небольшой работы, показавшей эффективность применения кофермента Q при идиопатической дилатационной кардиомиопатии у детей в возрасте от двух месяцев до одиннадцати лет.[33] Дети после стабилизации состояния в дополнение к традиционной терапии получали кофермент Q в дозе 10 мг/кг в сутки. В результате проводимого лечения было зафиксировано достоверное улучшение сердечной функции. У 5 из 6 детей отмечено уменьшение класса сердечной недостаточности на 2 класса, у шестого ребёнка — на 1 класс. Также было отмечено улучшение фракции укорочения (на 17-30 %), увеличение фракции выброса (на 40-60 %).
Опубликованы результаты более крупного исследования эффективности и безопасности препаратов кофермента Q для лечения идиопатической хронической дилатационной кардиомиопатии у детей.[34] Пятнадцать детей в возрасте от шести месяцев до шестнадцати лет получали 3 мг/кг в сутки кофермента Q в дополнение к обычной терапии на протяжении по меньшей мере девяти месяцев. По результатам исследования было отмечено улучшение класса сердечной недостаточности, что свидетельствует об улучшении сердечной функции.
Нарушения сердечного ритма и проводимости
В разделе не хватает ссылок на источники (см. рекомендации по поиску). |
Показана роль дегенеративно-дистрофических и свободнорадикальных процессов в патогенезе нарушений сердечного ритма и проводимости у детей. Эффективность кофермента Q изучали в комплексной терапии детей с нарушениями сердечного ритма. При экстрасистолии II—III функционального класса кофермент Q оказывал общее противоаритмическое действие в 63 % случаев, вызывая у четверти больных полное подавление аритмии. У детей с рефрактерными желудочковыми и суправентрикулярными тахиаритмиями препараты кофермента Q увеличивают эффективность традиционных противоаритмических препаратов и предупреждают возникновение осложнений.
Также показана эффективность применения препаратов кофермента Q у детей с нарушенными процессами реполяризации (хронические тахиаритмии, синдром удлиненного интервала Q-Т, кардиомиопатии, экстрасистолии, синдром слабости синусового узла).[21]
Комплексная терапия часто болеющих детей
По мнению некоторых ученых одним из факторов риска попадания ребенка в группу «часто болеющих детей» является дефицит энергии. Поэтому таким детям целесообразно применять препараты, улучшающие процессы энергетического обмена. Применение препаратов кофермента Q позволяет существенно улучшить состояние здоровья часто болеющих детей, стабилизируя в том числе механизмы вегетативной регуляции и клеточного энергообмена.[3]
Вегетативная дистония
Прием препаратов кофермента Q помогает корректировать дисфункции миокарда у детей с вегетативной дистонией, способствует уменьшению других ее клинических проявлений (нарушения сна, утомляемость, головные боли, кардиалгии).[35]
Пиелонефрит
Многие заболевания почек сопровождаются значительной активацией перекисного окисления липидов и снижением содержания антиоксидантов в крови. В связи с этим при некоторых воспалительных заболеваниях неспецифической этиологии, наряду с общепринятым медикаментозным лечением оправдано назначение антиоксидантов. Применение кофермента Q в комплексной терапии пиелонефрита у детей в период стихания заболевания способствует снижению активности перекисного окисления липидов, повышению активности внутриклеточных ферментов и АОА-плазмы в целом, способствует детоксикации и улучшению аппетита.[36]
Таким образом, препараты кофермента Q эффективны в комплексной терапии заболеваний различной этиологии. Прием препаратов кофермента Q способствует также улучшению сна, повышает уровень восприятия физических и интеллектуальных нагрузок, нормализует механизмы вегетативной регуляции.[источник не указан 3128 дней]
Примечания
- ↑ 1 2 Березов Т. Т., Коровкин Б. Ф. Биологическая химия: учебник. — М.: Медицина, 1998. — 704 с.
- ↑ PMC3257126 "The CoQ10 normal value range in human plasma is 0.8–1.2 mg/L."
- ↑ 1 2 Ключников С. О., Гнетнева Е. С. Убихинон. Теория и клиническая практика // Педиатрия им. Сперанского. — 2008. — № 3.
- ↑ Trevisson E, Dimauro S, Navas P, Salviati L (October 2011). "Coenzyme Q deficiency in muscle". Curr. Opin. Neurol. 24 (5): 449—56. doi:10.1097/WCO.0b013e32834ab528. PMID 21844807.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ "Relative Bioavailability of Two Forms of a Novel Water-Soluble Coenzyme Q10". Annals of Nutrition and Metabolism. 52 (4): 281—7. 2008. doi:10.1159/000129661. PMID 18645245.
- ↑ White, J. Coenzyme Q10–for health professionals (PDQ®) (англ.). National Cancer Institute (14 мая 2014). Дата обращения: 29 июня 2014.
- ↑ Mathiowitz E, Jacob JS, Jong YS, Carino GP, Chickering DE, Chaturvedi P, Santos CA, Vijayaraghavan K, Montgomery S, Bassett M, Morrell C Biologically erodable microspheres as potential oral drug delivery systems.//Nature, 1997 ;386(6623):410-4
- ↑ C-H Hsu, Z Cui, RJ Mumper and M Jay. Preparation and Characterization of Novel Coenzyme Q10 Nanoparticles Engineered from Microemulsion Precursors. AAPS PharmSciTech. 2003; 32:269-280
- ↑ Joshi SS, Sawant SV, Shedge A, Halpner AD. Comparative bioavailability of two novel coenzyme Q10 preparations in humans. Int J Clin Pharmacol Ther 2003 Jan;41(1):42-48
- ↑ Каленикова Е.И., Городецкая Е.А., Медведев О.С. Фармакокинетика коэнзима Q10 // Бюллетень экспериментальной биологии и медицины. – 2008. – Т. 146. – № 9, стр 288
- ↑ Madmani, M.E.; Yusuf Solaiman, A.; Tamr Agha, K.; Madmani, Y.; Shahrour, Y.; Essali, A.; Kadro, W. (2 June 2014). "Coenzyme Q10 for heart failure". Heart Group. Cochrane Database of Systematic Reviews. John Wiley & Sons (6): Art. no. CD008684. doi:10.1002/14651858.CD008684.pub2 – via The Cochrane Library.
{{cite journal}}: Неизвестный параметр|displayauthors=игнорируется (|display-authors=предлагается) (справка); Неизвестный параметр|nopp=игнорируется (|no-pp=предлагается) (справка); Неизвестный параметр|subscription=игнорируется (|url-access=предлагается) (справка) "no convincing evidence to support or refute" - ↑ Flowers, N; Hartley, L; Todkill, D; Stranges, S; Rees, K (4 December 2014). "Co-enzyme Q10 supplementation for the primary prevention of cardiovascular disease". The Cochrane database of systematic reviews. 12: CD010405. doi:10.1002/14651858.CD010405.pub2. PMID 25474484.
- ↑ 1 2 Mortensen SA. Overview of coenzyme Q10 as adjunctive therapy in chronic heart failure. Rationale, design and end-points of «Q-symbio» — a multinational trial // Biofactors. — 2003. — № 18. — Р. 79-89. — PMID 14695923
- ↑ 1 2 Kuklinski B, Weissenbacher E, Fahnrich A. Coenzyme Q10 and antioxidants in acute myocardial infarction // Molecular Aspects of Medicine. — 1994. — № 15. — P.143-147.
- ↑ 1 2 3 Singh RB, Neki NS et al. Effect of coenzyme Q10 on risk of atherosclerosis in patients with recent myocardial infarction // Molecular and Cell Biochemistry. — 2003. — № № 1-2. — Р. 75-82. — PMID 12841346
- ↑ Ланкин В. З., Капелько В. И., Руге Э. К., Тихазе А. К., Беленков Ю. Н. Коэнзим Q10: физиологическая функция и перспективы использования в комплексной терапии заболеваний сердечно-сосудистой системы. Пособие для врачей. — М.: Медпрактика-М. — 2008. — С. 22.
- ↑ 1 2 3 Rosenfeldt F, Haas SJ, Krum H. Hadj A, Ng K, Leon JY, Watts GF. Coenzym Q10 in the treatment of hypertension: a meta-analysis of clinical trials // Journal of Human Hypertension. — 2007. — № 21(4). — Р. 297—306.
- ↑ Singh RB, Niaz MA, Rastogi SS. et al. Effect of hydrosoluble coenzyme Q10 on blood pressures and insulin resistance in hypertensive patients with coronary artery disease // Journal of Human Hypertension. — 1999. — V.13. — № 3. — Р. 203—208. — PMID 10204818.
- ↑ Langsjoen PH, Folkers K, Lyson K, Muratsu K, Lyson T, Langsjoen P. Pronounced increase of survival of patients with cardiomyopathy when treated with coenzyme Q10 and conventional therapy // International Journal of Tissue Reaction. — 1990. — V.12. — № 3. — Р. 163—168
- ↑ 1 2 Langsjoen PH, Langsjoen A, Willis R, Folkers K.Treatment of hypertrophic cardiomyopathy with coenzyme Q10 // Molecular Aspects of Medicine. — 1997. — № 18. Р. 145—151.
- ↑ 1 2 Кравцова Л. А., Березницкая В. В., Школьникова М. А. Применение коэнзима Q10 в кардиологической практике // Российский вестник перинатологии и педиатрии. — 2007. — Т. 52. — № 6. — С. 51-58.
- ↑ Morisco C, Nappi A, Argenziano L et al. Noninvasive evaluation of cardiac hemodynamic during exercise in patients with chronic heart failure: effects of short-term coenzyme Q10 treatment // Molecular Aspects of Medicine. — 1994. — № 15. — Р. 155—163.
- ↑ Mortensen SA, Vadhanavikit S, Folkers K. Deficiency of coenzyme Q10 in myocardial failure // Drugs under Experimental and Clinical Research. — 1984. — № 7. — Р. 497—502.
- ↑ Baggio E, Gandini R et al . Italian multicenter study on the safety and efficacy of coenzyme Q10 as adjunctive therapy in heart failure. CoQ10 Drug Surveillance Investigators // Molecular Aspects of Medicine. — 1994 — № 15. — Р. 287—294.
- ↑ Littarru (2007). "Coenzyme Q10 and statins: biochemical and clinical implications". Mitochondrion: S168-74. PMID 17482884.
{{cite journal}}:|first2=пропущен|last2=(справка);|first3=пропущен|last3=(справка); Шаблон цитирования имеет пустые неизвестные параметры:|1=(справка) - ↑ Marcoff (2007). "The role of coenzyme Q10 in statin-associated myopathy: a systematic review". J Am Coll Cardiol. 49 (23): 2231—7. PMID 17560286.
{{cite journal}}:|first2=пропущен|last2=(справка); Шаблон цитирования имеет пустые неизвестные параметры:|1=(справка) - ↑ Lamperti (2005). "Muscle coenzyme Q10 level in statin-related myopathy". Arch Neurol. 62 (11): 1709—12. PMID 16286544.
{{cite journal}}:|first2=пропущен|last2=(справка) - ↑ Laaksonen (1995). "Decreases in serum ubiquinone concentrations do not result in reduced levels in muscle tissue during short-term simvastatin treatment in humans". Clin Pharmacol Ther. 57 (1): 62–6. PMID 7828383.
{{cite journal}}:|first2=пропущен|last2=(справка) - ↑ Päivä (2005). "High-dose statins and skeletal muscle metabolism in humans: a randomized, controlled trial". Clin Pharmacol Ther. 78 (1): 60–8. PMID 16003294.
{{cite journal}}:|first2=пропущен|last2=(справка) - ↑ Suzuki (2008). "Atorvastatin-induced changes in plasma coenzyme Q10 and brain natriuretic peptide in patients with coronary artery disease". Int Heart J. 49 (4): 423–33. PMID 18753726.
{{cite journal}}:|first2=пропущен|last2=(справка) - ↑ Young (2007). "Effect of coenzyme Q10 supplementation on simvastatin-induced myalgia". Am J Cardiol. 100 (9): 1400–3. PMID 17950797.
{{cite journal}}:|first2=пропущен|last2=(справка);|first3=пропущен|last3=(справка) - ↑ Caso (2007). "Effect of coenzyme Q10 on myopathic symptoms in patients treated with statins". Am J Cardiol. 99 (10): 1409–12. PMID 17493470.
{{cite journal}}:|first2=пропущен|last2=(справка) - ↑ Elshershari H, Ozer S, Ozkutlu S, Ozme S. Potential usefulness of coenzyme Q10 in the treatment of idiopathic dilated cardiomyopathy in children. // International Journal of Cardiology. — 2003. — V. 88. — № 1. — Р. 101—102.
- ↑ 26.Soongswang J, Sangtawesin C, Durongpisitkul K, Laohaprasitiporn D, Nana A, Punlee K, Kangkagate C. The effect of coenzyme Q10 on idiopathic chronic dilated cardiomyopathy in children. // Pediatric Cardiology. — 2005. — № 4. — Р.361-366.
- ↑ Коровина Н. А., Творогова Т. М., Тарасова А. А., Захарова И. Н., Хрунова К. М. Эффективность энерготропной терапии при вегетативной дистонии с кардиальными изменениями у детей и подростков // Российский вестник перинатологии и педиатрии. — 2008. — № 6.
- ↑ Захарова И. Н., Обыночная Е. Г., Скоробогатова Е. В., Малашина О. А. Влияние антиоксиданта на основе убихинона на активность перекисного окисления липидов и антиоксидантную защиту при пиелонефрите у детей // Педиатрия. — 2005. — № 4.