Линезолид
| Линезолид | |
|---|---|
 | |
 | |
| Химическое соединение | |
| ИЮПАК | (S)-N-({3-[3-фторо-4-(морфонил-4-ил)фенил]-2-оксо-1,3-оксазолидин-5-ил}метил)ацетамид |
| Брутто-формула | C16H20FN3O4 |
| Молярная масса | 337.346 г/моль |
| CAS | 165800-03-3 |
| PubChem | 441401 |
| DrugBank | APRD01073 |
| Состав | |
| Классификация | |
| АТХ | J01XX08 |
| Фармакокинетика | |
| Биодоступн. | ~100 % (перорально) |
| Связывание с белками плазмы | низкая (31 %) |
| Метаболизм | в печени (50-70 %, CYP not involved) |
| Период полувывед. | 4.2-5.4 ч (короче у детей) |
| Экскреция | непочечная, почками и с калом |
| Лекарственные формы | |
| гранулы для приготовления суспензии для приёма внутрь; раствор для инфузий; таблетки, покрытые плёночной оболочкой. | |
| Способы введения | |
| внутривенное, пероральное | |
| Другие названия | |
| Зивокс® (Zivox®), Амизолид (Amizolid), Зеникс (Zenix), Линезолид-Тева (Linezolid-Teva) | |
Линезолид (МНН) — синтетический антибиотик, используемый для лечения тяжёлых инфекционных заболеваний, вызванных грамположительными бактериями, которые устойчивы к другим антибиотикам. Представитель класса оксазолидинонов, линезолид является активным по отношению к большинству грамположительных бактерий, которые вызывают болезни, включая стрептококки, устойчивые к ванкомицину энтерококки и метициллин-резистентный золотистый стафилококк.[1] Основными показаниями линезолида являются инфекционные заболевания кожи, мягких тканей и пневмония (в частности, госпитальная пневмония), хотя становится популярным его использование при различных других инфекционных заболеваниях.
Открытый в 1990-х годах и впервые одобренный для использования в 2000 году, линезолид был первым, и до 2014 года единственным, коммерчески доступным антибиотиком класса оксазолидинона. В 2014 году в США был одобрен к применению следующий антибиотик этого класса — тедизолид. Как ингибитор синтеза белков, линезолид останавливает рост бактерий, нарушая у них биосинтез белка. Хотя многие антибиотики действуют подобным образом, точный механизм действия линезолида представляется уникальным для класса оксазолидинонов. Устойчивость бактерий к линезолиду остаётся очень низкой (первые сообщения были в 1999 году), однако она может возрасти.
При приёме внутрь в течение коротких периодов линезолид относительно безопасен; он может быть использован у пациентов всех возрастов и у людей с заболеваниями печени или почечной недостаточностью. Общие побочные эффекты краткосрочного приёма включают головную боль, диарею и тошноту. Длительное применение, однако, связано с серьёзными побочными эффектами; линезолид может вызвать подавление функции костного мозга и тромбоцитопению, особенно при его использовании более двух недель. Применение линезолида на более длительный период может привести к периферической невропатии (которая может быть необратимой), поражению зрительного нерва и лактатацидозу (накопление молочной кислоты в организме). Всё это возникает, скорее всего, в связи с токсическим поражением митохондрий.
Линезолид является достаточно дорогим препаратом, а курс лечения может стоить до нескольких тысяч долларов США;[2] тем не менее, он представляется более рентабельным, чем сопоставимые антибиотики,[3] главным образом в связи с возможностью перехода от внутривенного на пероральный метод введения, как только состояние пациента стабилизируется, без необходимости коррекции доз.
История[править | править код]
Оксазолидиноны были известны как ингибиторы моноаминоксидазы с конца 1950-х годов. Их антибактериальные свойства были обнаружены исследователями E.I. duPont de Nemours в 1970-х годах.[4] В 1978 году DuPont запатентовала ряд производных оксазолидинона как эффективные в лечении бактериальных и грибковых заболеваний растений, а в 1984 году другой патент описал их эффективность в лечении бактериальных инфекций у млекопитающих.[4][5] В 1987 году учёные DuPont представили подробное описание оксазолидинонов как новый класс антибиотиков с новым механизмом действия.[4][6] Однако обнаружилось, что синтезированные в те времена соединения были токсичны для печени и разработки были прекращены.[7]
Компания Pharmacia & Upjohn (теперь часть Pfizer) начала свою собственную программу исследований оксазолидинона в 1990-х годах. Исследования соединений «структура-активность» привели к разработке нескольких подклассов производных оксазолидинона с различными профилями безопасности и антимикробной активности. Два соединения рассматривались как кандидаты в лекарства: эперезолид (кодовое название PNU-100592) и линезолид (PNU-100766).[8][9] На доклинических стадиях разработок они были схожи по антибактериальной активности и безопасности, поэтому они перешли в фазу I клинических испытаний с целью выявления любых различий в фармакокинетике.[7][10] Было обнаружено, что линезолид имеет фармакокинетические преимущества. Его можно принимать только два раза в день, в то время как эперезолид необходимо принимать 3 раза в день для достижения аналогичного эффекта. Поэтому линезолид был выбран для дальнейших исследований.[8] FDA разрешило применение линезолида 18 апреля 2000 года.[11] В последующим препарат был разрешён в Бразилии (июнь 2000 г.),[12] Великобритании (январь 2001),[9][13] Японии и Канаде (апрель 2001),[14][15][16] Европе (в течение 2001 года),[17] и в других странах Латинской Америки и Азии.[15]
На сегодняшний день (февраль 2019 года) линезолид — один из двух антибиотиков-оксазолидинонов, доступных на фармакологическом рынке (вместе с тедизолидом).[18] Другие представители этого класса в стадии разработки, например посизолид (AZD2563),[19] ранбезолид (RBX 7644),[20] торезолид (TR-701),[18][21] и радезолид (RX-1741).[22]
Спектр активности[править | править код]
Линезолид эффективен против всех клинически значимых грамположительных бактерий, клеточная стенка которых содержит толстый слой пептидогликанов и они не имеют наружной мембраны. К ним относят Enterococcus faecium и Enterococcus faecalis (включая ванкомицин-устойчивые энтерококки), золотистый стафилококк (включая метициллин-устойчивый золотистый стафилококк, англ. MRSA), Streptococcus agalactiae, пневмококк, Streptococcus pyogenes, зеленящие стрептококки, Listeria monocytogenes и Corynebacterium (последние наиболее восприимчивы к линезолиду с минимальной ингибирующей концентрацией обычно ниже 0,5 мг/л).[1][5][23] Линезолид также весьма активен in vitro против некоторых микобактерий.[5] Предполагают, что он очень эффективен против Nocardia, но из-за высокой стоимости и потенциально серьёзных побочных эффектов, авторы рекомендовали комбинировать с другими антибиотиками или применять только как резервный антибиотик в случаях, когда традиционное лечение не эффективно.[24]
Считают, что линезолид обладает бактериостатическим действием против большинства микроорганизмов (то есть, он останавливает их рост и размножение, фактически не убивая их), но также обладает бактерицидным действием в отношении стрептококков.[1][25] Некоторые авторы отмечают, что, несмотря на его бактериостатическое действие in vitro, линезолид «ведёт себя» как бактерицидный антибиотик in vivo, поскольку он ингибирует образование токсинов стафилококков и стрептококков.[8] Он также обладает постантибиотиковым действием на большинство бактерий от одного до четырёх часов, что означает временное подавление роста бактерий даже после прекращения приёма препарата.[26]
Грамотрицательные бактерии[править | править код]
Линезолид не имеет клинически значимого действия на большинство грамотрицательных бактерий. Pseudomonas и энтеробактерии, например, не восприимчивы к его действию.[25] In vitro он активен в отношении Pasteurella multocida,[1][27] фузобактерий, Moraxella catarrhalis, легионелл, бордетелл, Elizabethkingia meningoseptica и умеренно активен (с минимальной подавляющей концентрацией для 90 % штаммов 8 мг/л) в отношении гемофильной инфекции.[25][28] Линезолид также показал хороший эффект как препарат второй линии для лечения инфекций Capnocytophaga.[29][30]
Подобные антибиотики[править | править код]
Спектр активности линезолида в отношении грамположительных бактерий похож на спектр гликопептидного антибиотика ванкомицина, который уже давно входит в стандарт лечения инфекций MRSA и эти 2 препарата часто сравнивают.[26][31] К другим подобным антибиотикам относят тейкопланин, квинупристин/дальфопристин (Synercid, сочетание двух стрептограминов, не активен в отношении Е. faecalis)[7] и даптомицин (Cubicin, липопептид). Также некоторые препараты находятся на стадии разработки, такие как цефтобипрол, далбаванцин и телаванцин. Только линезолид можно применять перорально.[26] В будущем оритаванцин и иклаприм могут стать альтернативой пероральной форме линезолида. Оба препарата находятся на ранней стадии клинических разработок.[26]
Показания[править | править код]
Основное показание линезолида — лечение тяжёлых инфекций, вызванных грамположительными бактериями, устойчивыми к другим антибиотикам. Препарат не должен применяться против бактерий, которые чувствительны к антибиотикам с более узким спектром действия, таким как пенициллины и цефалоспорины. В популярной прессе и научной литературе, линезолид был назван «резервным антибиотиком», который следует использовать с осторожностью как препарат «последней инстанции» в отношении потенциально неразрешимых инфекций.[32][33]
В США, FDA-утверждёнными показаниями для использования линезолида являются: ванкомицин-устойчивые энтерококковые инфекции с или без бактериемии; госпитальные и внегоспитальные пневмонии, вызванные золотистым стафилококком или пневмококком; осложнённые кожные инфекции (англ. cSSSI), вызванные чувствительными бактериями, в том числе инфекции диабетической стопы, если осложняется остеомиелитом, и неосложнённые инфекции кожи и мягких тканей, вызванные S. pyogenes или золотистым стафилококком. Производитель не рекомендует использование линезолида при внегоспитальных пневмониях или неосложнённых инфекциях кожи и мягких тканей, вызванных MRSA.[1] В Великобритании пневмония и cSSSI — единственные показания, отмеченные в маркировке продукции.[13]
Полагают, что линезолид безопасен и эффективен для применения у детей и новорождённых так же, как и у взрослых.[26]
Инфекции кожи и мягких тканей[править | править код]
Крупный мета-анализ рандомизированных контролируемых исследований показал, что линезолид эффективнее гликопептидных антибиотиков (например, ванкомицина и тейкопланина) и бета-лактамных антибиотиков, при лечении инфекций кожи и мягких тканей (англ. SSTIs), вызванных грамположительными бактериями[34]. Также небольшие исследования подтвердили превосходство линезолида над тейкопланином при лечении всех тяжёлых грамположительных инфекций.[35]
При лечении синдрома диабетической стопы, линезолид, как полагают, дешевле и эффективнее ванкомицина.[36] В открытом исследовании 2004 года линезолид был также эффективен, как и ампициллин/сульбактам, ко-амоксиклав и намного эффективнее у пациентов с язвами нижних конечностей и без остеомиелита, но со значительно более высоким уровнем побочных эффектов.[37][38] Однако мета-анализ 2008 года 18 рандомизированных контролируемых исследований показал, что лечение линезолидом бывает неэффективным так же часто, как и лечение другими антибиотиками, независимо от наличия или отсутствия у больного остеомиелита.[39]
Некоторые авторы рекомендуют применение комбинации более дешёвых и более экономически эффективных препаратов (например, ко-тримоксазола с рифампицином или клиндамицином) перед назначением линезолида при лечении SSTI, когда восприимчивость возбудителя это позволяет.[38][40]
Пневмония[править | править код]
Как полагают, нет существенной разницы в отношении эффективности лечения между линезолидом, гликопептидами или соответствующими бета-лактамными антибиотиками при лечении пневмонии.[34] Клинические руководства по лечению внегоспитальной пневмонии, разработанные Американским торакальным обществом и Обществом инфекционных заболеваний Америки, рекомендуют линезолид как резервный антибиотик для случаев, когда MRSA подтверждена как возбудитель или когда предполагается MRSA инфекция на основе клинических проявлений.[41] Руководство Британского торакального общества не рекомендует его для лечения первой линии, а скорее как альтернативу ванкомицину.[42] Линезолид также приемлем как препарат второй линии при лечении внегоспитальной пневмококковой пневмонии, когда существует устойчивость к пенициллину.[41]
Руководства США рекомендуют как линезолид, так и ванкомицин в качестве препарата первой линии для лечения госпитальных (нозокомиальных) пневмоний MRSA.[43] Некоторые исследования показали, что линезолид лучше, чем ванкомицин против внутригоспитальных пневмоний, особенно вентилятор-ассоциированной пневмонии[англ.], вызванной MRSA, возможно потому, что проникновение линезолида в бронхиальную жидкость значительно выше, чем ванкомицина. Однако поднятые несколько вопросов по дизайну исследования ставят под сомнение результаты, которые указывают на превосходство линезолида.[38] Несмотря на это, преимущества линезолида включают высокую биодоступность (так как он позволяет легко переходить на пероральную терапию), а также тот факт, что нарушение функции почек не является препятствием для его использования (в то время как достичь правильной дозировки ванкомицина у больных с почечной недостаточностью очень сложно).[43]
Неутверждённые показания[править | править код]
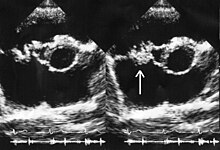
Традиционно считается, что так называемые «глубокие» инфекции, такие как остеомиелит или инфекционный эндокардит, следует лечить бактерицидными антибиотиками, а не бактериостатическими. Тем не менее, доклинические исследования были проведены для оценки эффективности линезолида при этих инфекциях[8] и препарат успешно применяется для их лечения в клинической практике. Полагают, что линезолид является оправданным терапевтическим вариантом для инфекционного эндокардита, вызванного несколькими устойчивыми грамположительными бактериями, несмотря на отсутствие высококачественных доказательств в пользу такого применения.[45][46] Результаты лечения энтерококкового эндокардита варьировали, в некоторых случаях лечение было успешно, а в других ответа на терапию не было.[47][48][49][50][51][52] Доказательства низкого и среднего качества также установили возможность его использования при инфекционных поражениях в костях и суставах, в том числе при хроническом остеомиелите, хотя побочные эффекты вызывают серьёзную озабоченность при длительном применении препарата.[53][54][55][56][57][58]
В сочетании с другими препаратами линезолид был использован для лечения туберкулёза.[59] Оптимальная доза для этой цели не была установлена. У взрослых дозировки 1 и 2 раза в день были использованы с достижением хорошего эффекта. Часто требуется много месяцев лечения и скорость развития побочных эффектов сильно зависит от дозы.[60][61] Недостаточно надёжных доказательств эффективности и безопасности этого показания для постоянного применения.[26]
Линезолид изучен в качестве альтернативы ванкомицину при лечении фебрильной нейтропении у онкологических больных, при подозрении на грамположительную инфекцию.[62] Он также является одним из немногих антибиотиков, которые диффундируют в стекловидное тело и поэтому линезолид может быть эффективен при лечении эндофтальмита, вызванного чувствительными бактериями. Опять же, мало доказательств для его использования при таком состоянии, так как инфекционный эндофтальмит широко и эффективно лечится ванкомицином, который вводится непосредственно в глаз.[38]
Инфекции центральной нервной системы[править | править код]
В исследованиях на животных пневмококкового менингита, было обнаружено, что линезолид хорошо проникает в спинномозговую жидкость, но его эффективность меньше, чем у других антибиотиков.[5][63] Полагают, что не появится достаточное количество доказательств высокого качества в пользу рутинного применения линезолида для лечения бактериального менингита. Тем не менее, линезолид успешно применяется во многих случаях инфекций центральной нервной системы, включая менингит, вызванных чувствительными бактериями, а также он был предложен как оправданный выбор при этих показаниях, когда варианты лечения ограничены или когда другие антибиотики не эффективны.[29][64] Руководство Общества по инфекционным болезням Америки рекомендует линезолид как препарат выбора при менингите VRE и в качестве альтернативы ванкомицину при менингите MRSA.[65] Считают, что линезолид превосходит ванкомицин при лечении внегоспитальной MRSA инфекции центральной нервной системы, хотя и очень мало сообщений было опубликовано о случаях таких инфекций (по состоянию на 2009 год).[66]
Катетер-ассоциированные инфекции[править | править код]
В марте 2007 года, FDA сообщил о результатах рандомизированного открытого клинического испытания в III фазе, где сравнивался линезолид с ванкомицином при лечении катетер-ассоциированных инфекций крови. Пациентам получаемое лечение ванкомицином может быть заменено на оксациллин или диклоксациллин, если бактерии, вызывающие инфекцию, восприимчивы, а пациенты в обеих группах (линезолида и ванкомицина) при необходимости могут получать специфическое лечение в отношении грамотрицательных бактерий.[67] Само исследование было опубликовано в январе 2009 года.[68]
Линезолид ассоциировался с большей смертностью, чем сравниваемые с ним антибиотики. Когда были собраны данные по всем участникам, исследование показало, что 21,5 % из тех, кто получал линезолид, умерли по сравнению с 16 % умерших в группе, где его не получали. Такая разница объясняется недостаточной эффективностью линезолида в лечении только грамотрицательных инфекций или смешанной грамположительной/грамотрицательной инфекции. Только в группе участников с грамположительной инфекцией безопасность и эффективность линезолида и ванкомицина оказались одинаковы.[67][68] В свете этих результатов, FDA издало предупреждение для работников здравоохранения, что линезолид не одобрен для лечения катетер-ассоциированных инфекций или инфекций, вызванных грамотрицательными бактериями.[67]
Побочные эффекты[править | править код]
При использовании в течение короткого периода линезолид является относительно безопасным препаратом.[31] Общие побочные эффекты линезолида (возникающие у более чем 1 % людей, принимающих линезолид) включают диарею (по сведениям, у 3-11 % участников клинических испытаний), головную боль (1-11 %), тошноту (3-10 %), рвоту (1-4 %), сыпь (2 %), запор (2 %), изменение восприятия вкуса (1-2 %) и изменение цвета языка (0.2-1 %).[2] Могут возникать грибковые инфекции, такие как оральный и вагинальный кандидоз, так как линезолид подавляет бактериальную флору в организме и открывает нишу для грибов (так называемый антибиотиковый кандидоз).[2] Менее распространённые (и потенциально более серьёзные) побочные эффекты — аллергические реакции, панкреатит и повышение уровня трансаминаз, что может быть признаком поражения печени.[2][9] В отличие от некоторых антибиотиков, таких как эритромицин, и хинолонов, линезолид не влияет на интервал QT на ЭКГ, который показывает электрическую проводимость сердца.[9][69] У детей побочные эффекты такие, как и у взрослых.[69]
Как почти все антибиотики, линезолид ассоциирован с возникновением Clostridium difficile-ассоциированной диареи (CDAD) и псевдомембранозного колита, хотя последний редок, возникая у одного из двух тысяч пациентов в клинических испытаниях.[2][9][69][70] C. difficile , как полагают, восприимчив к линезолиду in vitro и препарат даже рассматривают для возможного лечения CDAD.[71]
Длительное применение[править | править код]
Подавление функции костного мозга, проявляющееся в частности тромбоцитопенией (уменьшение количества тромбоцитов), может возникнуть при лечении линезолидом; полагают, что это единственный побочный эффект, который возникает значительно чаще при использовании линезолида, чем при применении гликопептидов или бета-лактамов.[34] Он редко возникает у больных, получающих препарат в течение 14 дней или меньше, но встречается гораздо чаще у пациентов, которые получают линезолид более длительным курсом или у которых есть почечная недостаточность.[9][72]
Длительное использование линезолида также ассоциировано с периферической невропатией и оптической невропатией, которые является наиболее распространёнными после нескольких месяцев лечения и могут быть необратимыми.[73][74][75][76] Хотя механизм повреждения всё ещё не совсем понятен, токсическое повреждение митохондрий предполагают в качестве причины;[77][78] линезолид является токсичным для митохондрий, вероятно, из-за сходства митохондриальной и бактериальной рибосом.[79] Лактатацидоз, потенциально опасное для жизни накопление молочной кислоты в организме, может также возникать в связи с митохондриальной токсичностью.[77] Из-за этих эффектов длительного лечения, производитель рекомендует еженедельно проводить клинический анализ крови во время терапии линезолидом для контроля за возможным подавлением функции костного мозга и рекомендует проводить лечение не более 28 дней.[1][9] Протокол более интенсивного мониторинга для раннего выявления токсичности у тяжелобольных пациентов, получающих линезолид, был разработан и предложен группой исследователей в Мельбурне, Австралия. Протокол включает проведение два раза в неделю анализов крови и функциональных проб печени; измерение уровня лактата в сыворотке крови для раннего обнаружения лактатацидоза; оценка всех лекарств принимаемых пациентом, отменяя назначение тех, которые могут взаимодействовать с линезолидом и периодические осмотры глаз и оценка неврологического статуса у пациентов, которые должны получать линезолид более четырёх недель.[80]
Побочные эффекты длительного применения линезолида были впервые выявлены в ходе постмаркетингового наблюдения. Подавление функции костного мозга не было выявлено в ходе III фазы исследований, в которых лечение не превышало 21 дней. Хотя у некоторых участников ранних исследований возникала тромбоцитопения, она оказалась обратимой и не возникала значительно чаще, чем в контрольной группе (где участники не принимали линезолид).[5] Были также постмаркетинговые сообщения о судорогах и, по состоянию на июль 2009 года, одиночные случаи паралича Белла (паралич лицевого нерва) и токсичном поражении почек.[69]
Химия[править | править код]
При физиологическом рН, линезолид существует в незаряженном состоянии. Он умеренно растворим в воде (приблизительно 3 мг/мл), с log Р 0,55.[26]
Фармакокинетика[править | править код]

Одним из преимуществ линезолид является его высокая биодоступность (около 100 %) при пероральном применении. Это означает, что пациенты, получающие линезолид внутривенно, могут начать принимать препарат перорально, как только их состояние позволяет, в то время как схожие антибиотики (например, ванкомицин и квинупристин/дальфопристин) могут назначаться только внутривенно.[81] При приёме линезолида с пищей возможно некоторое замедление его абсорбции, но площадь под кривой не изменяется.[26]
Линезолид обладает низкой способностью связывания с белками плазмы (примерно 31 %, но значения сильно варьируют) и кажущийся объём распределения в равновесном состоянии составляет около 40-50 литров.[2] Пик концентрации в сыворотке крови (С макс) достигается через 1-2 часа после введения препарата. Линезолид хорошо распределяется во всех тканях в организме, кроме костного матрикса и белой жировой ткани.[8] Примечательно, что концентрация линезолида в жидкости эпителия слизистой оболочки нижних дыхательных путей по крайней мере одинакова, а зачастую и выше, чем таковая в сыворотке крови (некоторые авторы сообщают, что концентрация в бронхиальной жидкости в четыре раза выше, чем в сыворотке крови), чем можно объяснить его эффективность при лечении пневмонии. Концентрация в спинномозговой жидкости варьирует; пик концентрации в СМЖ ниже, чем сыворотки крови из-за медленной диффузии через гемато-энцефалический барьер и корыта концентрации в СМЖ выше по той же причине.[26] Средний период полураспада составляет три часа у детей, четыре часа у подростков и пять часов у взрослых.[1]
Линезолид метаболизируется в печени путём окисления морфолинового кольца без участия системы цитохрома Р450. Этот метаболический путь приводит к образованию двух крупных неактивных метаболитов (что каждый приходится около 45 % и 10 % дозы выделяется в устойчивом состоянии), одного малого метаболита и нескольких следовых метаболитов, ни один из которых приходится более 1 % выделяется дозы.[82] Клиренс линезолида зависит от возраста и пола; он самый быстрый у детей (на долю которого приходится более короткий период полураспада) и, вероятно, на 20 % ниже у женщин, чем у мужчин.[1][82][83]
Применение в особых группах населения[править | править код]
Взрослым и детям старше 12 лет линезолид обычно назначается каждые 12 часов перорально или внутривенно.[5][81] Детям младшего возраста и младенцам препарат назначается каждые 8 часов.[84] Нет точной дозировки для лиц пожилого возраста, людей с лёгкой или умеренной печёночной недостаточностью или для пациентов с нарушениями функции почек.[2] Люди, нуждающихся в гемодиализе, должны получать линезолид после процедуры, так как диализ удаляет 30-40 % дозы из организма, нет точной дозировки для пациентов, которые находятся на непрерывной гемофильтрации[2], хотя и более частое введение может быть оправдано в некоторых случаях.[26] По данным одного исследования, вводить линезолид, возможно, требуется чаще у пациентов с ожогами, которые поражают более 20 % площади тела, когда увеличивается непочечный клиренс препарата.[85]
Линезолид в США имеет класс С для беременных, то есть не было никаких достаточных исследований его безопасности при использовании у беременных и хотя исследования на животных показали умеренную токсичность для плода, преимущество использования препарата может превышать риск.[1] Он также проникает в грудное молоко, хотя клиническое значение этого неизвестно.[28]
Механизм действия[править | править код]

Оксазолидиноны являются ингибиторами синтеза белка: они останавливают рост и размножение бактерий, нарушая трансляцию белков на рибосомах. Хотя механизм действия полностью не понятен,[86] линезолид, вероятно, действует на первом этапе синтеза белков — инициации — в отличие от большинства других ингибиторов синтеза белка, которые препятствуют элонгации.[81][87]
Препарат делает это путём предотвращения образования инициирующего комплекса, состоящего из 30S и 50S субъединиц рибосомы, тРНК и мРНК. Линезолид связывается с 23S частью 50S субъединицы (центр действия пептидилтрансферазы),[88] рядом с областью связывания хлорамфеникола, линкомицина и других антибиотиков. В связи с этим уникальным механизмом действия, перекрёстная резистентность между линезолидом и другими ингибиторами синтеза белка возникает очень редко или вовсе отсутствует.[5][26]
В 2008 году кристаллическая структура линезолида, связанная с 50S субъединицей рибосомы архея Haloarcula marismortui, была выделена группой учёных из Йельского университета и хранится в Protein Data Bank.[89] Другая группа учёных в 2008 году определила структура линезолида, связанного с 50S субъединицей Deinococcus radiodurans. Авторы предложили уточнённую модель механизма действия оксазолидинонов, установив, что линезолид занимает А область 50S рибосомной субъединицы, вызывая конформационные изменения, что предотвращает попадание тРНК и, в итоге, заставляя тРНК отделиться от рибосомы.[90]
Устойчивость[править | править код]
О приобретённой устойчивости к линезолиду сообщалось ещё в 1999 году, у двух пациентов с тяжёлой инфекцией Энтерококкус фэциум со множественной лекарственной устойчивостью.[25] Линезолид-устойчивый золотистый стафилококк был впервые обнаружен в 2001 году.[91]
В США устойчивость к линезолиду мониторируется и отслеживается с 2004 года в рамках программы под названием LEADER. Устойчивость остаётся стабильной и чрезвычайно низкой.[92] Похожая международная программа — Zyvox Annual Appraisal of Potency and Spectrum Study или ZAAPS — действует с 2002 года. В 2007 году общая устойчивость к линезолиду в 23 странах была меньше чем 0,2 % и не существовала среди стрептококков. Устойчивость была выявлена только в Бразилии, Китае, Ирландии и Италии, среди коагулазонегативных стафилококков (0,28 % проб устойчивости), энтерококков (0,11 %) и золотистых стрептококков (0,03 %).[93]
Механизм устойчивости[править | править код]
Собственная устойчивость большинства грамотрицательных бактерий к линезолиду связана с активностью истечения насосов, которые активно «выкачивают» линезолид из клетки быстрее, чем он накапливается.[8][94]
У грамположительных бактерий обычно развивается устойчивость к линезолиду в результате точечной мутации, известной как G2576T , при которой основание гуанина заменяется тимином в аллели 2576 генов, кодирующих 23S рибосомальную РНК.[95][96] Это наиболее распространённый механизм устойчивости стафилококков.[97] Другие механизмы были обнаружены у пневмококков (в том числе мутации в РНК метилтрансферазе, который метилирует G2445 из 23S рРНК, и мутации вызывают повышение экспрессии гена транспортёра ABC)[98] и у эпидермального стафилококка.[99][100]
Взаимодействия с другими лекарственными средствами[править | править код]
Линезолид является слабым ингибитором моноаминоксидазы (ИМАО) и не должен применяться одновременно с другими ИМАО, с продуктами, содержащими большое количество тирамина (такие как свинина, сыры, алкогольные напитки, копчёные и солёные продукты) и с серотонинергическими препаратами. Существуют постмаркетинговые сообщения о возникновении серотонинового синдрома, когда линезолид принимался одновременно или вскоре после отмены серотонинергических препаратов, особенно селективных ингибиторов обратного захвата серотонина, таких как пароксетин и сертралин.[9][101][102][103] Он может также усиливать гипертензивный эффект симпатомиметических препаратов, таких как псевдоэфедрин или фенилпропаноламин.[5][104] Линезолид также не должен сочетаться с петидином (меперидином) ни при каких обстоятельствах из-за риска серотонинового синдрома.
Линезолид не влияет на систему цитохрома P450 (CYP), которая отвечает за метаболизм многих лекарств и, следовательно, не имеет CYP связанных взаимодействий.[1]
Фармакоэкономика[править | править код]
Линезолид довольно дорогой препарат: курс лечения может стоить несколько тысяч долларов США, не учитывая другие расходы (например само пребывание в стационаре). Однако внутривенное введение линезолида может быть заменено на пероральный приём без ущерба для эффективности, пациенты могут быть выписаны из больницы относительно рано и продолжать лечение на дому, в то время как домашнее лечение инъекционными антибиотиками может быть нецелесообразным.[3] Сокращение продолжительности пребывания в стационаре снижает общую стоимость лечения, хотя линезолид может быть более дорогим, чем похожие антибиотики.
Были проведены исследования в ряде стран с различными моделями системы здравоохранения для оценки экономической эффективности линезолида по сравнению с гликопептидами, такими как ванкомицин или тейкопланин. В большинстве стран, линезолид был более рентабельным, чем сопоставимые антибиотики для лечения госпитальной пневмонии и инфекций кожи либо из-за более эффективного лечения и лучшей выживаемости либо за счёт снижения общих затрат на лечение.[3]
Примечания[править | править код]
- ↑ 1 2 3 4 5 6 7 8 9 10 Pfizer. ZYVOX (linezolid) Label Information (PDF) (20 июня 2008). Дата обращения: 24 августа 2008. Архивировано 9 июня 2012 года.
- ↑ 1 2 3 4 5 6 7 8 Lexi-Comp. Linezolid. The Merck Manual Professional (август 2008). Дата обращения: 14 мая 2009. Архивировано 9 июня 2012 года. Проверено 14 мая 2009 года.
- ↑ 1 2 3 Grau S., Rubio-Terrés C. Pharmacoeconomics of linezolid (англ.) // Expert Opinion on Pharmacotherapy[англ.] : journal. — 2008. — April (vol. 9, no. 6). — P. 987—1000. — ISSN 1465-6566. — doi:10.1517/14656566.9.6.987. — PMID 18377341.
- ↑ 1 2 3 Brickner S.J. Oxazolidinone antibacterial agents (неопр.) // Current Pharmaceutical Design[англ.]. — 1996. — Т. 2, № 2. — С. 175—194. Detailed review of the discovery and development of the whole oxazolidinone class, including information on synthesis and structure-activity relationships.
- ↑ 1 2 3 4 5 6 7 8 Moellering R.C. Linezolid: the first oxazolidinone antimicrobial (неопр.) // Annals of Internal Medicine[англ.]. — 2003. — January (т. 138, № 2). — С. 135—142. — ISSN 0003-4819. — PMID 12529096. Архивировано 25 февраля 2006 года.
- ↑ Slee A.M., Wuonola M.A., McRipley R.J., et al. Oxazolidinones, a new class of synthetic antibacterial agents: in vitro and in vivo activities of DuP 105 and DuP 721 (англ.) // Antimicrobial Agents and Chemotherapy[англ.] : journal. — 1987. — November (vol. 31, no. 11). — P. 1791—1797. — ISSN 0066-4804. — PMID 3435127. — PMC 175041. Архивировано 11 июня 2011 года.
- ↑ 1 2 3 Livermore D.M. Quinupristin/dalfopristin and linezolid: where, when, which and whether to use? (англ.) // Journal of Antimicrobial Chemotherapy[англ.] : journal. — 2000. — September (vol. 46, no. 3). — P. 347—350. — ISSN 0305-7453. — doi:10.1093/jac/46.3.347. — PMID 10980159. Архивировано 2 февраля 2009 года.
- ↑ 1 2 3 4 5 6 Barbachyn M.R., Ford C.W. Oxazolidinone structure-activity relationships leading to linezolid (англ.) // Angewandte Chemie : journal. — 2003. — May (vol. 42, no. 18). — P. 2010—2023. — ISSN 1433-7851. — doi:10.1002/anie.200200528. — PMID 12746812.
- ↑ 1 2 3 4 5 6 7 8 French G. Safety and tolerability of linezolid (англ.) // Journal of Antimicrobial Chemotherapy[англ.] : journal. — 2003. — May (vol. 51, no. Suppl 2). — P. ii45—53. — ISSN 0305-7453. — doi:10.1093/jac/dkg253. — PMID 12730142. Обзор. Включает в себя подробное обсуждение гематологических побочных эффектов линезолида.
- ↑ Ford C.W., Zurenko G.E., Barbachyn M.R. The discovery of linezolid, the first oxazolidinone antibacterial agent (англ.) // Current Drug Targets – Infectious Disorders : journal. — 2001. — August (vol. 1, no. 2). — P. 181—199. — ISSN 1568-0053. — doi:10.2174/1568005014606099. — PMID 12455414.
- ↑ Drug Approval Package: Zyvox. FDA Center for Drug Evaluation and Research (20 ноября 2001). Дата обращения: 17 января 2009. Архивировано 10 января 2008 года. Всесторонний обзор процесса утверждения FDA. Включает подробные обзоры химии и фармакологии линезолида, переписка между FDA и Pharmacia & Upjohn, и административных документов.
- ↑ ANVISA. Resolução nº 474, de 5 de junho de 2000 (порт.). National Health Surveillance Agency (5 июня 2000). Дата обращения: 19 мая 2009. Архивировано из оригинала 9 июня 2012 года.
- ↑ 1 2 [No authors listed]. Zyvox 600 mg Film-Coated Tablets, 100 mg/5 ml Granules for Oral Suspension, 2 mg/ml Solution for Infusion – Summary of Product Characteristics (SPC). electronic Medicines Compendium (24 июня 2009). Дата обращения: 3 июля 2009. Архивировано из оригинала 9 июня 2012 года.
- ↑ Irinoda K., Nomura S., Hashimoto M. [Antimicrobial and clinical effect of linezolid (ZYVOX), new class of synthetic antibacterial drug] (яп.) // Nippon Yakurigaku Zasshi. — 2002. — Октябрь (т. 120, № 4). — С. 245—252. — ISSN 0015-5691. — doi:10.1254/fpj.120.245. — PMID 12425150.
- ↑ 1 2 "Canada Approves Marketing Of Zyvoxam (Linezolid) For Gram Positive Infections" (Press release). 2001-05-08. Архивировано 28 августа 2008. Дата обращения: 18 мая 2009.
- ↑ Karlowsky J.A., Kelly L.J., Critchley I.A., Jones M.E., Thornsberry C., Sahm D.F. Determining Linezolid's baseline in vitro activity in Canada using gram-positive clinical isolates collected prior to its national release (англ.) // Antimicrobial Agents and Chemotherapy[англ.] : journal. — 2002. — June (vol. 46, no. 6). — P. 1989—1992. — ISSN 0066-4804. — doi:10.1128/AAC.46.6.1989-1992.2002. — PMID 12019122. — PMC 127260.
- ↑ "Pharmacia Corporation Reports 17% Increase In Second-Quarter Earnings-Per-Share Driven By 61% Increase In Pharmaceutical Earnings" (Press release). 2001-07-25. Архивировано 26 мая 2022. Дата обращения: 19 мая 2009.
- ↑ 1 2 Livermore D.M., Mushtaq S., Warner M., Woodford N. Activity of oxazolidinone TR-700 against linezolid-susceptible and -resistant staphylococci and enterococci (англ.) // Journal of Antimicrobial Chemotherapy[англ.] : journal. — 2009. — April (vol. 63, no. 4). — P. 713—715. — ISSN 0305-7453. — doi:10.1093/jac/dkp002. — PMID 19164418.
- ↑ Howe R.A., Wootton M., Noel A.R., Bowker K.E., Walsh T.R., MacGowan A.P. Activity of AZD2563, a novel oxazolidinone, against Staphylococcus aureus strains with reduced susceptibility to vancomycin or linezolid (англ.) // Antimicrobial Agents and Chemotherapy[англ.] : journal. — 2003. — November (vol. 47, no. 11). — P. 3651—3652. — ISSN 0066-4804. — doi:10.1128/AAC.47.11.3651-3652.2003. — PMID 14576139. — PMC 253812.
- ↑ Kalia V., Miglani R., Purnapatre K.P., et al. Mode of action of Ranbezolid against staphylococci and structural modeling studies of its interaction with ribosomes (англ.) // Antimicrobial Agents and Chemotherapy[англ.] : journal. — 2009. — April (vol. 53, no. 4). — P. 1427—1433. — ISSN 0066-4804. — doi:10.1128/AAC.00887-08. — PMID 19075051. — PMC 2663096.
- ↑ "Trius Completes Enrollment In Phase 2 Clinical Trial Evaluating Torezolid (TR-701) In Patients With Complicated Skin And Skin Structure Infections" (Press release). 2009-01-27. Архивировано 14 февраля 2009. Дата обращения: 17 мая 2009.
- ↑ Rx 1741. Rib-X Pharmaceuticals (2009). Дата обращения: 17 мая 2009. Архивировано из оригинала 15 июля 2011 года.
- ↑ Jones R.N., Stilwell M.G., Hogan P.A., Sheehan D.J. Activity of linezolid against 3,251 strains of uncommonly isolated gram-positive organisms: report from the SENTRY Antimicrobial Surveillance Program (англ.) // Antimicrobial Agents and Chemotherapy[англ.] : journal. — 2007. — April (vol. 51, no. 4). — P. 1491—1493. — doi:10.1128/AAC.01496-06. — PMID 17210770. — PMC 1855453.
- ↑ Jodlowski T.Z., Melnychuk I., Conry J. Linezolid for the treatment of Nocardia spp. infections (англ.) // Annals of Pharmacotherapy[англ.] : journal. — 2007. — October (vol. 41, no. 10). — P. 1694—1699. — ISSN 1060-0280. — doi:10.1345/aph.1K196. — PMID 17785610.
- ↑ 1 2 3 4 [No authors listed]. Linezolid (неопр.) // Drugs & Therapy Perspectives. — 2001. — Т. 17, № 9. — С. 1—6. Архивировано 21 мая 2013 года. Бесплатный полный текст с регистрацией на Medscape.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 Herrmann D.J., Peppard W.J., Ledeboer N.A., Theesfeld M.L., Weigelt J.A., Buechel B.J. Linezolid for the treatment of drug-resistant infections (англ.) // Expert Review of Anti-infective Therapy[англ.] : journal. — 2008. — December (vol. 6, no. 6). — P. 825—848. — ISSN 1478-7210. — doi:10.1586/14787210.6.6.825. — PMID 19053895.
- ↑ [No authors listed]. Animal Bites and Pasteurella multocida: Information for Healthcare Staff. Health Protection Agency (5 августа 2008). Дата обращения: 16 мая 2009. Архивировано из оригинала 9 июня 2012 года. Проверено 2009-05-15.
- ↑ 1 2 Davaro R. E., Glew R. H., Daly J. S. Oxazolidinones, quinupristin-dalfopristin, and daptomycin // Infectious diseases (неопр.) / Gorbach S. L., Bartlett J. G., Blacklow N. R.. — Hagerstown, MD: Lippincott Williams & Wilkins[англ.], 2004. — С. 241—243. — ISBN 0-7817-3371-5.
- ↑ 1 2 Sabbatani S., Manfredi R., Frank G., Chiodo F. Linezolid in the treatment of severe central nervous system infections resistant to recommended antimicrobial compounds (англ.) // Le Infezioni in Medicina : journal. — 2005. — June (vol. 13, no. 2). — P. 112—119. — ISSN 1124-9390. — PMID 16220032. Архивировано 22 июля 2011 года. Архивированная копия. Дата обращения: 3 января 2011. Архивировано 22 июля 2011 года.
- ↑ Geisler W.M., Malhotra U., Stamm W.E. Pneumonia and sepsis due to fluoroquinolone-resistant Capnocytophaga gingivalis after autologous stem cell transplantation (неопр.) // Bone Marrow Transplantation. — 2001. — December (т. 28, № 12). — С. 1171—1173. — ISSN 0268-3369. — doi:10.1038/sj.bmt.1703288. — PMID 11803363.
- ↑ 1 2 Marino P. L., Sutin K. M. Antimicrobial therapy // The ICU book (неопр.). — Hagerstown, MD: Lippincott Williams & Wilkins[англ.], 2007. — С. 817. — ISBN 0-7817-4802-X.
- ↑ Wroe, David (2002-02-28). "An antibiotic to fight immune bugs". The Age. Архивировано 27 января 2010. Дата обращения: 16 мая 2009.
- ↑ Wilson A.P., Cepeda J.A., Hayman S., Whitehouse T., Singer M., Bellingan G. In vitro susceptibility of Gram-positive pathogens to linezolid and teicoplanin and effect on outcome in critically ill patients (англ.) // Journal of Antimicrobial Chemotherapy[англ.] : journal. — 2006. — August (vol. 58, no. 2). — P. 470—473. — ISSN 0305-7453. — doi:10.1093/jac/dkl233. — PMID 16735420.
- ↑ 1 2 3 Falagas M.E., Siempos I.I., Vardakas K.Z. Linezolid versus glycopeptide or beta-lactam for treatment of Gram-positive bacterial infections: meta-analysis of randomised controlled trials (англ.) // The Lancet : journal. — Elsevier, 2008. — January (vol. 8, no. 1). — P. 53—66. — ISSN 1473-3099. — doi:10.1016/S1473-3099(07)70312-2. — PMID 18156089. структурированным рефератом, с оценки качества имеющихся на СД Архивная копия от 4 октября 2011 на Wayback Machine
- ↑ Tascini C., Gemignani G., Doria R., et al. Linezolid treatment for gram-positive infections: a retrospective comparison with teicoplanin (англ.) // Journal of Chemotherapy (Florence, Italy) : journal. — 2009. — June (vol. 21, no. 3). — P. 311—316. — ISSN 1120-009X. — PMID 19567352.
- ↑ Chow I., Lemos E.V., Einarson T.R. Management and prevention of diabetic foot ulcers and infections: a health economic review (англ.) // PharmacoEconomics : journal. — 2008. — Vol. 26, no. 12. — P. 1019—1035. — ISSN 1170-7690. — doi:10.2165/0019053-200826120-00005. — PMID 19014203.
- ↑ Lipsky B.A., Itani K., Norden C. Treating foot infections in diabetic patients: a randomized, multicenter, open-label trial of linezolid versus ampicillin-sulbactam/amoxicillin-clavulanate (англ.) // Clinical Infectious Diseases[англ.] : journal. — 2004. — January (vol. 38, no. 1). — P. 17—24. — ISSN 1058-4838. — doi:10.1086/380449. — PMID 14679443.
- ↑ 1 2 3 4 Pigrau C., Almirante B. [Oxazolidinones, glycopeptides and cyclic lipopeptides] (исп.) // Enfermedades Infecciosas y Microbiología Clínica. — 2009. — Апрель (т. 27, № 4). — С. 236—246. — doi:10.1016/j.eimc.2009.02.004. — PMID 19406516.
- ↑ Vardakas K.Z., Horianopoulou M., Falagas M.E. Factors associated with treatment failure in patients with diabetic foot infections: An analysis of data from randomized controlled trials (англ.) // Diabetes Research and Clinical Practice : journal. — 2008. — June (vol. 80, no. 3). — P. 344—351. — ISSN 0168-8227. — doi:10.1016/j.diabres.2008.01.009. — PMID 18291550.
- ↑ Grammatikos A., Falagas M.E. Linezolid for the treatment of skin and soft tissue infection (англ.) // Expert Review of Dermatology[англ.] : journal. — 2008. — Vol. 3, no. 5. — P. 539—548. — doi:10.1586/17469872.3.5.539.
- ↑ 1 2 Mandell L.A., Wunderink R.G., Anzueto A., et al. Infectious Diseases Society of America/American Thoracic Society consensus guidelines on the management of community-acquired pneumonia in adults (англ.) // Clinical Infectious Diseases[англ.] : journal. — 2007. — March (vol. 44, no. Suppl 2). — P. S27—72. — ISSN 1058-4838. — doi:10.1086/511159. — PMID 17278083.
- ↑ BTS Pneumonia Guidelines Committee. BTS guidelines for the management of community acquired pneumonia in adults – 2004 update. British Thoracic Society (30 апреля 2004). Дата обращения: 30 июня 2009. Архивировано из оригинала 9 июня 2012 года.
- ↑ 1 2 American Thoracic Society, Infectious Diseases Society of America. Guidelines for the management of adults with hospital-acquired, ventilator-associated, and healthcare-associated pneumonia (англ.) // American Journal of Respiratory and Critical Care Medicine[англ.] : journal. — 2005. — February (vol. 171, no. 4). — P. 388—416. — ISSN 1073-449X. — doi:10.1164/rccm.200405-644ST. — PMID 15699079.
- ↑ Koya D., Shibuya K., Kikkawa R., Haneda M. Successful recovery of infective endocarditis-induced rapidly progressive glomerulonephritis by steroid therapy combined with antibiotics: a case report (англ.) // BMC Nephrology : journal. — 2004. — December (vol. 5, no. 1). — P. 18. — doi:10.1186/1471-2369-5-18. — PMID 15610562. — PMC 544880. Архивировано 3 мая 2013 года.
- ↑ Pankey G.A., Sabath L.D. Clinical relevance of bacteriostatic versus bactericidal mechanisms of action in the treatment of Gram-positive bacterial infections (англ.) // Clinical Infectious Diseases[англ.] : journal. — 2004. — March (vol. 38, no. 6). — P. 864—870. — ISSN 1058-4838. — doi:10.1086/381972. — PMID 14999632.
- ↑ Falagas M.E., Manta K.G., Ntziora F., Vardakas K.Z. Linezolid for the treatment of patients with endocarditis: a systematic review of the published evidence (англ.) // Journal of Antimicrobial Chemotherapy[англ.] : journal. — 2006. — August (vol. 58, no. 2). — P. 273—280. — ISSN 0305-7453. — doi:10.1093/jac/dkl219. — PMID 16735427.
- ↑ Babcock H.M., Ritchie D.J., Christiansen E., Starlin R., Little R., Stanley S. Successful treatment of vancomycin-resistant Enterococcus endocarditis with oral linezolid (англ.) // Clinical Infectious Diseases[англ.] : journal. — 2001. — May (vol. 32, no. 9). — P. 1373—1375. — ISSN 1058-4838. — doi:10.1086/319986. — PMID 11303275.
- ↑ Ang J.Y., Lua J.L., Turner D.R., Asmar B.I. Vancomycin-resistant Enterococcus faecium endocarditis in a premature infant successfully treated with linezolid (англ.) // The Pediatric Infectious Disease Journal[англ.] : journal. — 2003. — December (vol. 22, no. 12). — P. 1101—1103. — ISSN 0891-3668. — doi:10.1097/01.inf.0000101784.83146.0c. — PMID 14688576.
- ↑ Archuleta S., Murphy B., Keller M.J. Successful treatment of vancomycin-resistant Enterococcus faecium endocarditis with linezolid in a renal transplant recipient with human immunodeficiency virus infection (англ.) // Transplant Infectious Disease : journal. — 2004. — September (vol. 6, no. 3). — P. 117—119. — ISSN 1398-2273. — doi:10.1111/j.1399-3062.2004.00059.x. — PMID 15569227.
- ↑ Zimmer S.M., Caliendo A.M., Thigpen M.C., Somani J. Failure of linezolid treatment for enterococcal endocarditis (англ.) // Clinical Infectious Diseases[англ.] : journal. — 2003. — August (vol. 37, no. 3). — P. e29—30. — ISSN 1058-4838. — doi:10.1086/375877. — PMID 12884185.
- ↑ Tsigrelis C., Singh K.V., Coutinho T.D., Murray B.E., Baddour L.M. Vancomycin-resistant Enterococcus faecalis endocarditis: linezolid failure and strain characterization of virulence factors (англ.) // Journal of Clinical Microbiology : journal. — 2007. — February (vol. 45, no. 2). — P. 631—635. — ISSN 0095-1137. — doi:10.1128/JCM.02188-06. — PMID 17182759. — PMC 1829077.
- ↑ Berdal J.E., Eskesen A. Short-term success, but long-term treatment failure with linezolid for enterococcal endocarditis (англ.) // Scandinavian Journal of Infectious Diseases[англ.] : journal. — 2008. — Vol. 40, no. 9. — P. 765—766. — ISSN 0036-5548. — doi:10.1080/00365540802087209. — PMID 18609208.
- ↑ Falagas M.E., Siempos I.I., Papagelopoulos P.J., Vardakas K.Z. Linezolid for the treatment of adults with bone and joint infections (англ.) // International Journal of Antimicrobial Agents : journal. — 2007. — March (vol. 29, no. 3). — P. 233—239. — ISSN 0924-8579. — doi:10.1016/j.ijantimicag.2006.08.030. — PMID 17204407. Обзор.
- ↑ Bassetti M., Vitale F., Melica G., et al. Linezolid in the treatment of Gram-positive prosthetic joint infections (англ.) // Journal of Antimicrobial Chemotherapy[англ.] : journal. — 2005. — March (vol. 55, no. 3). — P. 387—390. — ISSN 0305-7453. — doi:10.1093/jac/dki016. — PMID 15705640.
- ↑ Aneziokoro C.O., Cannon J.P., Pachucki C.T., Lentino J.R. The effectiveness and safety of oral linezolid for the primary and secondary treatment of osteomyelitis (англ.) // Journal of Chemotherapy (Florence, Italy) : journal. — 2005. — December (vol. 17, no. 6). — P. 643—650. — ISSN 1120-009X. — PMID 16433195.
- ↑ Senneville E., Legout L., Valette M., et al. Effectiveness and tolerability of prolonged linezolid treatment for chronic osteomyelitis: a retrospective study (англ.) // Clinical Therapeutics[англ.] : journal. — 2006. — August (vol. 28, no. 8). — P. 1155—1163. — ISSN 0149-2918. — doi:10.1016/j.clinthera.2006.08.001. — PMID 16982292.
- ↑ Rao N., Hamilton C.W. Efficacy and safety of linezolid for Gram-positive orthopedic infections: a prospective case series (англ.) // Diagnostic Microbiology and Infectious Disease : journal. — 2007. — October (vol. 59, no. 2). — P. 173—179. — ISSN 0732-8893. — doi:10.1016/j.diagmicrobio.2007.04.006. — PMID 17574788.
- ↑ Papadopoulos A., Plachouras D., Giannitsioti E., Poulakou G., Giamarellou H., Kanellakopoulou K. Efficacy and tolerability of linezolid in chronic osteomyelitis and prosthetic joint infections: a case-control study (англ.) // Journal of Chemotherapy (Florence, Italy) : journal. — 2009. — April (vol. 21, no. 2). — P. 165—169. — ISSN 1120-009X. — PMID 19423469.
- ↑ von der Lippe B., Sandven P., Brubakk O. Efficacy and safety of linezolid in multidrug resistant tuberculosis (MDR-TB)—a report of ten cases (англ.) // Journal of Infection[англ.] : journal. — 2006. — February (vol. 52, no. 2). — P. 92—6. — ISSN 0163-4453. — doi:10.1016/j.jinf.2005.04.007. — PMID 15907341.
- ↑ Park I.N., Hong S.B., Oh Y.M., et al. Efficacy and tolerability of daily-half dose linezolid in patients with intractable multidrug-resistant tuberculosis (англ.) // Journal of Antimicrobial Chemotherapy[англ.] : journal. — 2006. — September (vol. 58, no. 3). — P. 701—704. — ISSN 0305-7453. — doi:10.1093/jac/dkl298. — PMID 16857689.
- ↑ Fortún J., Martín-Dávila P., Navas E., et al. Linezolid for the treatment of multidrug-resistant tuberculosis (англ.) // Journal of Antimicrobial Chemotherapy[англ.] : journal. — 2005. — July (vol. 56, no. 1). — P. 180—185. — ISSN 0305-7453. — doi:10.1093/jac/dki148. — PMID 15911549.
- ↑ Jaksic B., Martinelli G., Perez-Oteyza J., Hartman C.S., Leonard L.B., Tack K.J. Efficacy and safety of linezolid compared with vancomycin in a randomized, double-blind study of febrile neutropenic patients with cancer (англ.) // Clinical Infectious Diseases[англ.] : journal. — 2006. — March (vol. 42, no. 5). — P. 597—607. — ISSN 1058-4838. — doi:10.1086/500139. — PMID 16447103. Критика в doi:10.1086/504431 , автор ответить в doi:10.1086/504437 .
- ↑ Cottagnoud P., Gerber C.M., Acosta F., Cottagnoud M., Neftel K., Täuber M.G. Linezolid against penicillin-sensitive and -resistant pneumococci in the rabbit meningitis model (англ.) // Journal of Antimicrobial Chemotherapy[англ.] : journal. — 2000. — December (vol. 46, no. 6). — P. 981—985. — ISSN 0305-7453. — doi:10.1093/jac/46.6.981. — PMID 11102418. Архивировано 6 декабря 2009 года.
- ↑ Ntziora F., Falagas M.E. Linezolid for the treatment of patients with central nervous system infection (англ.) // Annals of Pharmacotherapy[англ.] : journal. — 2007. — February (vol. 41, no. 2). — P. 296—308. — ISSN 1060-0280. — doi:10.1345/aph.1H307. — PMID 17284501. структурированным рефератом, с оценки качества имеющихся на СД Архивная копия от 2 сентября 2011 на Wayback Machine .
- ↑ Tunkel A.R., Hartman B.J., Kaplan S.L., et al. Practice guidelines for the management of bacterial meningitis (англ.) // Clinical Infectious Diseases[англ.] : journal. — 2004. — November (vol. 39, no. 9). — P. 1267—1284. — ISSN 1058-4838. — doi:10.1086/425368. — PMID 15494903.
- ↑ Naesens R., Ronsyn M., Druwé P., Denis O., Ieven M., Jeurissen A. Central nervous system invasion by community-acquired methicillin-resistant Staphylococcus aureus: case report and review of the literature (англ.) // Journal of Medical Microbiology[англ.] : journal. — Microbiology Society[англ.], 2009. — June (vol. 58, no. Pt 9). — P. 1247—1251. — ISSN 0022-2615. — doi:10.1099/jmm.0.011130-0. — PMID 19528145.
- ↑ 1 2 3 [No authors listed]. Linezolid (marketed as Zyvox) – Healthcare Professional Sheet. U.S. Food and Drug Administration (16 марта 2007). Дата обращения: 15 сентября 2010. Архивировано 9 июня 2012 года.
- ↑ 1 2 Wilcox M.H., Tack K.J., Bouza E., et al. Complicated skin and skin-structure infections and catheter-related bloodstream infections: noninferiority of linezolid in a phase 3 study (англ.) // Clinical Infectious Diseases[англ.] : journal. — 2009. — January (vol. 48, no. 2). — P. 203—212. — ISSN 1058-4838. — doi:10.1086/595686. — PMID 19072714.
- ↑ 1 2 3 4 Metaxas E.I., Falagas M.E. Update on the safety of linezolid (англ.) // Expert Opinion on Drug Safety[англ.] : journal. — 2009. — July (vol. 8, no. 4). — P. 485—491. — ISSN 1474-0338. — doi:10.1517/14740330903049706. — PMID 19538105.
- ↑ Zabel L.T., Worm S. Linezolid contributed to Clostridium difficile colitis with fatal outcome (англ.) // Infection : journal. — 2005. — June (vol. 33, no. 3). — P. 155—157. — ISSN 0300-8126. — doi:10.1007/s15010-005-4112-6. — PMID 15940418.
- ↑ Peláez T., Alonso R., Pérez C., Alcalá L., Cuevas O., Bouza E. In vitro activity of linezolid against Clostridium difficile (англ.) // Antimicrobial Agents and Chemotherapy[англ.] : journal. — 2002. — May (vol. 46, no. 5). — P. 1617—1618. — ISSN 0066-4804. — doi:10.1128/AAC.46.5.1617-1618.2002. — PMID 11959617. — PMC 127182.
- ↑ Lin Y-H, Wu V-C, Tsai I-J, et al. High frequency of linezolid-associated thrombocytopenia among patients with renal insufficiency (англ.) // International Journal of Antimicrobial Agents : journal. — 2006. — October (vol. 28, no. 4). — P. 345—351. — ISSN 0924-8579. — doi:10.1016/j.ijantimicag.2006.04.017. — PMID 16935472.
- ↑ Narita M., Tsuji B.T., Yu V.L. Linezolid-associated peripheral and optic neuropathy, lactic acidosis, and serotonin syndrome (англ.) // Pharmacotherapy : journal. — 2007. — August (vol. 27, no. 8). — P. 1189—1197. — ISSN 0277-0008. — doi:10.1592/phco.27.8.1189. — PMID 17655517.
- ↑ Bressler A.M., Zimmer S.M., Gilmore J.L., Somani J. Peripheral neuropathy associated with prolonged use of linezolid (англ.) // The Lancet : journal. — Elsevier, 2004. — August (vol. 4, no. 8). — P. 528—531. — ISSN 1473-3099. — doi:10.1016/S1473-3099(04)01109-0. — PMID 15288827.
- ↑ Chao C.C., Sun H.Y., Chang Y.C., Hsieh S.T. Painful neuropathy with skin denervation after prolonged use of linezolid (англ.) // Journal of Neurology, Neurosurgery & Psychiatry[англ.] : journal. — 2008. — January (vol. 79, no. 1). — P. 97—9. — ISSN 0022-3050. — doi:10.1136/jnnp.2007.127910. — PMID 17766431.
- ↑ Saijo T., Hayashi K., Yamada H., Wakakura M. Linezolid-induced optic neuropathy (англ.) // American Journal of Ophthalmology[англ.] : journal. — 2005. — June (vol. 139, no. 6). — P. 1114—1116. — ISSN 0002-9394. — doi:10.1016/j.ajo.2004.11.047. — PMID 15953450.
- ↑ 1 2 Soriano A., Miró O., Mensa J. Mitochondrial toxicity associated with linezolid (англ.) // The New England Journal of Medicine : journal. — 2005. — November (vol. 353, no. 21). — P. 2305—2306. — ISSN 0028-4793. — doi:10.1056/NEJM200511243532123. — PMID 16306535.
- ↑ Javaheri M., Khurana R.N., O'hearn T.M., Lai M.M., Sadun A.A. Linezolid-induced optic neuropathy: a mitochondrial disorder? (англ.) // British Journal of Ophthalmology[англ.] : journal. — 2007. — January (vol. 91, no. 1). — P. 111—115. — ISSN 0007-1161. — doi:10.1136/bjo.2006.102541. — PMID 17179125. — PMC 1857552.
- ↑ McKee E.E., Ferguson M., Bentley A.T., Marks T.A. Inhibition of mammalian mitochondrial protein synthesis by oxazolidinones (англ.) // Antimicrobial Agents and Chemotherapy[англ.] : journal. — 2006. — June (vol. 50, no. 6). — P. 2042—2049. — ISSN 0066-4804. — doi:10.1128/AAC.01411-05. — PMID 16723564. — PMC 1479116.
- ↑ Bishop E., Melvani S., Howden B.P., Charles P.G., Grayson M.L. Good clinical outcomes but high rates of adverse reactions during linezolid therapy for serious infections: a proposed protocol for monitoring therapy in complex patients (англ.) // Antimicrobial Agents and Chemotherapy[англ.] : journal. — 2006. — April (vol. 50, no. 4). — P. 1599—1602. — ISSN 0066-4804. — doi:10.1128/AAC.50.4.1599-1602.2006. — PMID 16569895. — PMC 1426936.
- ↑ 1 2 3 Ament P.W., Jamshed N., Horne J.P. Linezolid: its role in the treatment of gram-positive, drug-resistant bacterial infections (англ.) // American Family Physician[англ.] : journal. — 2002. — February (vol. 65, no. 4). — P. 663—670. — ISSN 0002-838X. — PMID 11871684. Архивировано 24 июля 2008 года.
- ↑ 1 2 Slatter J.G., Stalker D.J., Feenstra K.L., ; Peng, GW; Shobe, E.M. et al. Pharmacokinetics, metabolism, and excretion of linezolid following an oral dose of [14C]linezolid to healthy human subjects (англ.) // Drug Metabolism and Disposition[англ.] : journal. — 2001. — 1 August (vol. 29, no. 8). — P. 1136—1145. — ISSN 0090-9556. — PMID 11454733. Архивировано 7 января 2009 года.
- ↑ Sisson T.L., Jungbluth G.L., Hopkins N.K. Age and sex effects on the pharmacokinetics of linezolid (англ.) // European Journal of Clinical Pharmacology[англ.] : journal. — 2002. — January (vol. 57, no. 11). — P. 793—797. — ISSN 0031-6970. — doi:10.1007/s00228-001-0380-y. — PMID 11868801.
- ↑ Buck M.L. Linezolid use for resistant Gram-positive infections in children (англ.) // Pediatric Pharmacotherapy : journal. — 2003. — June (vol. 9, no. 6). Архивировано 5 июня 2011 года.
- ↑ Lovering A.M., Le Floch R., Hovsepian L., et al. Pharmacokinetic evaluation of linezolid in patients with major thermal injuries (англ.) // Journal of Antimicrobial Chemotherapy[англ.] : journal. — 2009. — March (vol. 63, no. 3). — P. 553—559. — ISSN 0305-7453. — doi:10.1093/jac/dkn541. — PMID 19153078.
- ↑ Skripkin E., McConnell T.S., DeVito J., et al. Rχ-01, a new family of oxazolidinones that overcome ribosome-based linezolid resistance (англ.) // Antimicrobial Agents and Chemotherapy[англ.] : journal. — 2008. — October (vol. 52, no. 10). — P. 3550—3557. — ISSN 0066-4804. — doi:10.1128/AAC.01193-07. — PMID 18663023. — PMC 2565890.
- ↑ Swaney S.M., Aoki H., Ganoza M.C., Shinabarger D.L. The oxazolidinone linezolid inhibits initiation of protein synthesis in bacteria (англ.) // Antimicrobial Agents and Chemotherapy[англ.] : journal. — 1998. — 1 December (vol. 42, no. 12). — P. 3251—3255. — ISSN 0066-4804. — PMID 9835522. — PMC 106030. Архивировано 17 января 2011 года.
- ↑ Colca J.R., McDonald W.G., Waldon D.J., et al. Cross-linking in the living cell locates the site of action of oxazolidinone antibiotics (англ.) // Journal of Biological Chemistry : journal. — 2003. — June (vol. 278, no. 24). — P. 21972—21979. — ISSN 0021-9258. — doi:10.1074/jbc.M302109200. — PMID 12690106. Архивировано 15 декабря 2005 года.
- ↑ Ippolito J.A., Kanyo Z.F., Wang D., et al. Crystal structure of the oxazolidinone antibiotic linezolid bound to the 50S ribosomal subunit (англ.) // Journal of Medicinal Chemistry[англ.] : journal. — 2008. — June (vol. 51, no. 12). — P. 3353—3356. — ISSN 0022-2623. — doi:10.1021/jm800379d. — PMID 18494460.
- ↑ Wilson D.N., Schluenzen F., Harms J.M., Starosta A.L., Connell S.R., Fucini P. The oxazolidinone antibiotics perturb the ribosomal peptidyl-transferase center and effect tRNA positioning (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 2008. — September (vol. 105, no. 36). — P. 13339—13344. — ISSN 0027-8424. — doi:10.1073/pnas.0804276105. — PMID 18757750. — PMC 2533191.
- ↑ Tsiodras S., Gold H.S., Sakoulas G., et al. Linezolid resistance in a clinical isolate of Staphylococcus aureus (англ.) // The Lancet : journal. — Elsevier, 2001. — July (vol. 358, no. 9277). — P. 207—208. — ISSN 0140-6736. — doi:10.1016/S0140-6736(01)05410-1. — PMID 11476839.
- ↑ Jones R.N., Ross J.E., Castanheira M., Mendes R.E. United States resistance surveillance results for linezolid (LEADER Program for 2007) (англ.) // Diagnostic Microbiology and Infectious Disease : journal. — 2008. — December (vol. 62, no. 4). — P. 416—426. — ISSN 0732-8893. — doi:10.1016/j.diagmicrobio.2008.10.010. — PMID 19022153.
- ↑ Jones R.N., Kohno S., Ono Y., Ross J.E., Yanagihara K. ZAAPS International Surveillance Program (2007) for linezolid resistance: results from 5591 Gram-positive clinical isolates in 23 countries (англ.) // Diagnostic Microbiology and Infectious Disease : journal. — 2009. — June (vol. 64, no. 2). — P. 191—201. — ISSN 0732-8893. — doi:10.1016/j.diagmicrobio.2009.03.001. — PMID 19500528.
- ↑ Schumacher A., Trittler R., Bohnert J.A., Kümmerer K., Pagès J.M., Kern W.V. Intracellular accumulation of linezolid in Escherichia coli, Citrobacter freundii and Enterobacter aerogenes: role of enhanced efflux pump activity and inactivation (англ.) // Journal of Antimicrobial Chemotherapy[англ.] : journal. — 2007. — June (vol. 59, no. 6). — P. 1261—1264. — ISSN 0305-7453. — doi:10.1093/jac/dkl380. — PMID 16971414.
- ↑ Saager B., Rohde H., Timmerbeil B.S., et al. Molecular characterisation of linezolid resistance in two vancomycin-resistant (VanB) Enterococcus faecium isolates using Pyrosequencing (англ.) // European Journal of Clinical Microbiology & Infectious Diseases[англ.] : journal. — 2008. — September (vol. 27, no. 9). — P. 873—878. — ISSN 0934-9723. — doi:10.1007/s10096-008-0514-6. — PMID 18421487.
- ↑ Besier S., Ludwig A., Zander J., Brade V., Wichelhaus T.A. Linezolid resistance in Staphylococcus aureus: gene dosage effect, stability, fitness costs, and cross-resistances (англ.) // Antimicrobial Agents and Chemotherapy[англ.] : journal. — 2008. — April (vol. 52, no. 4). — P. 1570—1572. — ISSN 0066-4804. — doi:10.1128/AAC.01098-07. — PMID 18212098. — PMC 2292563.
- ↑ Scheetz M.H., Knechtel S.A., Malczynski M., Postelnick M.J., Qi C. Increasing incidence of linezolid-intermediate or -resistant, vancomycin-resistant Enterococcus faecium strains parallels increasing linezolid consumption (англ.) // Antimicrobial Agents and Chemotherapy[англ.] : journal. — 2008. — June (vol. 52, no. 6). — P. 2256—2259. — ISSN 0066-4804. — doi:10.1128/AAC.00070-08. — PMID 18391028. — PMC 2415807.
- ↑ Feng J., Lupien A., Gingras H., et al. Genome sequencing of linezolid-resistant Streptococcus pneumoniae mutants reveals novel mechanisms of resistance (англ.) // Genome Research[англ.] : journal. — 2009. — May (vol. 19, no. 7). — P. 1214—1223. — ISSN 1088-9051. — doi:10.1101/gr.089342.108. — PMID 19351617. — PMC 2704432.
- ↑ Lincopan N., de Almeida L.M., Elmor de Araújo M.R., Mamizuka E.M. Linezolid resistance in Staphylococcus epidermidis associated with a G2603T mutation in the 23S rRNA gene (англ.) // International Journal of Antimicrobial Agents : journal. — 2009. — April (vol. 34, no. 3). — P. 281—282. — ISSN 0924-8579. — doi:10.1016/j.ijantimicag.2009.02.023. — PMID 19376688.
- ↑ Liakopoulos A., Neocleous C., Klapsa D., et al. A T2504A mutation in the 23S rRNA gene responsible for high-level resistance to linezolid of Staphylococcus epidermidis (англ.) // Journal of Antimicrobial Chemotherapy[англ.] : journal. — 2009. — July (vol. 64, no. 1). — P. 206—207. — ISSN 0305-7453. — doi:10.1093/jac/dkp167. — PMID 19429927.
- ↑ Lawrence K.R., Adra M., Gillman P.K. Serotonin toxicity associated with the use of linezolid: a review of postmarketing data (англ.) // Clinical Infectious Diseases[англ.] : journal. — 2006. — June (vol. 42, no. 11). — P. 1578—1583. — ISSN 1058-4838. — doi:10.1086/503839. — PMID 16652315.
- ↑ Huang V., Gortney J.S. Risk of serotonin syndrome with concomitant administration of linezolid and serotonin agonists (англ.) // Pharmacotherapy : journal. — 2006. — December (vol. 26, no. 12). — P. 1784—1793. — ISSN 0277-0008. — doi:10.1592/phco.26.12.1784. — PMID 17125439.
- ↑ Waknine, Yael. FDA Safety Changes: Mirena, Zyvox, Orencia. Medscape (5 сентября 2008). Дата обращения: 6 сентября 2008. Архивировано 2 декабря 2008 года. в свободном доступе с регистрации.
- ↑ Stalker D.J., Jungbluth G.L. Clinical pharmacokinetics of linezolid, a novel oxazolidinone antibacterial (англ.) // Clinical Pharmacokinetics[англ.] : journal. — 2003. — Vol. 42, no. 13. — P. 1129—1140. — ISSN 0312-5963. — doi:10.2165/00003088-200342130-00004. — PMID 14531724.