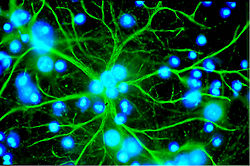
Гематоэнцефалический барьер

1. Эпендима
2. Нейрон
3. Аксон
4. Олигодендроцит
5. Астроцит
6. Миелин
7. Микроглия
8. Капилляр

Гема́тоэнцефали́ческий барье́р (гемато-энцефалический барьер, ГЭБ)[1] (от др.-греч. αἷμα, род. п. αἵματος — «кровь» и др.-греч. ἐγκέφαλος — «головной мозг») — физиологический гистогематический барьер между кровеносной системой и центральной нервной системой. ГЭБ имеют все позвоночные.
Главная функция ГЭБ — поддержание гомеостаза мозга. Он защищает нервную ткань от циркулирующих в крови микроорганизмов, токсинов, клеточных и гуморальных факторов иммунной системы, которые воспринимают ткань мозга как чужеродную. ГЭБ выполняет функцию высокоселективного фильтра, через который из артериального русла в мозг поступают питательные, биоактивные вещества; в направлении венозного русла с глимфатическим потоком выводятся продукты жизнедеятельности нервной ткани.
Вместе с тем, наличие ГЭБ затрудняет лечение многих заболеваний центральной нервной системы, так как он не пропускает целый ряд лекарственных препаратов.
Развитие концепции гематоэнцефалического барьера[править | править код]


Первое свидетельство о существовании ГЭБ было получено в 1885 году Паулем Эрлихом. Он обнаружил, что введённый в кровеносное русло крысы краситель распространился по всем органам и тканям, кроме мозга[2]. В 1904 году он высказал неверное предположение о том, что краситель не проникает в ткань мозга при внутривенном введении, так как не имеет к ней сродства[3]. Южноафриканский хирург Эдвин Гольдман (1862—1913), ученик Эрлиха, обнаружил в 1909 году, что введённый внутривенно краситель трипановый синий не проникает в ткань мозга, но окрашивает сосудистое сплетение его желудочков[4]. В 1913 году он показал, что краситель, введенный в спинномозговую жидкость собаки или лошади, проникает в ткань головного и спинного мозга, а периферические органы и ткани при этом не окрашиваются[5]. На основании этих опытов Гольдман предположил наличие барьера между мозгом и кровью, который задерживает нейротоксические вещества[6].
В 1898 году венские патологи Артур Бидль (1869—1933) и Рудольф Краус (1868—1932) показали, что при введении жёлчных кислот в кровеносное русло нейротоксический эффект не возникал, однако при инъекции непосредственно в ткань мозга развивалась кома[7]. Немецкий невролог Макс Левандовский повторил опыты Бидля и Крауса с гексацианоферратом калия. Получив схожие результаты, он впервые использовал термин «Blut-Hirn-Schranke» (перегородка между кровью и мозгом, 1900), принятый впоследствии также и в англоязычной литературе (blood-brain barrier)[8][9].
В 1915 году швейцарский нейроанатом Константин фон Монаков в Цюрихе предположил, что хориоидное сплетение и нейроглия выполняют барьерную функцию.[10] В последующие годы им совместно с сотрудниками было опубликовано несколько сугубо гистологических трудов, посвящённых хориоидному сплетению, которое один из его учеников (чилийский психоаналитик Фернандо Альенде-Наварро, 1890—1981) в публикации 1925 года именует «экто-мезодермальным барьером» (фр. barrière ecto-mésodermique).

Термин «гематоэнцефалический барьер» (фр. barrière hémato-encéphalique) был введён в научный обиход[10] швейцарским, а затем советским физиологом Линой Соломоновной Штерн (первой женщиной — членом Академии наук СССР)[12] в совместном со своими студентами Эрнестом Ротлиным (1888—1972) и Раймондом Готье (1885—1957) сообщении Женевскому медицинскому обществу (Société de Biologie et Médecine) за 21 апреля 1921 года[13][14]:
Между кровью, с одной стороны, и спинномозговой жидкостью, с другой, есть особый аппарат или механизм, способный просеивать вещества, обыкновенно присутствующие в крови или случайно проникшие в неё. Мы предлагаем называть этот гипотетический механизм, пропускающий одни вещества и замедляющий или останавливающий проникновение других веществ, гематоэнцефалическим барьером.[15][16]
Первые сообщения Лины Штерн и Эрнеста Ротлина на заседании Société de physique et d’histoire naturelle de Genève и их публикация в Schweizer Archiv für Neurologie und Psychiatrie о наличии защитного барьера между мозгом и кровяным руслом относятся к 1918 году.[17] Штерн и Ротлину посредством тончайшей канюли удалось ввести 1 мг кураре в пространство четвёртого желудочка экспериментального животного и зафиксировать медленную диффузию нейротоксина из спинномозговой жидкости сквозь лептоменингиальные мембраны в глубокие ядра мозжечка. В 1921 году выходит первая обзорная статья Л. С. Штерн в Schweizer Archiv für Neurologie und Psychiatrie, а в 1923 году её влиятельная работа «La barrière hémato-encéphalique dans les conditions normales et pathologiques», включённая в двухтомный коллективный сборник, посвящённый 70-летию Константина фон Монакова (1853—1930) и изданный тем же журналом.[18] В последнем обзоре, помимо обобщения экспериментальных и гистологических исследований ГЭБ, его роли в нормальной физиологии и нейропатологии, Штерн также рассматривает и его роль в фармакодинамике и фармакокинетике нейротропных препаратов. В последующие годы Штерн, основываясь на анализе обширного экспериментального материала, сформулировала положения о ГЭБ и определила его значение для деятельности центральной нервной системы[19]. В 1935 году под её редакцией был опубликован первый коллективный сборник, целиком посвящённый данной теме («Гемато-энцефалический барьер», М.—Л.: Биомедгиз, 1935). За исследования гематоэнцефалического барьера Л. С. Штерн в 1943 году была награждена Сталинской премией, денежную составляющую которой она передала на строительство санитарного самолёта.[20]
В 1930-х годах было сформулировано различие между гематоэнцефалическим и гематоли́кворным барьером[6][21][22].
Морфологические структуры, ответственные за ГЭБ, были детально изучены в 1960-х годах методами электронной микроскопии[23][24].
Функции[править | править код]
Масса головного мозга человека составляет приблизительно 2 % от массы его тела. При этом потребление кислорода центральной нервной системой составляет 20 % от общего потребления кислорода организмом. Также, в противоположность другим органам, мозг обладает наименьшими запасами питательных веществ. Нервные клетки не могут обеспечить свои энергетические потребности путём одного лишь анаэробного гликолиза. Прекращение поступления крови к мозгу в течение нескольких секунд приводит к потере сознания, а через 10 минут наступает гибель нейронов[23]. Такие энергетические потребности головного мозга обеспечиваются за счёт активного транспорта кислорода и питательных веществ через ГЭБ[25].
Нормальное функционирование мозга возможно также лишь в условиях электролитного и биохимического гомеостаза. Колебания pH, концентрации калия в крови и других показателей не должны влиять на состояние нервной ткани. Циркулирующие в кровеносном русле нейромедиаторы не должны проникать в нервную ткань, где они могли бы изменить активность нейронов[23]. Также мозг должен быть защищён от попадания в него чужеродных агентов, таких как ксенобиотики и патогенные микроорганизмы. ГЭБ — это также и иммунологический барьер, так как он непроницаем для многих микроорганизмов, антител и лейкоцитов[26][27].
Система кровеносных сосудов центральной нервной системы имеет ряд структурно-функциональных особенностей, отличающих их от сосудов других органов и тканей. Эти особенности обеспечивают функции питания, выведения продуктов жизнедеятельности и поддержания гомеостаза[23].
Нарушения ГЭБ могут вызывать поражения центральной нервной системы. Целый ряд неврологических заболеваний напрямую или косвенно связан с повреждением ГЭБ[25].
Строение[править | править код]



Основным элементом структуры ГЭБ являются эндотелиальные клетки. Особенностью церебральных сосудов является наличие плотных контактов между эндотелиальными клетками. В структуру ГЭБ также входят перици́ты и астроци́ты[23]. Межклеточные промежутки между эндотелиальными клетками, перицитами и астроцитами нейроглии ГЭБ меньше, чем промежутки между клетками в других тканях организма. Эти три вида клеток являются структурной основой ГЭБ не только у человека, но и у большинства позвоночных[28][29].
Эндотелий[править | править код]
Капиллярные сосуды выстланы эндотелиальными клетками. Эндотелий сосудов большинства тканей содержит открытые промежутки (фенестра́ции) диаметром около 50 нм и межклеточные щели от 100 до 1000 нм. Через эти промежутки вода и растворённые в ней вещества циркулируют между кровью и межклеточным пространством. Отличительной особенностью сосудов центральной нервной системы является отсутствие как фенестраций, так и межклеточных щелей между эндотелиальными клетками[30]. Таким образом, эндотелиальная выстилка капилляров мозга является сплошной[31].
Другим отличием эндотелия церебральных капилляров от периферических является низкое содержание в них пиноцито́зных пузырьков (вези́кул)[9][32].
Количество митохондрий в эндотелиальных клетках сосудов мозга в 5-10 раз выше, чем в эндотелии периферических сосудов. Столь высокое содержание митохондрий связано со значительными энергетическими потребностями эндотелиальных клеток ГЭБ, осуществляющих активный транспорт и обмен веществ[27]. (Митохондрии — это органеллы, в которых происходит синтез молекул АТФ, являющихся основным источником энергии для клеток.)
ГЭБ является также метаболическим или ферментативным (энзиматическим) барьером[6][33][34][35][36]. На поверхности клеточных мембран эндотелиальных клеток ГЭБ находится целый ряд ферментов, причём в значительно большем количестве, чем на мембранах других клеток паренхимы. Это такие ферменты, как гамма-глутамилтрансфераза и фосфатаза (в частности глюкоза-6-фосфатаза), катехол-О-метилтрансфераза, моноаминоксидаза и цитохром Р450[37][38][39]. Благодаря высокой концентрации ферментов в эндотелиальных клетках ГЭБ многие вещества метаболизируются при транспортировании через цитоплазму этих клеток[9]. Высота (размер в направлении, перпендикулярном стенке сосуда) эндотелиальной клетки ГЭБ составляет от 3 до 5 мкм (для сравнения, высота энтероцитов, эпителиальных клеток кишечника, - 17-30 мкм)[40]

Соотношение холестерина к фосфолипидам в эндотелиальных клетках ГЭБ такое же, как и в эндотелиальных клетках периферических сосудов, и составляет ≈ 0,7[41]. Пассивный транспорт через клеточные мембраны ГЭБ происходит так же, как и пассивная диффузия в других эндотелиальных клетках[42]. В мембранах эндотелиальных клеток содержится большое количество каналов, проницаемых для молекул воды. Они допускают диффузию воды между мозгом и кровеносной системой[43].
Благодаря отсутствию фенестраций и небольшому числу пиноцитарных везикул эндотелиальная выстилка капилляров мозга становится механическим барьером для крупных молекул и инородных веществ. Кроме этого, ГЭБ обладает значительным электрическим сопротивлением — около 1500—2000 Ом. (для сравнения, электрическое сопротивление для стенок капилляров мышечной ткани составляет лишь 30 Ом.)[44]
Плотные контакты[править | править код]
Эндотелиальные клетки сосудов мозга плотно прилегают друг к другу. Между их стенками образуются так называемые плотные контакты, роль которых в обеспечении ГЭБ состоит в том, что они предотвращают проникновение в ткань мозга различных нежелательных веществ из кровеносного русла[45][46]. Плотные контакты между эндотелиальными клетками блокируют межклеточный (парацеллюля́рный) пассивный транспорт[47][48][49]. При этом блокируется парацеллюлярный транспорт веществ как из кровеносного русла в ткань мозга, так и в обратном направлении — из мозга в кровь[29].
Большое количество трансмембранных белков, таких как окклюди́н, разнообразные клауди́ны и замыкательные адгезионные молекулы связывают латеральные отделы клеточных стенок между собой, участвуют в формировании плотных контактов и делают возможным межклеточный транспорт и обмен веществ[50]. Основными белками, обеспечивающими адгезию эндотелиальных клеток и формирование плотных контактов, являются клаудин-5 и клаудин-12[51]. Нокаут гена CLDN5, ответственного за синтез белка клаудина-5, приводил у экспериментальных мышей к тому, что их ГЭБ становился проницаемым для молекул с молярной массой до 800 г/моль. Такие генетически изменённые животные умирали через несколько часов после рождения[52].
Базальная мембрана[править | править код]

Эндотелиальные клетки полностью покрывают подлежащий белковый слой, называемый база́льной мембраной[31]. Толщина базальной мембраны колеблется от 40 до 50 нм. Она различима только под электронным микроскопом. Состоит в основном из коллагена IV типа, гепаринсульфат-протеоглика́нов, ламини́нов, фибронекти́на и других белков внеклеточного матрикса. Со стороны мозга базальная мембрана ограничена плазматической мембраной пластинчатых окончаний отростков астроцитов[9][47].
Перициты (подоциты)[править | править код]

Перициты, ранее называвшиеся по имени первооткрывателя Шарля Мари Бенджами́на Руже́ (1824—1904) клетками Руже[53], являются составной частью ГЭБ[54]. Они обладают несколькими важными для его функционирования свойствами: способностью к сокращению, регулированию функций эндотелия и макрофага́льной активностью[55].

Около 20 % поверхности эндотелиальных клеток церебральных капилляров покрыто относительно маленькими, овальными перицитами. Каждая 2—4-я эндотелиальная клетка имеет контакт с клеткой-перицитом[29]. В основном перициты располагаются в местах контакта эндотелиальных клеток[56][57]. Перициты имеются практически во всех артериолах, венулах и капиллярах организма. Уровень покрытия ими эндотелиального слоя капилляра коррелирует с проницаемостью сосудистой стенки. В органах и тканях с проницаемой сосудистой стенкой они могут мигрировать из кровеносного русла в межклеточное пространство. Так, например, в капиллярах скелетной мускулатуры соотношение перициты: эндотелиоци́ты составляет 1:100[58][59].
Перициты, как и эндотелиоциты, располагаются на базальной мембране[31].
Также перициты синтезируют целый ряд вазоактивных веществ[59] и играют важную роль в а́нгиогене́зе[60][61].
Клеточные контакты перицит — эндотелиоцит[править | править код]
Перициты крепко связаны с эндотелиоцитами. Эта связь осуществляется благодаря трём типам контактов: щелевым соединениям, фокальным адгезиям и инвагинациям мембраны одной клетки в полость другой[55]. Щелевые соединения непосредственно связывают цитоплазму двух клеток, являясь проницаемыми для ионов и небольших молекул[62]. С помощью фокальных адгезий осуществляется прочная механическая связь двух типов клеток[63]. Инвагинации участков цитоплазмы одной клетки в другую обеспечивают как механическое связывание, так и межклеточный обмен веществ[55][64].
Благодаря тесным контактам клетки опосредованно влияют на митотическую активность, экспрессию генов и, соответственно, фенотип друг друга[60].
Сократительная функция[править | править код]
Перициты содержат большое количество способного к сокращению белка актина. Благодаря этой своей структурной особенности они в состоянии изменять просвет капилляров и таким образом регулировать местное кровяное давление[65][66].
Макрофагальная активность[править | править код]
Данное свойство характерно только для церебральных перицитов. В капиллярной сети мозга они выполняют функцию макрофагов. Соответственно в цитоплазме церебральных перицитов располагается большое количество лизосом. В культуре тканей доказана способность перицитов к фагоцитозу[55][67][68] и презентации антигенов[69][70].
Макрофагальные свойства перицитов образуют «вторую линию защиты мозга» от нейротоксических молекул, которые преодолели барьер эндотелиальных клеток[71]. Таким образом они являются важной составной частью иммунной системы мозга. Сбой макрофагальной активности перицитов может стать одним из факторов развития целого ряда аутоиммунных заболеваний. Имеются данные об опосредованной роли перицитов в развитии болезни Альцгеймера[72][73].
Астроциты[править | править код]

Астроциты — большие нейроглиальные клетки звёздчатой формы. Своими отростками они выстилают стенки мозговых капилляров со стороны мозговой ткани. В то же время, несмотря на то, что пластинчатыми окончаниями их клеточных отростков выстлано около 99 % капиллярных сосудов, астроциты не выполняют прямой барьерной функции[29][74]. Астроциты тесно взаимодействуют с эндотелиальными клетками. Между ними осуществляется постоянный обмен веществ[75]. Астроглиальные клетки индуцируют возникновение и формирование ГЭБ. При проведении экспериментов по пересадке сосудов мозга в периферические органы и наоборот — периферических сосудов в ткань головного мозга, отмечено формирование ГЭБ в периферических сосудах, пересаженных в мозг (образование плотных контактов, перестройка эндотелиальных клеток), и разобщение эндотелиальных клеток и появление фенестраций между ними при пересадке мозговых сосудов[23][76]. Также in vitro показано влияние астроцитов на фенотип эндотелия. В клеточной культуре, содержащей астроциты и эндотелиоциты, отмечено более плотное расположение эндотелия по сравнению с его чистой клеточной культурой[77].
Астроциты выделяют целый ряд веществ, которые влияют на проницаемость эндотелия[78]. Эндотелиоциты в свою очередь выделяют ингибирующий лейкемию фактор (LIF), цитоки́н интерлейки́н-6, которые воздействуют на процесс дифференциации астроцитов[78]. Расстояние от пластинчатых окончаний отростков астроцитов до клеток эндотелия и перицитов составляет всего лишь 20 нм[31][79].
Главными задачами астроглиальных клеток является обеспечение нейронов питательными веществами и поддержание необходимой концентрации электролитов внеклеточного пространства[78][80]. Астроциты синтезируют большую часть необходимого клеткам мозга холестерина. Холестерин не проникает через ГЭБ. В то же время в ткани мозга находится 25 % от общего холестерина организма. Бо́льшая его часть входит в состав миелина, который окутывает отростки нейронов аксоны. Нарушения процессов миелинизации нервных волокон вызывают развитие демиелинизирующих заболеваний, в частности рассеянный склероз[81].
Пластинчатые окончания отростков астроцитов неплотно покрывают со стороны мозга базальную мембрану сосудистой стенки с расположенными на ней эндотелиоцитами и перицитами. За счёт этого между эндотелиоцитами и тканью мозга возможна прямая диффузия различных веществ[78].
Заболевания, при которых происходит прямое или опосредованное поражение астроцитов (например, болезнь Альцгеймера, астроцитомы), сопровождаются нарушением функционирования ГЭБ.
Области мозга без ГЭБ[править | править код]
ГЭБ имеется в капиллярах большинства областей мозга, но не во всех. В циркумвентрикулярных органах ГЭБ отсутствует:
- Самое заднее поле (лат. area postrema) ромбовидной ямки (дна IV желудочка) — располагается между треугольником блуждающего нерва (лат. trigonum nervi vagi) с окаймляющим его самостоятельным канатиком (лат. funiculus separans) и бугорком тонкого ядра[82]
- Шишковидное тело (лат. corpus pineale) (синоним — эпифиз)
- Нейрогипофиз
- Прикреплённая пластинка (лат. lamina affixa) — эмбриональный остаток стенки конечного мозга, покрывающий верхнюю поверхность таламуса. Медиально она истончается, образует извитую пластинку — сосудистую ленту (лат. tenia choroidea)[83]
- Субфорника́льный орган
- Субкомиссура́льный орган
Данная гистологическая особенность имеет своё обоснование. Так например, нейрогипофиз выделяет в кровь гормоны, которые не могут пройти через ГЭБ, а нейроны дна IV желудочка (лат. area postrema) улавливают в крови наличие токсических веществ и стимулируют рвотный центр[84]. Защитным барьером соседней с данными образованиями мозговой ткани является скопление таницитов. Они представляют собой клетки эпендимы с плотными контактами[85].
Мозговой кровоток[править | править код]
В среднем просвет капилляра мозгового сосуда составляет около 40 мкм[86]. Наибольшая их плотность отмечена в коре головного мозга — от 300 до 800 капилляров на 1 мм³ ткани[23].
Суммарная поверхность стенок сосудов мозга составляет 12[87] — 20[88] м². Ежеминутно через сосудистую сеть мозга протекает около 610 мл крови со средней скоростью 1 мм/с создавая давление на её стенки 15-35 мм рт. ст.[27] Через капиллярное русло мозга она проходит значительно быстрее (в среднем за 5 секунд), чем в других органах и тканях (для сравнения, в кишечнике, площадь сосудов которого достигает 180 м² среднее время прохождения крови (англ. mean transit time) равно 40 часам[89][90], а в печени с 70 м² — 30 секундам[91][92][93].
Развитие[править | править код]
До конца XX века считалось, что у эмбриона и новорождённых ГЭБ не сформирован в полной степени и соответственно не выполняет своей функции. Причиной этого до сих пор широко распространённого мнения являются недостатки ранее проводившихся физиологических опытов. Эксперименты заключались во введении либо связанных с белками красителей, либо других маркеров взрослым животным и эмбрионам. Первые подобные опыты проводились в 1920 году[94]. Маркеры, вводимые эмбрионам, проникали в ткань мозга и спинномозговую жидкость, в то время как у взрослых животных — нет. В ходе данных экспериментов был допущен ряд методических ошибок (использование чрезмерного объёма вводимого вещества, повышение осмотического давления), из-за которых происходило частичное повреждение сосудистой стенки и соответственно маркер попадал в ткань мозга[95][96][97]. При правильной постановке экспериментов пассажа маркера через сосудистую сеть отмечено не было[98][99][100].
В крови плода в большом количестве содержатся молекулы таких веществ как альбумин, α1-фетопротеин и трансферрин, отсутствуя при этом в межклеточном пространстве ткани мозга[101]. В эмбриональном эндотелии обнаружен транспортёр Р-гликопротеин[102]. Это свидетельствует о наличии ГЭБ в пренатальном периоде. В ходе развития организма происходит дальнейшее совершенствование ГЭБ[101].
Для небольших поляризованных молекул, например инулина и сахарозы, проницаемость ГЭБ эмбриона и новорожденного значительно выше, чем у взрослых[103][104][105]. Схожий эффект отмечен и для ионов[106]. Транспорт аминокислот и инсулина через ГЭБ значительно ускорен, по всей видимости, в связи с большой потребностью в них растущего мозга[107][108][109][110].
С другой стороны, в мозге эмбриона имеется дополнительный, отсутствующий у взрослых, барьер на границе между ликвором и тканью мозга — так называемые ремневы́е контакты (англ. Strap Junctions) между клетками эпендимы[111].
Эволюция[править | править код]
В ходе эволюции нервной ткани позвоночных происходит увеличение её объёма. Бо́льшая масса мозга требует лучшего обеспечения питательными веществами и выведения ненужных и отработанных веществ. Это привело к развитию густой капиллярной сети в ткани мозга. Следующим этапом эволюции стало появление защитного барьера от циркулирующих в крови токсичных для нейронов веществ — ксенобиотиков и токсинов[28][112].
У многих беспозвоночных ГЭБ отсутствует. У них эндотелий капилляров нервной ткани не образует сплошной выстилки сосудистой стенки. У высших беспозвоночных — насекомых, ракообразных и головоногих[113] — защитный барьер между нейронами и кровью представлен исключительно глиальной тканью[114]. В этом случае речь идёт о глиальном гематоэнцефалическом барьере[115].
У всех видов позвоночных имеется ГЭБ, и у большинства из них он образован преимущественно клетками эндотелия сосудистой стенки, скреплёнными между собой плотными контактами. Только у пластиножаберных (среди них акул и скатов), а также семейства осетровых рыб ГЭБ формируется периваскулярными астроцитами. Из этого следует, что в процессе эволюции, вероятно, происходит расширение функций эндотелиальных клеток сосудов головного мозга, которые перенимают на себя барьерные функции.
Структурные различия глиального и эндотелиального гематоэнцефалических барьеров достаточно велики. Эндотелиальный барьер имеет целый ряд преимуществ. Одним из них является строгое разграничение функций эндотелиальных клеток и клеток астрогли́и, которые обеспечивают гомеостаз внеклеточной среды вещества мозга[114].
Гематоликворный барьер[править | править код]
Кроме гематоэнцефалического барьера существует также гематоликворный, который отделяет центральную нервную систему от кровеносного русла. Он образован эпителиальными клетками с плотными контактами, выстилающими сосудистое сплетение желудочков мозга[116][117]. Гематоликворный барьер также играет свою роль в поддержании гомеостаза мозга. Через него из крови в омывающую мозг спинномозговую жидкость поступают витамины, нуклеотиды и глюкоза. Общий вклад гематоликворного барьера в процессы обмена между мозгом и кровью невелик. Суммарная поверхность гематоликворного барьера сосудистых сплетений желудочков мозга приблизительно в 5000 раз меньше в сравнении с площадью гематоэнцефалического.
Кроме гематоэнцефалического и гематоликворного барьеров в организме человека существуют гематоплацента́рный, гематотестикуля́рный, гематоклубо́чковый, гематоретина́льный, гематоти́мусный и гематолёгочный барьеры.
Транспорт веществ через ГЭБ[править | править код]

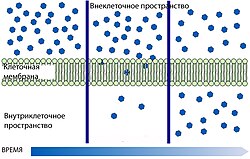
Гематоэнцефалический барьер не только задерживает и не пропускает целый ряд веществ из крови в вещество мозга, но и выполняет противоположную функцию — транспортирует необходимые для метаболизма ткани мозга вещества. Гидрофобные вещества и пептиды проникают в мозг либо с помощью специальных транспортных систем, либо через каналы клеточной мембраны. Для большинства других веществ возможна пассивная диффузия[6][36].
Межклеточный транспорт[править | править код]
В капиллярах периферических органов и тканей транспорт веществ осуществляется в основном через фенестра́ции сосудистой стенки и межклеточные промежутки. В норме между клетками эндотелия сосудов мозга такие промежутки отсутствуют. В связи с этим питательные вещества проникает в мозг лишь через клеточную мембрану[118]. Вода, глицерин и мочевина являются примерами тех небольших поляризованных молекул, которые могут свободно диффундировать через плотные контакты между эндотелиальными клетками ГЭБ[119].
Свободная диффузия[править | править код]

Самой простой формой транспорта через ГЭБ является свободная (или пассивная) диффузия. Она может осуществляться как через клеточные мембраны эндотелиоцитов, так и через плотные межклеточные контакты. Для диффузии веществ движущей силой является разница концентраций. Диффузия веществ пропорциональна градиенту концентраций в кровеносном русле и ткани мозга. Для неё не требуется затрат клеточной энергии[120].
Липофи́льные структурные элементы клеточной мембраны, а также плотные межклеточные контакты снижают количество веществ, которые могут свободно диффундировать через ГЭБ. Проницаемость ГЭБ напрямую зависит от липофильности каждого конкретного вещества[121].
Проницаемость ГЭБ также зависит от молярной массы вещества. Молекулы с массой более 500 г/моль не могут диффундировать через ГЭБ. В то же время ГЭБ не является механическим барьером, который свободно пропускает молекулы меньшего размера и не пропускает большего. Процесс клеточной диффузии является динамическим, при этом он легче для веществ с молярной массой 200 г/моль, чем для веществ с 450 г/моль[41][122]. Чем липофильнее и меньше вещество, тем легче оно диффундирует через клеточную мембрану[6].

Немецким биофизиком Германном Тро́йбле в 1971 году была высказана гипотеза о транспорте молекул с низкой массой через клеточную мембрану. Согласно ей они проникают в клетку через небольшие промежутки между цепями жирных кислот двойного слоя мембраны. Эти промежутки изменчивы, их образование не требует клеточной энергии[123][124][125][126]. Теория Тройбле была спектроскопически доказана в 1974 году[127][128].
Прогноз и исследования проницаемости ГЭБ тем или иным веществом возможно проводить как in vitro[36][122][129][130][131] так и in silico[132].
Липофильность и небольшая молекулярная масса не являются гарантией проницаемости ГЭБ для каждого конкретного вещества. Высокомолекулярные соединения (например, моноклона́льные антитела, рекомбина́нтные белки и другие) удерживаются ГЭБ[133].
Канальцевая проницаемость[править | править код]
Небольшие полярные вещества, например молекулы воды, с трудом могут диффундировать через гидрофобные отделы клеточной мембраны эндотелиоцита. Несмотря на это доказана высокая проницаемость ГЭБ для воды[134].
В клеточной мембране эндотелиоцита располагаются специальные гидрофильные каналы — аквапоры. В эндотелии периферических сосудов они образованы белком аквапорином-1 (AQP1), экспрессия которого ингибируется астроцитами в клетках сосудов мозга[135]. На поверхности мембран клеток капиллярной сети мозга представлены в основном аквапорин-4 (AQP4) и аквапорин-9 (AQP9)[136].
Через аквапоры происходит регуляция содержания воды в веществе мозга. Они делают возможным быструю диффузию воды как в направлении мозга так и в направлении сосудистого русла в зависимости от осмотического градиента концентраций электролитов[137]. Для глицерина, мочевины и ряда других веществ на поверхности клеточных мембран формируются собственные каналы — акваглицеропорины. В ГЭБ они представлены в основном белком аквапорином-9 (который также образует аквапоры)[138].

Процесс транспорта молекул через специализированные каналы осуществляется быстрее активного переноса с помощью специальных белков транспортёров. В то же время различные биологически активные вещества могут активировать или инактивировать транспортные каналы расположенные на клеточных мембранах[118].
Облегчённая диффузия[править | править код]
Особой формой диффузии через клеточную мембрану является облегчённая диффузия. Целый ряд необходимых для мозга веществ, как например, глюкоза и многие аминокислоты, полярны и слишком велики для непосредственной диффузии через клеточную мембрану. Для них на поверхности клеточных мембран эндотелиоцитов располагаются специальные транспортные системы. Например, для глюкозы и аскорбиновой кислоты (витамина С)[139] это GLUT-1-транспортёр. Их количество на поверхности обращённой в полость сосуда в 4 раза больше, чем на обращённой к мозгу.
Кроме транспортёров глюкозы на поверхности эндотелия располагаются множество белковых молекул выполняющих подобную функцию для других веществ. Так например MCT-1 и MCT-2 ответственны за перенос лактата, пирувата, мевалоновой кислоты, бутиратов и ацетатов. SLC7 транспортирует аргинин, лизин и орнитин. В геноме мыши выявлено 307 генов отвечающих за синтез SLC-белков, ответственных за облегчённую диффузию через клеточную мембрану различных веществ[140].
Транспортёры могут осуществлять перенос веществ в одном либо двух направлениях[141]. В отличие от активного транспорта облегчённая диффузия направлена в сторону пространства (внутри- или внеклеточного) с меньшей концентрацией вещества и не требует затрат клеточной энергии.
Активный транспорт[править | править код]

В отличие от пассивного транспорта, не требующего затрат энергии, активный заключается в переносе веществ в пространство с большей концентрацией вещества и требует больших затрат клеточной энергии, получаемой при распаде молекул АТФ[118]. При активном транспорте веществ из кровеносного русла в ткань мозга говорят о притоке вещества (англ. influx), в обратном направлении — об оттоке (англ. efflux).
В ГЭБ располагаются активные транспортёры энкефалина[142][143], антидиуретического гормона[144], [D-пеницилламин2,D-пеницилламин5]-энкефалина (DPDPE)[145].
Первым идентифицированным Efflux-транспортёром ГЭБ[146] является Р-гликопротеин, который закодирован геном MDR1.[147][148]
Впоследствии были открыты относящийся к классу ABC-транспортёров Multidrug Resistance-Related Proteine (MRP1)[149], Breast Cancer Resistance Proteine (BCRP)[150][151] расположенный преимущественно на обращённой в просвет сосуда поверхности[152][153].
Некоторые Efflux- и Influx-транспортёры являются стереоселективными, то есть переносят лишь определённый стереоизомер (энантиомер) того или иного вещества. Так например, D-изомер аспарагиновой кислоты является прекурсором N-метил-D-аспартата (NMDA), который влияет на секрецию различных гормонов: лютеинизирующего гормона, тестостерона или окситоцина[154]. L-изомеры аспарагиновой и глутаминовой кислоты являются стимулирующими аминокислотами и их избыток токсичен для ткани мозга[155]. Efflux-транспортёр ASCT2 (аланин-серин-цистеин-транспортёр) ГЭБ выводит в кровеносное русло L-изомер аспарагиновой кислоты, чьё накопление имеет токсический эффект. Необходимый для формирования NMDA D-изомер поступает в мозг с помощью других транспортных белков (EAAT, SLC1A3, SLC1A2, SLC1A6)[25][156][157].
В эпилептогенной ткани в эндотелии и астроцитах представлено большее количество белка Р-гликопротеина по сравнению с нормальной тканью мозга[158][159].
На клеточных мембранах эндотелиоцитов располагаются также транспортёры анионов (OAT и OATP)[160][161]. Большое количество Efflux-транспортёров выводят из эндотелиоцитов целый ряд веществ в кровеносное русло[120].
Для многих молекул до сих пор не ясно выводятся ли они путём активного транспорта (с затратами клеточной энергии) или путём облегчённой диффузии[25].
Везикулярный транспорт[править | править код]
Рецептор-опосредованный трансцитоз[править | править код]

С помощью рецептор-опосредованного трансцито́за происходит перенос больших молекул. На обращённой в просвет сосуда поверхности клетки расположены специальные рецепторы для опознавания и связывания определённых веществ[23]. После контакта рецептора с веществом-мишенью происходит их связывание, участок мембраны инвагинируется в полость клетки и образуется внутриклеточный пузырёк — везикула. Затем она перемещается к обращённой к нервной ткани поверхности эндотелиальной клетки, сливается с ней и высвобождает связанные вещества. Таким образом во внеклеточное пространство мозга переносятся состоящий из 679 аминокислот белок трансферрин массой 75,2 кДа[162], липопротеины низкой плотности из которых образуется холестерин[130][163], инсулин[164] и другие пептидные гормоны[23].
Абсорбцио-опосредованный трансцитоз[править | править код]
Одним из подвидов везикулярного транспорта является абсорбцио-опосредованный трансцитоз. Отмечается «прилипание» ряда положительно заряженных веществ (катионов) к отрицательно заряженной клеточной мембране с последующем образованием везикулярного пузырька и его переносом к противоположной поверхности клетки. Данный вид транспорта также называется катионным. Он проходит относительно быстрее рецептор-опосредованного трансцитоза[165][166][167][168].
Исследование проницаемости[править | править код]
Появление большого количества новых лекарственных веществ сделало изучение степени проницаемости ГЭБ для различных веществ крайне актуальным. Это относится не только к тем препаратам, которые используются в неврологии и нейрохирургии и чьё действие непосредственно зависит от их способности преодолевать ГЭБ, но и тем, которые используются в других областях медицины[169]. Для исследования проницаемости ГЭБ применяется ряд методов. Классическим является проведение опытов на живых организмах (in vivo). Новые достижения науки сделали возможными эксперименты на клеточных культурах (in vitro), а также моделирование процесса на компьютере (in silico)[170]. Результаты, полученные у млекопитающих (in vivo), могут быть использованы для описания проницаемости ГЭБ для того или иного вещества у человека.
Физические основы[править | править код]
Для определения проницаемости ГЭБ Ренкином (1959) и Кроне (1965) предложена модель, которая основывается на исследовании одного капилляра. Несмотря на свою упрощённость, она приближена к реальности[171]. На основании данной модели определяется величина Кроне-Ренкина, которая показывает, какая часть вещества при прохождении через кровеносное русло мозга проникнет через ГЭБ[172]. При её значении менее 0,2 ГЭБ слабопроницаем для вещества, при 0,2-0,8 — умеренно проницаем[171].
Исследования in silico[править | править код]
Симуляция процесса с использованием ЭВМ проводится в самых ранних фазах исследования. Высчитывается уровень свободной диффузии, учитывая ряд характеристик вещества: его липофильность, молярную массу, количество водородных связей и др.[170]
Исследования in vitro[править | править код]
Опыты in vitro проводятся для изучения транспортных процессов на клеточном уровне на изолированных капиллярах[36]. В ходе эксперимента у подопытного животного выделяются сосуды. Обязательным является сохранение в них метаболической активности[173]. Затем они помещаются между растворами с различными концентрациями исследуемых веществ. Молекулы могут быть маркированы. Метод позволяет определить проницаемость ГЭБ для конкретного вещества, а также процессы его переноса[170][174][175].
Исследования in vivo[править | править код]
Первым, кто провёл in vivo исследования ГЭБ, был Пауль Эрлих. Эксперименты по проницаемости тех или иных веществ через ГЭБ заключаются в их непосредственном введении в кровеносное русло, а затем определении содержания в ткани мозга. По Вальтеру (F. Walter, 1929), вещества, применяемые с этой целью, должны удовлетворять следующим требованиям: распределяться в крови и цереброспинальной жидкости до того, как наступает их выделение, не расщепляться в организме и не связываться с белками; они не должны изменять состояние ГЭБ и приносить вред организму[19]. Лишь при выполнении этих условий возможно определение проницаемости ГЭБ для определённого вещества in vivo.
Повреждения ГЭБ[править | править код]
Повреждения ГЭБ у человека наблюдаются при целом ряде заболеваний. Их коррекция рассматривается как терапевтическая стратегия[176].
Синдром дефицита белка GLUT-1[править | править код]
Синдром дефицита белка GLUT-1 (G93.4 по международной классификации болезней ВОЗ[177]) — редкое аутосомно-доминантное наследственное заболевание, при котором отмечается нарушение синтеза белка GLUT-1, который ответственен за проницаемость ГЭБ для глюкозы и аскорбиновой кислоты. Заболевание проявляется в раннем детском возрасте. Недостаток поступления в ткань мозга глюкозы вызывает развитие микроцефалии, психомоторных нарушений, атаксии и целого ряда других неврологических расстройств[178].
Наследственная мальабсорбция фолиевой кислоты[править | править код]
Наследственная мальабсорбция фолиевой кислоты (D52.8 по международной классификации болезней ВОЗ[177]) — редкое аутосомно-рецессивное наследственное заболевание, при котором отмечается недостаток синтеза белка, обеспечивающего проницаемость ГЭБ для фолиевой кислоты.
Болезнь Альцгеймера[править | править код]
Нарушение функционирования ГЭБ при болезни Альцгеймера приводит к увеличению количества амилоида β в мозге. Снижение количества спинномозговой жидкости приводит к повышению концентрации нейротоксичных веществ. Нейроваскулярная гипотеза патогенеза болезни Альцгеймера предполагает, что накопление амилоида β также связано с нарушением функционирования транспортеров, опосредующих перенос вещества из мозга в кровь, например, P-гликопротеина и LRP1. При воспалительных процессах повышается захват амилоида β перицитами, что приводит к их гибели. Кроме того, при болезни Альцгеймера снижена эффективность транспорта инсулина через ГЭБ, играющего нейропротекторную роль[176].
Сахарный диабет[править | править код]
Сахарный диабет (E10-E14 по международной классификации болезней ВОЗ[177]) является заболеванием, при котором возникает целый ряд функциональных и структурных изменений различных органов и тканей организма. Также отмечаются значительные изменения ГЭБ, которые проявляются в физикохимической перестройке мембраны эндотелиальных клеток и плотных контактов между ними[179].
Рассеянный склероз[править | править код]
См. также Хроническая цереброспинальная венозная недостаточность
Рассеянный склероз (G35 по международной классификации болезней ВОЗ[177]) — хроническое прогрессирующее заболевание нервной системы, при котором отмечается преимущественное поражение белка миелина ткани мозга.
Сосуды мозга здоровых людей непроницаемы для клеток крови, в том числе иммунных клеток. У больных рассеянным склерозом происходит миграция активированных Т-лимфоцитов в паренхиму мозга через ГЭБ, повышается уровень провоспалительных цитокинов — γ-интерферона, ФНО-α, ИЛ-1 и других; активируются В-лимфоциты. В результате начинают синтезироваться антитела к белку миелину, что приводит к формированию очагов воспалительной демиелинизации[180].
Ишемический инсульт[править | править код]

Ишемический инсульт (I63 по международной классификации болезней ВОЗ[177]) — острое нарушение мозгового кровообращения, обусловленное недостаточностью поступления крови к участкам центральной нервной системы.
Ишемический инсульт приводит к высвобождению оксидантов, протеолитических ферментов и цитокинов в ткани мозга, что в итоге вызывает развитие цитотоксического отёка и изменение проницаемости ГЭБ[181]. В результате запускается процесс миграции лейкоцитов через эндотелий в ткань мозга, которые вызывают в том числе поражение здоровых клеток нервной ткани[182][183].
Бактериальная инфекция центральной нервной системы[править | править код]
Лишь немногие попадающие в кровь патогенные микроорганизмы способны проникать через ГЭБ. К ним относятся менингококки (лат. Neisseria meningitidis), некоторые виды стрептококков — в том числе пневмококки (лат. Streptococcus pneumoniae), гемофильная палочка (лат. Haemophilus influenzae), листерии, кишечные палочки (лат. Escherichia coli) и ряд других. Все они могут вызывать воспалительные изменения как мозга — энцефалит, так и его оболочек — менингит. Точный механизм проникновения этих патогенов через ГЭБ до конца не изучен, однако показано, что воспалительные процессы оказывают влияние на этот механизм[184]. Так, воспаление, вызванное листериями, может привести к тому, что ГЭБ становится проницаемым для данных бактерий. Прикрепившись к эндотелиоцитам капилляров мозга, листерии выделяют целый ряд липополисахаридов и токсинов, которые в свою очередь воздействуют на ГЭБ, делая его проницаемым для лейкоцитов. Проникшие в ткань мозга лейкоциты запускают воспалительный процесс, в результате которого ГЭБ пропускает и бактерии[184].
Пневмококки секретируют фермент группы гемолизинов, который образует поры в эндотелии, через которые и проникает бактериальный агент[185].
Менингококки и E. coli проникают через ГЭБ трансэндотелиально[184].
Вирусы и ГЭБ[править | править код]
Кроме бактерий, через ГЭБ в ткань мозга могут проникать некоторые вирусы. К ним относятся цитомегаловирус, вирус иммунодефицита человека (ВИЧ)[186] и Т-лимфотропный вирус человека (HTLV-1).
Опухоли головного мозга[править | править код]
Внутримозговые опухоли головного мозга (глиобластомы, метастазы в мозг и др.) выделяют целый ряд веществ[184], которые дезинтегрируют работу ГЭБ и нарушают его избирательную проницаемость. Такие повреждения гематоэнцефалического барьера вокруг опухоли может вызвать вазогенный отёк мозга[187].
Проницаемость ГЭБ для антибактериальных препаратов[править | править код]
ГЭБ избирательно проницаем для различных лекарственных веществ, что учитывается в медицине при назначении препаратов для лечения заболеваний центральной нервной системы (ЦНС). Такие препараты должны проникать в ткань мозга к клеткам-мишеням. Также имеет значение то, что при инфекционно-воспалительных заболеваниях ЦНС проницаемость ГЭБ повышается, и через него могут проходить те вещества, для которых он в нормальном состоянии служил непреодолимой преградой. Особенно актуально это для антибактериальных препаратов.
Проникновение антибактериальных препаратов через ГЭБ[188]
| Хорошо | Хорошо при воспалении | Плохо даже при воспалении | Не проникают |
|---|---|---|---|
| Изониазид | Азтреонам | Гентамицин | Клиндамицин |
| Пефлоксацин | Амикацин | Карбенициллин | Линкомицин |
| Рифампицин | Амоксициллин | Макролиды | |
| Хлорамфеникол | Ампициллин | Норфлоксацин | |
| Ко-тримоксазол | Ванкомицин | Стрептомицин | |
| Меропенем | Ломефлоксацин | ||
| Офлоксацин | |||
| Цефалоспорины III—IV поколения | |||
| Ципрофлоксацин | |||
| Левофлоксацин |
См. также[править | править код]
- Гистогематический барьер
- Гематоофтальмологический барьер
- Гематотимусный барьер
- Гематотестикулярный барьер
- Гематоплацентарный барьер
- Гематосаливарный барьер
Примечания[править | править код]
- ↑ Кассиль, 1971.
- ↑ P. Ehrlich. Das Sauerstoff-Bedürfniss des Organismus: Eine Farbenanalytische Studie // August Hirschwald, Berlin (die Habilitationsschrift von Paul Ehrlich). — 1885. — С. 167.
- ↑ P. Ehrlich. Ueber die Beziehungen von chemischer Constitution, Verteilung und Pharmakologischer Wirkung // Gesammelte Arbeiten zur Immunitaetsforschung. August Hirschwald, Ber. — 1904. — С. 574.
- ↑ E. E. Goldmann. Die äußere und innere Sekretion des gesunden und kranken Organismus im Lichte der vitalen Färbung // Beitr Klin Chirurg. — 1909. — № 64. — С. 192–265.
- ↑ E. E. Goldmann. Vitalfärbung am Zentralnervensystem // Abh. K. Preuss. Akad. Wiss. Phys. Med. — 1913. — № 1. — С. 1–60.
- ↑ 1 2 3 4 5 S. Nobmann. Isolierte Gehirn-Kapillaren als in vitro-Modell der Blut-Hirn Schranke // Диссертация. Гейдельбергский университет им. Рупрехта-Карла. — 2001. Архивировано 3 июля 2007 года.
- ↑ A. Biedl, R. Kraus. Über eine bisher unbekannte toxische Wirkung der Gallensäuren auf das zentrale Nervensystem // Zentralblatt Innere Medizin. — 1898. — № 19. — С. 1185–1200.
- ↑ M. Lewandowsky. Zur Lehre von der Cerebrospinal Flüssigkeit // Zentralblatt Klinische Medizin. — 1900. — № 40. — С. 480–494.
- ↑ 1 2 3 4 B. T. Hawkins, T. P. Davis. The blood-brain barrier/neurovascular unit in health and disease // Pharmacol Rev. — 2005. — № 57. — С. 173–185. Архивировано 18 февраля 2019 года.
- ↑ 1 2 Constantin von Monakow (1853—1930) and Lina Stern (1878—1968): early explorations of the plexus choroideus and the blood-brain barrier (недоступная ссылка)
- ↑ L’Université de Genève «Lina Stern». Дата обращения: 2 июля 2010. Архивировано 18 октября 2017 года.
- ↑ В. Б. Малкин «Трудные годы Лины Штерн». Дата обращения: 2 июля 2010. Архивировано 23 февраля 2008 года.
- ↑ L. Stern. Le liquide céphalorachidien au point de vue de ses rapports avec la circulation sanguine et avec les éléments nerveux de l’axe cérébrospinal. Schweiz Arch Neurol Psychiat 11:373—378, 1921; L. Stern, R. Gautier. Recherches sur le liquide céphalo-rachidien I: Rapports enter le liquide céphalorachdien et la circulation sanguine. Arch int Physiol 17:138—192, 1921; L. Stern, R. Gautier. Recherches sur le liquide céphalo-rachidien II: Les rapports enter le liquide céphalorachdien et les élments nerveux de l’axe cérébrospinal. Arch Int Physiol 17:391—448, 1922.
- ↑ A. A. Vein. Lina Stern: Science and fate // Neurologie-Abteilung der Universität Leiden. — 2006. Архивировано 2 января 2018 года.
- ↑ Lina Stern. Дата обращения: 1 июля 2010. Архивировано 11 апреля 2010 года.
- ↑ Die Struktur Der Blut-Hirn- Und Der Blut-Liquor-Schranke — eine Literaturstudie, стр. 6. Дата обращения: 1 июля 2010. Архивировано 11 января 2011 года.
- ↑ L. Stern, E. Rothlin. Effets de l’action directe du curare sur les différentes parties du cervelet. Schweizer Archiv für Neurologie und Psychiatrie 3:234—254, 1918.
- ↑ L. Stern, R. Gautier. Recherches sur le liquide céphalo-rachidien III: Arch Intern Physiol 18:403—436, 1923; L. Stern. La barrière hémato-encéphalique dans les conditions normales et dans les conditions pathologiques. Schweiz Arch Neurol Psychiat 13:604—616, 1923.
- ↑ 1 2 Гемато-энцефалический барьер // Большая медицинская энциклопедия / Гл. ред. Б. В. Петровский. — 3-е изд. — М.:: Советская энциклопедия, 1977. — Т. V (Гамбузия-Гипотиазид). — С. 127—129. — 576 с.
- ↑ J. J. Dreifuss, N. Tikhonov «Lina Stern (1878—1968): Physiologin und Biochemikerin, erste Professorin an der Universität Genf und Opfer stalinistischer Prozesse»
- ↑ F. K. Walter. Die allgemeinen Grundlagen des Stoffaustausches zwischen dem Zentralnervensystem und dem übrigen Körper // Arch Psychiatr Nervenkr. — 1930. — № 101. — С. 195–230.
- ↑ H. Spatz. Die Bedeutung der vitalen Färbung für die Lehre vom Stoffaustausch zwischen dem Zentralnervensystem und dem übrigen Körper // Arch Psychiatr Nervenkr. — 1933. — С. 267–358.
- ↑ 1 2 3 4 5 6 7 8 9 S. Wolf, B. Seehaus, Minol K. und andere. Die Blut-Hirn-Schranke: Eine Besonderheit des cerebralen Mikrozirkulationssystems // Naturwissenschaften. — 1996. — № 83. — С. 302—311. (недоступная ссылка)
- ↑ Reese TS, Karnovsky MJ. Fine structural localization of a blood-brain barrier to exogenous peroxidase // J Cell Biol. — 1967. — № 34. — С. 207–217. Архивировано 18 февраля 2019 года.
- ↑ 1 2 3 4 S. Ohtsuki. New Aspects of the Blood–Brain Barrier Transporters; Its Physiological Roles in the Central Nervous System // Biological & Pharmaceutical Bulletin. — 2004. — № 27 (10). — С. 1489–1496. (недоступная ссылка)
- ↑ W. Risau, B. Engelhardt, H. Wekerle. Immune function of the blood-brain barrier: incomplete presentation of protein (auto-) antigens by rat brain microvascular endothelium in vitro // The Journal of Cell Biology. — 1990. — № 110. — С. 1757–1766. Архивировано 17 апреля 2011 года.
- ↑ 1 2 3 B. Bauer. In vitro Zellkulturmodelle der Blut-Hirn-Schranke zur Untersuchung der Permeation und P-Glykoprotein-Interaktion von Arzneistoffen // Диссертация. Гейдельбергский университет им. Рупрехта-Карла. — 2002. (недоступная ссылка)
- ↑ 1 2 M. Bundgaard, N. J. Abbott. All vertebrates started out with a glial blood-brain barrier 4-500 million years ago // Glia. — 2008. — № 56. — С. 699–708. Архивировано 4 июня 2016 года.
- ↑ 1 2 3 4 W. M. Pardridge. Molecular biology of the blood–brain barrier // Mol Biotechnol. — 2005. — № 30 (1). — С. 57–70. Архивировано 19 февраля 2019 года.
- ↑ J. C. Lee. Evolution in the concept of the blood-brain barrier phenomen // Progress in neuropathology. — Verlag Grune und Stratton, 1971. — Т. 1. — С. 84–145. — ISBN 0-88167-188-6.
- ↑ 1 2 3 4 M. Pavelka, J. Roth. Funktionelle Ultrastruktur. — Verlag Springer. — С. 234–235. — ISBN 3-211-83563-6..
- ↑ R. S. el-Bacha, A. Minn. Drug metabolizing enzymes in cerebrovascular endothelial cells afford a metabolic protection to the brain // Cell Mol Biol. — 1999. — № 45. — С. 15–23. Архивировано 4 июня 2016 года.
- ↑ Chat M, Bayol-Denizot C, Suleman G, Roux F, Minn A. Drug metabolizing enzyme activities and superoxide formation in primary and immortalized rat brain endothelial cells // Life Sci. — 1998. — № 62. — С. 151–163. Архивировано 27 мая 2016 года.
- ↑ Minn A, Ghersi-Egea JF, Perrin R, Leininger B, Siest G. Drug metabolizing enzymes in the brain and cerebral microvessels // Life Sci. — 1991. — № 116. — С. 65–82. Архивировано 18 февраля 2019 года.
- ↑ 1 2 3 4 Takakura Y, Audus KL, Borchardt RT. Blood-brain barrier: transport studies in isolated brain capillaries and in cultured brain endothelial cells // Adv Pharmacol. — 1991. — № 22. — С. 137–165. Архивировано 18 февраля 2019 года.
- ↑ Méresse S, Dehouck MP, Delorme P, Bensaïd M, Tauber JP, Delbart C, Fruchart JC, Cecchelli R. Bovine brain endothelial cells express tight junctions and monoamine oxidase activity in long-term culture // J Neurochem. — 1989. — № 53. — С. 1363–1371. Архивировано 19 февраля 2019 года.
- ↑ Perrin R, Minn A, Ghersi-Egea JF, Grassiot MC, Siest G. Distribution of cytochrome P450 activities towards alkoxyresorufin derivatives in rat brain regions, subcellular fractions and isolated cerebral microvessels // Biochem Pharmacol. — 1990. — № 40. — С. 2145–2151. Архивировано 18 февраля 2019 года.
- ↑ Bendayan R, Lee G, Bendayan M. Functional expression and localization of P-glycoprotein at the blood brain barrier // Res Tech. — 2002. — № 57. — С. 365–380. Архивировано 29 мая 2016 года.
- ↑ Su Y, Sinko PJ. Drug delivery across the blood-brain barrier: why is it difficult? how to measure and improve it? // Expert Opin Drug Deliv. — 2006. — № 3. — С. 419–435. Архивировано 4 июня 2016 года.
- ↑ 1 2 Fischer H, Gottschlich R, Seelig A. Blood-brain barrier permeation: molecular parameters governing passive diffusion // J Membr Biol. — 1998. — № 165. — С. 201–211. Архивировано 26 мая 2016 года.
- ↑ U. Fagerholm. The highly permeable blood-brain barrier: an evaluation of current opinions about brain uptake capacity // J Membr Biol. — 2007. — № 12. — С. 1076–1082. Архивировано 20 февраля 2019 года.
- ↑ Nico B, Frigeri A, Nicchia GP, Quondamatteo F, Herken R, Errede M, Ribatti D, Svelto M, Roncali L. Role of aquaporin-4 water channel in the development and integrity of the blood-brain barrier // J Cell Sci. — 2001. — № 114. — С. 1297–1307. Архивировано 19 февраля 2019 года.
- ↑ Butt AM, Jones HC, Abbott NJ. Electrical resistance across the blood-brain barrier in anaesthetized rats: a developmental study // J Physiol. — 1990. — № 429. — С. 47—62. Архивировано 26 мая 2016 года.
- ↑ P. Claude, D. A. Goodenough. Fracture faces of zonulae occludentes from "tight" and "leaky" epithelia // J Cell Biol. — 1973. — № 58. — С. 390—400. Архивировано 25 июня 2016 года.
- ↑ Wolburg H, Neuhaus J, Kniesel U, Krauss B, Schmid EM, Ocalan M, Farrell C, Risau W. Modulation of tight junction structure in blood-brain barrier endothelial cells. Effects of tissue culture, second messengers and cocultured astrocytes // J Cell Sci. — 1994. — № 107. — С. 1347–1357. Архивировано 4 июня 2016 года.
- ↑ 1 2 H. B. Newton. Advances in strategies to improve drug delivery to brain tumors // Expert Rev Neurother. — 2006. — № 6. — С. 1495–1509. Архивировано 29 мая 2016 года.
- ↑ J. L. Madara. Tight junction dynamics: is paracellular transport regulated? // Cell. — 1988. — № 53. — С. 497–498. Архивировано 21 мая 2016 года.
- ↑ H. C. Bauer et al. Proteins of the tight junctions in the blood-brain barrier // Blood-spinal Cord and Brain Barriers in Health and Disease. — Verlag Elsevier, 2004. — С. 1–10.
- ↑ Cecchelli R, Berezowski V, Lundquist S, Culot M, Renftel M, Dehouck MP, Fenart L. Modelling of the blood-brain barrier in drug discovery and development // Nat Rev Drug Discov. — 2007. — № 6. — С. 650–661. Архивировано 19 мая 2016 года.
- ↑ Matter K, Balda MS. Holey barrier: claudins and the regulation of brain endothelial permeability // J Cell Biol. — 2003. — № 161. — С. 459–460. Архивировано 18 февраля 2019 года.
- ↑ Nitta T, Hata M, Gotoh S, Seo Y, Sasaki H, Hashimoto N, Furuse M, Tsukita S. Size-selective loosening of the blood-brain barrier in claudin-5-deficient mice // J Cell Biol. — 2003. — № 161. — С. 653–660. Архивировано 22 февраля 2017 года.
- ↑ P. Dore-Duffy. Pericytes: pluripotent cells of the blood brain barrier // Curr Pharm Des. — 2008. — № 14. — С. 1581—1593. Архивировано 18 февраля 2019 года.
- ↑ Balabanov R, Dore-Duffy P. Role of the CNS microvascular pericyte in the blood-brain barrier // J Neurosci Res. — 1998. — № 53. — С. 637—644. Архивировано 18 февраля 2019 года.
- ↑ 1 2 3 4 Rucker HK, Wynder HJ, Thomas WE. Cellular mechanisms of CNS pericytes // Brain Res Bull. — 2000. — № 51. — С. 363—369. Архивировано 18 февраля 2019 года.
- ↑ P. A. D'Amore. Culture and Study of Pericytes // Cell Culture Techniques in Heart and Vessel Research. — Verlag Springer, 1990. — С. 299. — ISBN 3-540-51934-3..
- ↑ N. J. Abbott. Neurobiology. Glia and the blood-brain barrier // Nature. — 1987. — № 325. — С. 195. Архивировано 20 мая 2016 года.
- ↑ Lai CH, Kuo KH. The critical component to establish in vitro BBB model: Pericyte // Brain Res Brain Res Rev. — 2005. — № 50. — С. 258—265. Архивировано 18 февраля 2019 года.
- ↑ 1 2 Shepro D, Morel NM. Pericyte physiology // FASEB. — 1993. — № 7. — С. 1031–1038. Архивировано 18 февраля 2019 года.
- ↑ 1 2 Sims DE. Diversity within pericytes // Clin Exp Pharmacol Physiol. — 2000. — № 27. — С. 842–846. Архивировано 19 мая 2016 года.
- ↑ Engelhardt B. Development of the blood-brain barrier // Cell Tissue Res. — 2003. — № 314. — С. 119–129. Архивировано 18 февраля 2019 года.
- ↑ Fujimoto K. Pericyte-endothelial gap junctions in developing rat cerebral capillaries: a fine structural study // Anat Rec. — 1995. — № 242. — С. 562—565. Архивировано 3 июня 2016 года.
- ↑ Díaz-Flores L, Gutiérrez R, Varela H, Rancel N, Valladares F. Microvascular pericytes: A review of their morphological and functional characteristics // Histol Histopath. — 1991. — № 6. — С. 269–286. Архивировано 18 февраля 2019 года.
- ↑ D. E. Sims. Recent advances in pericyte biology--implications for health and disease // Can J Cardiol. — 1991. — № 7. — С. 431–443. Архивировано 20 февраля 2019 года.
- ↑ Herman IM, D'Amore PA. Microvascular pericytes contain muscle and nonmuscle actins // J Cell Biol. — 1985. — № 101. — С. 43–52. Архивировано 18 февраля 2019 года.
- ↑ Hirschi KK, D'Amore PA. Pericytes in the microvasculature // Cardiovasc Res. — 1996. — № 32. — С. 687—698. Архивировано 29 мая 2016 года.
- ↑ Mato M, Ookawara S, Sugamata M, Aikawa E. Evidence for the possible function of the fluorescent granular perithelial cells in brain as scavengers of high-molecular-weight waste products // Experientia. — 1984. — № 40. — С. 399—402. Архивировано 29 мая 2016 года.
- ↑ Balabanov R, Washington R, Wagnerova J, Dore-Duffy P. CNS microvascular pericytes express macrophage-like function, cell surface integrin alphaM, and macrophage marker ED-2 // Microvasc Res. — 1996. — № 52. — С. 127—142. Архивировано 18 февраля 2019 года.
- ↑ Hickey WF, Kimura H. Perivascular microglial cells of the CNS are bone marrow-derived and present antigen in vivo // Science. — 1988. — № 239. — С. 290—292. Архивировано 18 февраля 2019 года.
- ↑ Fabry Z, Sandor M, Gajewski TF, Herlein JA, Waldschmidt MM, Lynch RG, Hart MN. Differential activation of Th1 and Th2 CD4+ cells by murine brain microvessel endothelial cells and smooth muscle/pericytes // J Immunol. — 1993. — № 151. — С. 38—47. Архивировано 18 февраля 2019 года.
- ↑ Krause D, Kunz J, Dermietzel R. Cerebral pericytes - a second line of defense in controlling blood-brain barrier peptide metabolism // Adv Exp Med Biol. — 1993. — № 331. — С. 149—152. Архивировано 18 февраля 2019 года.
- ↑ Thomas WE. Brain macrophages: on the role of pericytes and perivascular cells // Brain Res Brain Res Rev. — 1999. — № 31. — С. 42—57. Архивировано 20 февраля 2019 года.
- ↑ Iadecola C. Neurovascular regulation in the normal brain and in Alzheimer's disease // Nat Rev Neurosci. — 2004. — № 5. — С. 347—360. Архивировано 4 июня 2016 года.
- ↑ Johanson CE. Permeability and vascularity of the developing brain: cerebellum vs cerebral cortex // Brain Res. — 2004. — № 190. — С. 3–16. Архивировано 18 февраля 2019 года.
- ↑ Neuhaus J, Risau W, Wolburg H. Induction of blood-brain barrier characteristics in bovine brain endothelial cells by rat astroglial cells in transfilter coculture // Ann N Y Acad Sci. — 1991. — № 633. — С. 578–580. Архивировано 18 февраля 2019 года.
- ↑ Stewart PA, Wiley MJ. Developing nervous tissue induces formation of blood-brain barrier characteristics in invading endothelial cells: a study using quail–chick transplantation chimeras // Dev Biol. — 1981. — № 84. — С. 183–192. Архивировано 3 июля 2016 года.
- ↑ Raub TJ, Kuentzel SL, Sawada GA. Permeability of bovine brain microvessel endothelial cells in vitro: barrier tightening by a factor released from astroglioma cells // Exp Cell Res. — 1992. — № 199. — С. 330–340. Архивировано 18 февраля 2019 года.
- ↑ 1 2 3 4 Abbott NJ. Astrocyte-endothelial interactions and blood-brain barrier permeability // J Anat. — 2002. — № 200. — С. 629–638. Архивировано 19 февраля 2019 года.
- ↑ Paulson OB, Newman EA. Does the release of potassium from astrocyte endfeet regulate cerebral blood flow? // Science. — 1987. — № 237. — С. 896—898. Архивировано 28 мая 2016 года.
- ↑ Abbott NJ, Rönnbäck L, Hansson E. Astrocyte-endothelial interactions at the blood-brain barrier // Nat Rev Neurosci. — 2006. — № 7. — С. 41–53. Архивировано 3 июля 2016 года.
- ↑ Björkhem I, Meaney S. Brain cholesterol: long secret life behind a barrier // Arterioscler Thromb Vasc Biol. — 2004. — № 24. — С. 806—815. Архивировано 2 июля 2017 года.
- ↑ Синельников Р. Д., Синельников Я. Р. Атлас анатомии человека в 4 томах. Т.4. — М.:: Медицина, 1996. — С. 82. — 320 с. — ISBN 5-225-02723-7.
- ↑ Синельников Р. Д., Синельников Я. Р. Атлас анатомии человека в 4 томах. Т.4. — М.:: Медицина, 1996. — С. 56. — 320 с. — ISBN 5-225-02723-7.
- ↑ Duvernoy HM, Risold PY. The circumventricular organs: an atlas of comparative anatomy and vascularization // Brain Res Rev. — 2007. — № 56. — С. 119—147.
- ↑ C. Lohmann. Die Blut-Hirn-Schranke in vitro: Regulation der Permeabilität durch Matrixmetalloproteasen // Диссертация. Вестфальский университет имени Вильгельма. — 2003. Архивировано 24 февраля 2013 года.
- ↑ W. M. Pardridge. Peptide Drug Delivery to the Brain. — Raven Press, 1991. — С. 123. — ISBN 0-88167-793-0.
- ↑ Chiou WL, Barve A. Linear correlation of the fraction of oral dose absorbed of 64 drugs between humans and rats // Pharm Res. — 1998. — № 15. — С. 1792—1795. Архивировано 19 мая 2016 года.
- ↑ Goodwin JT, Clark DE. In silico predictions of blood-brain barrier penetration: considerations to "keep in mind" // J Pharmacol Exp Ther. — 2005. — № 315. — С. 477—483. Архивировано 20 мая 2016 года.
- ↑ Lindstedt L, Schaeffer PJ. Use of allometry in predicting anatomical and physiological parameters of mammals // Lab Anim. — 2002. — № 36. — С. 1—19. Архивировано 18 февраля 2019 года.
- ↑ Lindstedt L, Schaeffer PJ. A proposed blood circulation model for Reference Man // Health Phys. — 1995. — № 69. — С. 187—201. Архивировано 18 февраля 2019 года.
- ↑ Willmann S, Schmitt W, Keldenich J, Lippert J, Dressman JB. A physiological model for the estimation of the fraction dose absorbed in humans // J Med Chem. — 2004. — № 47. — С. 4022—4031. Архивировано 28 мая 2016 года.
- ↑ Fagerholm U, Johansson M, Lennernäs H. Comparison between permeability coefficients in rat and human jejunum // J Med Chem. — 1996. — № 13. — С. 1336—1342. Архивировано 21 мая 2016 года.
- ↑ Leggett RW, Williams LR. Suggested reference values for regional blood volumes in humans // Health Phys. — 1991. — № 60. — С. 139—154. Архивировано 18 февраля 2019 года.
- ↑ G. B. Wislocki. Experimental studies on fetal absorption. I. The vitally stained fetus // Contrib Embryol Carnegie Inst. — 1920. — № 5. — С. 45—52.
- ↑ Wakai S, Hirokawa N. Development of the blood-brain barrier to horseradish peroxidase in the chick embryo // Cell Tissue Res. — 1978. — № 195. — С. 195—203. Архивировано 27 мая 2016 года.
- ↑ Risau W, Hallmann R, Albrecht U. Differentiation-dependent expression of proteins in brain endothelium during development of the blood-brain barrier // Dev Biol. — 1986. — № 117. — С. 537—545. Архивировано 29 октября 2012 года.
- ↑ Reynolds ML, Evans CA, Reynolds EO, Saunders NR, Durbin GM, Wigglesworth JS. Intracranial haemorrhage in the preterm sheep fetus // Early Hum Dev. — 1979. — № 3. — С. 163—186. Архивировано 18 февраля 2019 года.
- ↑ L. Stern, R. Peyrot. Le fonctionnement de la barrière hémato-éncephalique aux divers stades de développement chez les diverses espèces animales // Compte Rendu des Societe de Biologie (Paris). — 1927. — № 96. — С. 1124–1126.
- ↑ L. Stern et al. Le fonctionnement de la barrière hémato-éncephalique aux divers stades de développement chez les diverses espèces animales // Compte Rendu Soc Biol. — 1929. — № 100. — С. 231–233.
- ↑ Saunders NR, Habgood MD, Dziegielewska KM. Barrier mechanisms in the brain, II. Immature brain // Clin Exp Pharmacol Physiol. — 1999. — № 26. — С. 85–91. Архивировано 2 июня 2016 года.
- ↑ 1 2 N. R. Saunders. Development of the blood–brain barrier to macromolecules // The Fluids and Barriers of the Eye and Brain / M. B. Segal. — Verlag MacMillan. — Raven Press, 1991. — С. 128—155. — ISBN 0-8493-7707-2.
- ↑ Schumacher U, Mollgård K. The multidrug-resistance P-glycoprotein (Pgp, MDR1) is an early marker of blood-brain barrier development in the microvessels of the developing human brain // Histochem Cell Biol. — 1997. — № 108. — С. 179–182. Архивировано 4 июня 2016 года.
- ↑ Dziegielewska KM, Evans CA, Malinowska DH, Møllgård K, Reynolds JM, Reynolds ML, Saunders NR. Studies of the development of brain barrier systems to lipid insoluble molecules in fetal sheep // J Physiol. — 1979. — № 292. — С. 207–231. Архивировано 18 февраля 2019 года.
- ↑ Ferguson RK, Woodbury DM. Penetration of 14C-inulin and 14C-sucrose into brain, cerebrospinal fluid and skeletal muscle of developing rats // Exp Brain Res. — 1969. — № 7. — С. 181–194. Архивировано 26 мая 2016 года.
- ↑ Habgood MD, Knott GW, Dziegielewska KM, Saunders NR. The nature of the decrease in blood-cerebrospinal fluid barrier exchange during postnatal brain development in the rat // J Physiol. — 1993. — № 468. — С. 73–83. Архивировано 26 мая 2016 года.
- ↑ C. E. Johanson. Ontogeny of the blood–brain barrier // Implications of the Blood–Brain Barrier and Its Manipulation / E. A. Neuwelt. — Plenum Press, 1989. — С. 157—198.
- ↑ Braun LD, Cornford EM, Oldendorf WH. Newborn rabbit blood-brain barrier is selectively permeable and differs substantially from the adult // J Neurochem. — 1980. — № 34. — С. 147–152. Архивировано 19 февраля 2019 года.
- ↑ Cornford EM, Braun LD, Oldendorf WH. Developmental modulations of blood–brain barrier permeability as an indicator of changing nutritional requirements in the brain // Pediatr Res. — 1982. — № 16. — С. 324–328. Архивировано 4 июня 2016 года.
- ↑ Brenton DP, Gardiner RM. Transport of L-phenylalanine and related amino acids at the ovine blood-brain barrier // J Physiol. — 1988. — № 402. — С. 497–514. Архивировано 4 июня 2016 года.
- ↑ Frank HJ, Jankovic-Vokes T, Pardridge WM, Morris WL. Enhanced insulin binding to blood–brain barrier in vivo and to brain microvessels in vitro in newborn rabbits // Diabetes. — 1985. — № 34. — С. 728–733. Архивировано 18 февраля 2019 года.
- ↑ Saunders NR, Knott GW, Dziegielewska KM. Barriers in the immature brain // Cell Mol Neurobiol. — 2000. — № 20. — С. 29–40. Архивировано 26 мая 2016 года.
- ↑ Abbott NJ, Bundgaard M. Electron-dense tracer evidence for a blood-brain barrier in the cuttlefish Sepia officinalis // J Neurocytol. — 1992. — № 21. — С. 276–294. Архивировано 28 мая 2016 года.
- ↑ Abbott NJ, Pichon Y. The glial blood-brain barrier of crustacea and cephalopods: a review // J Physiol (Paris). — 1982. — № 21. — С. 304–313. Архивировано 3 июня 2016 года.
- ↑ 1 2 Abbott NJ. Dynamics of CNS barriers: evolution, differentiation, and modulation // Cell Mol Neurobiol. — 2005. — № 25. — С. 5–23. Архивировано 18 февраля 2019 года.
- ↑ N. J. Abbott. Comparative physiology of the blood-brain barrier // Physiology and pharmacology of the bloodbrain barrier / M. W. B. Bradbury. — Springer-Verlag, 1992. — С. 371—396. — ISBN 0-387-54492-5.
- ↑ N. Hettenbach. Einfluss chronischer elektromagnetischer Befeldung mit Mobilfunkstrahlen (GSM und UMTS) auf die Integrität der Blut-Hirn-Schranke von Ratten // Диссертация. Мюнхенский университет Людвига-Максимилиана. — 2008.
- ↑ S. I. Rapoport. Blood-brain Barrier in Physiology and Medicine. — Raven Press, 1976. — ISBN 0-89004-079-6.
- ↑ 1 2 3 M. Fromm. Physiologie des Menschen // Transport in Membranen und Epithelien / R. F. Schmidt, F. Lang. — Verlag Springer. — С. 41—54. — ISBN 978-3-540-32908-4.
- ↑ I. Sauer. Apolipoprotein E abgeleitete Peptide als Vektoren zur Ьberwindung der Blut-Hirn-Schranke // Диссертация. Свободный университет Берлина. — 2004. Архивировано 10 ноября 2011 года.
- ↑ 1 2 Egleton RD, Davis TP. Development of neuropeptide drugs that cross the blood-brain barrier // NeuroRx. — 2005. — № 2. — С. 44—53. Архивировано 18 февраля 2019 года.
- ↑ Oldendorf WH. Lipid solubility and drug penetration of the blood brain barrier // Proc Soc Exp Biol Med. — 1974. — № 147. — С. 813—815. Архивировано 19 февраля 2019 года.
- ↑ 1 2 R. Kaliszan, M. Markuszewski. Brain/blood distribution described by a combination of partition coefficient and molecular mass // International Journal of Pharmaceutics. — 1996. — № 145. — С. 9—16.
- ↑ Träuble H. Carriers and specificity in membranes. 3. Carrier-facilitated transport. Kinks as carriers in membranes // Neurosci Res Program Bull. — 1971. — № 9. — С. 361—372. Архивировано 18 февраля 2019 года.
- ↑ Träuble H. Phase transitions in lipids. Possible switch processes in biological membranes // Naturwissenschaften. — 1971. — № 58. — С. 277—284. Архивировано 29 мая 2016 года.
- ↑ O. Vostowsky. Chemie der Naturstoffe - Lipoproteine und Membranen // Эрлангенский университет. — 2005. — № 58. — С. 42. Архивировано 29 мая 2016 года.
- ↑ W. Hoppe, R. D. Bauer. Biophysik. — Verlag Birkhäuser, 1982. — С. 447—448. — ISBN 0-387-11335-5.
- ↑ Seelig A, Seelig J. The dynamic structure of fatty acyl chains in a phospholipid bilayer measured by deuterium magnetic resonance // Biochemistry. — 1974. — № 13. — С. 4839—4845. Архивировано 18 февраля 2019 года.
- ↑ A. Elbert. Die Permeation kleiner polarer Moleküle durch Phospholipidmodellmembranen // Диссертация. Университет Кайзерслаутерна. — 1999. Архивировано 10 ноября 2011 года.
- ↑ Seelig A, Gottschlich R, Devant RM. A method to determine the ability of drugs to diffuse through the blood-brain barrier // Proc Natl Acad Sci U S A. — 1994. — № 91. — С. 68—72. Архивировано 18 февраля 2019 года.
- ↑ 1 2 Dhopeshwarkar GA, Mead JF. Uptake and transport of fatty acids into the brain and the role of the blood-brain barrier system // Adv Lipid Res. — 1973. — № 11. — С. 109—142. Архивировано 18 февраля 2019 года.
- ↑ Gerebtzoff G, Seelig A. In silico prediction of blood-brain barrier permeation using the calculated molecular cross-sectional area as main parameter // J Chem Inf Model. — 2006. — № 46. — С. 2638—2650. Архивировано 18 февраля 2019 года.
- ↑ Seelig A, Gottschlich R, Devant RM. A method to determine the ability of drugs to diffuse through the blood-brain barrier // Proc Natl Acad Sci USA. — 1994. — № 91. — С. 68—72. Архивировано 18 февраля 2019 года.
- ↑ Pardridge WM. The blood-brain barrier: bottleneck in brain drug development // NeuroRx. — 2005. — № 2. — С. 3—14. Архивировано 19 февраля 2019 года.
- ↑ W. H. Oldendorf. Measurement of brain uptake of radiolabeled substances using a tritiated water internal standard // Brain Res. — 1970. — № 24. — С. 372–376. Архивировано 18 февраля 2019 года.
- ↑ Dolman D, Drndarski S, Abbott NJ, Rattray M. Induction of aquaporin 1 but not aquaporin 4 messenger RNA in rat primary brain microvessel endothelial cells in culture // J Neurochem. — 2005. — № 93. — С. 825—833. Архивировано 1 июня 2016 года.
- ↑ Bloch O, Manley GT. The role of aquaporin-4 in cerebral water transport and edema // Neurosurg Focus. — 2007. — № 22 (E3). Архивировано 18 февраля 2019 года.
- ↑ Verkman AS. More than just water channels: unexpected cellular roles of aquaporins // J Cell Sci. — 2005. — № 118. — С. 3225—3232. Архивировано 22 февраля 2017 года.
- ↑ Badaut J, Brunet JF, Regli L. Aquaporins in the brain: from aqueduct to "multi-duct" // Metab Brain Dis. — 2007. — № 3—4. — С. 251—263. Архивировано 19 февраля 2019 года.
- ↑ Agus DB, Gambhir SS, Pardridge WM, Spielholz C, Baselga J, Vera JC, Golde DW. Vitamin C crosses the blood-brain barrier in the oxidized form through the glucose transporters // J Clin Invest. — 1997. — № 100. — С. 2842—2848. Архивировано 26 мая 2016 года.
- ↑ Dahlin A, Royall J, Hohmann JG, Wang J. Expression profiling of the solute carrier gene family in the mouse brain // J Pharmacol Exp Ther. — 2009. — № 329. — С. 558—570. Архивировано 23 сентября 2017 года.
- ↑ Cornford EM, Hyman S. Blood-brain barrier permeability to small and large molecules // Adv Drug Deliv Rev. — 1999. — № 36. — С. 145—163. Архивировано 3 июня 2016 года.
- ↑ Zloković BV, Lipovac MN, Begley DJ, Davson H, Rakić L. Transport of leucine-enkephalin across the blood-brain barrier in the perfused guinea pig brain // J Neurochem. — 1987. — № 49. — С. 310—315. Архивировано 18 февраля 2019 года.
- ↑ Zlokovic BV, Mackic JB, Djuricic B, Davson H. Kinetic analysis of leucine-enkephalin cellular uptake at the luminal side of the blood-brain barrier of an in situ perfused guinea-pig brain // J Neurochem. — 1989. — № 53. — С. 1333—40. Архивировано 18 февраля 2019 года.
- ↑ Zlokovic BV, Hyman S, McComb JG, Lipovac MN, Tang G, Davson H. Kinetics of arginine-vasopressin uptake at the blood-brain barrier // Biochim Biophys Acta. — 1990. — № 1025. — С. 191—198. Архивировано 18 февраля 2019 года.
- ↑ Thomas SA, Abbruscato TJ, Hruby VJ, Davis TP. The entry of [D-penicillamine2,5enkephalin into the central nervous system: saturation kinetics and specificity] // J Pharmacol Exp Ther. — 1997. — № 280. — С. 1235—1240. Архивировано 18 февраля 2019 года.
- ↑ Begley DJ. ABC transporters and the blood-brain barrier // Curr Pharm Des. — 2004. — № 10. — С. 1295—1312. Архивировано 3 июля 2016 года.
- ↑ Rao VV, Dahlheimer JL, Bardgett ME, Snyder AZ, Finch RA, Sartorelli AC, Piwnica-Worms D. Choroid plexus epithelial expression of MDR1 P glycoprotein and multidrug resistance-associated protein contribute to the blood-cerebrospinal-fluid drug-permeability barrier // Proc Natl Acad Sci USA. — 1999. — № 96. — С. 3900—5. Архивировано 18 февраля 2019 года.
- ↑ Thiebaut F, Tsuruo T, Hamada H, Gottesman MM, Pastan I, Willingham MC. Immunohistochemical localization in normal tissues of different epitopes in the multidrug transport protein P170: evidence for localization in brain capillaries and crossreactivity of one antibody with a muscle protein // J Histochem Cytochem. — 1989. — № 37. — С. 159—164. Архивировано 26 мая 2016 года.
- ↑ Seetharaman S, Barrand MA, Maskell L, Scheper RJ. Multidrug resistance-related transport proteins in isolated human brain microvessels and in cells cultured from these isolates // J Neurochem. — 1998. — № 70. — С. 1151—1159. Архивировано 26 мая 2016 года.
- ↑ Cooray HC, Blackmore CG, Maskell L, Barrand MA. Localisation of breast cancer resistance protein in microvessel endothelium of human brain // Neuroreport. — 2002. — № 13. — С. 2059—2063. Архивировано 29 мая 2016 года.
- ↑ Eisenblätter T, Galla HJ. A new multidrug resistance protein at the blood-brain barrier // Biochem Biophys Res Commun. — 2002. — № 293. — С. 1273—1278. Архивировано 18 февраля 2019 года.
- ↑ Tanaka Y, Abe Y, Tsugu A, Takamiya Y, Akatsuka A, Tsuruo T, Yamazaki H, Ueyama Y, Sato O, Tamaoki N, et al. Ultrastructural localization of P-glycoprotein on capillary endothelial cells in human gliomas // Virchows Arch. — 1994. — № 425. — С. 133—138. Архивировано 18 февраля 2019 года.
- ↑ de Lange EC. Potential role of ABC transporters as a detoxification system at the blood-CSF barrier // Adv Drug Deliv Rev. — 2004. — № 56. — С. 1793—1809. Архивировано 20 февраля 2019 года.
- ↑ Wolosker H, Panizzutti R, De Miranda J. Neurobiology through the looking-glass: D-serine as a new glial-derived transmitter // Neurochem Int. — 2002. — № 41. — С. 327—332. Архивировано 18 февраля 2019 года.
- ↑ Zorumski CF, Olney JW. Excitotoxic neuronal damage and neuropsychiatric disorders // Pharmacol Ther. — 1993. — № 59. — С. 145—165. Архивировано 18 февраля 2019 года.
- ↑ Hosoya K, Sugawara M, Asaba H, Terasaki T. Blood-brain barrier produces significant efflux of L-aspartic acid but not D-aspartic acid: in vivo evidence using the brain efflux index method // J Neurochem. — 1999. — № 73. — С. 1206—1211. Архивировано 26 мая 2016 года.
- ↑ Palacín M, Estévez R, Bertran J, Zorzano A. Molecular biology of mammalian plasma membrane amino acid transporters // Physiol Rev. — 1998. — № 78. — С. 969—1054. Архивировано 26 мая 2016 года.
- ↑ Löscher W, Potschka H. Blood-brain barrier active efflux transporters: ATP-binding cassette gene family // NeuroRx. — 2005. — № 2. — С. 86—98. Архивировано 18 февраля 2019 года.
- ↑ Tishler DM, Weinberg KI, Hinton DR, Barbaro N, Annett GM, Raffel C. MDR1 gene expression in brain of patients with medically intractable epilepsy // NeuroRx. — 1995. — № 36. — С. 1—6. Архивировано 21 мая 2016 года.
- ↑ Kusuhara H, Sekine T, Utsunomiya-Tate N, Tsuda M, Kojima R, Cha SH, Sugiyama Y, Kanai Y, Endou H. Molecular cloning and characterization of a new multispecific organic anion transporter from rat brain // J Biol Chem. — 1999. — № 274. — С. 13675—13680. Архивировано 18 февраля 2019 года.
- ↑ Gao B, Stieger B, Noé B, Fritschy JM, Meier PJ. Localization of the organic anion transporting polypeptide 2 (Oatp2) in capillary endothelium and choroid plexus epithelium of rat brain // J Histochem Cytochem. — 1999. — № 47. — С. 1255—1264. Архивировано 26 мая 2016 года.
- ↑ Roberts RL, Fine RE, Sandra A. Receptor-mediated endocytosis of transferrin at the blood-brain barrier // J Cell Sci. — 1993. — № 104. — С. 521—532. Архивировано 28 мая 2016 года.
- ↑ Dehouck B, Dehouck MP, Fruchart JC, Cecchelli R. Upregulation of the low density lipoprotein receptor at the blood-brain barrier: intercommunications between brain capillary endothelial cells and astrocytes // J Cell Biol. — 1994. — № 126. — С. 465—473. Архивировано 18 мая 2016 года.
- ↑ Duffy KR, Pardridge WM, Rosenfeld RG. Human blood-brain barrier insulin-like growth factor receptor // Metabolism. — 1988. — № 37. — С. 136—140. Архивировано 4 июня 2016 года.
- ↑ Tamai I, Sai Y, Kobayashi H, Kamata M, Wakamiya T, Tsuji A. Structure-internalization relationship for adsorptive-mediated endocytosis of basic peptides at the blood-brain barrier // J Pharmacol Exp Ther. — 1997. — № 280. — С. 410—415. Архивировано 4 июня 2016 года.
- ↑ Smith MW, Gumbleton M. Endocytosis at the blood-brain barrier: from basic understanding to drug delivery strategies // J Drug Target. — 2006. — № 14. — С. 191—214. Архивировано 19 февраля 2019 года.
- ↑ Hervé F, Ghinea N, Scherrmann JM. CNS delivery via adsorptive transcytosis // J Drug Target. — 2008. — № 10. — С. 455—472. Архивировано 18 февраля 2019 года.
- ↑ Scherrmann JM. Drug delivery to brain via the blood-brain barrier // Vascul Pharmacol. — 2002. — № 38. — С. 349—354. Архивировано 18 февраля 2019 года.
- ↑ Bodor N, Buchwald P. Recent advances in the brain targeting of neuropharmaceuticals by chemical delivery systems // Adv Drug Deliv Rev. — 1999. — № 36. — С. 229—254. Архивировано 18 февраля 2019 года.
- ↑ 1 2 3 Bickel U. How to measure drug transport across the blood-brain barrier // NeuroRx. — 2005. — № 2. — С. 15—26. Архивировано 18 февраля 2019 года.
- ↑ 1 2 J. Fenstermacher, L. Wei. Measuring local cerebral capillary permeability-surface area products by quantitative autoradiography // Introduction to the Blood-brain Barrier / W. M. Pardridge. — Cambridge University Press, 1998. — С. 122—132. — ISBN 0-521-58124-9.
- ↑ C. Crone, D. G. Levitt. Capillary permeability to small solutes // Handbook of Physiology. — American Physiological Society, 1984. — С. 375—409.
- ↑ Lasbennes F, Gayet J. Capacity for energy metabolism in microvessels isolated from rat brain // Neurochem Res. — 1984. — № 9. — С. 1—10. Архивировано 18 февраля 2019 года.
- ↑ Miller DS, Nobmann SN, Gutmann H, Toeroek M, Drewe J, Fricker G. Xenobiotic transport across isolated brain microvessels studied by confocal microscopy // Mol Pharmacol. — 2000. — № 58. — С. 1357—1367. Архивировано 18 февраля 2019 года.
- ↑ Huwyler J, Pardridge WM. Examination of blood-brain barrier transferrin receptor by confocal fluorescent microscopy of unfixed isolated rat brain capillaries // J Neurochem. — 1998. — № 70. — С. 883—886. Архивировано 18 февраля 2019 года.
- ↑ 1 2 Banks W. A. From blood-brain barrier to blood-brain interface: new opportunities for CNS drug delivery (англ.) // Nat. Rev. Drug Discov. — 2016. — Vol. 15, no. 4. — P. 275—292. — doi:10.1038/nrd.2015.21.
- ↑ 1 2 3 4 5 Сайт всемирной организации здоровья. Дата обращения: 15 мая 2010. Архивировано 25 марта 2013 года.
- ↑ De Vivo DC, Trifiletti RR, Jacobson RI, Ronen GM, Behmand RA, Harik SI. Defective glucose transport across the blood-brain barrier as a cause of persistent hypoglycorrhachia, seizures, and developmental delay // NEJM. — 1991. — № 325. — С. 703—709. Архивировано 14 мая 2016 года.
- ↑ Horani MH, Mooradian AD. Effect of diabetes on the blood brain barrier // Curr Pharm Des. — 2003. — № 9. — С. 833—840.
- ↑ Correale J, Villa A. The blood-brain-barrier in multiple sclerosis: functional roles and therapeutic targeting // Autoimmunity. — 2007. — № 40. — С. 148—160.
- ↑ Dirnagl U, Iadecola C, Moskowitz MA. Pathobiology of ischaemic stroke: an integrated view // Trends Neurosci. — 1999. — № 22. — С. 391—397. Архивировано 22 февраля 2017 года.
- ↑ Kuroda S, Siesjö BK. Reperfusion damage following focal ischemia: pathophysiology and therapeutic windows // Clin Neurosci. — 1997. — № 4. — С. 199—212.
- ↑ Planas AM, Gorina R, Chamorro A. Signalling pathways mediating inflammatory responses in brain ischaemia // Biochem Soc Trans. — 2006. — № 34. — С. 1267—1270.
- ↑ 1 2 3 4 Weiss N, Miller F, Cazaubon S, Couraud PO. The blood-brain barrier in brain homeostasis and neurological diseases // Biochim Biophys Acta. — 2009. — № 1788. — С. 842—857. Архивировано 18 февраля 2019 года.
- ↑ Zysk G, Schneider-Wald BK, Hwang JH, Bejo L, Kim KS, Mitchell TJ, Hakenbeck R, Heinz HP. Pneumolysin is the main inducer of cytotoxicity to brain microvascular endothelial cells caused by Streptococcus pneumoniae // Infect Immun. — 2001. — № 69. — С. 845—852.
- ↑ Banks WA, Freed EO, Wolf KM, Robinson SM, Franko M, Kumar VB. Transport of human immunodeficiency virus type 1 pseudoviruses across the blood-brain barrier: role of envelope proteins and adsorptive endocytosis // J Virol. — 2001. — № 75. — С. 4681—4691. Архивировано 20 мая 2016 года.
- ↑ Квитницкий-Рыжов Ю. Н. Современное учение об отёке и набухании головного мозга. — Здоров’я. — Київ, 1988.
- ↑ А. В. Кузнецов, О. Н. Древаль. Посттравматические менингит и менингоэнцефалит // Клиническое руководство по черепно-мозговой травме / Под редакцией А. Н. Коновалова, Л. Б. Лихтермана, А. А. Потапова. — М.:: "Антидор", 2002. — Т. 3. — С. 420. — 632 с. — 1100 экз. — ISBN 5-900833-13-5.
Литература[править | править код]
- Гемато-энцефалический барьер / Кассиль Г. Н. // Газлифт — Гоголево. — М. : Советская энциклопедия, 1971. — (Большая советская энциклопедия : [в 30 т.] / гл. ред. А. М. Прохоров ; 1969—1978, т. 6).
- Штерн Л. С. Гемато-энцефалический барьер. М.—Л.: Биомедгиз, 1935.
- Майзелис М. Я. Гемато-энцефалический барьер и его регуляция. — М. : Медицина, 1961.
- Кассиль Г. Н. Гемато-энцефалический барьер: Анатомия, физиология. Методы исследования. Клиника.. — М. : Издательство АН СССР, 1963.
- Кассиль Г. Н. Мозговой барьер // Наука и жизнь : журнал. — 1986. — № 11. — С. 97-101.
Ссылки[править | править код]
 Медиафайлы по теме Гематоэнцефалический барьер на Викискладе
Медиафайлы по теме Гематоэнцефалический барьер на Викискладе- Подраздел учебника «Физиология человека» под редакцией В. М. Покровского, Г. Ф. Коротько посвящённый ГЭБ Архивная копия от 24 ноября 2009 на Wayback Machine
- Научно-популярная статья д.м.н. Г.Кассиля о ГЭБ опубликованная в журнале Наука и жизнь в 1986 году Архивная копия от 9 июня 2010 на Wayback Machine
- Определение и краткое описание ГЭБ Е. В. Трифонова
- Краткое описание ГЭБ на сайте medbiol.ru Архивная копия от 5 ноября 2010 на Wayback Machine
- Гематоэнцефалический барьер Архивная копия от 29 октября 2012 на Wayback Machine эмбриона данио-рерио, конфокальная фотография, Дженнифер Л. Петерс, Майкл Р. Тэйлор, St. Jude Children’s Research Hospital, 2012 г.
- Открыть ворота гематоэнцефалического барьера Оксана Семячкина-Глушковская, доктор биологических наук, Саратовский государственный университет им. Н. Г. Чернышевского «Наука и жизнь» № 7, 2015 Архивная копия от 8 декабря 2015 на Wayback Machine
Эта статья входит в число избранных статей русскоязычного раздела Википедии. |