Глиобластома
| Глиобластома | |
|---|---|
 Гистологический срез глиобластомы | |
| МКБ-11 | XH7F82 |
| МКБ-10 | C71 |
| МКБ-9 | 191 |
| МКБ-О | M9440/3 |
| OMIM | 137800 |
| DiseasesDB | 29448 |
| eMedicine | neuro/147 med/2692 |
| MeSH | D005909 |
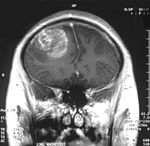
Мультиформная глиобластóма (англ. Glioblastoma multiforme, GBM) — наиболее частая и наиболее агрессивная форма опухоли мозга, которая составляет до 52 % первичных опухолей мозга и до 20 % всех внутричерепных опухолей. Несмотря на то что глиобластома является наиболее частой первичной опухолью мозга, на 100 000 жителей Европы и Северной Америки регистрируется всего 2—3 случая заболевания[1]. Термин «глиобластома» подразумевает два варианта этой болезни: гигантоклеточная глиобластома и глиосаркома.
Факторы риска[править | править код]
Причина большинства случаев неясна.[2] Наиболее известным фактором риска является воздействие ионизирующего излучения, в том числе излучение компьютерной томографии.[3][4] Около 5% случаев развивается в результате некоторых наследственных синдромов.[5]
Генетика[править | править код]
К нередким факторам риска относятся генетические заболевания, такие как нейрофиброматоз, синдром Ли-Фраумени, туберозный склероз или синдром Турко.[5] К факторам риска также относится предшествующая лучевая терапия.[2] По неизвестным причинам она чаще встречается у мужчин.[6]
Экология[править | править код]
Другие ассоциации включают воздействие курения, пестицидов, работу в нефтеперерабатывающей промышленности или на производстве резины.[7]
Глиобластома была связана с вирусами SV40,[8] HHV-6,[9][10] и цитомегаловирусом.[11]
Другое[править | править код]
Были проведены исследования, чтобы выяснить, является ли потребление копченого мяса фактором риска. По состоянию на 2003 г. риск не был подтвержден.[12] Аналогичным образом в качестве факторов риска изучались воздействие формальдегида и электромагнитных полей в жилых помещениях, например от сотовых телефонов и электропроводки в домах. По состоянию на 2015 г. не было доказано, что они вызывают ГБМ.[5][13][14]
Причины[править | править код]
По неизвестным причинам глиобластома встречается чаще у мужчин[15]. Большинство случаев глиобластомы носят спорадический характер, без генетической предрасположенности. Не установлена связь между глиобластомой и курением[16], потреблением консервированного мяса[17] или воздействием электромагнитного поля[18][19][20][21][22]. Возможно, фактором риска является потребление алкоголя[23]. Заболеваемость глиобластомой связана с вирусами SV40[24], ВГЧ-6[25][26] и цитомегаловирусом[27]. Есть небольшая зависимость глиобластомы от ионизирующего излучения[28]. Анализ 2006 года связывает эту опухоль головного мозга с воздействием свинца на рабочем месте[29]. Замечена связь случаев опухоли мозга и малярии. Предполагается, что малярийный комар, переносчик малярии, может передавать вирус или другой агент, который может увеличить риск глиобластомы[30].
Лечение[править | править код]

При лечении может применяться химиотерапия, лучевая терапия и хирургическое лечение. Если опухоль нельзя удалить или удаляется менее 90 % её объёма, то такое лечение является паллиативным, нерадикальным, так как опухоль с большей вероятностью продолжит свой рост. Медиана выживаемости для пациентов, в отношении которых применялась лучевая и химиотерапия с темозоломидом, составляет 15 месяцев[31]. Медиана выживаемости без лечения составляет 3 месяца, в то же время довольно часто пациенты проживают 1—2 года[32]. Хотя серьёзных исследований эффективности хирургического лечения при данном заболевании не проводилось, хирургия остаётся стандартным методом лечения[33].
Доклинические испытания[править | править код]
Кетогенная метаболическая терапия в сочетании с лучевой, химиотерапией и гипербарической оксигенацией позволяет увеличить оксидативный стресс в клетках опухоли, одновременно ограничивая доступ к глюкозе и глютамину.[34]
Животные модели[править | править код]
По данным одного исследования, в мышиной модели глиобластомы, вызванной точечной делецией в гене p53, накопление мутантных белков p53 отмечается сначала в субвентрикулярной зоне, откуда и начинается распространение клеток прогениторно-подобного фенотипа, дающих начало опухоли[35][36].
Генетические нарушения при глиобластоме[править | править код]
Наиболее частые генетические нарушения при первичных глиобластомах — это: утрата гетерозиготности (LOH) 10q (69%), затем амплификация EGFR (34%), мутация TP53 (31%), гомозиготная делеция p16INK4a (31%) и мутации PTEN (24%). Во вторичных глиобластомах часты мутации TP53 и LOH 10q (65% и 63%), в то время как другие генетические нарушения редки[37].
См. также[править | править код]
Примечания[править | править код]
- ↑ Louis DN, Ohgaki H, Wiestler OD, Cavenee WK, Burger PC, Jouvet A, Scheithauer BW, Kleihues P, The 2007 WHO Classification of Tumours of the Central Nervous System Acta Neuropathol (2007) 114:97-109. PMID 17618441
- ↑ 1 2 Chapter 5.16 // World Cancer Report 2014. — World Health Organization, 2014. — ISBN 978-9283204299.
- ↑ Smoll NR, Brady Z, Scurrah KJ, Lee C, Berrington de González A, Mathews JD. Computed tomography scan radiation and brain cancer incidence. Neuro-Oncology. 2023 Jan 14;https://doi.org/10.1093/neuonc/noad012
- ↑ Smoll NR, Brady Z, Scurrah K, Mathews JD. Exposure to ionizing radiation and brain cancer incidence: The Life Span Study cohort. Cancer Epidemiology. 2016 Jun;42:60–5.
- ↑ 1 2 3 Alifieris C, Trafalis DT (August 2015). "Glioblastoma multiforme: Pathogenesis and treatment". Pharmacology & Therapeutics. 152: 63—82. doi:10.1016/j.pharmthera.2015.05.005. PMID 25944528.
- ↑ Ohgaki H, Kleihues P (June 2005). "Population-based studies on incidence, survival rates, and genetic alterations in astrocytic and oligodendroglial gliomas". Journal of Neuropathology and Experimental Neurology. 64 (6): 479—489. doi:10.1093/jnen/64.6.479. PMID 15977639.
- ↑ Использование онколитических вирусов для лечения глиобластомы и других неизлечимых форм рака мозга. Дата обращения: 14 октября 2022. Архивировано 4 июня 2023 года.
- ↑ Vilchez RA, Kozinetz CA, Arrington AS, Madden CR, Butel JS (June 2003). "Simian virus 40 in human cancers". The American Journal of Medicine. 114 (8): 675—684. doi:10.1016/S0002-9343(03)00087-1. PMID 12798456.
- ↑ Crawford JR, Santi MR, Thorarinsdottir HK, Cornelison R, Rushing EJ, Zhang H, et al. (September 2009). "Detection of human herpesvirus-6 variants in pediatric brain tumors: association of viral antigen in low grade gliomas". Journal of Clinical Virology. 46 (1): 37—42. doi:10.1016/j.jcv.2009.05.011. PMC 2749001. PMID 19505845.
- ↑ Chi J, Gu B, Zhang C, Peng G, Zhou F, Chen Y, et al. (November 2012). "Human herpesvirus 6 latent infection in patients with glioma". The Journal of Infectious Diseases. 206 (9): 1394—1398. doi:10.1093/infdis/jis513. PMID 22962688.
- ↑ McFaline-Figueroa JR, Wen PY (February 2017). "The Viral Connection to Glioblastoma". Current Infectious Disease Reports. 19 (2): 5. doi:10.1007/s11908-017-0563-z. PMID 28233187. S2CID 30446699.
- ↑ Huncharek M, Kupelnick B, Wheeler L (2003). "Dietary cured meat and the risk of adult glioma: a meta-analysis of nine observational studies". Journal of Environmental Pathology, Toxicology and Oncology. 22 (2): 129—137. doi:10.1615/JEnvPathToxOncol.v22.i2.60. PMID 14533876.
- ↑ Kan P, Simonsen SE, Lyon JL, Kestle JR (January 2008). "Cellular phone use and brain tumor: a meta-analysis". Journal of Neuro-Oncology. 86 (1): 71—78. doi:10.1007/s11060-007-9432-1. PMID 17619826. S2CID 23460254.
- ↑ Hardell L, Carlberg M, Hansson Mild K (August 2009). "Epidemiological evidence for an association between use of wireless phones and tumor diseases". Pathophysiology. 16 (2—3): 113—122. doi:10.1016/j.pathophys.2009.01.003. PMID 19268551.
- ↑ Ohgaki, Hiroko; Kleihues, Paul. Population-Based Studies on Incidence, Survival Rates, and Genetic Alterations in Astrocytic and Oligodendroglial Gliomas (англ.) // Journal of Neuropathology & Experimental Neurology : journal. — 2005. — Vol. 64, no. 6. — P. 479—489. — PMID 15977639. Архивировано 9 января 2016 года.
- ↑ Zheng, Tongzhang; Cantor, Kenneth P.; Zhang, Yawei; Chiu, Brian C. H.; Lynch, Charles F. Risk of Brain Glioma not Associated with Cigarette Smoking or Use of Other Tobacco Products in Iowa (англ.) // Cancer Epidemiology, Biomarkers & Prevention : journal. — 2001. — Vol. 10, no. 4. — P. 413—414. — PMID 11319186. Архивировано 14 августа 2013 года.
- ↑ Wheeler, Lamar; Huncharek, Michael; Kupelnick, Bruce. Dietary Cured Meat and the Risk of Adult Glioma: A Meta-Analysis of Nine Observational Studies (англ.) // Journal of Environmental Pathology, Toxicology and Oncology : journal. — 2003. — Vol. 22, no. 2. — P. 129—137. — doi:10.1615/JEnvPathToxOncol.v22.i2.60. — PMID 14533876.
- ↑ Savitz, David A.; Checkoway, Harvey; Loomis, Dana P. Magnetic Field Exposure and Neurodegenerative Disease Mortality among Electric Utility Workers (англ.) // Epidemiology : journal. — 1998. — Vol. 9, no. 4. — P. 398—404. — doi:10.1097/00001648-199807000-00009. — PMID 9647903.
- ↑ Inskip, Peter D.; Tarone, Robert E.; Hatch, Elizabeth E.; Wilcosky, Timothy C.; Shapiro, William R.; Selker, Robert G.; Fine, Howard A.; Black, Peter M.; Loeffler, Jay S. Cellular-Telephone Use and Brain Tumors (англ.) // The New England Journal of Medicine. — 2001. — Vol. 344, no. 2. — P. 79—86. — doi:10.1056/NEJM200101113440201. — PMID 11150357.
- ↑ Kan, Peter; Simonsen, Sara E.; Lyon, Joseph L.; Kestle, John R. W. Cellular phone use and brain tumor: A meta-analysis (англ.) // Journal of Neuro-Oncology : journal. — 2007. — Vol. 86, no. 1. — P. 71—8. — doi:10.1007/s11060-007-9432-1. — PMID 17619826.
- ↑ Hardell, Lennart; Carlberg, Michael; Hansson Mild, Kjell. Epidemiological evidence for an association between use of wireless phones and tumor diseases (англ.) // Pathophysiology : journal. — 2009. — Vol. 16, no. 2—3. — P. 113—122. — doi:10.1016/j.pathophys.2009.01.003. — PMID 19268551.
- ↑ "Минздрав Израиля: с начала эпохи мобильной связи заболеваемость раком мозга не выросла". Новости Израиля. Архивировано из оригинала 30 января 2018. Дата обращения: 29 января 2018.
- ↑ Baglietto, Laura; Giles, Graham G.; English, Dallas R.; Karahalios, Amalia; Hopper, John L.; Severi, Gianluca. Alcohol consumption and risk of glioblastoma; evidence from the Melbourne collaborative cohort study (англ.) // International Journal of Cancer : journal. — 2011. — Vol. 128, no. 8. — P. 1929. — doi:10.1002/ijc.25770.
- ↑ Vilchez, Regis A; Kozinetz, Claudia A; Arrington, Amy S; Madden, Charles R; Butel, Janet S. Simian virus 40 in human cancers (англ.) // The American Journal of Medicine. — 2003. — Vol. 114, no. 8. — P. 675—684. — doi:10.1016/S0002-9343(03)00087-1. — PMID 12798456.
- ↑ Crawford, JR; Santi, MR; Thorarinsdottir, HK; Cornelison, R; Rushing, EJ; Zhang, H; Yao, K; Jacobson, S; MacDonald, T.J. Detection of human herpesvirus-6 variants in pediatric brain tumors: Association of viral antigen in low grade gliomas (англ.) // Journal of clinical virology : the official publication of the Pan American Society for Clinical Virology : journal. — 2009. — Vol. 46, no. 1. — P. 37—42. — doi:10.1016/j.jcv.2009.05.011. — PMID 19505845. — PMC 2749001.
- ↑ Chi, J.; Gu, B.; Zhang, C.; Peng, G.; Zhou, F.; Chen, Y.; Zhang, G.; Guo, Y.; Guo, D. Human Herpesvirus 6 Latent Infection in Patients with Glioma (англ.) // The Journal of Infectious Diseases : journal. — 2012. — Vol. 206, no. 9. — P. 1394—1398. — doi:10.1093/infdis/jis513. — PMID 22962688.
- ↑ «Target acquired» Архивная копия от 5 июля 2009 на Wayback Machine, The Economist, May 29th, 2008
- ↑ Cavenee, W.K. High-grade gliomas with chromosome 1p loss (неопр.) // Journal of Neurosurgery. — 2000. — Т. 92, № 6. — С. 1080—1081. — PMID 10839286.
- ↑ Van Wijngaarden, Edwin; Dosemeci, Mustafa. Brain cancer mortality and potential occupational exposure to lead: Findings from the National Longitudinal Mortality Study, 1979–1989 (англ.) // International Journal of Cancer : journal. — 2006. — Vol. 119, no. 5. — P. 1136—1144. — doi:10.1002/ijc.21947. — PMID 16570286.
- ↑ Lehrer, Steven. Anopheles mosquito transmission of brain tumor (англ.) // Medical Hypotheses. — 2010. — Vol. 74, no. 1. — P. 167—168. — doi:10.1016/j.mehy.2009.07.005. — PMID 19656635.
- ↑ Johnson, Derek R.; O'Neill, Brian Patrick. Glioblastoma survival in the United States before and during the temozolomide era (англ.) // Journal of Neuro-Oncology : journal. — 2011. — Vol. 107, no. 2. — P. 359—364. — doi:10.1007/s11060-011-0749-4. — PMID 22045118.
- ↑ Krex, D.; Klink, B.; Hartmann, C.; Von Deimling, A.; Pietsch, T.; Simon, M.; Sabel, M.; Steinbach, J. P.; Heese, O. Long-term survival with glioblastoma multiforme (англ.) // Brain. — Oxford University Press, 2007. — Vol. 130, no. 10. — P. 2596—2606. — doi:10.1093/brain/awm204.
- ↑ Van Meir, E. G.; Hadjipanayis, C. G.; Norden, A. D.; Shu, H. K.; Wen, P. Y.; Olson, J. J. Exciting New Advances in Neuro-Oncology: The Avenue to a Cure for Malignant Glioma (англ.) // CA: A Cancer Journal for Clinicians : journal. — 2010. — Vol. 60, no. 3. — P. 166—193. — doi:10.3322/caac.20069. — PMID 20445000. — PMC 2888474.
- ↑ Daniela D. Weber, Sepideh Aminazdeh-Gohari, Barbara Kofler. Ketogenic diet in cancer therapy // Aging (Albany NY). — 2018-02-11. — Т. 10, вып. 2. — С. 164—165. — ISSN 1945-4589. — doi:10.18632/aging.101382. Архивировано 20 августа 2018 года.
- ↑ Wang Y., Yang J., Zheng H., Tomasek G.J., Zhang P., McKeever P.E., Lee E.Y., Zhu Y. Expression of mutant p53 proteins implicates a lineage relationship between neural stem cells and malignant astrocytic glioma in a murine model (англ.) // Cancer Cell : journal. — 2009. — June (vol. 15, no. 6). — P. 514—526. — doi:10.1016/j.ccr.2009.04.001. — PMID 19477430. Архивировано 20 октября 2018 года.
- ↑ (недоступная ссылка с 30-09-2016 [2757 дней])Источником самого распространённого рака мозга могут быть нейральные стволовые клетки (недоступная ссылка) — сайт Академии Сеченова.
- ↑ Hiroko Ohgaki et al. Genetic Pathways to Glioblastoma (англ.) // Cancer Research. — American Association for Cancer Research, 2004. — October (vol. 64, no. 19). — P. 6892. — doi:10.1158/0008-5472.CAN-04-1337. Архивировано 16 января 2017 года.
В другом языковом разделе есть более полная статья Glioblastoma (исп.). |