Хлорид аммония
| Хлорид аммония | |||
|---|---|---|---|
| |||
 | |||
| Общие | |||
| Систематическое наименование |
Хлорид аммония | ||
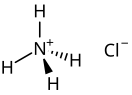
| Хим. формула | NH4Cl | ||
| Физические свойства | |||
| Состояние | бесцветные кубические кристаллы | ||
| Молярная масса | 53,49 г/моль | ||
| Плотность | 1,526 г/см³ | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 337,6 °C | ||
| • сублимации | 337,6 (с разл.) °C | ||
| • кипения | 520 °C[1][2] | ||
| Энтальпия | |||
| • образования | -314,2 кДж/моль | ||
| Давление пара | 1 ± 1 мм рт.ст.[3] | ||
| Химические свойства | |||
| Растворимость | |||
| • в воде | 37,2 г/100 г (20 °C) | ||
| Классификация | |||
| Рег. номер CAS | 12125-02-9 | ||
| PubChem | 25517, 12820921, 518533 и 21924987 | ||
| Рег. номер EINECS | 235-186-4 | ||
| SMILES | |||
| InChI | |||
| RTECS | BP4550000 | ||
| ChEBI | 31206 | ||
| ChemSpider | 23807 | ||
| Безопасность | |||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||

Хлорид аммония (хлористый аммоний; техническое название — нашаты́рь) — неорганическое соединение, соль аммония с химической формулой NH4Cl, белый кристаллический слегка гигроскопичный порошок без запаха.
В природе хлорид аммония представлен минералом нашатырь, от араб. ﻧﺸﺎﺩﺭ (nūšādir) — «аммиак»[4].
Физические свойства
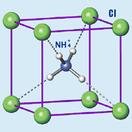
Бесцветные или белые кристаллы кубической сингонии (а = 0,38758 нм, z = 1, пространственная группа Pm3m). Относительная плотность = 1,526. Кубическая модификация стабильна ниже температуры 184,3 °C. Соединение возгоняется при 337,6 °C с разложением на аммиак и соляную кислоту[5][6] (правильнее: хлороводород или хлористый водород HCl).
Хорошо растворим в воде (37,2 г / 100 мл), жидком аммиаке. Водные растворы вследствие гидролиза имеют слабокислую реакцию. Температура кипения насыщенных водных растворов 116 °C[5].
Растворимость (безводного вещества в безводном растворителе): в этаноле — 0,6 г/100 г, в метаноле — 3,3 г/100 г.
| 0 °C | 10 °C | 20 °C | 30 °C | 40 °C | 50 °C | 60 °C | 70 °C | 80 °C | 90 °C | 100 °C |
|---|---|---|---|---|---|---|---|---|---|---|
| 29,4 | 33,3 | 37,2 | 41,4 | 45,8 | 50,4 | 55,2 | 60,2 | 65,6 | 71,3 | 77,3 |
Химические свойства
- реагирует с щелочами с выделением аммиака[6]:
- реагирует с нитратом серебра с выпадением белого осадка хлорида серебра, темнеющего при действии света[6]:
- реагирует с нитритом натрия при нагревании, с образованием хлорида натрия, азота и воды:
- под действием электрического тока разлагается с образованием хлористого азота
Получение
В промышленности хлорид аммония получают упариванием маточного раствора, остающегося после отделения гидрокарбоната натрия NaHCO3 после реакции, в которой углекислый газ пропускают через раствор аммиака и хлорида натрия.
В лаборатории хлорид аммония получают взаимодействием хлороводорода с аммиаком при пропускании их через раствор NaCl.
Иногда используют реакцию взаимодействия аммиака с хлором:
Реакция взаимодействия аммиака и соляной кислоты:
Применение
- азотное удобрение (до 25 % N) для нейтральных и щелочных почв под культуры, слабо реагирующие на избыток хлора (сахарная свёкла, рис, кукуруза);
- зарегистрирован в качестве пищевой добавки E510, в скандинавских странах и Финляндии применяется как пищевая приправа, в том числе в составе лакричных конфет «Tyrkisk Peber» «Salmiakki» и т. д.;
- используют при пайке как флюс (для удаления оксидной плёнки с поверхностей металлов);
- в гальванических элементах как компонент электролита;
- в медицине при отёках сердечного происхождения и для усиления действия диуретиков;
- в лабораторных технологиях — для лизиса эритроцитов;
- как дымообразователь;
- в фотографии как компонент быстрого фиксажа, для получения тиосульфата аммония непосредственно в растворе[7].
Примечания
- ↑ AMMONIUM CHLORIDE
- ↑ David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ http://www.cdc.gov/niosh/npg/npgd0029.html
- ↑ Криштофович А. Н. Геологический словарь / отв. ред. Спижарский Т. Н. — Москва: Госгеолтехиздат, 1955. — Т. II М—Я. — С. 66. — 449 с., переиздание «Книга по требованию» ISBN 9785458366540.
- ↑ 1 2 Крашенинников, 1988.
- ↑ 1 2 3 Гурлев, 1988, с. 286.
- ↑ Гурлев, 1988, с. 285—286.
Литература
- Гурлев Д. С. Справочник по фотографии (обработка фотоматериалов). — К.: Тэхника, 1988.
- Крашенинников С. А. Амммония хлорид // Химическая энциклопедия : в 5 т. / Гл. ред. И. Л. Кнунянц. — М.: Советская энциклопедия, 1988. — Т. 1: А — Дарзана. — С. 155. — 623 с. — 100 000 экз. — ISBN 5-85270-008-8.
В другом языковом разделе есть более полная статья Ammonium chloride (англ.). |