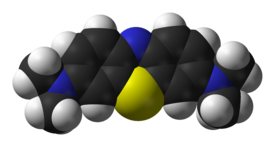
Метиленовый синий
| Метиленовый синий | |
|---|---|
  | |
 | |
| Общие | |
| Хим. формула | C16H18ClN3S |
| Физические свойства | |
| Молярная масса | 319,85 г/моль |
| Термические свойства | |
| Температура | |
| • плавления | 100—110 °C (с разл.) |
| • разложения | 105 ± 10 °C[1] |
| Классификация | |
| Рег. номер CAS | 61-73-4 |
| PubChem | 6099 |
| Рег. номер EINECS | 200-515-2 |
| SMILES | |
| InChI | |
| ChEBI | 6872 |
| ChemSpider | 5874 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |

Метиленовый синий (лат. Methylenum coeruleum; N,N,N',N'-тетраметилтионина хлорид тригидрат, 3,7-бисдиметиламинофенотиазин хлорид, метиловая синь, метиленовый голубой) — органическое соединение, тиазиновый краситель с химической формулой C16H18ClN3S или в виде кристаллогидрата C16H18ClN3S·H2O. Представляет собой тёмно-зеленые кристаллы с бронзовым блеском. Используется в медицине, аналитической химии, красильной промышленности и фотографии.
История[править | править код]
Метиленовый синий был впервые синтезирован в 1876 году Генрихом Каро, работавшим на BASF. Тем самым он положил начало развитию химии фенотиазинов[2].
Физические свойства[править | править код]
Малорастворим в воде, этаноле, практически нерастворим в диэтиловом эфире и хлороформе. Легко восстанавливается: E0 = +0,53 В. В водных растворах мономерная форма поглощает свет при длине волны λmax = 668 нм, димер — в λmax = 612 нм; константа димеризации Кдим = 5,00⋅103 (pH 4—5,5).
При низких температурах раствор метиленового синего приобретает фиолетовый окрас.
Получение[править | править код]
Получают из N,N-диметиланилина[3].
Применение[править | править код]

Органический основной тиазиновый краситель, применяется для окраски хлопка, шерсти и шёлка в ярко-голубой цвет, однако краска разрушается на свету. В аналитической химии применяется для определения хлоратов, перхлоратов, катионов ртути, олова, магния, кальция, кобальта, кадмия.
В медицине используется в качестве антисептика для лечения инфекций ротовой полости и мочеполовых путей. Относится к списку жизненно важных препаратов ВОЗ для лечения метгемоглобинемии (антидот при отравлении цианидами, угарным газом и сероводородом). Имеются сообщения о высокой эффективности этого соединения при лечении болезни Альцгеймера[4][5]. В онкологии это мощный фотосенсибилизатор, особенно активно работающий при воздействии света и способствующий разрушению патологических клеток.
Используют в микроскопии как красящее вещество, так как метиленовый синий интенсивно окрашивает некоторые ткани живого организма. Чеслав Хенцинский, работая в Одесском медицинском университете, разработал на его основе с использованием эозина в 1888 году метод двойного окрашивания клеток крови и кровяных паразитов, позволившего выявлять паразитов крови, в частности возбудителей малярии и в 1889 году защитил по этой теме докторскую диссертацию «К учению о микроорганизмах малярии»[6]. Впервые его использовал для окраски нервной ткани (1889) М. Д. Лавдовский[7].
В результате этих разработок он стал первым применённым в медицине веществом, не существовавшим до этого в живой природе.
В аквариумистике применяется довольно часто во время инкубирования икры в качестве антисептика.
В водоочистке применяется при тестировании активированного угля по ГОСТ 4453-74[8].
В фотографии может использоваться как десенсибилизатор в значительном разведении. В высокой концентрации вместо десенсибилизирующего действия оказывает вуалирование[9].
Метиленовый синий давно используется в медицине в качестве антидота против некоторых токсинов[10]. Метиленовый синий имеют потенциал в качестве симптоматического лечения сепсиса[11][12][13][14].
Летом 2020 года в российских популярных СМИ появились публикации о том, что испытания на людях якобы показали, что водный раствор красителя метиленовый синий, применяемый либо внутрь, либо ингаляционно, может достаточно быстро уничтожить в организме коронавирус SARS-CoV-2[15]. Также, согласно этим публикациям, раствор метиленового синего усиливает свою активность в 10 раз при воздействии красного света (фотодинамической терапии) с длиной волны 665 нм на зону носоглотки и груди[15][16]. Учитывая, что речь идёт всего лишь о публикациях в популярных СМИ, а не в научных журналах, и что полноценное клиническое исследование так и не было проведено, к теории об эффективности лечения коронавирусной инфекции данным методом необходимо подходить крайне осторожно.
Также метиленовый синий используется при отравлении угарным газом, для лечения метгемоглобинемии, инфекций мочеполовой системы, септического шока, малярии и как противовирусный препарат[источник не указан 1202 дня][17][18].
Противопоказания[править | править код]
Метиленовый синий является ингибитором моноаминоксидазы, поэтому его внутреннее применение на фоне приёма антидепрессантов группы селективных ингибиторов обратного захвата серотонина может привести к развитию серотонинового синдрома[19][20][21].
См. также[править | править код]
Примечания[править | править код]
- ↑ Methylene blue
- ↑ Derek Burton, W. David Ollis. Шестичленные гетероциклы // Общая органическая химия = Comprehensive Organic Chemistry / Под ред. Н. К. Кочеткова. — М.: Химия, 1985. — Т. 9. — С. 627—635. — 800 с.
- ↑ Ельцов, 1985, с. 166—167.
- ↑ Lauren Gravitz. Drugs: A tangled web of targets (англ.) // Nature. — 2011. — Vol. 475. — P. S9—S11. — doi:10.1038/475S9a. Архивировано 23 июля 2011 года.
- ↑ D. X. Medina, A. Caccamo, S. Oddo. Methylene Blue Reduces Aβ Levels and Rescues Early Cognitive Deficit by Increasing Proteasome Activity (англ.) // Brain Pathology. — 2011. — Vol. 21, no. 2. — P. 140—149. — doi:10.1111/j.1750-3639.2010.00430.x. Архивировано 19 мая 2012 года.
- ↑ Ссылки Chenzinsky C: Zur lehre von mikroorganismus des malaria-fiebers. Zentralbl Bakteriol 83:457, 1888 и Хенцинский Ч. И. «К учению о микроорганизмах малярии». Дисс. Одесса,1889. в статье А. В. Безрукова «К 120-й годовщине открытия эффекта Романовского». Дата обращения: 26 июня 2020. Архивировано 27 ноября 2021 года.
- ↑ Сутулов Л. С. Лавдовский Михаил Дормидонтович // Большая медицинская энциклопедия : в 30 т. / гл. ред. Б. В. Петровский. — 3-е изд. — М. : Советская энциклопедия, 1980. — Т. 12 : Криохирургия — Ленегр. — 536 с. : ил.
- ↑ ГОСТ 4453-74 Архивная копия от 23 января 2015 на Wayback Machine.
- ↑ Теренин, 1947, с. 298.
- ↑ Ряженов В. В., Хрущов Н. Г. Метиленовый синий // Большая медицинская энциклопедия : в 30 т. / гл. ред. Б. В. Петровский. — 3-е изд. — М. : Советская энциклопедия, 1981. — Т. 15 : Меланома — Мудров. — 576 с. : ил.
- ↑ Гипотеза Чёрной королевы Архивная копия от 12 июля 2020 на Wayback Machine // Статья от 16.04.2020 г. Сайт «Академгородок». Мошкин Ю. М.
- ↑ Tristan de Jong, Victor Guryev, Yury M. Moshkin. Discovery of pharmaceutically-targetable pathways and prediction of survivorship for pneumonia and sepsis patients from the view point of ensemble gene noise, April 11, 2020
- ↑ Учёные предложили способ лечения пациентов с тяжелой формой COVID-19 Архивная копия от 12 июля 2020 на Wayback Machine // Статья от 27.04.2020 г. ИЦиГ СО РАН.
- ↑ Для симптоматического лечения COVID-19 можно использовать «метиленовую синьку» Архивная копия от 12 июля 2020 на Wayback Machine // Статья от 27.04.2020 г. на сайте «Наука из первых рук»
- ↑ 1 2 Учёные Сеченовского университета выявили эффективность метиленового синего при лечении коронавируса Архивная копия от 16 декабря 2020 на Wayback Machine, 31 июля 2020
- ↑ «Синька» против коронавируса: как появилось открытие российских учёных Архивная копия от 2 августа 2020 на Wayback Machine // Статья в РБК. Е. Олиярник.
- ↑ Заражённых коронавирусом предложили лечить раствором синего красителя Архивная копия от 15 июля 2020 на Wayback Machine // Статья от 25.06.2020 г. ИА «ТАСС».
- ↑ Лечение коронавируса синькой выявило «синдром Кулибина» Архивная копия от 13 июля 2020 на Wayback Machine // Статья от 01.07.2020 г. «Московский комсомолец». Е. Пичугина
- ↑ Метиленовый синий: риск развития серотонинового синдрома при совместном применении с ингибиторами обратного захвата серотонина. - ФГБУ НЦЭСМП Минздрава. www.regmed.ru. Дата обращения: 9 июля 2020. Архивировано 9 июля 2020 года.
- ↑ Совместное применение Метиленового синего с ингибиторами обратного захвата серотонина — риск развития серотонинового синдрома. www.rlsnet.ru. Дата обращения: 9 июля 2020. Архивировано 12 июля 2020 года.
- ↑ #. Methylene Blue and the Risk of Serotonin Toxicity (англ.). Anesthesia Patient Safety Foundation. Дата обращения: 9 июля 2020. Архивировано 9 июля 2020 года.
Литература[править | править код]
- Лабораторный практикум по синтезу промежуточных продуктов и красителей / под ред. Ельцова А. В. — Л.: Ленинград-«Химия», 1985.
- Теренин А. Н. Фотохимия красителей и родственных органических соединений. — Л.: Издательство Академии Наук СССР, 1947.
- Химический энциклопедический словарь. Под ред. Кнунянц И. Л., М.: Советская энциклопедия, 1983. С. 331—332
- Беликов В. Г. Учебное пособие по фармацевтической химии. М.: Медицина, 1979. С. 328