Витамин A: различия между версиями
| [непроверенная версия] | [непроверенная версия] |
| Строка 227: | Строка 227: | ||
Наиболее ранним симптомом [[гиповитаминоз]]а является [[никталопия|куриная слепота]] — резкое снижение темновой адаптации. Характерными являются поражения эпителиальных тканей: кожи ([[фолликулярный гиперкератоз]]), слизистых оболочек кишечника (вплоть до образования язв), бронхов (частые [[бронхит]]ы), мочеполовой системы (легкое инфицирование). Дерматиты сопровождаются патологической пролиферацией, кератинизацией и слущиванием эпителия. [[Десквамация]] эпителия слезных каналов может приводить к их закупорке и уменьшению смачивания роговицы глаза — она высыхает ([[ксерофтальмия]]) и размягчается ([[кератомаляция]]) с образованием язв и «бельма». Поражение роговицы может развиваться очень быстро, так как нарушение защитных свойств эпителия приводит к вторичным инфекциям. При недостатке витамина также начинается отставание в росте<ref name="Витамины" />. |
Наиболее ранним симптомом [[гиповитаминоз]]а является [[никталопия|куриная слепота]] — резкое снижение темновой адаптации. Характерными являются поражения эпителиальных тканей: кожи ([[фолликулярный гиперкератоз]]), слизистых оболочек кишечника (вплоть до образования язв), бронхов (частые [[бронхит]]ы), мочеполовой системы (легкое инфицирование). Дерматиты сопровождаются патологической пролиферацией, кератинизацией и слущиванием эпителия. [[Десквамация]] эпителия слезных каналов может приводить к их закупорке и уменьшению смачивания роговицы глаза — она высыхает ([[ксерофтальмия]]) и размягчается ([[кератомаляция]]) с образованием язв и «бельма». Поражение роговицы может развиваться очень быстро, так как нарушение защитных свойств эпителия приводит к вторичным инфекциям. При недостатке витамина также начинается отставание в росте<ref name="Витамины" />. |
||
Надлежащее обеспечение, но не избыток витамина А, особенно важен для беременных и кормящих женщин для нормального развития плода и в грудное молоко<ref>{{cite journal |author=Strobel M, Tinz J, Biesalski HK |title=The importance of beta-carotene as a source of vitamin A with special regard to pregnant and breastfeeding women |journal=Eur J Nutr |volume=46 Suppl 1 |pages=I1–20 |year=2007 |pmid=17665093 |doi=10.1007/s00394-007-1001-z}}</ref><ref>{{cite journal |author=Schulz C, Engel U, Kreienberg R, Biesalski HK |title=Vitamin A and beta-carotene supply of women with gemini or short birth intervals: a pilot study |journal=Eur J Nutr |volume=46 |issue=1 |pages=12–20 |year=2007 |pmid=17103079 |doi=10.1007/s00394-006-0624-9}}</ref>. Недостатки не могут быть компенсированы послеродовой добавкой. |
|||
Метаболическая активность витамина ингибируется в результате потребления алкоголя во время беременности и характеризуется такой же тератогенностью, что и материнский дефицит витамина А<ref name="Crabb DW, et al. 2001 207S-217S">{{cite journal |author=Crabb DW, et al.|title=Alcohol and Retinoids|journal=Alcoholism: Clinical and Experimental Research |volume=25 Suppl 5 |pages=207S–217S |year=2001|doi=10.1111/j.1530-0277.2001.tb02398.x}}</ref>. |
|||
== Гипервитаминоз == |
== Гипервитаминоз == |
||
Версия от 19:20, 29 июля 2013



Витамин А — группа близких по строению веществ, которая включает ретинол (витамин A1, аксерофтол), дегидроретинол (витамин А2), ретиналь (ретинен, альдегид витамина A1), ретиновую кислоту и несколько провитаминов — каротиноидов, среди которых наиболее важным является β-каротин. Жирорастворимый. Витамин А имеет много функций. Ретиналь является компонентом родопсина — основного зрительного пигмента. В форме ретиноевой кислоты он стимулирует рост и развитие. Ретинол является структурным компонентом клеточных мембран[1].
История открытия
В 1906 году Фредерик Хопкинс предположил, что помимо белков, жиров, углеводов и т. д., пища содержит ещё какие-то вещества, необходимые для человеческого организма, которые он назвал «accessory food factors».[2]
Открытие самого витамина А произошло в 1913 году. Две группы ученых, Элмер МакКоллум[англ.] (1859—1929) и Маргарет Дэвис (1887—1967) из университета Висконсин и Томас Осборн[англ.] (1859—1929) и Лафайет Мендель[англ.] (1872—1935) из Йельского университета независимо друг от друга после серии исследований пришли к выводу, что сливочное масло и желток куриного яйца содержат какое-то необходимое для нормальной жизнедеятельности вещество. На их экспериментах было показано, что мыши, питавшееся лишь комбинацией казеина, жира, лактозы, крахмала и соли страдали от воспаления глаз и диареи, кроме того умирали по происшествии около 60 дней. Если добавить сливочное масло, масло из печени трески или яйца, то они приходили в норму. Это означало, что требовалось не только наличие жира, но и какое-то другое вещество. МакКоллум также показал, что это вещество можно разрушить окислением или сильным нагреванием[2].
В 1920 году Джек Сесиль Драммонд[англ.] (1891—1952) предложил новую номенклатуру витаминов и после этого витамин приобрёл современное название[2].
В 1931 году швейцарский химик Пауль Каррер (1889—1971) описал химическую структуру витамина А. Его достижение был отмечено Нобелевской премией по химии в 1937 году. Гарри Холмс (1879—1958) и Рут Корбет кристаллизовали витамин А в 1937 году. В 1946 году Дэвид Адриан ван Дорп[англ.] (1915—1995) и Йозеф Фердинанд Аренс[нидерл.] (1914—2001) синтезировали витамин А. Отто Ислер (1920—1992) в 1947 году разработал промышленный метод синтеза[2].
Роль витамина А в зрении была открыта биохимиком Джорджем Уайлдом (1906—1997), за что он получил Нобелевскую премию в 1967 году[2].
Физико-химические свойства
Вещества группы витамина А являются кристаллическими веществами. Нерастворимы в воде, хорошо растворимы в органических растворителях[3].
Ретинол разлагается кислородом воздуха. Все соединения склонны к цис-транс-изомеризации, особенно по связям 11 и 13, однако кроме 11-цис-ретиналя все двойные связи имеют транс-конфигурацию[3].
| Соединение | Молярная масса | Температура плавления, °С | λмакс (этанол), нм |
|---|---|---|---|
| Ретинол | 286,46 | 64 | 324-325 |
| Ретиналь | 284,45 | 61-64 | 375 |
| Ретиноевая кислота | 300,45 | 181 | 347 |
| Ретинолпальмитат | 328,5 | 57-58 | 326 |
| Ретинолацетат | 524,8 | 28-29 | 325-328 |
Суточная потребность
| Возрастная категория | Норма употребления, мкг | Максимальное количество, мкг |
|---|---|---|
| Младенцы | 400 (0—6 мес.), 500 (7—12 мес.) | 600 |
| Дети | 300 (1—3 года), 400 (4—8 года) | 600 (1—3 года), 900 (4—8 года) |
| Мужчины | 600 (9—13 лет), 900 (14—>70 лет) | 1700 (9—13 лет), 2800 (14—18 лет), 3000 (19—>70 лет) |
| Женщины | 600 (9—13 лет), 700 (14—>70 лет) | 1700 (9—13 лет), 2800 (14—18 лет), 3000 (19—>70 лет) |
| Беременные | 750 (<19 лет), 770 (19 — >50 лет) | 2800 (<19 лет), 3000 (19 — >50 лет) |
| Лактация | 1200 (<19 лет), 1300 (19 — >50 лет) | 2800 (<19 лет), 3000 (19 — >50 лет) |
Строение и формы витамина А
В продуктах животного происхождения содержится во всех формах, однако так как чистый ретинол нестабилен, то основная часть находится в виде сложных эфиров (в промышленности в основном выпускается в виде пальмитата или ацетата) ретинола[5].
Витамин А представляет собой циклический непредельный спирт, состоящий из β-иононового кольца и боковой цепи из двух остатков изопрена и первичной спиртовой группы. В организме окисляется до ретиналя (витамин А-альдегид) и ретиноевой кислоты. Депонируется в печени в виде ретинилпальмитата, ретинилацетата и ретинилфосфата[1].
В растениях содержатся провитамины А — некоторые каротиноиды. Предшественником витамина могут быть две группы структурно близких веществ: каротины (α-, Β- и γ-каротины) и ксантофиллы (β-криптоксантин). Каротиноиды также являются изопреноидными соединениями, α и γ-каротины содержат по одному β-иононовому кольцу и при окислении образуется одна молекула ретинола, а в β-каротине — два иононовых кольца, следовательно он обладает большей биологической активностью и из него образуется две молекулы ретинола[1].
Плотоядные животные, такие как, например, кошачьи из-за отсутствия 15-15'-диоксигеназы не могут преобразовать каротиноиды в ретиналь (в результате ни один из каротиноидов не является формой витамина А для этих видов)[6].
Пищевые источники
Ретинол присутствует только в продуктах животного происхождения, особенно много его в печени морских рыб и млекопитающих. Источником витамина для человека могут также быть каротины. Они нетоксичны в высоких дозах, но не могут полностью заменить ретинол, так как лишь ограниченное количество способно превратиться в витамин А. Наибольшее количество β-каротина содержится в различных сортах моркови, но его концентрация может резко варьироваться от сорта к сорту (от 8 до 25 мг на 100 г). Хорошим источником являются красный перец, зелёный лук, салат, тыква и томаты[1].
| Растительные (каротиноиды) | Животные (ретиноиды) |
|---|---|
| Зеленые и жёлтые овощи (морковь, тыква, сладкий перец, шпинат, брокколи, зелёный лук, зелень петрушки), бобовые (соя, горох), персики, абрикосы, яблоки, виноград, арбуз, дыня, шиповник, облепиха, черешня. | Рыбий жир, печень (особенно говяжья), икра, молоко, сливочное масло, маргарин, сметана, творог, сыр, яичный желток |
Неравнозначность ретиноидов и каротиноидов
Поскольку только часть каротиноидов могут преобразовываться в организме в витамин A, для сравнения ценности продуктов питания необходимо понимать, сколько употреблённых с пищей каротиноидов равноценны определённому количеству ретинола. Некоторая путаница возникает из-за того, что представление об эквивалентном количестве с течением времени менялось.
В течение многих лет использовалась система, основанная на международных единицах (МЕ). Одна МЕ равняется 0,3 мкг ретинола, 0,6 мкг β-каротина или 1,2 мкг других каротиноидов, являющихся провитаминами A.
Позднее стали использовать другую единицу — эквивалент ретинола (ЭР). 1 ЭР соответствовал 1 мкг ретинола, 2 мкг растворённого в жире β-каротина (из-за плохой растворимости в большинстве витаминных комплексов β-каротин растворён лишь частично), 6 мкг β-каротина в обычной пище (т.к. усвояемость в этом случае ниже, чем в случае растворённого в жире β-каротина) или 12 мкг α-каротина, γ-каротина или β-криптоксантина в пище (т.к. из молекул этих каротиноидов образуется на 50 % меньше ретинола по сравнению с молекулами β-каротина)[7].
Более поздние исследования показали, что в действительности усваиваемость каротиноидов в два раза ниже по сравнению с тем, что считалось ранее. В связи с этим в 2001 Институт медицины США вводит очередную новую единицу — эквивалент активности ретинола (RAE). 1 RAE соответствует 1 мкг ретинола, 2 мкг растворённого в жире β-каротина, 12 мкг «пищевого» β-каротина или 24 мкг оставшихся провитаминов.[7]
| Вещество и химическое окружение | Микрограмм эквивалента активности ретинола на 1 микрограмм вещества |
|---|---|
| ретинол | 1 |
| бета-каротин, растворённый в жире | 1/2 |
| бета-каротин в пище | 1/12 |
| альфа-каротин в пище | 1/24 |
| гамма-каротин в пище | 1/24 |
| бета-криптоксантин в пище | 1/24 |
Метаболизм

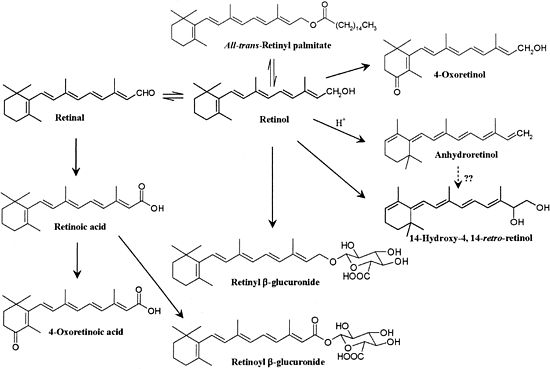
Усвоение витамина А из продуктов и лекарственной формы происходит с участием специальной гидролазы поджелудочной железы и слизистой оболочки тонкой кишки. У детей до 6 месяцев гидролазы функционируют недостаточно. Для всасывания важно наличие достаточного количества жирной пищи и жёлчи. Всасывание происходит в составе мицелл, затем в энтероцитах они включаются в состав хиломикронов[1]. Попавший в клетку эпителия кишечника витамин вновь превращается в эфир пальмитиновой кислоты и в таком виде поступает в лимфу, а затем в кровь. Из мышцы всасывается только ацетат ретинола[8].
В крови витамин А соединяется со специальным белком, связывающим ретинол (БСР), синтезируемым в печени, ретиноевая кислота соединяется с альбумином[5]. Белок обеспечивает растворимость ретинола, защиту от окисления и транспорт в различные ткани. Препарат, не связанный с белком, токсичен. Затем образовавшийся комплекс (витамин А + БСР) соединяется еще с одним белком — транстиретином, препятствующим фильтрации препарата в почках. По мере использования тканями витамина А происходит его отщепление от вышеназванных белков и поступление в ткани[8].
Главное место накопления витамина - печень (90%), в меньших количествах также хранится в почках, жировой ткани и надпочечниках)[5].
Поступление ретинола к плоду через плаценту в последнем триместре беременности регулируется специальным механизмом, вероятно с фетальной стороны. Избыток витамина А депонируется в печени в виде эфира с пальмитиновой кислотой. Депо препарата в печени принято считать достаточным, если оно превышает 20 мкг/г её ткани — у новорожденного и 270 мкг/г ткани — у взрослого. Показателем содержания витамина А в печени служит и его уровень в плазме крови: если он меньше 10 мкг/дл, то у человека гиповитаминоз. У доношенного ребенка запасов витамина А хватает на 2—3 месяца[8].
В клетках органов-мишеней есть специальные цитозольные рецепторы, распознающие и связывающие комплекс ретиноид + ретинол-связывающий белок (РСБ). В сетчатке глаза ретинол превращается в ретиналь, а в печени он подвергается биотрансформации, превращаясь сначала в активные метаболиты (в ретиналь, а затем в ретиноевую кислоту, которая выводится с желчью в виде глюкуронидов), а затем в неактивные продукты, выводимые почками и кишечником. Попав в кишечник, препарат участвует в энтерогепатической циркуляции. Элиминация осуществляется медленно: за 21 день из организма исчезает всего 34 % введенной дозы. Поэтому довольно велика опасность кумуляции препарата при повторных приемах[8][1].
Взаимодействие
Синергистом витамина А является витамин Е, который способствует сохранению ретинола в активной форме, всасыванию из кишечника и его анаболическим эффектам. Витамин А нередко назначают вместе с витамином D. При лечении гемералопии его следует назначать вместе с рибофлавином, никотиновой кислотой. Нельзя одновременно с витамином А назначать холестирамин, активированный уголь, нарушающие его всасывание[8].
Роль
Витамин А имеет следующие фармакологические эффекты[8]:
1. Синтез ферментов, необходимых для активирования фосфоаденозинфосфосульфата (ФАФС), входящего в состав:
а) мукополисахаридов: хондроитинсерной кислоты и сульфогликанов — компонентов соединительной ткани, хрящей, костей; гиалуроновой кислоты — основного межклеточного вещества; гепарина;
б) сульфоцереброзидов;
в) таурина (входит в состав таурохолевой желчной кислоты, стимулирует синтез соматотропного гормона, участвует в синаптической передаче нервного импульса, обладает антикальциевым эффектом);
г) ферментов печени, участвующих в метаболизме эндогенных и экзогенных веществ.
2. Синтез соматомединов А1, А2, В и С, способствующих синтезу белков мышечной ткани; включению фосфатов и тимидина в ДНК, пролина в коллаген, уридина в РНК.
3. Гликолизирование полипептидных цепей:
а) гликопротеинов крови (а1 — макроглобулин и др.);
б) гликопротеинов, являющихся компонентами клеточных и субклеточных (митохондриальных и лизосомальных) мембран, что имеет огромное значение для завершения фагоцитоза;
в) гликопротеина — фибронектина, участвующего в межклеточном взаимодействии, за счет чего происходит торможение роста клеток.
4. Синтез половых гормонов, а также интерферона, иммуноглобулина А, лизоцима.
5. Синтез ферментов эпителиальных тканей, предупреждающих преждевременную кератинацию.
6. Активация рецепторов для кальцитриола (активного метаболита витамина D).
7. Синтез родопсина в палочках сетчатки, необходимого для сумеречного зрения.
Участие витамина в процессе зрения

Витамин А в форме ретиналя играет важную роль в зрении. 11-Цис-ретиналь связывается с белком опсином, образуя пигмент пурпурно-красного цвета родопсин — основной зрительный пигмент, участвующий в создании зрительного сигнала. Механизм образования зрительного сигнала таков[1]:
- Квант света стимулирует мембранные рецепторы наружного сегмента палочек сетчатки.
- Абсорбция света родопсином изомеризирует 11-цис-связь в ретинале в транс-связь. Такая транс-структура называется батородопсином (активированным родопсином). Транс-ретиналь имеет бледно-жёлтый оттенок, поэтому при освещении родопсин обесцвечивается.
- При освобождении протона из батородопсина образуется метародопсин, гидролитический распад которого даёт опсин и транс-ретиналь. Фотохимическая цепь в батородопсине служит для активации G-белка, называемого трансдуцином. Трансдуцин активируется ГТФом.
- Комплекс трансдуцин — ГДФ активирует специфическую фосфодиэстеразу, которая расщепляет цГМФ.
- Далее ГМФ стимулирует стимулирует каскад событий, генерирующих зрительный сигнал в мозге: перекрытие NA+-K+ сигналов → деполяризация мембраны → возникновение электрического импульса → преобразование импульса в зрительное восприятие в мозге.
Образование цис-ретиналя из транс-формы, катализируемое ретинальизомеразой, является медленным процессом, протекающим на свету. Оно лишь частично протекает в сетчатке, основное место синтеза — печень. В сетчатке под действием дегидрогеназы транс-ретиналь превращается в транс-ретинол, а затем поступает в кровь, где связывается с БСР и транспортируется в печень. Там ретинолизомераза превращает транс-ретинол в цис-ретинол, а потом с помощью NAD+-зависимой дегидрогеназы в цис-ретиналь, который затем поступает в сетчатку. Синтез родопсина из цис-ретиналя и опсина протекает в темноте. Полное восстановление родопсина у человека занимает около 30 минут.[1]
Подобный процесс проходит и в колбочках. Сетчатка содержит три вида колбочек, каждый из которых одним из трёх видов йодопсина, поглощающих синий, зелёный и красный цвет. Все три пигмента тоже содержат 11-цис-ретиналь, но различаются по природе опсина. Некоторые формы цветовой слепоты (дальтонизм) вызваны врождённым отсутствием синтеза одного из трёх типов опсина в колбочках или синтезом дефектного опсина[9].
Участие витамина А в антиоксидантной защите организма
Благодаря наличию двух сопряженных двойных связей в молекуле ретинол способен взаимодействовать со свободными радикалами, в том числе и со свободными радикалами кислорода. Эта важнейшая особенность витамина позволяет считать его эффективным антиоксидантом. Ретинол также значительно усиливает антиоксидантное действие витамина Е. Вместе с токоферолом и витамином С он активирует включение селена в состав глутатионпероксидазы. Витамин А способен поддерживать SH-группы в восстановленном состоянии (им тоже присуща антиоксидантная функция). Однако витамин А может проявить себя и как прооксидант, так как он легко окисляется кислородом воздуха с образованием высокотоксичных перекисных продуктов. Витамин Е препятствует окислению ретинола[1].
Транскрипция генов
Витамин А и его производные действуют на специфические рецепторные белки в клеточных ядрах. Далее такой лиганд-рецепторный комлекс связывается с участками ДНК и вызывают дерепрессию генов, регулируя таким образом синтез белков, ферментов или компонентов тканей[8][1].
Гиповитаминоз

Дефицит витамина А по оценкам затрагивает примерно треть детей в возрасте до пяти лет во всем мире. Это уносит жизни 670 000 детей в возрасте до пяти в год[10]. Приблизительно 250,000-500,000 детей в развивающихся странах становятся слепыми каждый год в связи с дефицитом витамина А (в основном в Юго-Восточной Азии и Африке)[11].
Недостаток витамина А может произойти из-за первичной или вторичной недостаточности. Первичный дефицит витамина А возникает среди детей и взрослых, которые не потребляют нужное количество каротиноидов из фруктов и овощей или витамина А из животных и молочных продуктов. Ранний отказ от грудного вскармливания может также увеличить риск дефицита витамина А.
Вторичный дефицит витамина А связан с хроническим нарушением всасывания липидов, желчеобразования и хроническому воздействию окислителей, таких как сигаретный дым, и хронический алкоголизм. Витамин А - жирорастворимый витамин, и зависит от мицеллярной солюбилизации для дисперсии в тонком кишечнике, что приводит к плохому использованию витамина А с низким содержанием жиров. Дефицит цинка также может ухудшать всасывание, транспорт и метаболизм витамина А, поскольку он необходим для синтеза транспортных белков и в качестве кофактора для превращения ретинола в ретиналь. В недоедающих популяциях, общее низкое употребление витамина А и цинка усиливают выраженность дефицита витамина А. Исследование, проведенное в Буркина-Фасо показали значительное снижение заболеваемости малярией с комбинированным витамина А и цинка в детей младшего возраста[12].
Наиболее ранним симптомом гиповитаминоза является куриная слепота — резкое снижение темновой адаптации. Характерными являются поражения эпителиальных тканей: кожи (фолликулярный гиперкератоз), слизистых оболочек кишечника (вплоть до образования язв), бронхов (частые бронхиты), мочеполовой системы (легкое инфицирование). Дерматиты сопровождаются патологической пролиферацией, кератинизацией и слущиванием эпителия. Десквамация эпителия слезных каналов может приводить к их закупорке и уменьшению смачивания роговицы глаза — она высыхает (ксерофтальмия) и размягчается (кератомаляция) с образованием язв и «бельма». Поражение роговицы может развиваться очень быстро, так как нарушение защитных свойств эпителия приводит к вторичным инфекциям. При недостатке витамина также начинается отставание в росте[1].
Надлежащее обеспечение, но не избыток витамина А, особенно важен для беременных и кормящих женщин для нормального развития плода и в грудное молоко[13][14]. Недостатки не могут быть компенсированы послеродовой добавкой.
Метаболическая активность витамина ингибируется в результате потребления алкоголя во время беременности и характеризуется такой же тератогенностью, что и материнский дефицит витамина А[15].
Гипервитаминоз
Есть двав типа
Для гипервитаминоза характерны следующие симптомы: воспаление роговицы глаза, потеря аппетита, тошнота, увеличение печени, боли в суставах. Хроническое отравление витамином А наблюдается при регулярном употреблении высоких доз витамина, больших количеств рыбьего жира[1].
Случаи острого отравления со смертельным исходом возможны при употреблении в пищу печени акулы, белого медведя, морских животных, хаски[1][16][17],[18]. Европейцы начали сталкиватся с этим по крайней мере с 1597, когда Геррит де Веер и его люди серьезно заболели после того, как съели печень белого медведя[19] .
Острая форма проявляется в виде судорог, паралича. При хронической форме передозировки повышается внутричерепное давление, что сопровождается головной болью, тошнотой, рвотой. Одновременно возникает отёчность жёлтого пятна и связанные с этим нарушения зрения. Проявляются геморрагии, а также признаки гепато- и нефротоксического действия больших доз витамина А. Могут происходить спонтанные переломы костей[20][21].
Избыток витамина А может вызвать врожденные дефекты и поэтому не должна превышать рекомендуемой дневной нормы[22].
Для ликвидации гипервитаминоза назначают маннит, снижающий внутричерепное давление и ликвидирующий симптомы менингизма, глюкокортикоиды, ускоряющие метаболизм витамина в печени и стабилизирующие мембраны лизосом в печени и почках. Витамин Е тоже стабилизирует клеточные мембраны. Большие дозы витамина А нельзя назначать беременным (особенно на ранних стадиях беременности) и даже за полгода до беременности, так как очень велика опасность возникновения тератогенного эффекта[8].
Врождённые нарушения обмена витамина А
Гиперкаротинемия
Причиной заболевания является отсутствие кишечной β-каротиноксигеназы, катализирующей реакцию образования ретинола из каротинов. Основными симптомами являются куриная слепота и помутнение роговицы. Резко снижено содержание ретинола в крови[1].
Фолликулярный кератоз Дарье
Наследственное заболевание, наряду с изменениями кожи отмечаются отставание умственного развития и психозы. Типичны продольная исчерченность и зазубренность ногтей. Эффективно длительное назначение повышенных доз витамина А[1].
Показания к применению
- Профилактика и устранение гиповитаминоза. Специфических критериев выявления гиповитаминоза А не существует. Врач может ориентироваться на клинику (анорексия, замедление роста, низкая резистентность к инфекции, появление признаков менингизма, возникновение язвенного процесса на слизистых оболочках) и лабораторные данные (содержание витамина А в крови)[8].
- Инфекционные заболевания (вместе с витамином С)[8].
- Рахит (вместе с витамином D)[8].
- Никталопия (вместе с рибофлавином и никотиновой кислотой)[8].
- Кожные заболевания (псориаз, пустулезный дерматит и т. д.).
Существуют специальные препараты витамина А для лечения заболеваний кожи: изотретиноин (ретиноевая кислота) и этретинат (её этиловый эфир). Они во много раз активнее ретинола[8].
Примечания
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 Т.С.Морозкина, А.Г.Мойсеёнок. Витамины. — Минск: Асар, 2002. — С. 58-63.
- ↑ 1 2 3 4 5 Richard D. Semba. "On the 'Discovery' of Vitamin A" (англ.) // Annals of Nutrition and Metabolism. — 2012. — No. 61 (3). — P. 192–198. — doi:10.1159/000343124.
- ↑ 1 2 3 Кнунянц И. Л. и др. т.1 А-Дарзана // Химическая энциклопедия. — М.: Советская энциклопедия, 1988. — 623 с. — 100 000 экз.
- ↑ Dietary Reference Intakes: Vitamins.
- ↑ 1 2 3 Comprehensive Guide to Vitamin A.
- ↑ Retinol.
- ↑ 1 2 Jaspreet K.C. Ahuja, Jacob Exler and others. Composition of Foods Raw, Processed, Prepared USDA National Nutrient Database for Standard Reference.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 13 И.Б.Михайлов. Клиническая фармакология. — Санкт-Петербург: Фолиант, 1998. — С. 151-154.
- ↑ Т.Т.Березов, Б.Ф.Коровкин. Биологическая химия. — Москва: Медицина, 1998. — С. 212.
- ↑ Black, RE; Allen, LH; Bhutta, ZA; Caulfield, LE; De Onis, M; Ezzati, M; Mathers, C; Rivera, J; Maternal and Child Undernutrition Study Group (2008). "Maternal and child undernutrition: global and regional exposures and health consequences". Lancet. 371 (9608): 243—60. doi:10.1016/S0140-6736(07)61690-0. PMID 18207566.
- ↑ Office of Dietary Supplements. Vitamin A. National Institute of Health. Дата обращения: 8 апреля 2008.
- ↑ Zeba AN, Sorgho H, Rouamba N; et al. (2008). "Major reduction of malaria morbidity with combined vitamin A and zinc supplementation in young children in Burkina Faso: a randomized double blind trial". Nutr J. 7: 7. doi:10.1186/1475-2891-7-7. PMC 2254644. PMID 18237394.
{{cite journal}}: Явное указание et al. в:|author=(справка)Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) Википедия:Обслуживание CS1 (не помеченный открытым DOI) (ссылка) - ↑ Strobel M, Tinz J, Biesalski HK (2007). "The importance of beta-carotene as a source of vitamin A with special regard to pregnant and breastfeeding women". Eur J Nutr. 46 Suppl 1: I1—20. doi:10.1007/s00394-007-1001-z. PMID 17665093.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ Schulz C, Engel U, Kreienberg R, Biesalski HK (2007). "Vitamin A and beta-carotene supply of women with gemini or short birth intervals: a pilot study". Eur J Nutr. 46 (1): 12—20. doi:10.1007/s00394-006-0624-9. PMID 17103079.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ Crabb DW; et al. (2001). "Alcohol and Retinoids". Alcoholism: Clinical and Experimental Research. 25 Suppl 5: 207S—217S. doi:10.1111/j.1530-0277.2001.tb02398.x.
{{cite journal}}: Явное указание et al. в:|author=(справка) - ↑ Rodahl, K. (1943-07). "The vitamin A content and toxicity of bear and seal liver". Biochemical Journal. 37 (2): 166—168. ISSN 0264-6021. PMC 1257872. PMID 16747610.
{{cite journal}}: Неизвестный параметр|coauthors=игнорируется (|author=предлагается) (справка) - ↑ Walrus, liver, raw (Alaska Native). Mealographer. Дата обращения: 25 марта 2010.
- ↑ Moose, liver, braised (Alaska Native). Mealographer. Дата обращения: 15 октября 2012.
- ↑ Lips, Paul (2003). "Hypervitaminosis a and Fractures". New England Journal of Medicine. 348 (4): 347—9. doi:10.1056/NEJMe020167. PMID 12540650.
- ↑ Penniston, Kristina L. (2006). "The acute and chronic toxic effects of vitamin A". Am. J. Clin. Nutr. 83 (2): 191—201. PMID 16469975.
{{cite journal}}: Неизвестный параметр|coauthors=игнорируется (|author=предлагается) (справка) - ↑ Forsmo, Siri (2008). "Childhood Cod Liver Oil Consumption and Bone Mineral Density in a Population-based Cohort of Peri- and Postmenopausal Women: The Nord-Trøndelag Health Study". Am. J. Epidemiol. 167 (4): 406—411. doi:10.1093/aje/kwm320. PMID 18033763.
{{cite journal}}: Неизвестный параметр|coauthors=игнорируется (|author=предлагается) (справка) - ↑ Duester, G (2008). "Retinoic Acid Synthesis and Signaling during Early Organogenesis". Cell. 134 (6): 921—31. doi:10.1016/j.cell.2008.09.002. PMC 2632951. PMID 18805086.
Литература
- Semba R. D. On the 'discovery' of vitamin A. (англ.) // Annals of Nutrition and Metabolism. — 2012. — Vol. 61. — P. 192—198. — doi:10.1159/000343124. — PMID 23183288.