Вирус иммунодефицита человека: различия между версиями
| [отпатрулированная версия] | [отпатрулированная версия] |
Sirozha (обсуждение | вклад) |
Sirozha (обсуждение | вклад) |
||
| Строка 84: | Строка 84: | ||
Вирус иммунодефицита человека относят к семейству [[ретровирусы|ретровирусов]] (''Retroviridae''), роду лентивирусов (''[[Lentivirus]]''). Название ''Lentivirus'' происходит от латинского слова ''lente'' — медленный. Такое название отражает одну из особенностей вирусов этой группы, а именно — медленную и неодинаковую скорость развития инфекционного процесса в макроорганизме. Для лентивирусов также характерен длительный инкубационный период.<ref name= KurthBannert>{{cite book |editor=Kurth, R; Bannert, N |year=2010 |title=Retroviruses: Molecular Biology, Genomics and Pathogenesis |publisher=Caister Academic Press |isbn=978-1-904455-55-4}}</ref> |
Вирус иммунодефицита человека относят к семейству [[ретровирусы|ретровирусов]] (''Retroviridae''), роду лентивирусов (''[[Lentivirus]]''). Название ''Lentivirus'' происходит от латинского слова ''lente'' — медленный. Такое название отражает одну из особенностей вирусов этой группы, а именно — медленную и неодинаковую скорость развития инфекционного процесса в макроорганизме. Для лентивирусов также характерен длительный инкубационный период.<ref name= KurthBannert>{{cite book |editor=Kurth, R; Bannert, N |year=2010 |title=Retroviruses: Molecular Biology, Genomics and Pathogenesis |publisher=Caister Academic Press |isbn=978-1-904455-55-4}}</ref> |
||
Для вируса иммунодефицита человека характерна высокая частота генетических изменений, возникающих в процессе самовоспроизведения. Частота возникновения ошибок у ВИЧ составляет 10<sup>−3</sup> — 10<sup>−4</sup> ошибок / (геном * цикл репликации), что на несколько порядков больше аналогичной величины у эукариот. Длина генома ВИЧ составляет примерно 10<sup>4</sup> нуклеотидов. Из этого следует, что практически каждый вирус хотя бы на один нуклеотид отличается от своего предшественника. В природе ВИЧ существует в виде множества квази-видов, являясь при этом одной таксономической единицей. В процессе исследования ВИЧ всё-таки были обнаружены разновидности, которые значительно отличались друг от друга по нескольким признакам, в частности различной структурой генома. Разновидности ВИЧ обозначаются арабскими цифрами. На сегодняшний день известны ВИЧ-1, ВИЧ-2, ВИЧ-3, ВИЧ-4. |
Для вируса иммунодефицита человека характерна высокая частота генетических изменений, возникающих в процессе самовоспроизведения. Частота возникновения ошибок у ВИЧ составляет 10<sup>−3</sup> — 10<sup>−4</sup> ошибок / (геном * цикл репликации), что на несколько порядков больше аналогичной величины у эукариот. Длина генома ВИЧ составляет примерно 10<sup>4</sup> нуклеотидов. Из этого следует, что практически каждый вирус хотя бы на один нуклеотид отличается от своего предшественника. В природе ВИЧ существует в виде множества квази-видов, являясь при этом одной таксономической единицей<ref name=RobertsonDL>{{cite journal | author = Robertson DL, Hahn BH, Sharp PM | title = Recombination in AIDS viruses | journal = J Mol Evol. | volume = 40 | issue = 3 | pages = 249–59 | year = 1995 | pmid = 7723052 | doi = 10.1007/BF00163230 }}</ref><ref name="Rambaut_2004">{{cite journal | author = Rambaut A, Posada D, Crandall KA, Holmes EC | title = The causes and consequences of HIV evolution | journal = Nature Reviews Genetics | volume = 5 | issue = 52–61 | pages = 52–61 | date = January 2004 | pmid = 14708016 | doi = 10.1038/nrg1246 | url = http://tree.bio.ed.ac.uk/downloadPaper.php?id=242 }}</ref><ref name="pmid17960579">{{cite journal | author = Perelson AS, Ribeiro RM | title = Estimating drug efficacy and viral dynamic parameters: HIV and HCV | journal = Stat Med | volume = 27 | issue = 23 | pages = 4647–57 | date = October 2008 | pmid = 17960579 | doi = 10.1002/sim.3116 | url = }}</ref>. В процессе исследования ВИЧ всё-таки были обнаружены разновидности, которые значительно отличались друг от друга по нескольким признакам, в частности различной структурой генома. Разновидности ВИЧ обозначаются арабскими цифрами. На сегодняшний день известны ВИЧ-1, ВИЧ-2, ВИЧ-3, ВИЧ-4. |
||
* ВИЧ-1 — первый представитель группы, открытый в [[1983 год]]у. Является наиболее распространённой формой<ref name=bartlett>{{книга|автор=Джон Бартлетт|часть=Типы и подтипы ВИ|заглавие=Клинические аспекты ВИЧ-инфекции|ссылка часть=http://www.eurasiahealth.org/attaches/82168/MMHIV10_2.pdf|год=2009}} [http://www.webcitation.org/6A3qODrr7 Архив]</ref>. |
* ВИЧ-1 — первый представитель группы, открытый в [[1983 год]]у. Является наиболее распространённой формой<ref name=bartlett>{{книга|автор=Джон Бартлетт|часть=Типы и подтипы ВИ|заглавие=Клинические аспекты ВИЧ-инфекции|ссылка часть=http://www.eurasiahealth.org/attaches/82168/MMHIV10_2.pdf|год=2009}} [http://www.webcitation.org/6A3qODrr7 Архив]</ref>. |
||
Версия от 13:17, 20 июля 2014
- Эта статья о патогене — вирусе иммунодефицита человека. О заболевании — статья ВИЧ-инфекция. О терминальной стадии болезни — статья СПИД.
| Вирус иммунодефицита человека | ||||||
|---|---|---|---|---|---|---|
![Стилизованное изображение сечения ВИЧ[1]](http://upload.wikimedia.org/wikipedia/commons/thumb/e/ea/Human_Immunodeficency_Virus_-_stylized_rendering.jpg/275px-Human_Immunodeficency_Virus_-_stylized_rendering.jpg) Стилизованное изображение сечения ВИЧ[1] | ||||||
| Научная классификация | ||||||
|
Реалм: Царство: Pararnavirae Тип: Artverviricota Класс: Порядок: Семейство: Подсемейство: Род: Группа: Primate lentivirus group |
||||||
| Международное научное название | ||||||
| Primate lentivirus group | ||||||
| Виды | ||||||
|
||||||
| Группа по Балтимору | ||||||
| VI: оцРНК-ОТ-вирусы | ||||||
| ||||||
Ви́рус иммунодефици́та челове́ка — ретровирус из рода лентивирусов, вызывающий ВИЧ-инфекцию[3][4] — хроническое заболевание, сопровождающееся угнетением иммунной системы, появлением оппортунистических инфекций, а в случае отсутствия антиретровирусной терапии — иммунодефицитом и смертью в среднем через 9-11 лет после заражения[5][6].
Вирус передаётся через прямой контакт крови или поврежденной слизистой оболочки здорового человека с биологическими жидкостями зараженного человека: кровью, спермой, секретом влагалища, предсеменной жидкостью и грудным молоком. Передача вируса может происходить при незащищенном анальном, вагинальном или оральном сексе[7][8], переливании крови, использовании зараженных игл и шприцев (особенно потребителями инъекционных наркотиков)[9]; между матерью и ребёнком во время беременности, родов[10][11] или при грудном вскармливании[12] через указанные выше биологические жидкости. Вирус не передается бытовым путем, а также через слюну[13], слезы[13] и укусы насекомых[14].
Общие сведения
Диагностика
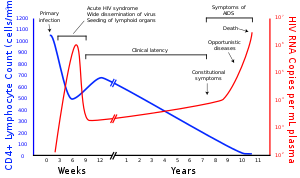
Обязательная проверка донорской крови в развитых странах в значительной степени сократила возможность передачи вируса при её использовании. Тестирование на ВИЧ беременных женщин позволяет своевременно начать приём лекарств и родить здорового ребёнка. Анализ крови позволяет обнаружить антитела к белкам вируса (ИФА), белки вируса (вестерн-блот), РНК вируса (ОТ-ПЦР)[15]. Определение вирусной нагрузки (подсчет количества копий РНК вируса в миллилитре плазмы крови) позволяет судить о стадии заболевания и эффективности лечения[16][17].
Известно, что принудительное тестирование населения бесперспективно с точки зрения сдерживания эпидемии и противоречит соблюдению прав человека. В России проведение теста без согласия человека является незаконным[18], однако существуют ситуации, в которых предоставление результатов тестирования на ВИЧ является обязательным, но не насильственным (донорство, трудоустройство медицинских работников, для иностранных граждан, получающих разрешение на пребывание в РФ, в местах лишения свободы при наличии клинических показаний)[19].
ВИЧ-инфекция
Вирус поражает клетки иммунной системы, имеющие на своей поверхности рецепторы CD4: Т-хелперы, моноциты, макрофаги, клетки Лангерганса и дендритные клетки. В ходе болезни у одного и того же человека возникают новые штаммы вируса, которые различаются по скорости воспроизведения и способности инфицировать[5][20]. Размножившись, вирусные частицы выделяются из пораженных клеток и внедряются в новые, цикл развития повторяется. Инфицированные вирусом Т-хелперы постепенно гибнут из-за разрушения вирусом, апоптоза или уничтожения Т-киллерами.
В процессе развития ВИЧ-инфекции число Т-хелперов снижается настолько, что организм уже не может противостоять возбудителям оппортунистических инфекций, которые неопасны или мало опасны для здоровых людей с нормально функционирующей иммунной системой. Ослабленный организм поражают бактериальные, грибковые, вирусные, протозойные инфекции, опухоли а также другие заболевания[21][22][23]. В отсутствие антиретровирусной терапии, смерть пациента вызвана не размножением вируса в клетках CD4+, а развитием оппортунистических заболеваний (вторичных по отношению к ВИЧ-инфекции).
Эпидемиология
В мире по состоянию на конец 2011 года заражены ВИЧ-инфекцией более 60 миллионов человек, из них 25 миллионов умерли, а 35 миллионов живут с ВИЧ-инфекцией[24]. Более двух третей ВИЧ-инфицированных населяют Африку к югу от пустыни Сахары[25]. Oколо 90 % всех случаев заражения ВИЧ в Восточной Европе и Центральной Азии приходится на Россию и Украину[26]. В 2007 году 57 % новых диагностированных случаев ВИЧ в Восточной Европе было обусловлено использованием зараженного инструментария для употребления инъекционных наркотиков[26]. По оценкам, в настоящее время в регионе инъекционные наркотики употребляют 3,7 миллиона человек, причем считается, что примерно четвёртая часть из них заражена ВИЧ[26]. В России по состоянию на конец 2013 года были заражены ВИЧ-инфекцией 798 тысяч человек, из них 153 тысячи умерли, а 645 тысяч живут с ВИЧ-инфекцией[27].
Лечение
Из 35 миллионов человек, живущих с ВИЧ-инфекцией, часть остаётся в живых благодаря приёму антиретровирусной терапии. Антиретровирусные препараты мешают вирусу размножаться в иммунных клетках человека: блокируя внедрение вирионов ВИЧ в иммунные клетки и нарушая на разных этапах процесс сборки новых вирионов. Своевременно начатое лечение антиретровирусными препаратами в сотни раз снижает риск наступления СПИДа и последующей смерти[28][29][30]. Антиретровирусные препараты у части пациентов вызывают побочные эффекты, в некоторых случаях даже требующие сменить схему лечения (поменять набор принимаемых лекарств).
Терапия назначается при снижении иммунитета и/или высокой вирусной нагрузке. В случае, если иммунитет сильный и вирусная нагрузка низкая — терапия не назначается по нескольким причинам. Во-первых, после назначения терапии лекарства нужно принимать ежедневно в одно и то же время и пожизненно, что само по себе создает неудобства для пациентов. Во-вторых, высокая стоимость месячного курса лекарств. Необходимые лекарства получают менее половины из 9,5 млн человек, нуждающихся в противовирусной терапии[31].
После проникновения вируса в клетку фермент обратная транскриптаза синтезирует провирусную ДНК, которую затем фермент интеграза встраивает в геном клетки человека. Наличие вирусной ДНК в хромосомах человека является причиной, из-за которой невозможно полное излечение от ВИЧ-инфекции и других ретровирусных заболеваний. В настоящее время идет поиск безопасных способов редактирования генома человека и исключения ДНК провируса[32].
Открытие


В 1981 году появились две научные статьи о необычных случаях развития пневмоцистной пневмонии и саркомы Капоши у мужчин-гомосексуалов[35][36]. До этого оба заболевания встречались редко и были характерны для совершенно разных групп пациентов: саркомой Капоши в основном болели пожилые мужчины средиземноморского происхождения, а пневмоцистной пневмонией — пациенты с лейкозом после интенсивной химиотерапии. Появление этих заболеваний, свидетельствующих о тяжелом иммунодефицитном состоянии, у молодых людей, не входящих в соответствующие группы риска, наблюдалось впервые[36]. Затем обнаружили такие же симптомы среди наркопотребителей, больных гемофилией A[37] и гаитян[38][39]. Также было обнаружено, что все пациенты имели очень низкое количество иммунных клеток CD4.[40][41][36]
В июле 1982 года для обозначения этого состояния был предложен термин синдром приобретённого иммунного дефицита (СПИД, AIDS)[42]. В сентябре 1982 года дано полноценное определение СПИДу на основании наблюдения ряда оппортунистических инфекций у четырёх групп пациентов, указанных выше[43][36].
В период с 1981 по 1984 год вышло несколько работ, связывающих опасность развития СПИДа с анальным сексом или с влиянием наркотиков[44][45][46][47][48][49]. Параллельно велись работы над гипотезой о возможной инфекционной природе СПИДа.
Вирус иммунодефицита человека независимо открыли в 1983 году в двух лабораториях: Институте Пастера во Франции под руководством Люка Монтанье и Национальном институте рака в США под руководством Роберта Галло. Результаты исследований, в которых из тканей пациентов впервые удалось выделить новый ретровирус, были опубликованы 20 мая 1983 года в журнале Science[50][51]. В этих статьях исследователи сообщили об обнаружении нового вируса (который первоначально отнесли к группе HTLV вирусов) и выдвинули предположение, что выделенные ими вирусы могут вызывать синдром приобретенного иммуного дефицита[36].
4 мая 1984 исследователи сообщили о выделении вируса, носившего на тот момент название HTLV-III, из лимфоцитов 26 из 72 обследованных больных в стадии СПИДа и 18 из 21 больных в стадии пре-СПИДа. Ни у кого из 115 здоровых гетеросексуальных индивидов контрольной группы вирус обнаружить не удалось. Исследователи отметили, что малый процент выделения вируса из крови больных вызван малым количеством Т4 лимфоцитов, в которых размножается вирус[52]. Также исследователи сообщили об обнаружении антител к вирусу[53], об идентификации ранее описанных у других вирусов и прежде неизвестных антигенов HTLV-III[54] о наблюдении размножения вируса в популяции лимфоцитов[55][36].
В 1986 было обнаружено, что вирусы, открытые в 1983 французскими и американскими исследователями, генетически идентичны. Первоначальные названия вирусов были упразднены и предложено одно общее название — вирус иммунодефицита человека[56]. В 2008 году Люк Монтанье и Франсуаза Барр-Синусси были удостоены Нобелевской премии в области физиологии и медицины «за открытие вируса иммунодефицита человека»[57].
Происхождение

HIV — вирус иммунодефицита человека
SIV — вирус иммунодефицита обезьян
Методом молекулярной филогении показано, что вирус иммунодефицита человека образовался в конце девятнадцатого или в начале двадцатого века[58][59][60][61][62].
Оба типа вируса иммунодефицита человека ВИЧ-1 и ВИЧ-2 возникли в Западной и Центральной Африке южнее Сахары и передались от обезьян к людям в результате зоонозиса. ВИЧ-1 возник на юге Камеруна через эволюцию эндемичного для этой местности вируса иммунодефицита обезьян SIV-cpz, который заражает диких шимпанзе подвида Pan troglodytes troglodytes[63][64]. ВИЧ-1, как полагают, перепрыгнул видовой барьер по крайней мере трижды и породил три группы вирусов: M, N и О[65].
ВИЧ-2 возник на территории Западной Африки (от южного Сенегала до запада Берега Слоновой Кости) через эволюцию вируса иммунодефицита обезьян SIV-smm, который заражает тёмно-коричневых мангобеев (Cercocebus atys) и узконосых обезьян[66]. Однако некоторые широконосые обезьяны, такие как ночные обезьяны являются устойчивыми к ВИЧ-1, возможно, из-за геномного слияния двух вирусных генов устойчивости[67].
Существует доказательство того, что те люди, которые участвуют в промыслах в качестве охотников на диких животных или поставщиков мяса в западной и центральной Африке, обычно приобретают вирус иммунодефицита обезьян[68]. Однако, вирус иммунодефицита обезьян — слабый вирус, он, как правило, подавляется иммунной системой человека в течение недели после заражения. Считается, что необходимо несколько передач вируса от человека к человеку в быстрой последовательности, чтобы вирусу хватило времени мутировать в ВИЧ[69]. Кроме того, благодаря относительно низкой скорости передачи от человека к человеку, вирус иммунодефицита обезьян может распространяться среди населения только в присутствии одного или более рискованных каналов передачи, которые, как полагают, отсутствовали в Африке до XX века. Предполагаемые высокорискованные каналы передачи, которые позволили вирусу приспособиться к людям и распространиться по всему обществу, зависят от предполагаемых сроков перехода от животного к человеку. Генетические исследования показывают, что последний общий предок ВИЧ-1 группы М датируется около 1910 года[70]. Сторонники этой даты связывают ВИЧ с появлением колониализма и роста больших колониальных африканских городов, что привело к социальным изменениям, включая более высокую степень беспорядочности половых отношений, распространение проституции и сопутствующее появление с высокой частотой язв половых органов (например, в результате сифилиса)[71]. Существует доказательство того, что скорость передачи ВИЧ во время вагинального полового акта, достаточно низкая при обычных условиях, может быть увеличена в десятки, если не в сотни раз, в том случае, если один из партнёров страдает от ЗППП в присутствии половых язв. О степени распространённости таких заболеваний в колониальных городах в начале 1900-х можно судить по следующим цифрам: в 1928 году по меньшей мере 45 % жительниц восточного Леопольдвиля (ныне — Киншаса) были проститутками, а в 1933 году около 15 % всех жителей этого же города были заражены одной из форм сифилиса[71].
Альтернативная точка зрения гласит, что небезопасная медицинская практика в Африке в годы после Второй мировой войны, такая как использование нестерильных многоразовых шприцов при массовых вакцинациях, инъекциях антибиотиков и противомалярийных средств, была началом, которое позволило вирусу приспосабливаться к людям и распространяться[69][72][73].
В результате ретроанализа образцов крови взятых после Второй мировой войны зафиксирован самый ранний документальный случай наличия ВИЧ в организме человека, кровь у которого взяли в 1959 году[74]. Вирус, возможно, присутствовал в Соединённых Штатах уже в 1966 году[75], но подавляющее большинство случаев заражения ВИЧ, идентифицированных за пределами тропической Африки, можно проследить до одного неустановленного человека, который заразился ВИЧ на Гаити, а затем перенес инфекцию в США около 1969 года[76].
Классификация
Вирус иммунодефицита человека относят к семейству ретровирусов (Retroviridae), роду лентивирусов (Lentivirus). Название Lentivirus происходит от латинского слова lente — медленный. Такое название отражает одну из особенностей вирусов этой группы, а именно — медленную и неодинаковую скорость развития инфекционного процесса в макроорганизме. Для лентивирусов также характерен длительный инкубационный период.[77]
Для вируса иммунодефицита человека характерна высокая частота генетических изменений, возникающих в процессе самовоспроизведения. Частота возникновения ошибок у ВИЧ составляет 10−3 — 10−4 ошибок / (геном * цикл репликации), что на несколько порядков больше аналогичной величины у эукариот. Длина генома ВИЧ составляет примерно 104 нуклеотидов. Из этого следует, что практически каждый вирус хотя бы на один нуклеотид отличается от своего предшественника. В природе ВИЧ существует в виде множества квази-видов, являясь при этом одной таксономической единицей[78][79][80]. В процессе исследования ВИЧ всё-таки были обнаружены разновидности, которые значительно отличались друг от друга по нескольким признакам, в частности различной структурой генома. Разновидности ВИЧ обозначаются арабскими цифрами. На сегодняшний день известны ВИЧ-1, ВИЧ-2, ВИЧ-3, ВИЧ-4.
- ВИЧ-1 — первый представитель группы, открытый в 1983 году. Является наиболее распространённой формой[81].
- ВИЧ-2 — другой вид вируса иммунодефицита человека, идентифицированный в 1986 году[82], генетически он очень близок к T-лимфотропному вирусу SIVsmm мангабеев, и в меньшей степени (около 60 %) к вирусу ВИЧ-1. Известно, что ВИЧ-2 менее патогенен и передается с меньшей вероятностью, чем ВИЧ-1. Отмечено, что люди, инфицированные ВИЧ-2, обладают также слабым иммунитетом и к ВИЧ-1.
- ВИЧ-3 — редкая разновидность, об открытии которой было сообщено в 1988 году[83]. Обнаруженный вирус не реагировал с антителами других известных групп, а также обладал значительными отличиями в структуре генома. Более распространённое наименование для этой разновидности — ВИЧ-1 подтип O[81].
- ВИЧ-4 — редкая разновидность вируса, обнаруженная в 1986 году[84].
Глобальная эпидемия ВИЧ-инфекции главным образом обусловлена распространением ВИЧ-1. ВИЧ-2 распространён преимущественно в Западной Африке, а также Анголе, Мозамбик, Бразилии и Индии. Редко встречается в Европе и США.[85][86] ВИЧ-3 и ВИЧ-4 не играют заметной роли в распространении эпидемии.
В подавляющем большинстве случаев, если не оговорено иначе, под ВИЧ подразумевается ВИЧ-1[87].
Родственные вирусы
К роду Lentivirus относят следующие виды:[88][89][5]
| Сокр. | Английское название | Русское название |
|---|---|---|
| EIAV | Equine infectious anemia virus | Вирус инфекционной анемии лошадей |
| OOP | Ovine Progressive Pneumonia | Вирус меди-висна овец |
| CAEV | Caprine-ovine arthritis-encephalitis virus | Вирус артрита-энцефалита коз и овец |
| BIV | Bovine immunodeficiency virus | Вирус иммунодефицита крупного рогатого скота |
| FIV | Feline immunodefitiency virus | Вирус иммунодефицита кошек |
| PLV | Puma lentivirus | Лентивирус пум |
| SIV | Simian immunedeficiency virus | Вирус иммунодефицита обезьян. Известно несколько штаммов этого вируса. Каждый штамм характерен для одного вида приматов: SIV-agm, SIV-cpz, SIV-mnd, SIV-mne, SIV-mac, SIV-sm, SIV-stm |
| HIV-1 | Human immunodeficiency virus-1 | Вирус иммунодефицита человека |
| HIV-2 | Human immunodeficiency virus-2 | Вирус иммунодефицита человека-2 |
Наиболее хорошо изученным является ВИЧ.
Строение вириона

Вирионы ВИЧ имеют вид сферических частиц, диаметр которых составляет около 100—120 нанометров. Это приблизительно в 60 раз меньше диаметра эритроцита.
В состав зрелых вирионов входит несколько тысяч белковых молекул различных типов. Капсид зрелого вириона, покрытый белком р24, имеет форму усечённого конуса. Иногда встречаются «многоядерные» вирионы, содержащие два или более нуклеоидов.
Внутри капсида находится белково-нуклеиновый комплекс: две нити вирусной РНК, вирусные ферменты (обратная транскриптаза, протеаза, интеграза) и белок p7. С капсидом также ассоциированы белки Nef и Vif (7-20 молекул Vif на вирион). Внутри вириона (и, вероятнее всего, за пределами капсида) обнаружен белок Vpr[7]:8-11. Сам капсид образован ~2,000 копиями вирусного белка p24. Стехиометрическое соотношение p24:gp120 в вирионе составляет 60-100:1, а p24:Pol примерно 10-20:1[7]:11. Кроме того, с капсидом ВИЧ-1 (но не ВИЧ-2) связываются ~200 копий клеточного циклофилина А[англ.], который вирус заимствует у заражённой клетки[90].
Капсид окружен оболочкой, образованной ~2,000 копий матриксного белка p17. Матриксная оболочка в свою очередь окружена двуслойной липидной мембраной, являющейся наружной оболочкой вируса. Она образована молекулами, захваченными вирусом во время его отпочковывания из клетки, в которой он сформировался. В липидную мембрану встроены 72 гликопротеиновых комплекса, каждый из которых образован тремя молекулами трансмембранного гликопротеина (gp41 или TM), служащими «якорем» комплекса, и тремя молекулами поверхностного гликопротеина (gp120 или SU)[90]. С помощью белка gp120 вирус присоединяется к рецептору CD4 и корецептору, находящихся на поверхности Т-лимфоцитов человека. Белки gp41 и в особенности gp120 интенсивно изучаются как мишени для разработки лекарств и вакцины против ВИЧ. В липидной мембране вируса также находятся мембранные белки клеток, в том числе человеческие лейкоцитарные антигены (HLA) классов I, II и молекулы адгезии[91].
Функции важных структурных белков ВИЧ-1
| Сокращение | Описание | Функции |
|---|---|---|
| gp41 (TM, transmembrane) | Трансмембранный гликопротеин массой 41 кДа | Располагается во внешнем слое липидной мембраны, играет роль «якоря», удерживающего молекулы белка gp120 |
| gp120 (SU, surface) | Гликопротеин массой 120 кДа | Наружный белок вириона. Нековалентно связан с трансмембранным белком gp41. С одной молекулой gp41 связаны 3 — 5 молекул gp120. Способен связывать рецептор CD4. Играет важную роль в процессе проникновения вируса в клетку. |
| p24 (CA, capsid) | Белок массой 24 кДа | Образует капсид вируса |
| p17 (MA, matrix) | Матриксный белок массой 17 кДа | Около двух тысяч молекул этого белка образуют слой толщиной 5 — 7 нм, располагающийся между внешней оболочкой и капсидом вируса. |
| p7 (NC, nucleocapsid) | Нуклеокапсидный белок массой 7 кДа | Входит в состав капсида вируса. Образует комплекс с вирусной РНК. |
Геном и кодируемые белки
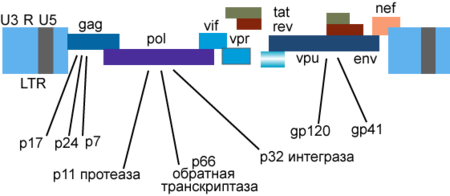
Генетический материал ВИЧ представлен двумя не связанными нитями положительно-смысловой (+)РНК[90]. Геном ВИЧ-1 имеет длину 9,000 нуклеотидов. Концы генома представлены длинными концевыми повторами (LTR), которые управляют продукцией новых вирусов и могут активироваться и белками вируса, и белками инфицированной клетки.
9 генов ВИЧ-1 кодируют, по крайней мере, 15 белков[93]. Ген pol — кодирует ферменты: обратную транскриптазу (RT), интегразу (IN) и протеазу (PR). Ген gag — кодирует полипротеин Gag/p55, расщепляемый вирусной протеазой (PR) до структурных белков p6, p7, p17, p24. Ген env — кодирует белок gp160, расщепляемый клеточной эндопротеазой фурином на структурные белки gp41 и gp120[7]:8-12. Другие шесть генов — tat, rev, nef, vif, vpr, vpu (vpx у ВИЧ-2) — кодируют белки, отвечающие за способность ВИЧ-1 инфицировать клетки и производить новые копии вируса. Репликация ВИЧ-1 in vitro возможна без генов nef, vif, vpr, vpu, однако данные белки необходимы для полноценной инфекции in vivo[94][95][96].
Gag
Полипротеин-предшественник Gag/p55 синтезируется с полноразмерной геномной РНК (которая в данном случае служит в качестве мРНК) в процессе стандартной кэп-зависимой трансляции, но синтез возможен и с помощью IRES, расположенного в 5'-нетранслируемой области мРНК. Локализация отдельных белков Gag, на которые расщепляется Gag/p55, следующая: p17…p24…p2…p7…p1…p6[7]:8. (р1 и р2 — соединительные пептиды; другие продукты расщепления Gag/p55 описаны выше.) Нерасщеплённый протеазой Gag/p55 содержит три основных домена: домен мембранной локализации (М, membrane targeting), домен взаимодействия (I, interaction) и «поздний» домен (L, late). Домен М, расположенный внутри области p17/МА, миристилируется и направляет Gag/p55 к плазматической мембране. Домен I, находящийся внутри области p7/NC, отвечает за межмолекулярные взаимодействия отдельных мономеров Gag/p55. Домен L, также локализованный в области p7/NC, опосредует отпочковывание (budding) дочерних вирионов от плазматической мембраны; в этом процессе участвует также р6 область полипротеина Gag/p55[7]:8.
Vpu
Двумя важными функциями белка Vpu являются: 1) деградация (разрушение) клеточного рецептора CD4 в эндоплазматическом ретикулуме путём привлечения убиквитин-лигазных комплексов, и 2) стимуляция выделения дочерних вирионов из клетки, путём инактивации интерферон-индуцируемого трансмембранного белка CD317/BST-2, получившего также название «tetherin» за его способность подавлять выделение вновь образовавшихся дочерних вирионов посредством их удержания на поверхности клетки[94][95][97][98][99][100].
Vpr
Белок Vpr необходим для репликации вируса в непролиферирующих клетках, в том числе макрофагах. Этот белок наряду с другими клеточными и вирусными промоторами активирует длинные концевые повторы генома ВИЧ. Белок Vpr играет важную роль в переносе провируса в ядро и вызывает задержку пролиферации клетки в периоде G2[101].
Vif
Белок Vif играет важную роль в поддержке репликации вируса. Штаммы, лишённые этого белка, не реплицируются в CD4±лимфоцитах, некоторых линиях T-лимфоцитов («недоступных клетках») и макрофагах. Эти штаммы способны проникать в клетки-мишени и начинать обратную транскрипцию, однако синтез провирусной ДНК остаётся незавершенным[101].
Nef
Белок Nef выполняет несколько функций. Он подавляет экспрессию молекул CD4 и HLA классов I и II на поверхности инфицированных клеток, и тем самым позволяет вирусу ускользать от атаки цитотоксических T-лимфоцитов CD8 и от распознавания лимфоцитами CD4. Белок Nef может также угнетать активацию T-лимфоцитов, связывая различные белки — компоненты систем внутриклеточной передачи сигнала[101].
У инфицированных вирусом иммунодефицита обезьян макак-резус активная репликация вируса и прогрессирование болезни возможны только при интактном гене nef. Делеции гена nef были обнаружены в штаммах ВИЧ, выделенных у группы австралийцев с длительным непрогрессирующим течением инфекции[102]. Однако у части из них со временем появились признаки прогрессирования инфекции, в том числе снижение числа лимфоцитов CD4. Таким образом, хотя делеции гена nef и могут замедлять репликацию вируса, гарантией от того, что заражение ВИЧ-инфекцией не произойдет, они не являются.
Tat и Rev
Регуляторные белки Tat и Rev накапливаются в ядре и связываются с определёнными участками вирусной РНК: первый с трансактивируемым регуляторным элементом (TAR) в области длинных концевых повторов, второй — с Rev-чувствительным регуляторным элементом (RRE) в области гена env. Белок Tat активирует транскрипцию промоторной области длинных концевых повторов и необходим для репликации вируса почти во всех культурах клеток. Белок Tat нуждается в клеточном кофакторе — циклине T1. Белки Tat и Rev стимулируют транскрипцию провирусной ДНК в РНК, элонгацию РНК и транспорт РНК из ядра в цитоплазму и необходимы для трансляции. Белок Rev обеспечивает также транспорт компонентов вируса из ядра и переключение синтеза регуляторных белков на синтез структурных[101].
Устойчивость к ВИЧ
Описаны случаи устойчивости людей к ВИЧ: проникновение вируса в иммунную клетку связано с его взаимодействием с поверхностным рецептором: белком CCR5, делеция (утеря участка гена) CCR5-дельта32 приводит к невосприимчивости её носителя к ВИЧ. Предполагается, что эта мутация возникла примерно две с половиной тысячи лет назад и со временем распространилась в Европе. Сейчас к ВИЧ фактически устойчив в среднем 1 % жителей Европы, 10-15 % европейцев имеют частичную сопротивляемость к ВИЧ [1]. Учёные Ливерпульского университета объясняют такую неравномерность тем, что мутация CCR5 усиливает сопротивляемость к бубонной чуме. Поэтому после эпидемий «чёрной смерти» 1347 года (а в Скандинавии ещё и 1711 года) доля этого генотипа выросла. Мутация в гене CCR2 также уменьшает шанс проникновения ВИЧ в клетку и приводит к задержке развития СПИД. Существует небольшой процент людей (около 10 % всех ВИЧ-положительных), в крови которых присутствует вирус, однако СПИД у них не развивается в течение долгого времени. Их называют нонпрогрессорами.
Обнаружено, что одним из главных элементов антивирусной защиты человека и других приматов является белок TRIM5a, способный распознавать капсид вирусных частиц и препятствовать размножению вируса в клетке. Данный белок у человека и других приматов имеет различия, которые обуславливают врожденную устойчивость шимпанзе к ВИЧ и родственным ему вирусам, а у человека — врожденную устойчивость к вирусу PtERV1[103].
Другой важный элемент антивирусной защиты — интерферон-индуцируемый трансмембранный белок CD317/BST-2 (bone marrow stromal antigen 2), получивший также название «tetherin» за его способность подавлять выделение вновь образовавшихся дочерних вирионов посредством их удержания на поверхности клетки[97][98][104]. CD317 — трансмембранный белок 2го типа с необычной топологией — трансмембранный домен рядом с N-концом и гликозилфосфатидилинозитол (GPI) на С-конце; между ними расположен внеклеточный домен[105]. Показано, что CD317 непосредственно взаимодействует со зрелыми дочерними вирионами, «привязывая» их к поверхности клетки[106]. Для объяснения механизма такого «привязывания» предложено четыре альтернативных модели, согласно которым две молекулы CD317 формируют параллельный гомодимер; один или два гомодимера связываются одновременно с одним вирионом и клеточной мембраной. При этом с мембраной вириона взаимодействуют либо оба мембранных «якоря» (трансмембранный домен и GPI) одной из молекул CD317, либо один из них[106]. Спектр активности CD317 включает, по крайней мере, четыре семейства вирусов: ретровирусы, филовирусы, аренавирусы и герпесвирусы[104]. Активность данного клеточного фактора ингибируется белками Vpu ВИЧ-1, Env ВИЧ-2 и SIV, Nef SIV, гликопротеином оболочки вируса Эбола и белком К5 герпесвируса саркомы Капоши[94][95][99][100][104][107][108][109]. Обнаружен кофактор белка CD317 — клеточный белок ВСА2 (Breast cancer-associated gene 2; Rabring7, ZNF364, RNF115) — Е3 убиквитин-лигаза класса RING. BCA2 усиливает интернализацию вирионов ВИЧ-1, «привязанных» белком CD317 к клеточной поверхности, в CD63+ внутриклеточные везикулы с их последующим разрушением в лизосомах[110].
Примечания
- ↑ James E. Rickman Human genes may predict AIDS progression rate // Los Alamos National Laboratory News Bulletin — Monday, July 14, 2003.
- ↑ Таксономия вирусов (англ.) на сайте Международного комитета по таксономии вирусов (ICTV).
- ↑ Weiss RA (May 1993). "How does HIV cause AIDS?". Science. 260 (5112): 1273—9. Bibcode:1993Sci...260.1273W. doi:10.1126/science.8493571. PMID 8493571.
- ↑ Douek DC, Roederer M, Koup RA (2009). "Emerging Concepts in the Immunopathogenesis of AIDS". Annu. Rev. Med. 60: 471—84. doi:10.1146/annurev.med.60.041807.123549. PMC 2716400. PMID 18947296.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ 1 2 3 NIAID/NIH: The Relationship Between the Human Immunodeficiency Virus and the Acquired Immunodeficiency Syndrome
- ↑ UNAIDS, WHO. 2007 AIDS epidemic update (PDF) 10 (декабрь 2007). Дата обращения: 12 марта 2008.
- ↑ 1 2 3 4 5 6 Levy J.A. HIV and the pathogenesis of AIDS. — USA: American Society for Microbiology, 2007. — ISBN 978-1-55581-393-2
- ↑ Rothenberg RB, Scarlett M, del Rio C, Reznik D, O’Daniels C (1998) «Oral transmission of HIV», AIDS 12:2095-2105
- ↑ Jpnh G Bartlett. [hopkons-hivguide.org Карманный справочник. Лечение ВИЧ-инфекции и СПИДа у взрослых]. — Медицинская школа Университета Джона Хопкинса, 2008. — 138 с.
- ↑ Cooper ER, Charurat M, Mofenson L, Hanson IC, Pitt J, Diaz C, Hayani K, Handelsman E, Smeriglio V, Hoff R, Blattner W; Women and Infants' Transmission Study Group. Combination antiretroviral strategies for the treatment of pregnant HIV-1-infected women and prevention of perinatal HIV-1 transmission.
- ↑ AIDSinfo.nih.gov Recommendations for Use of Antiretroviral Drugs in Pregnant HIV-1-Infected Women for Maternal Health and Interventions to Reduce Perinatal HIV-1 Transmission in the United States October 12, 2006
- ↑ HIV transmission through breastfeeding. A review of available evidence // Всемирная организация здравоохранения, 2007 — ISBN 9789241596596
- ↑ 1 2 CDC HIV Transmission, Разоблачение мифов о передаче ВИЧ бытовым путем, при поцелуях, укусах, через слюну, слезы и др., aids.gov: пути заражения ВИЧ, Слюна инфицированных лиц содержит невирулентные компоненты вируса
- ↑ Cathel Kerr. Bloodsucking fly blamed for transmitting HIV // The Lancet Infectious Diseases, Volume 2, Issue 5, Page 265, May 2002 doi:10.1016/S1473-3099(02)00279-7. Цитата: "Most bloodsucking insects are not capable of transmitting HIV because they inject saliva and ingest blood through different routes. However, S calcitrans might be an exception. "
- ↑ National HIV and STD Testing Resources
- ↑ Just Diagnosed with HIV AIDS : Understand Your Test Results : Viral Load
- ↑ Human Immunodeficiency Virus (HIV) Test
- ↑ Федеральный закон от 22 июля 1993 г. N 5487-1 «Основы законодательства Российской Федерации об охране здоровья граждан»
- ↑ Тест на ВИЧ с точки зрения права, Популярно о СПИД
- ↑ Alimonti JB, Ball TB, Fowke KR (2003). "Mechanisms of CD4+ T lymphocyte cell death in human immunodeficiency virus infection and AIDS". J. Gen. Virol. 84 (7): 1649—1661. doi:10.1099/vir.0.19110-0. PMID 12810858.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ Holmes CB, Losina E, Walensky RP, Yazdanpanah Y, Freedberg KA (2003). "Review of human immunodeficiency virus type 1-related opportunistic infections in sub-Saharan Africa". Clin. Infect. Dis. 36 (5): 656&dash, 662. doi:10.1086/367655. PMID 12594648.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ Guss DA (1994). "The acquired immune deficiency syndrome: an overview for the emergency physician, Part 1". J. Emerg. Med. 12 (3): 375—384. doi:10.1016/0736-4679(94)90281-X. PMID 8040596.
- ↑ Guss DA (1994). "The acquired immune deficiency syndrome: an overview for the emergency physician, Part 2". J. Emerg. Med. 12 (4): 491—497. doi:10.1016/0736-4679(94)90346-8. PMID 7963396.
- ↑ Борьба со СПИДом в России: как остановить болезнь? РИА Новости (30 ноября 2011). Дата обращения: 16 июня 2013. Архивировано 16 июня 2013 года.
- ↑ UNAIDS World AIDS Day Report 2011. UNAIDS World AIDS (2011). Дата обращения: 16 июня 2013. Архивировано 16 июня 2013 года.
- ↑ 1 2 3 UNAIDS: The Joint United Nations Programme on HIV/AIDS
- ↑ Федеральный центр СПИД: Справка ВИЧ-инфекция в Российской Федерации в 2013 г.
- ↑ Emery S, Neuhaus JA, Phillips AN et al. Major clinical outcomes in antiretroviral therapy (ART)-naive participants and in those not receiving ART at baseline in the SMART Study. J Infect Dis 2008; 197: 1133—1144.
- ↑ Katzenstein DA, Hammer SM, Hughes MD et al. The relation of virologic and immunologic markers to clinical outcomes after nucleoside therapy in HIV-infected adults with 200 to 500 CD4 cells per cubic millimeter. N Engl J Med 1996; 335: 1091—1098.
- ↑ Sterne JA, Herna´ n MA, Ledergerber B et al. Long-term effectiveness of potent antiretroviral therapy in preventing AIDS and death: a prospective cohort study. Lancet 2005; 366: 378—384.
- ↑ ВОЗ отзывает ставудин из-за побочных эффектов. Современный Портал о ВИЧ - актуальная информация из мира науки и медицины (1 декабря 2009). Дата обращения: 19 июня 2013. Архивировано 20 июня 2013 года.
- ↑ Антиретровирусная терапия online. Генетический ластик для ВИЧ
- ↑ Department of Health and Human Services. Centers for Disease Control and Prevention’s Public Health Image Library (PHIL), image #948.Проверено 27 июля 2012.
- ↑ Public Health Image Library. Scanning electron micrograph of HIV-1 virions budding from a cultured lymphocyte. See PHIL 10000 for a colorized view of this image, and PHIL 14270, for a black and white version, both viewed at a lower magnigication.
- ↑ Centers for Disease Control. Pneumocystis Pneumonia--Los Angeles. Morbidity and Mortality Weekly Report, 1981, v. 30, p. 250. (англ.). Дата обращения: 27 июля 2012.
- ↑ 1 2 3 4 5 6 AVERT History of AIDS Up to 1986
- ↑ "Pneumocystis carinii pneumonia among persons with hemophilia A". MMWR Morb. Mortal. Wkly. Rep. 31 (27): 365—7. July 1982. PMID 6815443.
- ↑ "Opportunistic infections and Kaposi's sarcoma among Haitians in the United States". MMWR Morb. Mortal. Wkly. Rep. 31 (26): 353—4, 360—1. July 1982. PMID 6811853.
- ↑ Cohen J (2006). "HIV/AIDS: Latin America & Caribbean. HAITI: making headway under hellacious circumstances". Science. 313 (5786): 470—3. doi:10.1126/science.313.5786.470b. PMID 16873641.
- ↑ Centers for Disease Control (CDC) (1982). "Persistent, generalized lymphadenopathy among homosexual males". MMWR Morb Mortal Wkly Rep. 31 (19): 249—251. PMID 6808340. Дата обращения: 31 августа 2011.
- ↑ Barré-Sinoussi F, Chermann JC, Rey F, Nugeyre MT, Chamaret S, Gruest J, Dauguet C, Axler-Blin C, Vézinet-Brun F, Rouzioux C, Rozenbaum W, Montagnier L (1983). "Isolation of a T-lymphotropic retrovirus from a patient at risk for acquired immune deficiency syndrome (AIDS)". Science. 220 (4599): 868—871. Bibcode:1983Sci...220..868B. doi:10.1126/science.6189183. PMID 6189183.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ The history of AIDS 1981—1986 (англ.)
- ↑ Centers for Disease Control. Current trends update on acquired immune deficiency syndrome (AIDS) --United States. Morbidity and Mortality Weekly Report, 1982, v. 31, p. 507. (англ.)
- ↑ Gottlieb et al. Pneumocystis carinii pneumonia and mucosal candidiasis in previously healthy homosexual men: evidence of a new acquired cellular immunodeficiency; N. Engl. J. Med. 1981, 305 1425—1431 (англ.)
- ↑ Durack D. T. Opportunistic infections and Kaposi’s sarcoma in homosexual men; N. Engl. J. Med.1981, 305 1465—1467 (англ.)
- ↑ Goedert et al. Amyl nitrite may alter T lymphocytes in homosexual men; Lancet 1982, 1 412—416 (англ.)
- ↑ Jaffe et al. National case-control study of Kaposi’s sarcoma and Pneumocystis carinii pneumonia in homosexual men: Part 1, Epidemiologic results; Ann. Int. Med. 1983, 99 145—151 (англ.)
- ↑ Mathur-Wagh et al. Longitudinal study of persistent generalized lymphadenopathy in homosexual men: Relation to acquired immunodeficiency syndrome; Lancet 1984, 1, 1033—1038 (англ.)
- ↑ Newell et al. Toxicity, immunosupprressive effects, and carcinogenic potential of volatile nitrites: possible relationship to Kaposi’s sarcoma; Pharmacotherapy, 1984, 4, 284—291 (англ.)
- ↑ Barre-Sinoussi F. et al. Isolation of a T-lymphotropic retrovirus from a patient at risk for acquired immune deficiency syndrome (AIDS). Science 1983, v. 220, p. 868. (англ.)
- ↑ Gallo R. et al. Isolation of human T-cell leukemia virus in acquired immune deficiency syndrome (AIDS). Science 1983, v. 220, p. 865. (англ.)
- ↑ Gallo R. et al. Frequent detection and isolation of cytopathic retroviruses (HTLV-III) from patients with AIDS and at risk for AIDS. Science 1984, v. 224, p. 500
- ↑ Sarngadharan M. et al. Antibodies reactive with human T-lymphotropic retroviruses (HTLV-III) in the serum of patients with AIDS. Science, 1984, v. 220, p. 506
- ↑ Schupbach J. et al. Serological analysis of a subgroup of human T-lymphotropic retroviruses (HTLV-III) associated with AIDS. Science, 1984, v. 220, p. 503
- ↑ Popovic M. et al. Detection, isolation, and continuous production of cytopathic retroviruses (HTLV-III) from patients with AIDS and pre-AIDS. Science, 1984, v. 220, p. 497
- ↑ Coffin J. et al. What to call the AIDS virus? Nature, 1986 v. 321, p. 10
- ↑ The Nobel Prize in Physiology or Medicine 2008 Press Release Harald zur Hausen, Françoise Barré-Sinoussi, Luc Montagnier
- ↑ Gao F, Bailes E, Robertson DL; et al. (1999). "Origin of HIV-1 in the Chimpanzee Pan troglodytes troglodytes". Nature. 397 (6718): 436—441. doi:10.1038/17130. PMID 9989410.
{{cite journal}}: Явное указание et al. в:|author=(справка)Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ Worobey M, Gemmel M, Teuwen DE; et al. (2008). "Direct evidence of extensive diversity of HIV-1 in Kinshasa by 1960". Nature. 455 (7213): 661—4. doi:10.1038/nature07390. PMID 18833279. Дата обращения: 31 марта 2009.
{{cite journal}}: Неизвестный параметр|month=игнорируется (справка); Явное указание et al. в:|author=(справка)Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ Salemi, M.; Strimmer, K; Hall, WW; Duffy, M; Delaporte, E; Mboup, S; Peeters, M; Vandamme, AM (2000). "Dating the common ancestor of SIVcpz and HIV-1 group M and the origin of HIV-1 subtypes by using a new method to uncover clock-like molecular evolution". The FASEB Journal. 15 (2): 276—78. doi:10.1096/fj.00-0449fje. PMID 11156935.
{{cite journal}}: Википедия:Обслуживание CS1 (не помеченный открытым DOI) (ссылка) - ↑ Korber, B.; Muldoon, M; Theiler, J; Gao, F; Gupta, R; Lapedes, A; Hahn, BH; Wolinsky, S; Bhattacharya, T (2000). "Timing the Ancestor of the HIV-1 Pandemic Strains". Science. 288 (5472): 1789—96. Bibcode:2000Sci...288.1789K. doi:10.1126/science.288.5472.1789. PMID 10846155.
- ↑ Worobey M, Gemmel M, Teuwen DE; et al. (2008). "Direct evidence of extensive diversity of HIV-1 in Kinshasa by 1960". Nature. 455 (7213): 661—4. Bibcode:2008Natur.455..661W. doi:10.1038/nature07390. PMID 18833279.
{{cite journal}}: Неизвестный параметр|month=игнорируется (справка); Явное указание et al. в:|author=(справка)Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ Gao F, Bailes E, Robertson DL; et al. (1999). "Origin of HIV-1 in the chimpanzee Pan troglodytes troglodytes". Nature. 397 (6718): 436—41. Bibcode:1999Natur.397..436G. doi:10.1038/17130. PMID 9989410.
{{cite journal}}: Неизвестный параметр|month=игнорируется (справка); Явное указание et al. в:|author=(справка)Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ Keele, B. F., van Heuverswyn, F., Li, Y. Y., Bailes, E., Takehisa, J., Santiago, M. L., Bibollet-Ruche, F., Chen, Y., Wain, L. V., Liegois, F., Loul, S., Mpoudi Ngole, E., Bienvenue, Y., Delaporte, E., Brookfield, J. F. Y., Sharp, P. M., Shaw, G. M., Peeters, M., and Hahn, B. H. (28 July 2006). "Chimpanzee Reservoirs of Pandemic and Nonpandemic HIV-1". Science. 313 (5786): 523—6. Bibcode:2006Sci...313..523K. doi:10.1126/science.1126531. PMC 2442710. PMID 16728595.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ Sharp, P. M.; Bailes, E.; Chaudhuri, R. R.; Rodenburg, C. M.; Santiago, M. O.; Hahn, B. H. (2001). "The origins of acquired immune deficiency syndrome viruses: where and when?" (PDF). Philosophical Transactions of the Royal Society B: Biological Sciences. 356 (1410): 867—76. doi:10.1098/rstb.2001.0863. PMC 1088480. PMID 11405934.
- ↑ Reeves, J. D. and Doms, R. W (2002). "Human Immunodeficiency Virus Type 2". J. Gen. Virol. 83 (Pt 6): 1253—1265. doi:10.1099/vir.0.18253-0. PMID 12029140.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ Goodier, J., and Kazazian, H. (2008). "Retrotransposons Revisited: The Restraint and Rehabilitation of Parasites". Cell. 135 (1): 23—35. doi:10.1016/j.cell.2008.09.022. PMID 18854152.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ Kalish ML, Wolfe ND, Ndongmo CD, McNicholl J, Robbins KE; et al. (2005). "Central African hunters exposed to simian immunodeficiency virus". Emerg Infect Dis. 11 (12): 1928—30. PMID 16485481.
{{cite journal}}: Явное указание et al. в:|author=(справка)Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ 1 2 Marx PA, Alcabes PG, Drucker E (2001). "Serial human passage of simian immunodeficiency virus by unsterile injections and the emergence of epidemic human immunodeficiency virus in Africa" (PDF). Philos Trans R Soc Lond B Biol Sci. 356 (1410): 911—20. doi:10.1098/rstb.2001.0867. PMC 1088484. PMID 11405938.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ Worobey, Michael; Gemmel, Marlea; Teuwen, Dirk E.; Haselkorn, Tamara; Kunstman, Kevin; Bunce, Michael; Muyembe, Jean-Jacques; Kabongo, Jean-Marie M.; Kalengayi, Raphaël M. (2008). "Direct evidence of extensive diversity of HIV-1 in Kinshasa by 1960" (PDF). Nature. 455 (7213): 661—4. Bibcode:2008Natur.455..661W. doi:10.1038/nature07390. PMID 18833279.
- ↑ 1 2 Sousa, João Dinis de; Müller, Viktor; Lemey, Philippe; Vandamme, Anne-Mieke; Vandamme, Anne-Mieke (2010). Martin, Darren P. (ed.). "High GUD Incidence in the Early 20th Century Created a Particularly Permissive Time Window for the Origin and Initial Spread of Epidemic HIV Strains". PLoS ONE. 5 (4): e9936. doi:10.1371/journal.pone.0009936. PMC 2848574. PMID 20376191.
{{cite journal}}: Википедия:Обслуживание CS1 (не помеченный открытым DOI) (ссылка) - ↑ Chitnis, Amit; Rawls, Diana; Moore, Jim (2000). "Origin of HIV Type 1 in Colonial French Equatorial Africa?". AIDS Research and Human Retroviruses. 16 (1): 5—8. doi:10.1089/088922200309548. PMID 10628811.
- ↑ Donald G. McNeil, Jr. (September 16, 2010). "Precursor to H.I.V. Was in Monkeys for Millennia". New York Times. Дата обращения: 17 сентября 2010.
Dr. Marx believes that the crucial event was the introduction into Africa of millions of inexpensive, mass-produced syringes in the 1950s. ... suspect that the growth of colonial cities is to blame. Before 1910, no Central African town had more than 10,000 people. But urban migration rose, increasing sexual contacts and leading to red-light districts.
{{cite news}}: Шаблон цитирования имеет пустые неизвестные параметры:|coauthors=(справка) - ↑ Zhu, T., Korber, B. T., Nahmias, A. J., Hooper, E., Sharp, P. M. and Ho, D. D. (1998). "An African HIV-1 Sequence from 1959 and Implications for the Origin of the epidemic". Nature. 391 (6667): 594—7. Bibcode:1998Natur.391..594Z. doi:10.1038/35400. PMID 9468138.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ Kolata, Gina (28 October 1987). "Boy's 1969 Death Suggests AIDS Invaded U.S. Several Times". The New York Times. Дата обращения: 11 февраля 2009.
- ↑ The emergence of HIV/AIDS in the Americas and beyond. Архивировано 28 марта 2012 года.
- ↑ Retroviruses: Molecular Biology, Genomics and Pathogenesis / Kurth, R; Bannert, N. — Caister Academic Press, 2010. — ISBN 978-1-904455-55-4.
- ↑ Robertson DL, Hahn BH, Sharp PM (1995). "Recombination in AIDS viruses". J Mol Evol. 40 (3): 249—59. doi:10.1007/BF00163230. PMID 7723052.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ Rambaut A, Posada D, Crandall KA, Holmes EC (January 2004). "The causes and consequences of HIV evolution". Nature Reviews Genetics. 5 (52—61): 52—61. doi:10.1038/nrg1246. PMID 14708016.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ Perelson AS, Ribeiro RM (October 2008). "Estimating drug efficacy and viral dynamic parameters: HIV and HCV". Stat Med. 27 (23): 4647—57. doi:10.1002/sim.3116. PMID 17960579.
- ↑ 1 2 Джон Бартлетт. Типы и подтипы ВИ // Клинические аспекты ВИЧ-инфекции. — 2009. Архив
- ↑ Clavel, F. et al. Isolation of a new human retrovirus from West African patients with AIDS. Science, 1986, v. 233, p. 343—346.
- ↑ Marx J.L. (1988). "Tracking variation in the AIDS virus family". Science. 241: 659—660.
- ↑ Molbak K., Lauritzen E., Fernandes D. (1986). "Antibodies to HTLV-IV associated with chronic fatal illnes resembling "slim" didease". Lancet. 8517: 1214—1215.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ HIV-2 Infection Surveillance --- United States, 1987--2009 За 12 лет с 1988 по 2010 в США зарегистрированы лишь 242 случая ВИЧ-инфекции
- ↑ Guidelines for the Use of Antiretroviral Agents in HIV-1-Infected Adults and Adolescents Инфекция ВИЧ-2 эндемичка в Западной Африке и имеет лишь ограниченное распространение за пределами этой зоны.
- ↑ HIV Strains: Types, Groups and Subtypes
- ↑ Gelderblom H.R., Ozel M., Pauli G. (1989). "Morphogenesis and morphology of HIV. Structure relations". Arch. Virol. 106: 1—13.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ Virus databases online
- ↑ 1 2 3 Turner B.G. et al. Structural biology of HIV. J. Mol. Biol., 1999 v. 285, p. 1-32.
- ↑ Association of Host Cell Surface Adhesion Receptors and Other Membrane Proteins with HIV and SIV RIMAS J. ORENTAS and JAMES E. K. HILDRETH. AIDS Research and Human Retroviruses. November 1993, 9(11): 1157—1165. doi:10.1089/aid.1993.9.1157.
- ↑ http://www.hiv.lanl.gov/content/sequence/HIV/COMPENDIUM/2008/frontmatter.pdf
- ↑ Fauci A. S. HIV and AIDS: 20 years of science. Nature Medicine, 2003, v. 9, p. 839—843
- ↑ 1 2 3 Guatelli J.C. (2010) «Interactions of Viral protein U (Vpu) with Cellular Factors», Current Topics in Microbiology and Immunology 339, 27-45
- ↑ 1 2 3 Nomaguchi M., Fujita M., Adachi A. (2008) «Role of HIV-1 Vpu protein for virus spread and pathogenesis», Microbes and Infection 10, 960—967
- ↑ Malim M.H., Emerman M. (2008) «HIV-1 accessory proteins — ensuring viral survival in a hostile environment», Cell Host and Microbe 3, 388—398
- ↑ 1 2 Neil S.J., Zang T. and Bieniaz P.D. (2008) «Tetherin inhibits retrovirus release and is antagonized by HIV-1 Vpu», Nature 451, 424—430
- ↑ 1 2 Van Damme N., Goff D., Katsura C., Jorgensen R.L., Mitchell R., Johnon M.C., Stephens E.B. and Guatelli J. (2008) «The interferon-induced protein BST-2 restricts HIV-1 release and is downregulated from the cell surface by the viral Vpu protein», Cel Host and Microbe 3, 245—252
- ↑ 1 2 Dube M, Bego MG, Paquay C, Cohen EA (2010) «Modulation of HIV-1-host interaction: role of the Vpu accessory protein», Retrovirology 7(1):114
- ↑ 1 2 Ruiz A, Guatelli JC, Stephens EB (2010) «The Vpu protein: new concepts in virus release and CD4 down-modulation», Current HIV Research 8, 240—252
- ↑ 1 2 3 4 Votteler, J. and Schubert, U. (2008) Human Immunodeficiency Viruses: Molecular Biology. Encyclopedia of Virology. (3rd ed.) 517—525
- ↑ J Virol. 2000 Nov;74(22):10581-8. Characterization of three nef-defective human immunodeficiency virus type 1 strains associated with long-term nonprogression. Australian Long-Term Nonprogressor Study Group. Rhodes DI1, Ashton L, Solomon A, Carr A, Cooper D, Kaldor J, Deacon N.
- ↑ Kaiser, Shariser (2007). "Restriction of an Extinct Retrovirus by the Human TRIM5α Antiviral Protein". Science. 316 (5832): 1756—1758.
{{cite journal}}: Неизвестный параметр|day=игнорируется (справка); Неизвестный параметр|month=игнорируется (справка) - ↑ 1 2 3 Tokarev A., Skasko M., Fitzpatrick K. and Guatelli J. (2009) «Antiviral activity of the interferon-induced cellular protein BST-2/tetherin», AIDS Research and Human Retroviruses 25, 1197—1210
- ↑ Kupzig S., Korolchuk V., Rolason R., Sugden A., Wilde A. and Banting G. (2003) «Bst2/HM1.24 is a raft-associated apical membrane protein with an unusual topology», Traffic 4, 694—709
- ↑ 1 2 Perez-Caballero D., Zang T., Ebrahimi A., McNatt M.W., Gregory D.A., Johnson M.C. and Bieniasz P.D. (2009) «Tetherin inhibits HIV-1 release by directly tethering virions to cells», Cell 139, 499—511
- ↑ Douglas JL, Gustin JK, Viswanathan K, Mansouri M, Moses AV, Früh K (2010) «The great escape: viral strategies to counter BST-2/tetherin», PLoS Pathogens 6(5): e1000913
- ↑ Kirchhoff F (2010) «Immune evasion and counteraction of restriction factors by HIV-1 and other primate lentiviruses», Cell Host and Microbe 8, 55-67
- ↑ Evans DT, Serra-Moreno R, Singh RK, Guatelli JC (2010) "BST-2/tetherin: a new component of the innate immune response to enveloped viruses ", Trends in Microbiology 18, 388—396
- ↑ Miyakawa K., Ryo A., Murakami T., Ohba K., Yamaoka S., Fukuda M., Guatelli J. and Yamamoto N. (2009) «BCA2/Rabring promotes tetherin-dependent HIV-1 restriction», PLoS Pathogens 5, e10000700
Литература
- Малый В. П. ВИЧ. СПИД. Новейший медицинский справочник. — М.: Эксмо, 2009. — 672 с. — ISBN 978-5-699-31017-3.
- Bushman F.D., Nabel G.J., Swanstrom R. (Editors). HIV: From biology to prevention and treatment. — Cold Spring Harbor, New York, USA: Cold Spring Harbor Laboratory Press, 2012. — 572 с. — ISBN 978-193611340-8.
- Pancino G., Silvestri G., Fowke K. (Editors). Models of protection against HIV/SIV: Avoiding AIDS in humans and monkeys. — UK-USA-Canada: Academic Press, 2012. — 345 с. — ISBN 978-0-12-387715-4.
- Pepin J. The origins of AIDS. — New York, USA: Cambridge University Press, 2011. — 293 с. — ISBN 978-0-52118637-7.
- Prasad V.R., Kalpana G.V. (Editors). HIV protocols. — Humana Press, 2009. — 457 с. — ISBN 978-1-58829-859-1.
- Sax P.E., Cohen C.J., Kuritzkes D.R. (Editors). HIV essentials. — Jones and Bartlett Learning, 2012. — 248 с. — ISBN 978-1-4496-5092-6.
- Spearman P., Freed E.O. (Editors). HIV interactions with host cell proteins. — Springer, 2009. — 204 с. — ISBN 978-3-642-02174-9.
- Weeks B.B., Alcamo I.E. AIDS: The biological basis. — USA - Canada - UK: Jones and Bartlett Publishers, 2010. — 360 с. — ISBN 978-0-7637-6324-4.
Статья является кандидатом в хорошие статьи с 19 июля 2014. |