Манноза
| Манноза | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
(2S,3S,4R,5R)-2,3,4,5,6-пентагидроксигексаналь (D-манноза), (2R,3R,4S,5S)-2,3,4,5,6-пентагидроксигексаналь (L-манноза) |
| Традиционные названия | манноза, манногексоза |
| Хим. формула | C6H12O6 |
| Физические свойства | |
| Состояние | твердое, кристаллическое |
| Молярная масса | 180,1559 ± 0,0074 г/моль |
| Плотность | 1,54 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 132 °C |
| Классификация | |
| Рег. номер CAS | 31103-86-3 |
| PubChem | 18950 |
| ChEBI | 37684 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
В статье не хватает ссылок на источники (см. рекомендации по поиску). |
Манноза — моносахарид с общей формулой C6H12O6 (изомер глюкозы); компонент многих полисахаридов и смешанных биополимеров растительного, животного и бактериального происхождения.
Строение[править | править код]
Манноза является эпимером глюкозы в положении C2 (то есть её пространственная конфигурация такая же, как у глюкозы, за исключением заместителей в положении углерода-2, которые расположены иначе).
Как и все гексозы, манноза находится в нескольких таутомерных формах — линейной и циклической (пиранозной и фуранозной). В растворе из изомеров преобладает α-D-маннопираноза (67 %).
| Изомеры D-маннозы | ||
|---|---|---|
| Линейная форма | Проекция Хеуорса | |
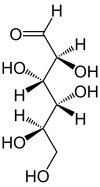 |
 α-D-маннофураноза |
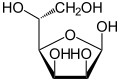 β-D-маннофураноза |
 α-D-маннопираноза |
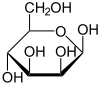 β-D-маннопираноза | |
α-D-маннофураноза — (2R,3S,4S,5R)-5-[(R)-1,2-дигидроксиэтил)]-оксолан-2,3,4-триол
α-L-маннофураноза — (2S,3R,4R,5S)-5-[(S)-1,2-дигидроксиэтил)]-оксолан-2,3,4-триол
β-D-маннофураноза — (2S,3S,4S,5R)-5-[(R)-1,2-дигидроксиэтил)]-оксолан-2,3,4-триол
β-L-маннофураноза — (2R,3R,4R,5S)-5-[(S)-1,2-дигидроксиэтил)]-оксолан-2,3,4-триол
α-D-маннопираноза — (2R,3S,4S,5R,6R)-6-(гидроксиметил)-оксан-2,3,4,5-тетраол
α-L-маннопираноза — (2S,3R,4R,5S,6S)-6-(гидроксиметил)-оксан-2,3,4,5-тетраол
β-D-маннопираноза — (2S,3S,4S,5R,6R)-6-(гидроксиметил)-оксан-2,3,4,5-тетраол
β-L-маннопираноза — (2R,3R,4R,5S,6S)-6-(гидроксиметил)-оксан-2,3,4,5-тетраол
Свойства[править | править код]
Манноза хорошо растворима в воде, имеет сладкий вкус; tпл 132 °C (в природе встречается только D-форма). Манноза относится к восстанавливающим сахарам, так как имеет альдегидную группу, поэтому для неё характерны химические свойства альдогексоз — реакция Толленса, гидрирование с образованием шестиатомного спирта — маннитола. Она дает положительную реакцию с раствором фелинговой жидкости.
Метаболизм[править | править код]
Манноза практически не метаболируется в организме человека[1]. Вследствие этого, манноза не влияет на углеводный обмен и не изменяет его, когда принимается внутрь, и, хотя следы её могут определяться в тканях с помощью радиоактивных маркеров, у человека около 90 % маннозы выводится в неизменном виде с мочой в течение 30-60 минут, а в течение 8 часов выводится 99 % маннозы. За это время уровень глюкозы практически не изменяется.
Применение[править | править код]
В последние годы были опубликованы исследования, в ходе которых было обнаружено, что способность D-маннозы предотвращать адгезию патогенных бактерий (таких как Escherichia coli, Klebsiella, Proteus, Enterococcus, Streptococcus) к уротелию делает эту молекулу очень эффективной против бактериального цистита и предотвращает рецидивы. Она может быть альтернативой или дополнением к антибиотикотерапии[2].
В настоящее время, опубликованные клинические исследования показали, что D-манноза как «биоидентичная» молекула является безопасной, хорошо переносимой, без побочных эффектов и риска передозировки, безопасной для людей с повышенным риском развития диабета и гипертонии.[3] В композиции с натуральным противоспалительным и щелочным веществом, D-манноза ещё более эффективно борется с бактериями в мочевом пузыре, а также с типичной симптоматикой цистита: воспалением, жжением при мочеиспускании, ургентностью, поллакиурией и т. д.[2]
Некоторые исследования показывают, что манноза, возможно, не только защищает организм от развития ожирения, но и обладает противораковыми свойствами, замедляя рост опухоли и усиливая эффективность действия химиотерапии[4].
Содержание в различных препаратах[править | править код]
В России в качестве лекарственного препарата не зарегистрирована.
Встречается в БАДах: Цистэль[5] (550 мг/капс, в суточной дозе — 902 мг D-маннозы, 143 мг экстракта толокнянки, в том числе арбутин 7 мг), Цистэль Пренатал[6](913 мг D-маннозы, 187 мг магния оксид) для беременных и кормящих женщин, Цистифлюкс[7] (саше 8 г, в том числе 500 мг D-маннозы, порошковый концентрат клюквенного сока, фруктоза, ароматизатор ягодная смесь, диоксид кремния)[8], Д-манноза[9] (капсулы массой 668 мг, содержание D-маннозы неизвестно, другие компоненты: листья толокнянки лекарственной, Е470, Е551, желатин)[10]. В других странах доступны такие БАД, как Now Foods D-манноза (500 мг/капс), Vibrant Health D-манноза (5000 мг). Deakos: Ausilium NAC[11] (Суточная доза, 2 флакона, содержит: n-ацетилцистеин — 400 мг, лактоферрин- 200 мг, экстракт Моринды цитрусолисной — 600 мг, d-манноза — 1000 мг); Ausilium 20 plus[12] (водорастворимый порошок, 1 доза содержит: d-манноза — 1000 мг, экстракт Моринды цитрусолисной — 400 мг, бикарбонат калия −195 мг); Ausilium Forte[12] (водорастворимый порошок, 1 доза содержит: d-манноза — 1000 мг, экстракт Моринды цитрусолисной — 400 мг, глицерофосфат кальция, оксид магния — миорелаксант); D-Mannoro[13] (порошок для сублингвального приёма, 1 доза содержит d-маннозу — 1000 мг).
Верхний уровень потребления D-маннозы не установлен, в клинической практике используются дозы до 3000 мг/сут.[14]
Нахождение в природе[править | править код]
Возможно, этот раздел содержит оригинальное исследование. |
В свободном виде обнаружена в плодах многих цитрусовых, анакардиевых и коринокарповых. Манноза имеется в некоторых грибах, например в лисичке обыкновенной (Cantharellus cibarius) и в грибах чайного дерева (золотой гриб) teatree mushroom.
Биохимия маннозы[править | править код]
Возможно, этот раздел содержит оригинальное исследование. |
Превращения маннозы в организме происходят с помощью активированной формы маннозы — гуанозиндифосфатманнозы (ГДФМ), которая служит донором остатка маннозы при биосинтезе маннанов и других биополимеров.
Примечания[править | править код]
- ↑ Direct utilization of mannose for mammalian glycoprotein biosynthesis. Oxford Journals, Life Sciences, Glycobiology, Volume 8, Number 3 Pp. 285—295. doi:10.1093/glycob/8.3.285, PMID 9451038
- ↑ 1 2 Porru D, Parmigiani A, Tinelli C, et al. Oral D-mannose in recurrent urinary tract infections in women: a pilot study (англ.) // Journal of Clinical Urology. : медицинский журнал. — 2014. — Январь (т. 7). — С. 208. — ISSN 3.
- ↑ A. Graziottin, P. P. Zanello. Current Progress in Obstetrics & Gynaecology Volume-x. — 2015.
- ↑ Биологи открыли сахар, убивающий раковые клетки - РИА Новости Архивная копия от 5 февраля 2021 на Wayback Machine
- ↑ Цистэль. www.lsgeotar.ru. Дата обращения: 4 октября 2019. Архивировано 10 июля 2020 года.
- ↑ Цистэль Пренатал. www.lsgeotar.ru. Архивировано 11 июля 2020 года.
- ↑ Цистифлюкс (неопр.) // lsgeotar. Архивировано 19 июня 2019 года.
- ↑ Цистифлюкс сертификат (неопр.) // nevacert.ru. Архивировано 11 июля 2020 года.
- ↑ Д-манноза (неопр.) // lsgeotar. Архивировано 19 июня 2019 года.
- ↑ Д-манноза (неопр.) // nevacert.ru. Архивировано 13 июля 2020 года.
- ↑ Marchiori D, Zanello P.P. Efficacy of N-acetylcysteine, D-mannose and Morinda citrifolia to Treat Recurrent Cystitis in Breast Cancer Survivals (англ.) // In Vivo. — 2017.. — Sep-Oct (№ 31).. — С. С. 931-936.. Архивировано 23 июля 2018 года.
- ↑ 1 2 Palleschi G1, Carbone A, Zanello PP, Mele R, Leto A, Fuschi A, Al Salhi Y, Velotti G, Al Rawashdah S, Coppola G, Maurizi A, Maruccia S, Pastore AL. Prospective study to compare antibiosis versus the association of N-acetylcysteine, D-mannose and Morinda citrifolia fruit extract in preventing urinary tract infections in patients submitted to urodynamic investigation. (англ.) // Arch Ital Urol Androl. — 2017. — 31 Mar ;89(1). — С. 45—50. Архивировано 22 марта 2018 года.
- ↑ Domenici L1, Monti M, Bracchi C, Giorgini M, Colagiovanni V, Muzii L, Benedetti Panici P. D-mannose: a promising support for acute urinary tract infections in women. A pilot study. (англ.) // Eur Rev Med Pharmacol Sci. — 2016. — Июль (т. 20(13):2920-5). Архивировано 4 марта 2020 года.
- ↑ Громова О.А., Торшин И.Ю., Тетруашвили Н.К. Систематический анализ исследований по D-маннозе и перспективы ее применения при рецидивирующих инфекциях мочеполовых путей у женщин репродуктивного возраста. // Акушерство, Гинекология и Репродукция. 2019;13(2):51–53. : журнал. — doi:10.17749/2313-7347.2019.13.2.119-131. Архивировано 19 июня 2019 года.