Борная кислота
| Борная кислота | |||
|---|---|---|---|
 | |||
 Кристаллы борной кислоты Кристаллы борной кислоты Пачка борной кислоты в лекарственной форме из сундука корабельного врача начала XX века, поднятая с затонувшего траулера Пачка борной кислоты в лекарственной форме из сундука корабельного врача начала XX века, поднятая с затонувшего траулера | |||
| Общие | |||
| Систематическое наименование |
Ортоборная кислота | ||
| Хим. формула | H3BO3 | ||
| Рац. формула | B(OH)3 | ||
| Физические свойства | |||
| Состояние | Твёрдое | ||
| Молярная масса | 61,83 г/моль | ||
| Плотность | 1,435 (+15 °C) г/см³ | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 170,9 °C, 444 K, 340 °F | ||
| • кипения | (573 K, 572 °F) 300 °C | ||
| Химические свойства | |||
| Константа диссоциации кислоты | 9,24 (I), 12,74 (II), 13,80 (III) | ||
| Растворимость | |||
| • в воде |
2,52 (0 °C) |
||
| Классификация | |||
| Рег. номер CAS | 10043-35-3 | ||
| PubChem | 7628 | ||
| Рег. номер EINECS | 233-139-2 | ||
| SMILES | |||
| InChI | |||
| Кодекс Алиментариус | E284 | ||
| RTECS | ED4550000 | ||
| ChEBI | 33118 | ||
| ChemSpider | 7346 | ||
| Безопасность | |||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
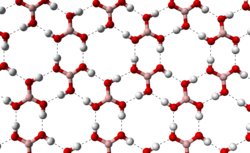
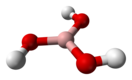
Бо́рная кислота́ (от лат. acidum Boricum, о́ртобо́рная кислота, химическая формула — H3BO3 или B(OH)3) — слабая кислородсодержащая неорганическая кислота, отвечающая высшей степени окисления бора (+3). Бесцветное кристаллическое вещество в виде чешуек, без запаха. Имеет слоистую триклинную решётку, в которой молекулы кислоты соединены водородными связями в плоские слои, слои соединены между собой межмолекулярными связями, длина которых составляет 272 пм.
Впервые была получена немецким химиком Вильгельмом Хомбергом в 1702 году.
История получения
[править | править код]Борная кислота впервые была синтезирована немецким химиком Вильгельмом Хомбергом в 1702 году в результате нагревания минерала буры и железного купороса и последующей многократной очистки полученного летучего вещества сублимацией. Хомберг описал его действие в качестве успокоительного средства и назвал полученное вещество "летучей седативной купоросной солью" (de sel volatile narcotique du vitriol). Название "седативная соль" (ит. sale sedative) надолго закрепилось за данным веществом, состав которого в то время оставался неизвестным[1]:[p. 489] [2] [a]. Антуан Лавуазье[4] и Гитон де Морво[5] ввели для данного соединения термин "борная кислота" (фр. acide borique), отмечая что её остаток, наряду с натрием, входит в состав буры. Состав борной кислоты был установлен в 1808 году вместе с открытием элемента бора независимо в работе Гемфри Дэви[6] и работе Жозефа Луи Гей-Люссака и Луи Жака Тенара[7]. Последние затем в 1811 году получили борную кислоту исходя из бора в результате его реакции горения в кислороде с последующим взаимодействием образующегося оксида бора с водой[8].
Хуберт Франц Хофер обнаружил борную кислоту в составе воды горячих источников Тосканы в 1778 году[9]. В 1799 году Паоло Масканьи открыл минерал сассолин, содержащий борную кислоту[10]. В 1818 году Франсуа де Лардерель открыл первое производство по добыче борной кислоты из природных источников Тосканы[1]:[p. 492].
Нахождение в природе
[править | править код]В природе свободная борная кислота встречается в виде минерала сассолина, в горячих источниках и минеральных водах.
Физические свойства
[править | править код]Борная кислота — это одноосновная кислота Льюиса, часто используемая в качестве инсектицида, антисептика, огнезащитного состава, поглотителя нейтронов или предшественника для получения иных химических составов.
При нагревании ортоборная кислота теряет воду и сначала переходит в метаборную кислоту, затем в тетраборную H2B4O7. При дальнейшем нагревании обезвоживается до борного ангидрида.
Водные растворы борной кислоты являются смесью полиборных кислот общей формулы Н3m-2nВmО3m-n. В природе встречается в виде минерала сассолина.
Расстояние между соседними слоями — 318 пм.
Химические свойства
[править | править код]Борная кислота проявляет очень слабые кислотные свойства. Она сравнительно мало растворима в воде. Её кислотные свойства обусловлены не отщеплением катиона Н+, а присоединением гидроксильного аниона:
- Ka = 5,8⋅10−10 моль/л; pKa = 9,24.
Она легко вытесняется из растворов своих солей большинством других кислот. Соли её, называемые боратами, производятся обычно от различных полиборных кислот, чаще всего — тетраборной Н2В4О7, которая является значительно более сильной кислотой, чем ортоборная.
Очень слабые признаки амфотерности B(OH)3 проявляет, образуя малоустойчивый гидросульфат бора В(HSO4)3.
При нейтрализации ортоборной кислоты щелочами в водных растворах не образуются ортобораты, содержащие ион (ВО3)3−, поскольку ортобораты гидролизуются практически полностью, вследствие слишком малой константы образования [В(ОН)4]−. В растворе образуются тетрабораты, метабораты или соли других полиборных кислот:
- Избытком щелочи они могут быть переведены в метабораты:
Мета- и тетрабораты гидролизуются, но в меньшей степени (реакции, обратные приведённым).
В подкисленных водных растворах боратов устанавливаются следующие равновесия:
При нагревании борная кислота растворяет оксиды металлов, образуя соли:
При избытке оксида образуется метаборат кальция:
При недостатке оксида образуется тетраборат кальция:
Взаимодействует с металлами при нагревании:
Термическое разложение борной кислоты происходит в две стадии при медленном нагревании:
Со спиртами в присутствии концентрированной серной кислоты образует эфиры:
- Кислота в данном случае отыгрывает роль водоотбирающего средства, и дополнительно протонирует ортоборатную кислоту для разрушения связей между бором и кислородом.
Образование борнометилового эфира В(ОСН3)3 является качественной реакцией на Н3ВО3 и соли борных кислот, при поджигании борнометиловый эфир горит красивым ярко-зелёным пламенем.
Получение
[править | править код]Борная кислота может быть получена путём смешения буры (тетрабората натрия) с минеральной кислотой, например, соляной:
Является продуктом гидролиза диборана или тригалогенидов бора[11]:
Борная кислота в медицине
[править | править код]Борный спирт (от лат. Solutio Acidi borici spirituosa) — раствор борной кислоты в этиловом спирте (как правило, в 70 % этаноле).
Спиртовые растворы борной кислоты в концентрации 0,5 %, 1 %, 2 %, 3 %, 5 % готовятся на 70 % этиловом спирте и применяются в качестве антисептика и как противозудное средство при обтирании здоровых участков кожи вокруг очагов пиодермии, а также в качестве ушных капель.
Борная кислота может быть опасна только при бесконтрольном приёме внутрь. Опасная концентрация в организме человека (а особенно ребёнка) может возникнуть при регулярном применении. Смертельная доза при отравлении пероральным приёмом для взрослого человека составляет 15-20 г, для детей — 4-5 г [12].
Борная кислота применяется в медицине с 1860-х годов как антисептическое средство, не раздражающее ран и не имеющее вкуса, запаха и цвета. В современной медицине противомикробная эффективность борной кислоты считается низкой.
Использование борной кислоты в качестве антисептического средства для детей, а также беременных и кормящих женщин было запрещено 2 февраля 1987 года Министерством здравоохранения СССР по рекомендации Фармакологического комитета с формулировкой: «…запретить использование борной кислоты в качестве антисептического средства у детей грудного возраста, а также у женщин в период беременности и лактации в связи с её низкой активностью и высокой токсичностью»[13].
Применение
[править | править код]- В ядерных реакторах в качестве поглотителя нейтронов, растворённого в теплоносителе ядерного реактора.
- Борное удобрение.
- В лабораториях для приготовления буферных растворов.
- В медицине — как самостоятельное дезинфицирующее средство для взрослых, а также в виде 2%-го раствора — для промывки кожи после попадания щелочей.
- На основе борной кислоты производятся различные комбинированные препараты (группа АТХ D08AD), например паста Теймурова.
- В пленочной фотографии — в составе мелкозернистых проявителей и кислых фиксажей для создания слабой кислотной среды.
- В пищевой промышленности зарегистрирована как пищевая добавка E284 (на территории России эта добавка не входит в список разрешённых к применению[14]).
- В ювелирном деле и пр. технике — как компонент флюсов для твердой (высокотемпературной) пайки, например, борная кислота и бура 1:1.
- В литейном производстве — связующее при кислой футеровке печей, компонент защиты струи от окисления при разливке магниевых сплавов.
- В быту — уничтожение тараканов, муравьёв, клопов.
- В производстве керамики, оптоволокна, стекловолокна, стекла[15],
- В качестве антипирена для защиты древесины,
- В составе электролитов для меднения и никелирования.
- Как люминофор или в качестве компонента люминофора для учебных экспериментов по люминесценции веществ.[16][17][18]
Примечания
[править | править код]- ↑ 1 2 Wisniak Jaime. Borax, Boric acid, and Boron ⎯ From exotic to commodity (англ.) // Indian Journal of Chemical Technology : журнал. — 2005. — July (vol. 12). — P. 488—500. — ISSN 0971457X.
- ↑ Homberg Willhelm. Essays de chimie (фр.) // Mémoires de l’Académie Royale des Sciences : журнал. — 1702. — P. 50—52.
- ↑ Artem R. Oganov. Boron under Pressure: Phase Diagram and Novel High-Pressure Phase // NATO Science for Peace and Security Series B: Physics and Biophysics. — Dordrecht: Springer Netherlands, 2010. — С. 207–225. — ISBN 978-90-481-9817-7. — doi:10.1007/978-90-481-9818-4_14.
- ↑ Lavoisier Antoine-Laurent. Traité élémentaire de chimie , présenté dans un ordre nouveau, et d'après les découvertes modernes (фр.). — 1789. — P. 265. — 558 p.
- ↑ Louis-Bernard Guyton de Morveau, Pierre-Auguste Adet, Claude-Louis Berthollet, Antoine Laurent Lavoisier, Jean-Henri Hassenfratz, comte Antoine-François de Fourcroy. Méthode de nomenclature chimique (фр.). — Paris: Académie Royale des Sciences, 1787. — 312 p. Архивировано 6 марта 2023 года.
- ↑ Davy H. Electro-Chemical Researches, on the Decomposition of the Earths; With Observations on the Metals Obtained from the Alkaline Earths, and on the Amalgam Procured from Ammonia (англ.) // Phil. Trans. R. Soc. Lond. : журнал. — 1808. — Vol. 98. — P. 337—370.
- ↑ Gay-Lussac J. L., Thenard L. J. Sur la décomposition et la recomposition de l’acide boracique (фр.) // Ann. Chim. Phys. : журнал. — 1808. — Vol. 68. — P. 169—174.
- ↑ Gay-Lussac J. L., Thenard L. J. Recherches Physico-Chimiques Faites sur la Pile, sur la Préparation Chimique et les Properiétés du Potassium et du Sodium, sur la Décomposition de l'Acide Boracique, sur les Acides fFuorique, Muriatique et Muriatique Oxigéné, sur l'Action Chimique de la Lumière, sur l'Analyse Végétale et Animale, etc. (фр.). — Deterville, Paris, 1811. — Vol. 1. — P. 300. — 402 p.
- ↑ Höefer H. F. Memoria Sopra il Sale Sedative Naturalle dell Toscane e del Borax che con quello si Compone (итал.). — Florence, 1778. — 61 p.
- ↑ Mascagni Paolo. Sopra il Sal Sedativo D'Homebergio o Sia Acido Boracico, Che si Trova ai Lagoni del Volterrano, e del Senese, e Sopra Diversi Borati Che Pur Ivi Si Trovano (итал.) // Memorie di matematica e di fisica della Societ`a italiana delle Scienze : журнал. — 1799. — V. 8, n. 2. — P. 487—515.
- ↑ Housecroft, C. E.; Sharpe, A. G. Chapter 13: The Group 13 Elements // Inorganic Chemistry (англ.). — 3rd. — Pearson, 2008. — P. 340. — ISBN 978-0-13-175553-6.
- ↑ Вредные вещества в промышленности. Справочник для химиков, инженеров и врачей / под ред. проф. Н. Ф. Лазарева. — Л.: Химия, 1977. — Т. 3. — С. 310. — 608 с.
- ↑ Прозоровский В. Коварная борная кислота // Наука и жизнь : журнал. — М., 2003. — Ноябрь (№ 11). — ISSN 0028-1263. Архивировано 14 января 2018 года.
- ↑ СанПиН 2.3.2.1293-03. Дата обращения: 23 декабря 2014. Архивировано 4 марта 2016 года.
- ↑ Применение борной кислоты. Дата обращения: 7 июля 2016. Архивировано 22 июля 2016 года.
- ↑ Исследовательская работа учащихся по химии. Твердофазный синтез люминофоров на основе борной кислоты. Дата обращения: 17 сентября 2019. Архивировано 28 марта 2022 года.
- ↑ Способы исследования люминофоров на базе школьного кабинета физики
- ↑ В. Н. Витер. Люминофоры на основе борной кислоты. Boric acid phosphors. (How to prepare variety luminophores from boric acid and organic compounds) // «Химия и химики» : электронный журнал. — К.: В. Н. Витер, 2017. — № 1. Архивировано 28 сентября 2019 года.
Комментарии
[править | править код]- ↑ В соответствии с современными представлениями речь скорее шла о получении метаборной кислоты HBO2, образующейся при дегидратации ортоборной кислоты H3BO3 при нагревании [3] .
Литература
[править | править код]- Карапетьянц М. Х. Дракин С. И. Общая и неорганическая химия. М.: «Химия», 1994
- Реми Г. «Курс неорганической химии» М.: «Иностранная литература», 1963
- М. Д. Машковский. Лекарственные средства. — М.: ООО «Новая волна», 2002. — Т. 2. — 608 с. — 25 000 экз. — ISBN 5-7864-0129-4.



![{\displaystyle {\mathsf {B(OH)_{3}+H_{2}O\rightarrow H[B(OH)_{4}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/64acca2a47da715749d1c5a357572c40db89e92f)


![{\displaystyle {\mathsf {3H[B(OH)_{4}]\rightleftarrows H^{+}+[B_{3}O_{3}(OH)_{4}]^{-}+5H_{2}O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f133f564e3cc3ee790fcc4bd357d169dd359ea94)
![{\displaystyle {\mathsf {[B_{3}O_{3}(OH)_{4}]^{-}+OH^{-}\rightleftarrows [B_{3}O_{3}(OH)_{5}]^{2-}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/602de5e5f6911e06bb8986fb8cf34a96185c4e61)



![{\displaystyle {\mathsf {H_{3}BO_{3}{\xrightarrow[{}]{107,5^{o}C}}HBO_{2}+\ H_{2}O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/576fbf0b98e49d69ca0d286cc5502592f1e6c392)
![{\displaystyle {\mathsf {2HBO_{2}{\xrightarrow[{}]{150^{o}C}}B_{2}O_{3}+\ H_{2}O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3841155d4f3b212db68d7400f91273e228289e5c)



