Пентадекан
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 3 декабря 2019 года; проверки требуют 3 правки.
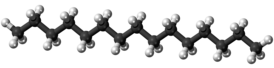
| Пентадекан | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
Пентадекан |
| Хим. формула | C15H32 |
| Рац. формула | CH3-(CH2)13-CH3 |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 212,42 г/моль |
| Плотность | 0,7685 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 9,9 °C |
| • кипения | 270,6 °C |
| • вспышки | 132 °C |
| Удельная теплота плавления | 164 Дж/г [1] |
| Оптические свойства | |
| Показатель преломления | 1,4310 |
| Классификация | |
| Рег. номер CAS | 629-62-9 |
| PubChem | 12391 |
| Рег. номер EINECS | 211-098-1 |
| SMILES | |
| InChI | |
| ChEBI | 28897 |
| ChemSpider | 11885 |
| Безопасность | |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Пентадека́н — ациклический углеводород (алкан) линейного строения, содержащий только одиночные связи. Имеет химическую формулу C15H32 или CH3—(CH2)13—CH3.
История[править | править код]
Пентадекан впервые был получен реакцией восстановления пентадециловой кислоты йодистым водородом и фосфором.
Физические свойства[править | править код]
Пентадекан — бесцветная жидкость. Не растворяется в воде, растворяется в этаноле и эфире.
| Температура кипения при пониженном давлении (°С) | |||||
|---|---|---|---|---|---|
| 1 мм | 10 мм | 40 мм | 100 мм | 400 мм | 760 мм |
| 93 | 136 | 168,7 | 195,0 | 243,4 | 270,6 |
Биологическая роль[править | править код]
Наряду с такими углеводородами, как тридекан и ундекан содержится в феромоне «тревоги» в выделениях муравьёв[2].
Как и тридекан или тетрадекан, участвует в реакции биодеградации. При этом эта реакция может выступать в качестве основного способа выведения алканов из организма[3].
Применение[править | править код]
- Компонент вазелинового масла, вазелина.
- Применяется как органический растворитель (ТУ 6-09-3689-74).
Примечания[править | править код]
- ↑ Доценко С. П., Марцинковский А. В., Данилин В. Н. Теплоаккумулирующие свойства н-парафинов, жирных кислот и многокомпонентных систем на их основе. Архивировано 5 марта 2016 года.
- ↑ Балаян В. Н., Короткий Р. М. Химический язык насекомых. — М.: «Агропромиздат», 1987. — С. 40. — 140 с.
- ↑ Wilkinson S., Nicklin S. and Faul J. L. Biodegradation of fuel oils and lubricants: Soil and water bioremediation options (англ.) // Biotransformations: Bioremediation Technology for Health and Environmental Protection. — 2002. — Т. 36. — С. 88.
Литература[править | править код]
- Справочник химика / Редкол.: Никольский Б. П. и др.. — 2-е изд., испр. — М.—Л.: Химия, 1966. — Т. 1. — 1072 с.
- Справочник химика / Редкол.: Никольский Б. П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Несмеянов А. Н., Несмеянов Н. А. Начала органической химии. В 2-х томах. — 2-е изд., перераб.. — М.: «Химия», 1974. — Т. 1. — 624 с.
- Пентадекан // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
