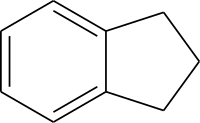
Индан
| Индан | |
|---|---|
 | |
| Общие | |
| Хим. формула | C9H10 |
| Физические свойства | |
| Молярная масса | 118.176 г/моль |
| Плотность | 0.965 г/см³ |
| Энергия ионизации | 8,3 электротранспорт[1] |
| Термические свойства | |
| Температура | |
| • плавления | −51,4 °C |
| • кипения | 176 °C |
| Классификация | |
| Рег. номер CAS | 496-11-7 |
| PubChem | 10326 |
| Рег. номер EINECS | 207-814-7 |
| SMILES | |
| InChI | |
| RTECS | NK3750000 |
| ChEBI | 37911 |
| ChemSpider | 9903 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Индан (2,3-дигидроинден, гидринден) — углеводород промежуточного класса, относящийся как к циклоалканам, так и к аренам.
Физические свойства[править | править код]
Бесцветная маслянистая жидкость, температура плавления — −51 °C, температура кипения 176°С[2]. В воде нерастворим, смешивается с этанолом и диэтиловым эфиром.
Химические свойства[править | править код]
Индан окисляется перманганатом калия в щелочной среде до фталевой кислоты. Дегидрирование при 470-530оC на оксиде хрома приводит к индену. При гидрировании на катализаторе (платина на угле) образует 1-метил-2-этилбензол.
Реагирует с бромом - продуктами реакции бромирования в среде уксусной кислоты являются 4-броминдан и 5-броминдан.
Концентрированной серной кислотой сульфируется с образованием индан-5-сульфокислоты. Хлорсульфоновая кислота превращает индан в смесь индан-4- и индан-5-сульфохлоридов.
Производные[править | править код]
Производные, включая составляющие, такие как 1-метил-индан и 2-метил-индан (где одна метильная группа присоединена к пятичленному углеродному кольцу), 4-метил-индан и 5-метил-индан (где одна метильная группа присоединена к бензольному кольцу), различные диметил-инданы, и различные лекарственные производные. Остальные производные могут быть получены косвенно, то есть реакцией диэтилфталата с этилацетатом, пользуясь металлическим натрием и этанолом как катализатор. В полях реакции этилового эфира индандиона, которая может реагировать с ионами натрия образуя соль. Добавление хлороводородной кислоты может привести к обратной реакции.
Индан может быть преобразован по каталитической реакции в другие ароматические вещества, например ксилол.
Другие производные, это, например 1,3-индандион.
Нахождение в природе[править | править код]
Индан обнаруживается в каменноугольной смоле (0,1%), а также в нафталиновой фракции нефти (0,9%)
Получение[править | править код]
Синтез индана осуществляют гидрированием индена над мелкодисперсным никелем при 200оС.
Применение[править | править код]
Индан является исходным веществом для синтеза 2-, 4- и 5-инданолов, которые используются при получении лекарственных средств.
Литература[править | править код]
- Кнунянц И. Л. и др. т.2 Даффа-Меди // Химическая энциклопедия. — М.: Советская энциклопедия, 1990. — 671 с. — 100 000 экз. — ISBN 5-85270-035-5.
Примечания[править | править код]
- ↑ David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ 45789 Indan OEKANAL®, analytical standard Архивная копия от 26 октября 2008 на Wayback Machine (англ.)
Это заготовка статьи об органическом веществе. Помогите Википедии, дополнив её. |
В другом языковом разделе есть более полная статья Indan (нем.). |