Лантаноиды

Лантано́иды (лантани́ды)[К 1] — семейство, состоящее из 15 химических элементов III группы 6-го периода периодической таблицы — металлов, с атомными номерами 57—71 (от лантана до лютеция)[1][2][3][4][5][6][7][8][9]. Все представители семейства имеют стабильные изотопы, кроме прометия. Название происходит от слова на древнегреческом языке λανθάνειν („скрытый“).
Скандий, иттрий и лантаноиды относятся к группе редкоземельных элементов (сокр. РЗЭ) и часто рассматриваются в этом контексте, однако распространенность отдельных элементов показывает, что редкими они не являются. В научных материалах для обозначения лантаноидов применяют вышеуказанный термин, включая в него иттрий и скандий, или по отдельности.
Запись Ln используется для указания на все или некоторые металлы, ионы, степени окисления, при записи химических формул и пр.
У всех лантаноидов, начиная с церия и заканчивая иттербием, заполняется 4f-подоболочка; у лантана 4f-электронов нет, а у лютеция — 14. Неспаренные 4f-электроны наделяют некоторые металлы различными ценными магнитными, спектроскопическими и люминесцентными свойствами. Более того, поскольку эти электроны хорошо экранированы внешними подоболочками (5s и 5p), спектральные характеристики сохраняются при добавлении лигандов. Все лантаноиды образуют катионы Ln3+ (некоторые ещё и Ln2+, Ln4+), ионный радиус которых постоянно уменьшается при увеличении атомного номера, — этот феномен известен как лантаноидное сжатие (то же самое проявляется у актиноидов)[10]. Непрерывно понижается осно́вность элементов от лантана до лютеция, что обуславливает различие в растворимости солей и в устойчивости их комплексных соединений[11].
Химическая связь с лантаноидами имеет почти всегда ионный характер. Лантаноиды — «тяжелые» акцепторы и имеют значительное сходство по своим свойствам с донором атомов — кислородом, из-за чего наиболее вероятными биологическими лигандами для них являются карбоксильные и фосфатные группы. Координационные числа для них могут быть от 6 до 12 (8—9 преимущественно в биологических системах)[10].
Публикация работы норвежским геохимиком Виктором Гольдшмидтом, в которой впервые был употреблен термин лантаноиды, произошла в 1925 г. (аналогично было дано название актиноидам в 1937 г.)[12][13][14].
| * | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu |
История[править | править код]
Очень много недоразумений, связанных с лантаноидами, в употреблении терминологии. Название «редкая земля» первоначально применялось для описания почти всех неизученных, неизвестных природных оксидов, и вплоть до 1920 г. к ним относили даже ThO2 и ZrO2. Примерно в то же время термин начали использовать для обозначения самих элементов, а также группы элементов, которые с большим трудом можно было отделить друг от друга[15][16].
Изначальное разделение элементов на цериевую («легкие земли»; La—Eu) и иттриевую («тяжелые земли»; Gd—Lu) группы основывалось на различии в растворимости двойных сульфатов, образованных лантаноидами, с сульфатами натрия или калия. В дальнейшем была установлена периодичность изменений свойств в группе, соответствовавшей их разделению на две подгруппы[11].
Термины «редкоземельные металлы» и «щелочноземельные металлы» — до сих пор использующиеся в химии — происходят от существительного слова «земля», бывшего в употреблении у алхимиков, ятрохимиков и ранних флогистонистов в качестве основного указания на огнестойкость, нерастворимость осадков, образованных после горения (окисления) или других глубинных химических взаимодействий в субстанциях. Только после 1750-х гг. химики начали понимать, что кремниевая земля (англ. silica), алюминиевая земля (англ. alumina), тальк, известь — все они являются разными землями, если судить по химическим свойствам. В 1779 г. к ним добавилась бариевая земля (англ. baryta), которую К. В. Шееле выделил из извести. А. Л. Лавуазье все пять земель в 1789 г. включил в свой список из 33 элементов, сделав примечание: они могут являться оксидами металлов с большим похождением на связь с кислородом, чем углеродом. Это и побудило многих химиков в начале XIX века восстанавливать известные земли и искать новые. Среди новых шести земель: циркониевой (1789, М. Клапрот), стронциевой (1790, А. Крофорд), бериллиевой (1798, Л. Н. Воклен) и ториевой (1829, Й. Берцелиус[К 2]) были открыты иттриевая (1794) и цериевая (1803). Открытие последней определило разницу между землями и обычными оксидами металлов, а в 1808 г. после того, как Г. Дэви восстановил электролизом щелочные земли до щелочноземельных металлов — кальция, бария, стронция и магния, — большинству химиков стало понятно, что истинные земли есть не что иное, как оксиды металлов[17].

Лантаноиды образуют самую большую группу элементов периодической системы, находящихся в природе. Их свойства настолько похожи, что с 1794 г., когда Юхан Гадолин выделил оксид иттрия, и вплоть до 1907 г. было сделано почти сто заявлений об открытии элементов[К 3]. Это объясняется тем, что в то время не существовало теста на индивидуальность элемента, а исследователям было непонятно, сколько же должно быть элементов в семействе, так как в периодической системе можно было поместить только один элемент — лантан. К 1913 г. на основании работы Г. Мозли уже стало понятно, что между лантаном и гафнием число элементов как раз равно четырнадцати[15]: при сравнении энергии рентгеновских спектров атомов элементов периодической таблицы и их атомного веса им были обнаружены пробелы, пропуски. Для устранения пропусков учёный счел необходимым расположить элементы в соответствии с химическими свойствами, а не увеличивающимся атомным весом. Его работа показала, что каждый элемент имеет постоянную величину — атомное число, увеличивающееся на постоянную величину от элемента к элементу. В конечном счёте лантаноиды были расположены в отдельном месте ниже основной таблицы. А в 1921 г. Нильсом Бором была предложена структура электронных орбиталей атома, которая объясняла проблему редкоземельных элементов[18]. (Лантаноиды часто называют и включают в понятие редкоземельные элементы, однако, например, лютеций по распространенности в земной коре превосходит серебро[3].)
Некоторое представление об их схожих химических свойствах можно получить из фактов истории изучения. Разделение различных элементов от содержащих их минералов заняло у ученых более ста лет[3][9], и даже вплоть до середины XX века (до развития ионообменной техники разделения) для получения в действительно чистом виде некоторых соединений редких лантаноидов требовалось до 40 000 повторений операции по фракционной перекристаллизации[19]. Например: в 1911 г. выделение чистого бромата тулия Ч. Джеймсом требовало около 15 000 таких операций[20], а за 15 лет Ж. Урбэном и его помощниками проведено суммарно около 20 000[21]. Указанный метод разделения является лишь одним из нескольких классических, и включает в себя некоторые свойства[20]:
- разница в основности позволяла при постепенном добавлении щелочи осадить в первую очередь менее осно́вные гидроксиды тяжелых лантаноидов;
- различия в растворимости таких солей, как оксалаты (например, возможность применения этого метода была обнаружена Карлом Мосандером при поиске способов получения чистых соединений эрбия и тербия[22][23]), двойные сульфаты и двойные нитраты.
Помимо вышеуказанных, существует возможность перевода в другие степени окисления, отличные от +3, например, CeIV, EuII. Указанный способ, применимый в отдельных случаях, позволял получать наиболее чистый продукт[20]. В настоящее время метод перекристаллизации является устаревшим, поскольку реакции ионного обмена и экстракция растворителем по сравнению с ним более быстры и менее трудоемки[24].
До 1840-х[править | править код]
| История открытия[К 4] | |||||
|---|---|---|---|---|---|
| Ат. номер | Элемент | Дата | Первооткрыватель | Происхождение названия | Источник |
| 57 | Лантан | 1839 | К. Мосандер | От греч. «скрываюсь» | [25][К 5] |
| 58 | Церий | 1803 | Й. Берцелиус и В. Хизингер; М. Клапрот |
В честь астероида Церера | [25] |
| 59 | Празеодим | 1885 | К. Ауэр фон Вельсбах | От греч. «зеленый» + «близнецы» | [25][26] |
| 60 | Неодим | 1885 | К. Ауэр фон Вельсбах | От греч. «новый» + «близнецы» | [25][26] |
| 61 | Прометий | 1947 | Дж. Марински, Л. Гленденин и Ч. Кориелл |
В честь Прометея | [25][27][11] |
| 62 | Самарий | 1879 | П. Лекок де Буабодран | По названию минерала самарскита | [25][28][29] |
| 63 | Европий | 1901 | Э. А. Демарсе | От слова Европа | [25][30][31] |
| 64 | Гадолиний | 1880 | Ж. Мариньяк | По названию минерала гадолинита | [25][32] |
| 65 | Тербий | 1843 | К. Мосандер | От названия городка Иттербю | [25][33] |
| 66 | Диспрозий | 1886 | П. Лекок де Буабодран | От греч. «труднодоступный» | [25][34][35] |
| 67 | Гольмий | 1879 | П. Т. Клеве | От старинного лат. Holmia — Стокгольм | [25][36] |
| 68 | Эрбий | 1843 | К. Мосандер | От названия городка Иттербю | [25][33] |
| 69 | Тулий | 1879 | П. Т. Клеве | От лат. Thule — «самая северная земля» | [25][36] |
| 70 | Иттербий | 1878 | Ж. Мариньяк | От названия городка Иттербю | [25][37] |
| 71 | Лютеций | 1907 | Ж. Урбэн; Ч. Джеймс | От лат. Lutetia — Париж | [38][39] |
Изучение и дальнейшая классификация лантаноидов берёт своё начало с конца XVIII века: летом 1787 года шведский офицер К. А. Аррениус в карьере вблизи города Иттербю нашёл неизвестный чёрный минерал, прозванный иттербитом (позднее переименован в гадолинит)[40]. Юхан Гадолин, изучая его в 1794 году, открыл в нём новую землю — оксид иттрия[К 6]. Таким образом, с открытия одного из соединений элемента, имеющего похожие химические свойства, но не входящего в семейство, продолжилось дальнейшее изучение минералов и открытие лантаноидов[41]. Химический анализ гадолинита привел к открытию 7 химических элементов иттриевой группы и ещё семи — цериевой, при изучении церита[42]. (Иттриевая и цериевая земли были двумя началами «путей» открытия элементов-лантаноидов[42].) Примечательно, что открытие множества лантаноидов произошло благодаря минералам из их общего места происхождения: известнейшее месторождение пегматита располагается возле Иттербю в Швеции[43].

Минерал церит, открытый в 1751 году А. Кронштедтом и содержащий редкоземельные элементы, послужил отправной точкой в открытии церия[43]. В 1803 году Вильгельм фон Хизингер и Йёнс Берцелиус в Швеции (и независимо от них Мартин Клапрот во Франции) нашли в минерале новую землю, названную цериевой в честь астероида Цереры[44][45]. После открытия французский химик Луи Воклен впервые исследовал его и показал, что цериевая земля может быть белой и оранжевой. Этот факт впервые указал на существование церия в двух валентных формах. Учёный восстановил землю и пришёл к выводу, что церий является металлом, не похожим на другие известные на тот момент[46]. Впоследствии (с 1839 по 1843 годы) Карл Мосандер доказал, что эта и ранее открытая — иттриевая — земли представляли собой смеси оксидов нескольких лантаноидов[20]. Элемент был выделен В. Хиллебрандом и Т. Нортоном в металлическом виде только в 1875 г[44].

В 1826 году Карл Мосандер — ученик, ассистент и один из близких друзей Й. Берцелиуса — исследовал цериевую землю и сделал заключение о её неоднородности: в ней мог содержаться минимум один новый элемент. Чтобы проверить это предположение, понадобилось много церита[47]. В 1839 году, добиваясь выделения из цериевой земли чистого препарата, учёный обработал её азотной кислотой и кристаллизовал соль, выпаривая воду. Он также установил, что эта соль (будучи загрязнённым нитратом церия[48]) при нагревании разлагается и превращается в желтоватое вещество. Обрабатывая этот жёлтый землистый остаток разведённой азотной кислотой было замечено, что интенсивно закрашенная его часть не растворяется в кислоте: это был диоксид церия, с которым впервые столкнулся Воклен[46][К 7]. После удаления нитрата церия из раствора, ученому удалось добыть новую, лантановую землю[48], название которой было предложено Берцелиусом и дано Мосандером 12 февраля 1839 г[49]. Элемент, являясь родоначальником группы элементов, был открыт вторым после церия лишь как примесь. Возможно, лантан был назван именно так потому, что «скрывался» от ученых на протяжении 36 лет[50]. В относительно чистом виде был получен в 1923 г[51].
В январе 1840 года Мосандеру удалось достичь успеха, выделив из аметистового раствора сульфата лантана две фракции:
- При нагреве раствора соли (тогда уже было известно, что её растворимость выше в холодной воде) с 9 до 40 °C, в осадок выпали кристаллы светло-аметистового цвета: сульфат лантановой земли с примесью оксида дидима[52]. При повторении с этими кристаллами вышеописанных действий 10—15 раз он получил бесцветные кристаллы (где присутствие оксида дидима было минимальным), которые, при реакции с щелочами и выпариванием воды, давали оксид белого цвета, предположительно, — истинный оксид лантана (в записной книжке учёный пометил его как Laa)[53].
- Вторая фракция была получена в растворе серной кислоты и оксида лантана: в результате реакции, осадились красные кристаллы сульфата дидимовой земли[52] (помеченной Lar, где r, предположительно, обозначает «красный», от швед. röd). Эти кристаллы при реакции с щелочами дали голубовато-фиолетовый оксид-гидрат, после выпаривания воды из которого остался оксид: «…Темно-коричневого цвета на поверхности, иногда светло-коричневого в изломах [трещинках]…»[54] При сильном нагревании до белого каления его цвет получался от загрязнённого белого до серо-зелёного, а на поверхности появлялись аметистово-красные кристаллы[55].
С этого момента учёный мог доказать, что аметистовый цвет солей оксидов церия и лантана вызван присутствием оксида Lar, а в коричневый они окрашивались при нагреве в воздухе до красного каления[55]. Карл Мосандер в 1842 году[56] назвал неизвестный оксид Lar — дидим (Di)[55], чтобы показать его связь с уже открытыми лантаном и церием[33][57][52]. После этого учёный убедился в том, что дидим был получен в чистом виде и больше к нему не возвращался[58], а данное им название «элементу» фигурировало в учебниках по химии того времени ещё 50 лет[56].
Задавшись вопросом о гомогенности образцов, из которых был получен иттрий, и вдохновлённый успехами, достигнутыми при исследовании церита, Карл Мосандер начал изучение гадолинита[59]. Осенью 1842 года учёный убедился, что образцы иттриевой земли, изолированные из гадолинита, церита, церина, ортита, — все они имели в своём составе помимо «истинного» оксида иттрия (поскольку давали бесцветные соли), ещё и неизвестный оксид жёлтого цвета, менее осно́вный, в растворах его солей — аметистовый. В феврале 1843 года этой земле было дано название о́диний (в честь бога Одина), однако результаты последующих экспериментов, проведённых в апреле, убедили его в том, что в земле было по меньшей мере три оксида. Из раствора азотной кислоты и оксида иттрия Мосандер, при фракционном осаждении, получил аммонийные осно́вные соли, при сильном нагревании которых получались три различных оксида, не похожих на ранее полученные. (Немногим ранее, в 1842 году Йёнсом Берцелиусом была проведена работа, которая подтверждала разделение иттриевой земли на три оксида, однако к апрелю 1843 года она все ещё оставалась ненапечатанной.) За наиболее осно́вным по характеру оксидом (белого цвета, в его солях — бесцветного) учёный оставил старое название — иттриевая земля, следующий — по убыванию основных свойств — был назван оксидом тербия, в чистом виде, предположительно, — белого цвета (растворы солей — розового[60]), и третий — оксид эрбия: при нагревании на воздухе оксид окрашивался в темный оттенок оранжево-желтого цвета, теряющийся при нагреве в атмосфере водорода (последние данные позволили сделать вывод о его двух валентных состояниях)[23]. Из определённо открытого на тот момент эрбия позднее выделили ещё иттербий и тулий[61].
Активность ученого привела к выводу о том, что семейство расширилось в 1843 году до шести элементов[62][63]: цериевые соединения имеют жёлтый цвет, лантановые — белый, дидимовые — красный, иттриевые и эрбиевые — белый, тербиевые — розовый[К 8]. Для доказательств открытия в то время требовалось получить данные о выделении (получении), цвете, форме кристаллов и способности образовывать соединения элементом[22]. Но даже несмотря на авторитет первооткрывателя, историю открытия тербия не раз брали под сомнение, например: Р. В. Бунзеном и П. Т. Клеве в иттриевой земле были найдены только два оксида[60]. Позднее учеными было повторно подтверждено существование элемента: исследования гадолинита Мариньяком (1878), изоляция элемента из самарскита Л. Смитом (в том же году), сообщение Ж.-Л. Соре об изучении спектров абсорбции элемента (1880), получение Ж. Урбэном чистых препаратов (начало XX века) — все они подтвердили исследования Мосандера[64][60]. Эрбий же был получен в довольно чистом металлическом виде в 1934 г[65].
Д. И. Менделеев придерживался мысли, которую потом подтвердил исследованиями, что редкоземельные элементы трёхвалентны. В итоге, в первой половине XIX века было установлено существование не только великой родины элементов, но и изучены некоторые индивидуальные свойства[66].
1843—1878[править | править код]
В 1848 г. умер Й. Берцелиус — видный учёный-химик, занимавшийся наукой почти 50 лет, — и в следующие 30 лет интерес ученых к органической химии затмил неорганическую: большинство соединений металлов научились получать традиционными методами фракционного осаждения и кристаллизации — стало понятным, что яркий период в истории открытий закончился[67]. Дальнейший прогресс требовал новых концепций и развития в технике изучения[63].

Тем не менее, изучение редкоземельных элементов не остановилось, несмотря на то, что в основном поначалу внимание было приковано к лантану, церию, дидиму. Новой заметной фигурой в изучении стал Жан Шарль Мариньяк, который немногим позднее выделил три новых элемента; им же были более точно определены атомные массы нескольких элементов (церия, лантана и дидима), доработан метод отделения, разработанный Мосандером, позволявший получить более чистые препараты. В 1848 г. вычислил атомный вес церия в реакции сульфата церия(III) с хлоридом бария (позже несколько раз менялся другими исследователями), а через год вычислил веса лантана и дидима. В 1853 г. детально изучил химические свойства дидима: цвет, кристаллы солей, растворимость, методы получения галогенидов, сульфидов, фосфатов, сульфатов, оксалатов, соединений с мышьяком; ещё через два года то же самое произвел с лантаном[68].
Необходимый для дальнейшего развития науки спектральным анализом шаг вперед был сделан Р. Бунзеном и Г. Кирхгофом в 1859 г[63].
Марк Делафонтен в 1864 г. принялся работать с гадолинитом: эрбий и его соединения были детально изучены различными методами, в том числе с применением газовой горелки. Им же были предоставлены довольно ясные доказательства открытия эрбия, но не тербия[69]. И если существование первого было окончательно подтверждено нахождением в солнечном спектре Ч. Янгом в 1872 г.[70], то присутствие в природе последнего отрицалось О. Поппом (отрицал существование и тербия, и эрбия[71]), Й. Баром, Р. Бунзеном, П. Т. Клеве. Результаты нескольких дальнейших исследований вплоть до начала 1880-х гг. приводили ко всё большей путанице: существование тербия то подтверждалось, то отрицалось, Делафонтен сообщал об открытии ещё нескольких «элементов» (мосандрия, филипия, деципия) и т. п.[К 9][69]

Понимание того, что элементы можно организовать в логический ряд, погруппно, как предполагалось периодической таблицей Д. И. Менделеева с 1869 г. пришло не сразу[63]. Она же позволяла увидеть направление для дальнейших открытий, дать «карту» в руки ученых, понимание чего заняло долгое время[72]. Так, например, примечание Делафонтена о том, что дидим не является гомогенным, было подтверждено Лекоком де Буабодраном в 1875 г. параллельным изучением спектров галлия (экаалюминия) — первого «эка»-элемента, предсказанного таблицей Д. И. Менделеева, отражавшей реальность существования элемента и имевшей под собой более сложное объяснение положения элементов[73]. Немногим ранее, в 1870 г. Д. И. Менделеев сам предсказал существование экабора (скандия)[74], спектры которого были обнаружены Л. Нильсоном в 1879 г., а годом позже — им же выделен оксид скандия с примесью иттербия из оксенита[75].
Открытие скандия ещё до обнаружения в природе значительно помогло в дальнейшем становлении и утверждении периодической системы химических элементов[75]. Более того, различные варианты положения элементов в таблице предоставлялись исследователями в попытке разрешить задачу положения редкоземельных элементов[76], поскольку существовал недостаток знаний в теории; в то время как большинство элементов хорошо подходило для определённых ячеек (мест) таблицы, редкоземельные металлы с их очень похожими свойствами все ещё оставались в неопределённом положении, служившим источником вдохновения для исследователей[77].
После 1870-х[править | править код]
Исследования Карла Густава Мосандера (1797—1858) побудили многих химиков исследовать минералы, содержащие церий и иттрий. Однако прогресс протекал медленно до тех пор, пока ученые в конце 1870-х гг. не научились изучать химические свойства с помощью спектроскопии (помимо совершенствования техники отделения). В последующие года прогресс в изучении и открытии элементов проходил намного быстрее[66][78]. Благодаря анализам спектров были открыты (или подтверждено существование) некоторые из представителей: тербий, иттербий, гольмий, тулий и самарий. С другой стороны, применение более чувствительной техники приводило и к ошибочным выводам: даже малое количество примеси в изучаемом препарате могло сильно изменить записанный спектр[79].
Жан Мариньяк достиг успеха, изолировав иттербиевую землю от иттриевой 22 октября 1878 г.[80] следующим образом: из смеси тербия с иттрием исследователь выделил эрбиевый осадок и сделал вывод о его неоднородности на основании того, что оксид неизвестного элемента (иттербия) был, как и его соли, бесцветным, в отличие от оксида эрбия[73]; тогда же исследователь сделал заключение о 3-валентном состоянии элемента и вычислил атомный вес — 172[81][К 10]. Эту землю проверил Л. Нильсон и другие ученые, почти полностью убедившиеся в чистоте, однако некоторыми считалось, что в ней присутствовали примеси. Среди последних оказались Ж. Урбэн во Франции и К. Ауэр фон Вельсбах в Австрии (позднее оба независимо друг от друга открыли лютеций, в 1907 и 1908 гг. соответственно), к такому же выводу пришли: У. Крукс (анонсировал открытие нескольких элементов), спектроскописты Ф. Экснер и Э. Гашек (1899), а Э. А. Демарсе, изучая спектры, в 1900 г. обнаружил элемент «Θ» и сделал примечание о его вхождении в состав земли Мариньяка[81].
Минерал самарскит (открыт Г. Розе в 1839 г. и назван в честь русского горного инженера) обратил на себя большое внимание исследователей в 1878 г.; М. Делафонтен, изучая образцы минерала, обнаружил отличный спектр абсорбции дидима от изолированного из церита. Являясь потенциальным источником новых элементов, минерал был изучен П. Э. Лекоком де Буабодраном, который обнаружил необъяснимые линии в спектре, предполагающие наличие нового элемента. Позднее было доказано, что его можно отделить от дидима и деципия на основании различных химических свойств, и 16 июля 1879 г. исследователь сообщил об открытии самария, впервые выделенного из минерала[64][73][82].

Пер Теодор Клеве в 1879 г., изучая эрбий, оставшийся после отделения от иттербия, пришел к выводу о неоднородности фракции: записанный Р. Аленом спектр помог понять, что в нём находится примесь. Исследователь разделил субстанцию на три фракции: первая была похожа на иттрий, вторая — на иттербий и третья — на эрбий. Среди предполагаемых линий спектра эрбия, одна (линия) присутствовала только во фракции близкой к иттербию, но не сам иттербий; вторая аналогично — только во фракции близкой к иттрию, но не сам иттрий; обе линии очень слабо присутствовали в спектре эрбиевой фракции. Учёный понял, что открыл два новых элемента и незамедлительно дал им названия: тулий и гольмий. Тогда же Клеве сделал примечание о том, что разделение элементов было неокончательным[83]. Как только это произошло, выяснилось, что годом раньше Ж.-Л. Соре обнаружил тот же самый спектр поглощения гольмия в образце эрбия, полученным от Ж. Мариньяка; исследователь обозначил его как элемент «X»[75]. Тогда же Лекок де Буабодран подтвердил исследования и Клеве, и Соре[84].

Неуверенность в присутствии новых элементов привела к интенсивному изучению самария, в результате чего произошло открытие двух лантаноидов: гадолиния и европия[85]. В 1880 г. Ж. Мариньяк принялся за изучение самарскита. Применяя фракционное осаждение и используя сульфат калия с последующим выделением оксалатов, были получены две потенциально новые земли: Yα и Yβ. Спектральный анализ Соре позволил предположить, что Yβ — самарий, а Yα не был похож ни на один из известных элементов, включая деципий[85]. В 1881 г. Делафонте получил более чистый деципий, позволивший сделать вывод о его схожести с элементом Yα и присутствии ранее примеси самария[84].
П. Э. Лекок де Буабодран (с одобрения Мариньяка) в 1880 г. предложил назвать элемент гадолинием, однако неизвестно, назван ли был этот элемент в честь Юхана Гадолина или минерала, или в честь обоих; тем не менее, гадолиний является единственным лантаноидом, у которого название происходит из иврита: корень гадол («великий») был выбран в качестве фамилии отцом ученого и происходит от названия фермы в Финляндии (фин. Maunala), на которой он жил[9]. В 1886 г. Мариньяк дал название элементу Yα — гадолиний[84].
Э. А. Демарсе в 1885 г. получил от П. Т. Клеве загрязнённые образцы самария и, подвергнув изучению линии спектров, усомнился в присутствии примесей. Данный вопрос оставался открытым на протяжении нескольких лет, и позднее даже Лекок де Буабодран и Демарсе сообщили об обнаружении примесей (в 1892 и 1893 гг.). Чистое соединение европия было получено Э. А. Демарсе в 1901 г. Немногим позднее Жорж Урбэн (1903 и 1904 гг.) сообщил о выделении европия из гадолиния, используя новый метод, где висмут являлся сепарирующим элементом[85].
В 1882 г. Б. Браунер сообщил (помимо Ж. Мариньяка в 1853, М. Делафонте в 1875 и П. Т. Клеве в 1882 гг.) о неоднородности дидима, пометив примесь записью Diγ, а годом позже подтвердил свои предположения. Спустя несколько лет, на протяжении которых К. Ауэр фон Вельсбах занимался отделением различных открытых лантаноидов, благодаря повторению более ста раз операций по фракционной кристаллизации (не осаждению) и анализу спектров, в 1885 г. были получены фракции празеодидима (зелетоватого цвета) и неодидима[86][87]. Позднее их названия были укорочены до празеодима и неодима, а в 1890 г. открытие было независимо подтверждено А. Беттендорфом[87]. Первым в относительно чистом металлическом виде в 1925 г. был получен неодим[88], в 1931 г. — празеодим[89].
Детальное изучения гольмия Лекоком де Буабодраном привело к открытию диспрозия в 1886 г. Новый элемент был назван так потому, что для его выделения потребовалось провести 32 утомительных операции по осаждению солей аммония и последующих 26 — по оксалатам; последующее изучение спектров и флуоресенции позволило открыть новый элемент[75]. Открытие диспрозия было воспринято химиками без обычного для того времени неверия и споров[84]; вплоть до 1950 г. металл (наравне с остальными РЗЭ) не мог быть получен в чистом виде до развития реакций ионного обмена и техники металлографического восстановления, разработанной во главе с Ф. Спеддингом[90].
Эта статья или раздел нуждается в переработке. |
К началу следующего века многие химики были убеждены в существовании следующих элементов: лантана, церия, празеодима, неодима, самария, гадолиния, тербия, диспрозия, гольмия, эрбия, тулия, иттербия[91].

Долгий путь изучения и нахождения большинства лантанидов в природе был закончен благодаря исследованиям Ж. Урбэна, который в 1907 г. (спустя более века с начала открытия церия[43]) в иттербии Ж. Мариньяка выявил наличие лютеция[66]. На год позже и независимо от Урбэна, в 1908 г. этот элемент был открыт К. Ауэром фон Вельсбахом, прозвавшим элемент кассиопеем[19]. Названия лютеций и кассиопей параллельно использовались на протяжении нескольких десятилетий, причем последний был в ходу в Германии и Австрии до 1950-х гг[79].
Если спектральный анализ дал возможность выявлять отдельные РЗЭ в разных породах, делать вывод о степени их чистоты, то он ничего не мог подсказать о начальной распространённости лантанидов, предвидеть существование новых элементов. На последний вопрос ответ был дан после исследования рентгеновских спектров РЗЭ. Так, с помощью закона Мозли было установлено, что лантан имеет порядковый номер 57, самый тяжёлый элемент из семейства лантаноидов — 71. После рентгеноспектрального установления порядковых номеров всех известных лантаноидов было обнаружено, что среди них нет элемента с номером 61[92]. Группа итальянских ученых из Флорентийского университета заявила об открытии флоре́нтия в 1924 г. Похожее сообщение об открытии илли́ния (в честь штата Иллинойс), прозвучавшее двумя годами позднее, так же являлось преждевременным[76].
Начались поиски данного элемента. Пятьдесят образцов лантаноидных минералов были подвергнуты тщательному исследованию в оптической и рентгеновской областях спектра — 61-го элемента не нашли. Немецкий химик Л. Прандтль предположил, что этого элемента либо не существует, либо его нахождение в природе так же мало, как и у технеция. Однако немецкая исследовательница И. Ноддак, которая была известна поисками элементов-аналогов марганца и особенно рения, выдвинула гипотезу о нестабильности атомов 61-го элемента, то есть о его радиоактивности: основанием для такой гипозеты являлось то, что 62-й элемент — самарий — имеет слабое радиоактивное излучение, и гипотеза подтвердилась. Атомы 61-го элемента были добыты благодаря ядерным реакциям[92]: в 1945 г. американские исследователи Дж. Маринский, Л. Гленденин и Ч. Кориелл получили 61 элемент[93] (в виде нуклида 147Pm) и химически идентифицировали два изотопа, используя ионообменную хроматографию. В 1947 г. были анонсированы его химические свойства для доказательства открытия, а годом позже дано название[94][95][96].
Тенденции в изучении[править | править код]
В 1937 г. В. Клемм и Г. Боммер подготовили РЗЭ в таком виде, который позволил им описать несколько из свойств металлов: описать их кристаллические структуры, магнитную восприимчивость, плотности, а также подтвердить данные Виктора Гольдшмидта от 1925 г. о лантаноидном сжатии (нем. die Lanthaniden-Kontraktion) при увеличении порядкового номера. Работа позволила сделать вывод о том, что элементы не так уж и сильно похожи друг на друга, судя по их свойствам, как в основном считалось ранее: были описаны дивалентные состояния у Eu и Yb, а валентность Ce оказалась больше 3+. Различия постепенно усиливались при их дальнейшем изучении[97][98][99].
С середины XX века различные вопросы, касающиеся систематики лантаноидов, Sc и Y, были предметом множества опубликованных работ, что привело, в общем и целом, к более глубокому пониманию химической, металлургической и физической природы 17 элементов[99]. Во время Второй мировой войны и в последующие годы была значительно изучена и расширена техника разделения РЗЭ с помощью ионообменных смол Ф. Спеддингом[К 11]. Сотни килограмм чистых оксидов элементов удалось разделить и наработать в Лаборатории Эймса. Параллельно этому, редкоземельные металлы становились понемногу доступными для применения и изучения их свойств. После 1957 г., в котором промышленность начала получение соединений высокой чистоты, цены на некоторые из них (от Eu до Lu) упали в среднем в 282 раза[97][К 12].
Изучение основных физических свойств, в частности магнетизма в металлах, сплавах и соединениях, являлось объектом интенсивного изучения со стороны ученых на протяжении нескольких десятилетий. В 1960-х — начало 1970-х гг. основное внимание сфокусировалось на «тяжелых» лантаноидах; «легкие» же привлекли своё внимание в 1970-х гг., когда стали доступными в виде кристаллов[100]. В те же годы начали появляться работы, связанные с влиянием металлов на организм человека[101]: радиоактивный 144Ce был найден в костях животных и моллюсках[102], а также в легких и лимфоузлах людей, вдыхавших радиоактивные аэрозоли[103]. В середине 1980-х гг. внимание ученых привлекли их антикоррозионные свойства: были опубликованы работы, в которых описывалось положительное влияние хлоридов РЗЭ на ингибирование коррозии некоторых металлов (например, алюминия) в хлор-содержащих электролитах[104][105][106].

Начиная с Манхэттенского проекта, США были центром по исследованию РЗЭ и связанных с ними технологий. В начале 1980-х гг. центр «силы» переместился в Японию из-за стремительного прогресса в электронике и автомобильной промышленности в стране, а в настоящее время — перемещается в Китай, возможно, благодаря тем же причинам (включая выгодное географическое расположение)[107].
Общее количество научных работ, зарегистрированных в Химической реферативной службе (англ. Chemical Abstracts Service), в 1990 г. составило приблизительно 490 000, из которых затрагивали тему изучения РЗЭ 18 000; в 2007 г. общее количество приблизилось к 1 000 000, из которых примерно 3 % касалось РЗЭ. Больше всего материалов публиковалось на темы, связанные с оксидами группы (до 5000 статей, 2008 г.), далее — спектроскопией (более 1400 статей, 2008 г.), магнетизмом (до 1400, 2006 г.), магнитами (так же), катализом и катализаторами (до 1400, 2008 г.)[107].
Нахождение в природе[править | править код]
| Важнейшие минералы редкоземельных элементов[108] | |||
|---|---|---|---|
| Название | Состав минерала | Содержание элементов цериевой группы, % |
Содержание элементов иттриевой группы, % |
| Монацит | Ортофосфаты РЗЭ и тория (Ln, Th) PO4 |
42—70 | 0,5—5 |
| Бастнезит | Фторокарбонаты РЗЭ (Ce, La) CO3F |
73—76 | 0,0—0,1 |
| Лопарит | Титанониобаты РЗЭ, кальция | 30,7—34 | 0,0—0,5 |
| Церит | Силикаты РЗЭ | 59,4—70 | — |
| Эвксенит | Титанониобаты РЗЭ, кальция (Y, Ca, Ce,) (Nb, Ta, Ti)2O6 |
0,2—4,3 | 18,2—28,1 |
| Ксенотим | Ортофосфаты РЗЭ YPO4 |
0,3—5 | 52—63 |
| Гадолинит | Силикаты РЗЭ, железа, бериллия | 2,9—7,9 | 31—46,6 |
| Самарскит | Танталониобат иттрия, эрбия и др. | 0,3—1,7 | 9,1—38 |
| Фергюсонит | Смесь танталониобатов, титанониобатов самария, иттрия, эрбия и железа |
0,9—6,2 | 31,2—42,3 |
| Пирохлор | (Na, Ca, Ce, Y, Th, U)2 (Nb, Ta, Ti, Fe)2O6 (OH, F) |
0,78—7,5 | 0,1—0,6 |
Лантаноиды достаточно широко распространены в природе. Их распространение в земной коре составляет 0,015 %[109]. Их общая концентрация приближается по значениям распространённости меди, свинца, цинка[109], олова, золота[19], мышьяка, которые не относятся к редким в природе элементам. На земле нет таких горных пород, в которых не было хотя бы мизерной примеси церия, лантана, празеодима, иттрия и т. п. Лантаниды содержатся в апатитах, баритах, гранитах, базальтах, пироксенитах, андезитах, глинах, в морской воде и т. д. Кроме того, их присутствие выявлено так же в каменном угле, нефти, в разных грунтах, животных и растениях[92].
| Геологическое распространение резервов металлов[110] | |
|---|---|
| Страна | Резервы оксидов, т |
| Китай | 55 000 000 |
| Страны СНГ | 19 000 000 |
| США | 13 000 000 |
| Индия | 3 100 000 |
| Австралия | 1 600 000 |
| Бразилия | 48 000 |
| Малайзия | 30 000 |
| Другие | 22 000 000 |
| Всего | 113 778 000 |
Тем не менее, лантаноиды все же довольно рассеянные элементы и не часто находятся в минералах, которые легко перерабатываются. Только некоторые страны (Индия, ЮАР) обладают достаточным количеством месторождений для получения концентратов, однако более 95 % всех месторождений расположено в Китае. Парадоксально, но из-за увеличения их роли в сельском хозяйстве и промышленности, выросло и их негативное влияние на окружающую среду[109]. В природе есть и более концентрированные скопления РЗЭ. Ещё в первой половине XIX века был выявлен ряд минералов, которые содержат в себе лантаниды. Содержание данной группы элементов в минералах приближается к 250 видам. Минералов, в которых РЗЭ составляют 5—8 % от массы, примерно 60—65 видов. Больше всего минералов содержат в себе церий и близких к нему элементов (цериевые металлы). Намного меньше известно минералов, содержащих в себе иттрий и тяжёлые лантаноиды[108].
Концентрация «легких» лантаноидов обычно выше, чем «тяжелых»: большинство месторождений элементов в своём составе имеют от 80 до 99 % соединений лантана, церия, празеодима и неодима. Металлы могут быть добыты в виде их оксидов или в чистом виде (мишметалл) с последующей сепарацией. Только лантан, церий, празеодим и иттрий добываются отдельно и составляют около четверти от общего производства[111].
Месторождения[править | править код]
Богатые месторождения лантаноидов (редкоземельных элементов) находятся в Индии; монацитовый песок залегает на береговых пляжах Траванкори, в Бразилии, Австралии, США, в Африке, в Скандинавии и др. В Европе минералы РЗЭ располагаются на Кольском полуострове, Урале, Украине, в Азии — в Казахстане, Сибири.
В июне 2011 г. исследователями из Японии были обнаружены обширные залежи металлов — лантаноидов и иттрия — на дне Тихого океана. В международных водах на 78 участках, находившихся на глубине от 3,5 до 6 км, было проведено изъятие залежей ила со дна[115]. По предположительным оценкам ученых, общий объём металлсодержащих осадков на дне океана составляет приблизительно более 110 млн т[116]. Исследованные места были выбраны таким образом, чтобы покрывать большую часть поверхности дна. Наиболее богатые на соединения (в основном это металлсодержащие осадки, цеолитовая глина, красная глина) участки располагаются от центральной (приблизительно 13°30′ с. ш. 175°00′ з. д.HЯ) до юго-восточной (15° ю. ш. 145° з. д.HЯ) областей океана. Тем не менее, до тех пор, пока глубина в 4—5 км, на которой расположено большинство богатого на оксиды РЗЭ ила, будет сильно влиять на экономическую и технологическую целесообразность добычи, залежи будут лишь оставаться весьма перспективным ресурсом для добычи[117].
Основными рудами, из которых добываются редкоземельные металлы, являются бастнезит, монацит, ксенотим и ионно-абсорбционные глины[118].
| Элементный состав некоторых месторождений металлов (в %)[118][119] | |||||||
|---|---|---|---|---|---|---|---|
| Маунт-Уэлд (CLD)[К 16] (Австралия) |
Маунт-Уэлд (Duncan)[К 16] (Австралия) |
Маунтин-Пасс (США) |
Баян-Обо (Китай) |
Гуандун (Китай) |
Сюньу (Китай) |
Луннань (Китай) | |
| Минерал | Вторичный монацит | Черчит | Бастнезит | Бастнезит | Ксенотим | Латерит | Латерит |
| Лантан | 25,57 | 23,93 | 33,2 | 23 | 1,2 | 43,4 | 1,82 |
| Церий | 46,9 | 39,42 | 49,1 | 50 | 3 | 2,4 | 0,4 |
| Празеодим | 4,92 | 4,85 | 4,34 | 6,2 | 0,6 | 9 | 0,7 |
| Неодим | 16,87 | 18,08 | 12 | 18,5 | 3,5 | 31,7 | 3 |
| Самарий | 2,29 | 2,87 | 0,8 | 0,8 | 2,2 | 3,9 | 2,8 |
| Европий | 0,49 | 0,77 | 0,1 | 0,2 | 0,2 | 0,5 | 0,1 |
| Гадолиний | 1,33 | 2,15 | 0,2 | 0,7 | 5 | 3 | 6,9 |
| Тербий | 0,13 | 0,29 | — | 0,1 | 1,2 | — | 1,3 |
| Диспрозий | 0,31 | 1,36 | — | 0,1 | 9,1 | — | 6,7 |
| Гольмий | 0,04 | 0,21 | — | — | 2,6 | — | 1,6 |
| Эрбий | 0,113 | 0,46 | — | — | 5,6 | — | 4,9 |
| Тулий | 0,01 | 0,04 | — | — | 1,3 | — | 0,7 |
| Иттербий | 0,05 | 0,2 | — | — | 6 | 0,3 | 2,5 |
| Лютеций | 0,02 | 0,03 | — | — | 1,8 | 0,1 | 0,4 |
Китай[править | править код]
В Китае находятся три основных района добычи полезных ископаемых: в Баотоу, Сычуане и Цзянси — на них приходится 88 % всех месторождений страны. В Баян-Обо (Баотоу, Внутренняя Монголия), сконцентрировано приблизительно 83 % месторождений Китая, в провинции Шаньдун — 8 %, в провинции Сычуань — 3 % (в данных провинциях расположены месторождения легких лантаноидов); в провинции Цзянси, расположенной на юге Китая, находится 3 % месторождений тяжелых лантаноидов[118][120].
Распространенность элементов в бастназите и монаците из Баян-Обо схожа: 26 % приходится на La2O3, 50 % — Ce2O3, 5 % — Pr2O3, 16 % — Nd2O3, 1 % Sm2O3 (другие — менее 1 %). В провинции Сычуань разрабатывается бастнезит со следующим составом: 37 % — La2O3, 47 % — Ce2O3, 4 % — Pr2O3, 10 % — Nd2O3 (другие — менее 1 %). На юго-востоке Китая известно о наличии латеритовой глины, содержащей РЗЭ; в нескольких провинциях, расположенных вокруг Цзянси, разрабатываются ион-абсорбирующие глины, которые показывают довольно различный состав: 2—30 % — La2O3, 1—7 % — Ce2O3 и Pr2O3, 3—30 % — Nd2O3, 2—7 % — Dy2O3[118][121][122]. Именно благодаря последним достигается мировое обеспечение металлами иттриевой группы; они же обычно и легче добываются из таких глин прямо на месте — этот процесс намного менее энергозатратен, чем добыча из твердых пород[114][123][124].
Другие разведанные места в провинциях Юньнань, Гуйчжоу и Сычуань включают в себя базальтовую кору выветривания, являющуюся объектом дальнейших исследований потенциальных месторождений[125].
Уровень добычи Китаем редкоземельных элементов в настоящее время составляет от 80 % и более от общемирового уровня[126].
Экономические аспекты[править | править код]
| Стоимость соединений металлов в 2009 (расчётная)[127] и 2011 гг[128]. | |||||
|---|---|---|---|---|---|
| Оксид металла | Чистота, % | Стоимость, долл США/кг | |||
| 2009 г. | 2011 г. | ||||
| Лантан | 99,99 | 30 | 100 | ||
| Церий | 96—99,50 | 30 | 100 | ||
| Празеодим | 96 | 38 | 225 | ||
| Неодим | 95 | 42 | 270 | ||
| Самарий | 99,90 | 130 | 118 | ||
| Европий | 99,99 | 1 600 | 3 300 | ||
| Гадолиний | 99,99 | 150 | 239 | ||
| Тербий | 99,99 | 900 | 2 750 | ||
| Диспрозий | 99 | 170 | 1 600 | ||
| Гольмий | 99,90 | 750 | — | ||
| Эрбий | 96 | 100 | 255 | ||
| Тулий | 99,90 | 1 500 | — | ||
| Иттербий | 99 | 325 | 450 | ||
| Лютеций | 99,99 | 1 800 | 4 000 | ||

Спрос на РЗЭ вырос за последние 35 лет с 30 000 т (1980-е гг.) до около 120 000 т (2010 г.), что выше показателя производства соединений металлов в 2011 г. — 112 000 т[116]. Потребление редкоземельных металлов в 2014 г. составило 120 148 т[129]. Проведённые исследования позволили спрогнозировать, что совокупный годовой темп роста (от англ. Compound Annual Growth Rate) спроса c 2014 по 2020 гг. будет составлять 3,9 % (со 120 148 т до 150 766 т) в основном благодаря сильному спросу на оксиды неодима, празеодима и диспрозия (среди остальных РЗЭ)[130].
Китаем в 2010 г. были наложены серьезные квоты: уменьшение объёма экспорта металлов составило почти 70 %, что отразилось пиковым ростом (2011) и падением (2012) цен[131], и как результат — мировая цена на La с 2009 по 2012 гг. выросла в 5 раз, на Sm и Tb — в 5,8, на Er — 6,3, на Ce и Pr — в 9, на Nd — в 11 и на Dy — в 12,4[132]. После этого события было положено начало множеству проектов по разработке мест добычи металлов в различных странах[131], а также изучению (возможных) новых[117][133][134][135][136], что привело к возрастанию ресурсов за пределами страны более чем в 7 раз — с 13,4 (2010) до 100,2 млн т (2015)[126].

По некоторым предположениям, в настоящее время рост цен может быть также вызван дисбалансом между спросом на отдельные редкоземельные металлы и их количественным содержанием в рудах[137].
Помимо поиска мест добычи, публикуются обзоры:
- возможности переработки и выделения металлов из первичных источников (например, благодаря гидрометаллургии)[138];
- из вторичных источников — отходов[139][140][141][142][143], например: из жестких дисков[144][145][146][147], люминесцентных ламп[148][149], NiMH аккумуляторов, составивших 8 % мирового потребления РЗЭ в 2010 г.[150][151], отработавших моторов электрических или гибридных автомобилей[152];
- вовсе отказа от их использования (при разработке двигателей для FEV- или HEV-автомобилей[153][154]). Тем не менее, отказаться от использования лантаноидов в пользу более дешевых элементов-заменителей или их соединений сложно: для большинства видов применения Eu, Dy, Tm, Yb и La найти замену данным элементам с относительно удовлетворительными характеристиками это невозможно или очень сложно; из всех лантаноидов найти замену проще для Sm, Pr и Nd[155][К 17].
Последние данные показывают, что уровень переработки РЗЭ составляет менее 1 % (2011 г.)[156][157] или 1—2 % (2013 г.)[158][159] по показателю EOL-RR (англ. end-of-life recycling rate — процент от количества металла, идущего на переработку, в отработавшем товаре).
Мнение о критически важном значении данных металлов для высоких технологий опубликовано Геологической службой США в 2002 г[160]. Европейская комиссия в 2010 г. так же признала группу критическими важными и обладающими средней важностью для экономики[5][161], а Институт энергии и транспорта, входящий в Центр совместных исследований, из-за рыночного риска и политических факторов выделил из них неодим и диспрозий[162]. В 2014 г. ЮНКТАД выпустил специальный доклад, в котором говорится о высокой степени зависимости от производства в Китае и важности элементов для оборонительных систем[5][163]. Многими экспертами[какими?] элементы признаются четвёртыми по важности после нефти, воды и железной руды[164], а иногда называются «витаминами» («промышленными витаминами», «витаминами для металлов»): добавление даже малых количеств может значительно усилить полезные свойства конечного продукта[165][166][167][168][169].
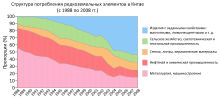
На примере Китая — страны, бывшей одновременно наибольшим производителем, потребителем и экспортёром РЗЭ[171][К 18], — можно сделать вывод о значительном изменении структуры потребления металлов за 20-летний период с 1988 по 2008 гг. Так, если в 1988 г. более половины (56 %) потребления приходилось на металлургическую промышленность и машинное оборудование, то в 1998 г. уже менее трети (30 %), а в 2008 г. — 15 %. Напротив, производство магнитов, люминофоров, полировальных порошков и т. д. в 1988 г. составляло менее 1 %, однако уже через 10 лет — 18 %, а в 2008 г. — 52 %. На другие сферы потребления — химическую, нефтяную, текстильную, светотехническую промышленности, сельское хозяйство, для производства стёкол, линз, керамических материалов — приходится до 56 % за каждый отдельный год промежутка. Ожидается значительное увеличение потребления металлов Китаем в будущем из-за увеличения числа иностранных компаний, переносящих своё производство и имеющих возможность купить их дешевле внутри страны, что позволяет уменьшить стоимость изготовления конечного продукта и является одной из основных стратегий страны, желающей удерживать контроль за промышленностью[170].
Свойства[править | править код]
Физические свойства[править | править код]
| Химический элемент | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Зарядовое число | 57 | 58 | 59 | 60 | 61 | 62 | 63 | 64 | 65 | 66 | 67 | 68 | 69 | 70 | 71 |
| Изображение |  |
 |
 |
— |  |
||||||||||
| Плотность, г/см³ | 6,162 | 6,77 | 6,77 | 7,01 | 7,26 | 7,52 | 5,244 | 7,9 | 8,23 | 8,54 | 8,79 | 9,066 | 9,32 | 6,90 | 9,841 |
| Температура плавления, °C | 920 | 795 | 935 | 1024 | 1042 | 1072 | 826 | 1312 | 1356 | 1407 | 1461 | 1529 | 1545 | 824 | 1652 |
| Температура кипения, °C | 3464 | 3443 | 3520 | 3074 | 3000 | 1794 | 1529 | 3273 | 3230 | 2567 | 2720 | 2868 | 1950 | 1196 | 3402 |
| Электронная конфигурация[К 19] | 5d1 | 4f15d1 | 4f3 | 4f4 | 4f5 | 4f6 | 4f7 | 4f75d1 | 4f9 | 4f10 | 4f11 | 4f12 | 4f13 | 4f14 | 4f145d1 |
| Металлическая решетка | ДГПУ | ГЦК | ДГПУ | ДГПУ | ДГПУ | Р | ОЦК | ГПУ | ГПУ | ГПУ | ГПУ | ГПУ | ГПУ | ГПУ | ГПУ |
| Металлический радиус, пм | 162 | 181.8 | 182,4 | 181,4 | 183,4 | 180,4 | 208,4 | 180,4 | 177,3 | 178,1 | 176,2 | 176,1 | 175,9 | 193,3 | 173,8 |
| Удельное сопротивление (при 25 °C), мкОм·см |
57—80 (при 20 °C) |
73 | 68 | 64 | — | 88 | 90 | 134 | 114 | 57 | 87 | 87 | 79 | 29 | 79 |
| Магнитная восприимчивость, χмоль /10−6(см3·моль−1) |
+95.9 | +2500 (β) | +5530(α) | +5930 (α) | — | +1278(α) | +30900 | +185000 (при 350 K) |
+170000 (α) | +98000 | +72900 | +48000 | +24700 | +67 (β) | +183 |
Известно, что атомы лантаноидов имеют следующие электронные конфигурации [Xe] 4fn6s2 и [Xe] 4fn−15d16s2 (где n — число от 1 до 14)[172]. У лантана ([Xe] 5d16s2) f-электронов нет, у церия один ([Xe] 4f15d16s2), у празеодима — 3. Далее с увеличением порядкового номера количество f-электронов постепенно увеличивается с половинным заполнением 4f-уровня у гадолиния (4f75d16s2) и полным его завершением у лютеция (4f145d16s2)[173].

У лантана, гадолиния и лютеция валентными являются 5d16s2-электроны, поэтому эти элементы в соединениях бывают исключительно трёхвалентными. У других лантаноидов валентные связи создаются с участием 4f-электронов. Однако для них так же свойственна валентность 3. Учитывая стабильность 4f0-, 4f7- и 4f14-конфигураций, элементы Eu ([Xe] 4f76s2) и Yb ([Xe] 4f146s2)[175] могут проявлять валентность 2, а Ce ([Xe] 4f15d16s2) и Tb ([Xe] 4f96s2) даже 4[173].
Первые потенциалы ионизации лантаноидов и вместе с ними РЗЭ малы: 5,61 (La)—5,64 эв (Sc). Вторые и третьи потенциалы тоже не очень высоки. К тому же дополнительная ионизация одного- или двухзарядных ионов легко осуществляется, потому что необходимая для этого энергия получается как выигрыш в энергии при формировании кристаллической решётки или гидратов меньших R3+. Отсюда, лантаниды легко образовывают ионы R3+. Поэтому и связи, созданные ими с другими элементами, имеют высокий процент ионности[173].
Все ионы лантаноидов Ln3+, за исключением La3+ и Lu3+, имеют неспаренные 4f-электроны. Это указывает на их парамагнетизм и характерные особенности ионных спектров. Поскольку внешние 5s2- и 5p6-подоболочки очень заметно экранируют 4f-орбитали, то 4fn-электроны практически не изменяются во всех их соединениях.
Лантаниды характеризуются серебристым цветом, ковкостью, низкой твёрдостью и средними температурами плавления, разброс в значениях которых составляет от 804 °C (церий) до 1700 °C (лютеций). Исходя из значений плотности лантаниды можно разделить на две группы: лёгкие и тяжелые. К первой группе относятся лантан, церий, празеодим, неодим, самарий, европий и гадолиний. Плотность этих металлов ниже 8 г/см³. Остальные элементы составляют вторую группу, в которых плотность, исключая иттербий, лежит в промежутке между 8,272 (тербий) и 9,482 г/см³ (лютеций)[176].
Для металлических лантаноидов свойственна парамагнитность. Парамагнитными являются и большинство трёхзарядных лантаноид-ионов. Некоторые из металлов-лантаноидов, кроме церия, сохраняют свои парамагнитные свойства даже при очень низких температурах (температура жидкого азота), другие — заметно изменяют свой парамагнетизм со сменой температуры[176].
Лантан и лантаноиды проводят тепло и электрический ток. Лучшей электропроводностью обладает иттербий, хуже — иттрий, лантан, церий, празеодим и неодим. Хуже всех проводят электричество гадолиний и тербий. Отсюда следует, что смена электропроводности с увеличением порядкового номера возрастает неравномерно. И из-за этого свойства лантаниды и делятся на две группы[177].
Ещё более неравномерным изменением характеризуется атомный объем лантаноидов. Зависимость атомного объёма или радиусов атомов лантаноидов от порядковых номеров имеет характер ломанной линии с пиками в начале, середине и в конце. Таким образом, смена физических свойств металлов-лантаноидов уже указывает на вторичную периодичность в этом семействе и разделение их на две группы: цериевую и иттриевую.
Важной физической особенностью лантанидов является их способность к поглощению тепловых нейтронов. В этом отношении особенно отличаются гадолиний, самарий, европий, диспрозий. К примеру, для церия поперечное сечение захвата тепловых нейтронов равно 0,73 барн, в то время как для гадолиния данное значение приравнивается к 46000. Кроме церия, плохо поглощают нейтроны иттрий (1,3 барн) и лантан (9,3 барн)[173].
В атоме лантаноидов заполняется глубоко лежащий четвёртый слой 4f14. Поэтому лантаноидов может быть только 14. Поскольку по мере увеличения заряда ядра структура двух внешних электронных оболочек не меняется, все лантаноиды имеют сходные химические свойства[178].
В природе лантаноиды сопутствуют друг другу. Выделение отдельных элементов химическими способами является очень трудной задачей ввиду большого сходства их свойств.
Полиморфизм[править | править код]
| Полиморфные модификации лантаноидов[179] | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Элемент | Модификация | Кристаллическая система |
Структура типа |
Параметры решетки, пм | Пространственная группа, символы Шёнфлиса и Пирсона |
Диапазон устойчивости | |||
| a | c | ||||||||
| Лантан | α-La | Гексагональная | α-La | 377,4 | 1217,1 | P63/mmc | D4 6h |
hP4 | Комн. темп. и давление |
| β-La | ГЦК | Cu | 530,45 | — | Fm3m | O5 h |
cF2 | > 613 K | |
| γ-La | ОЦК | W | 426,5 | — | Im3m | O9 h |
cI2 | > 1141 K | |
| β′-La | ГЦК | Cu | 517 | — | Fm3m | O5 h |
cF4 | > 2 ГПа | |
| Церий | α-Ce | ГЦК | Cu | 516,1 | — | Fm3m | O5 h |
cF4 | Комн. темп. и давление |
| β-Ce | Гексагональная | α-La | 367,3 | 1180,2 | P63/mmc | D4 6h |
hP4 | > 263 K | |
| γ-Ce | ГЦК | Cu | — | — | Fm3m | O5 h |
cF4 | < 95 K | |
| α′-Ce | ГЦК | Cu | 482 | — | Fm3m | O5 h |
cF4 | > 1,5 ГПа | |
| Ce-III | Орторомбическая | α-U | — | — | Cmcm | D17 2h |
oC4 | 5,1 ГПа | |
| Празеодим | α-Pr | Гексагональная | α-La | 367,21 | 1183,26 | P63/mmc | D4 6h |
hP4 | Комн. темп. и давление |
| β-Pr | ОЦК | W | 413 | — | Im3m | O9 h |
cI2 | > 1094 K | |
| γ-Pr | ГЦК | Cu | 488 | — | Fm3m | O5 h |
cF4 | > 4 ГПа | |
| Неодим | α-Nd | Гексагональная | α-La | 365,82 | 1179,66 | P63/mmc | D4 6h |
hP4 | Комн. темп. и давление |
| β-Nd | ОЦК | W | 413 | — | Im3m | O9 h |
cI2 | > 1135 K | |
| γ-Nd | ГЦК | Cu | 480 | — | Fm3m | O5 h |
cF4 | > 5 ГПа | |
| Прометий | α-Pm | Гексагональная | α-La | 365 | 1165 | P63/mmc | D4 6h |
hP4 | Комн. темп. и давление |
| β-Pm | ОЦК | W | — | — | Im3m | O9 h |
cI2 | > 1163 K | |
| Самарий | α-Sm | Тригональная | α-Sm | 362,9 | 2620,7 | R3m | D5 3d |
hR3 | Комп. темп. и давление |
| β-Sm | ОЦК | W | — | — | Im3m | O9 h |
cI2 | > 1190 K | |
| γ-Sm | Гексагональная | α-La | 361,8 | 1166 | P63/mmc | D4 6h |
hP4 | > 4 ГПа | |
| Гадолиний | α-Gd | ГПУ | Mg | 363,36 | 578,1 | P63/mmc | D4 6h |
hP2 | Комн. темп. и давление |
| β-Gd | ОЦК | W | 406 | — | Im3m | O9 h |
cI2 | > 1535 K | |
| γ-Gd | Тригональная | α-Sm | 361 | 2603 | R3m | D5 3d |
hR3 | > 3 ГПа | |
| Тербий | α-Tb | ГПУ | Mg | 360,55 | — | P63/mmc | D4 6h |
hP2 | Комн. темп. и давление |
| β-Tb | ОЦК | W | — | — | Im3m | O9 h |
cI2 | > 1589 K | |
| Tb-II | Тригональная | α-Sm | 341 | 2450 | R3m | D5 3d |
hR3 | > 6 ГПа | |
| Диспрозий | α-Dy | ГПУ | Mg | 359,15 | 565,01 | P63/mmc | D4 6h |
hP2 | Комн. темп. и давление |
| β-Dy | ОЦК | W | — | — | Im3m | O9 h |
cI2 | > 1243 K | |
| α′-Dy | Орторомбическая | — | a=359,5, b=618,4, c=567,8 | Cmcm | D17 2h |
oC4 | < 86 K | ||
| γ-Dy | Тригональная | α-Sm | 343,6 | 2483 | R3m | D5 3d |
hR3 | > 7,5 ГПа | |
| Гольмий | α-Ho | ГПУ | Mg | 357,78 | 561,78 | P63/mmc | D4 6h |
hP2 | Комн. темп. и давление |
| β-Ho | ОЦК | W | — | — | Im3m | O9 h |
cI2 | При высокой температуре | |
| γ-Ho | Тригональная | α-Sm | 334 | 2450 | R3m | D5 3d |
hR3 | > 4 ГПа | |
| Эрбий | α-Er | ГПУ | Mg | 355,92 | 558,5 | P63/mmc | D4 6h |
hP2 | Комн. темп. и давление |
| β-Er | ОЦК | W | — | — | Im3m | O9 h |
cI2 | При высокой температуре | |
| Тулий | α-Tm | ГПУ | Mg | 353,75 | 555,4 | P63/mmc | D4 6h |
hP2 | Комн. темп. и давление |
| β-Tm | ОЦК | W | — | — | Im3m | O9 h |
cI2 | При высокой температуре | |
| Tm-II | Тригональная | α-Sm | — | — | R3m | D5 3d |
hR3 | > 6 ГПа | |
| Иттербий | α-Yb | ГЦК | Cu | 548,48 | — | Fm3m | O5 h |
cF4 | Комн. темп. и давление |
| β-Yb | ОЦК | W | 444 | — | Im3m | O9 h |
cI2 | > 1005 K | |
| γ-Yb | ГПУ | Mg | 387,99 | 638,59 | P63/mmc | D4 6h |
hP2 | < 270 K | |
| Лютеций | α-Lu | ГПУ | Mg | 350,52 | 554,94 | P63/mmc | D4 6h |
hP2 | Комн. темп. и давление |
| β-Lu | ОЦК | W | — | — | Im3m | O9 h |
cI2 | > 1005 K | |
| Lu-II | Тригональная | α-Sm | — | — | R3m | D5 3d |
hR3 | > 23 ГПа | |
Для лантана и лантанидов полиморфизм характерен, так же как и для актиноидов. Так, лантан имеет три модификации (α-, β- и γ-лантан), церий — четыре (α-, β-, γ- и δ-церий). При нормальных условиях для лантаноидов характерна гексагональная решётка (за исключением церия)[177].
Химические свойства[править | править код]

Лантаноиды химически активны, они образуют прочные оксиды, галогениды, сульфиды, реагируют с водородом, углеродом, азотом, фосфором. Разлагают воду, растворяются в соляной, серной и азотной кислотах. В плавиковой и фосфорной кислотах лантаноиды устойчивы, так как покрываются защитными плёнками малорастворимых солей — фторидов и фосфатов.
С рядом органических соединений лантаноиды образуют комплексные соединения. Важное значение для разделения лантаноидов имеют комплексы с лимонной и этилендиаминтетрауксусной кислотой.
Первые образцы кристаллографически характеризуемых комплексных соединений ионов Tb2+, Pr2+, Gd2+, Lu2+ показали, что ионы всех Ln2+ (кроме, возможно, прометия) могут быть получены в растворах[180][181][182].
Для определения содержания лантаноидов в растворе может применяться кальцеиновый голубой[К 20][183][184].
Бинарные соединения[править | править код]
Оксиды и гидроксиды[править | править код]

Монооксиды LnO (где Ln = La, Ce, Pr, Nd, Sm, Eu, Tb, Ho, Er, Yb) являются механически стабильными, обладают хорошим сопротивлением к пластичной деформации и имеют металлический характер связи. Высокие значения модуля Юнга, по сравнению с модулем объемного сжатия и модулем сдвига, показывают, что монооксиды La, Ce, Nd, Sm, Eu, Ho, Er и Yb являются более жесткими по своему характеру, чем TbO; коэффициент Пуассона между всеми вышеуказанными монооксидами находится в промежутке от 0,23 до 0,409, что указывает на их устойчивость к внешней деформации. Благодаря расчётам распределения плотности электронного заряда по плоскости (100) в соединениях были подтверждены данные о ковалентной природе связи в LaO, SmO, EuO, ErO, HoO и ионной в CeO, PrO, NdO, TbO и YbO[185].
Галогениды[править | править код]
Иодид самария(II), применяющийся в органической химии в качестве одного из самых важных восстановителей в органическом синтезе[186], можно получить, например, высокотемпературным разложением его трииодида[187][188][189] или реакцией порошка самария с дииодоэтаном в безводном ТГФ в лабораторных условиях[190]. Соединения диспрозия(II) и тулия(II) являются более сильными восстановителями в органическом синтезе, чем соединения самария(II)[191][192][193][194].
Благодаря проведённым расчётам были получены экспериментальные данные о свойствах в соединениях LnX4 (Ln = Ce, Pr, Tb; X = F, Cl, Br, I), в которых 4f- и np-уровни (у лантаноидов и галогенидов соответственно) значительно накладываются друг на друга. Вклад 4f-уровня в связь Ln—X у тетрагалогенидов примерно на треть больше, чем у тригалогенидов (LnX3)[195].
Металлоорганические соединения[править | править код]
Обзоры в области синтеза металлоорганических соединений металлов группы публикуются на ежегодной основе[181][196][197][198][199].
Эффекты в 4f-подуровне[править | править код]
Схожесть химических свойств лантаноидов является следствием особенностей их атомной структуры: они имеют одинаковое количество и тип валентных электронов в последнем шестом слое, несмотря на увеличение атомного числа. Эти валентные электроны, компенсируя увеличенный позитивный заряд в ядре, заполняют частично занятый 4f-подуровень. А поскольку он остается незаполненным, лантаноиды имеют похожие химические свойства[200].
Из-за увеличивающихся сил притяжения между позитивным зарядом в ядре и негативным в 4f-подуровне[200] лантаноиды имеют тенденцию к потере трёх электронов (образуя LnIII)[172] и уменьшению их атомного радиуса. Но существуют и исключения, когда определённые ионы элементов принимают «необычные» ионные состояния, например: в осно́вной среде европий может взять электрон и принять 2-валентное состояние (Eu2+), а в кислой церий может потерять его и стать 4-валентным (Ce4+)[200].
Уникальные спектроскопические свойства атомов группы объясняются радиальным увеличением 4f-орбитали, которое в свою очередь меньше увеличения заполненных 5s2 и 5p6 подуровней. Данное свойство наделяет элементы особенным вниманием со стороны исследователей в области фотоники, в частности в вопросах генерации света, его усиления и преобразования[201].
Лантан и лютеций, лантаноиды и актиноиды[править | править код]
Первым, кто подтвердил факт того, что лантаноидов должно быть именно 15, был Генри Мозли в 1914 г[129]. К лантаноидам принято относить именно 15 элементов, однако даже в настоящее время не существует общего соглашения относительно положения лантана, то есть образуют ли эту группу элементы от лантана до лютеция или от церия до лютеция[15][1][202]. В декабре 2015 г. ИЮПАК создал проект по изучению данного вопроса[203]. В научной статье Пекка Пюуккё, финского профессора химии Хельсинкского университета, высказывается мнение о трёх различных выходах для расположения f-элементов в периодической таблице[204][К 21]:
- первый предполагает ряд из 14 элементов, от La до Yb и от Ac до No; Lu и Lr помещаются в подгруппу скандия;
- второй так же — 14 элементов, только от Ce до Lu и от Th до Lr, а La и Ac помещаются в подгруппу скандия;
- третий предполагает включение 15 элементов (La—Lu, Ac—Th), поскольку большинство элементов III-валентны, а их ионный и ковалентный радиусы образуют непрерывный ряд.
Похожие споры порождает вопрос о положении семейства в периодической таблице: для ответа на него было предложено несколько различных представлений о периодической классификации, в которых смешивались элементы d- и f-блока[205][206]. По поводу большинства открытых к 1906 г. лантаноидов, не умещающихся в таблице, Д. И. Менделеев написал следующее[207]:
Тут мое личное мнение ещё ни на чём определённом не остановилось, и тут я вижу одну из труднейших задач, представляемых периодической законностью.
Биохимические свойства[править | править код]
| Общая информация | ||||
|---|---|---|---|---|
| Символ | CAS | Содержание в сыворотке крови человека[208][К 22], пг/мл | Токсикологические данные[209] | LD50[209] |
| La | 7439-91-0 | 62,7 ± 7,1 | У животных: инъекция соединений лантана приводит к гипергликемии, низкому давлению, дегенерации селезёнки и изменений в печени | Оксид лантана(III), орально, крысы: более 8,5 г/кг; мыши, внутрибрюшно: 530 мг/кг |
| Ce | 7440-45-1 | 214 ± 22 | Церий — сильный восстановитель, самовоспламеняется на воздухе от 65 до 80 °C. Пары, выделяемые при его горении, токсичны. Инъекции животным больших доз церия приводили к смерти от сердечно-сосудистой недостаточности. Оксид церия(IV) сильный окислитель при высоких температурах, реагирует с легковоспламеняющимися органическими материалами | Оксид церия(IV), орально, крысы: 5 г/кг, внутрикожно: 1—2 г/кг, вдыхание паров: 5,05 мг/л |
| Pr | 7440-10-0 | 11,1 ± 1,5 | — | — |
| Nd | 7440-00-8 | 33,7 ± 4,2 | Соединения неодима не были тщательно исследованы на токсичность. Неодимовая пыль и соли являются сильными ирритантами глаз и слизистой оболочки, умеренно раздражают кожу | Оксид неодима(III), орально, крысы: более 5 г/кг, мыши, внутрибрюшечно: 86 мг/кг. Соединение является мутагеном |
| Pm | 7440-12-2 | — | Какие органы поражаются при взаимодействии с металлом неизвестно; возможно, может присутствовать в костной ткани | — (без учёта радиоактивных свойств) |
| Sm | 7440-19-9 | 5,8 ± 1,1 | Суммарное содержание металла у взрослого человека составляет приблизительно 50 мкг, преимущественно в печени и почках, 8 мкг растворены в крови. Нерастворимые соли нетоксичны, растворимые — малотоксичны. При попадании в организм в кровь попадает лишь 0,05 % солей металла, остальные выводятся естественным путём. Из крови, примерно, 45 % попадает в печень, 45 % оседает на поверхности костей, где может находиться до 10 лет; 10 % из общего числа выводится | — |
| Eu | 7440-53-1 | 0,82 ± 0,19 | Ясных признаков токсичности металла по сравнению с тяжелыми металлами нет | Хлорид европия(III), внутрибрюшно: 550 мг/кг, орально: 5 г/кг. Нитрат европия(III), внутрибрюшно: 320 мг/кг, орально: 5 г/кг |
| Gd | 7440-54-2 | 7,2 ± 1,4 | В свободном состоянии ионы металла высокотоксичны; хелатные соединения, применяемые в магнитно-резонансной томографии, считаются достаточно безопасными. Токсичность зависит от силы хелатирующего агента. Анафилактические реакции происходят редко: приблизительно в 0,03—0,1 % случаев | — |
| Tb | 7440-27-9 | 1,30 ± 0,22 | — | — |
| Dy | 7429-91-6 | 9,6 ± 1,1 | Растворимые соли металла (например, хлорид диспрозия, нитрат диспрозия) малотоксичны при попадании в организм. Нерастворимые соли токсичных свойств не проявляют | Смертельная доза хлорида диспрозия на человека: более 500 г |
| Ho | 7440-60-0 | 2,55 ± 0,54 | — | — |
| Er | 7440-52-0 | 9,5 ± 1,9 | — | — |
| Tm | 7440-30-4 | 1,69 ± 0,42 | Растворимые соли металла считаются малотоксичными в больших количествах, нерастворимые — нетоксичны. Тулий не принимается корнями растений и таким образом не попадает в пищевую цепочку человека | — |
| Yb | 7440-64-4 | 13,2 ± 3,2 | Все соединения стоит рассматривать как высокотоксичные, поскольку вызывают раздражение кожи и глаз; некоторые из соединений могут быть тератогенными | — |
| Lu | 7439-94-3 | 2,46 ± 0,58 | Металл низкотоксичен. Фторид лютеция опасен при вдыхании, вызывает раздражение кожи. Порошок оксида лютеция токсичен и при вдыхании, и при проглатывании. Растворимые соли металла малотоксичны, нерастворимые — токсичны | — |
Фармакологические свойства лантаноидов таковы, что их содержание в организме снижает кровяное давление, уровень холестерина и глюкозы, уменьшает аппетит, препятствует свертыванию крови и предотвращает атеросклероз у подопытных животных. Потенциальное преимущество использования веществ в медицине с такими фармакологическими свойствами не оставит их в стороне от исследователей. Некоторые комплексы лантаноидов оказывают противовоспалительное воздействие; например, флогодин (англ. phlogodyn) довольно широко применяется в Венгрии[210].
Лантаноиды оказывают различное физиологическое воздействие на растения и животных и в основном считаются низкотоксичными. Только в последнее время изучение сфокусировалось на экологических аспектах влияния и их потенциально вредном воздействии на качество жизни[109].
Существует гипотеза, что в живых организмах редкоземельные элементы выполняют одинаковую функцию с кальцием. Из-за этого они и скапливаются в органах, содержание кальция в которых больше по сравнению с остальными. В грунтах содержание РЗЭ достигает 0,24 %. Из грунтов данные элементы попадают в растения. Наблюдается повышенное содержание в люпине, сахарной свёкле, чернике, разных водорослях и некоторых других растениях. В молоке, крови и костях животных, выявлено присутствие металлов цериевой группы[92].
Применение[править | править код]
Использование в промышленности металлов лантаноидов и их соединений начало значительно увеличиваться с прошлого века, начиная с раннего применения малых количеств оксидов церия и тория для создания калильных сеток в конце XIX века и не ограничиваясь критически важными компонентами в широком спектре передовых технологий[211].
Области потребления РЗЭ в 1975 г.[212] Металлургия (45 %) Катализаторы, химикалии (36 %) Оптические стёкла, керамика (17 %) Люминофоры, электроника (2 %) |
До 1950-х[править | править код]

К концу XIX века стало понятным, что дешевые при добыче монацитовые пески, состоящие из соединений церия, лантана, неодима, празеодима и больших количеств тория, находятся на территории США и Бразилии. Карл Ауэр фон Вельсбах (который был не только ученым, но и хорошим бизнесменом) обнаружил, что добавление примеси одного из соединений вышеуказанных элементов к диоксиду тория, составлявшему основу газокалильной сетки, позволяет добиться более яркого света огня и времени горения, чем его предыдущий «актинофор» (запатентованная в 1886 г. ученым смесь оксидов лантана и циркония). Потребовалось немного времени, чтобы понять, что примесью являлся церий, и определить «совершенное» соотношение тория к церию в усовершенствованной им калильной сетке: 99 к 1[215], которое не изменялось на протяжении долгого времени[20].
4 ноября 1891 г. учёный раскрыл и показал своё изобретение публике в Вене — этот день был началом применения редкоземельных элементов в промышленности. Автор нашел первое применение для загадочных в то время элементов: порядка 90 000 ламп было продано в первые 9 месяцев после запуска их производства на фабрике в Атцгерсдорфе, к 1913 г. общее количество возросло до 300 млн штук[215] (для которых требовалась переработка 3 000 т монацитового песка[216]), в 30-е годы — достигло 5 млрд[129][212]. Самыми крупными покупателями были железнодорожные компании, применявшие их внутри помещений, поскольку обходились дешевле электричества; вне помещений лампы освещали, например, улицы Бомбея — первого города, применившего их[215].
В 1915 г. вышла в печать книга Rare Earths. Their Occurence. Chemistry. And Technology, в которой описывались (возможные) сферы применения, отличные от, например, калильных сеток[217]. Существовали предложения использовать соли церия для дубления, производства эмалей, протравного крашения ализарином. В химии, двойной сульфат церия пришелся лучше других металлов (меди, железа и марганца) для каталитического окисления анилина в анилиновый чёрный — это одно из самых ранних исследований, датированное 1874 г., с акцентом на технологическом применении металла; для получения альдегидов, хинонов и т. п. соединений из ароматических углеводородов предполагалось использовать окислительные свойства его сульфата в растворе кислоты. Добавление соединений церия в электрод дуговой лампы позволяло добиться, по утверждению изобретателей, более интенсивного свечения. Незначительное применение так же нашли: оксалат церия — в медицине; сульфат церия пришелся полезным для цветной и черно-белой фотографии; глубокий цвет высшего оксида празеодима позволял применять его в составе дидима для маркировки текстиля и т. д.[16]
Благодаря огромному коммерческому успеху сеток и параллельному ему процессу выделения тория с большим количеством лантаноидов, со временем обнаружилось, что электролиз расплава хлорида, получавшегося после удаления ториевого остатка, давал пирофорный мишметалл (50 % Ce, 25 % La, 25 % — другие лантаноиды), добавление к которому 30 % Fe позволяло получать идеальный легкий кремень. Помимо этого, металлы применяли в специальных стёклах для контроля поглощения при определённых длинах волн — этим исчерпывалось применение металлов вплоть до 1940-х гг[20].
После 1950-х[править | править код]
| Функциональное использование лантаноидов[118][218][219] | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| La | Ce | Pr | Nd | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | |
| Аккумуляторы | ||||||||||||||
| Катализаторы | ||||||||||||||
| Полировальные порошки | ||||||||||||||
| Металлургия | ||||||||||||||
| Магниты | ||||||||||||||
| Керамика | ||||||||||||||
| Стекло | ||||||||||||||
| Люминофоры | ||||||||||||||
| Другие | ||||||||||||||
| — основное, — незначительное, — функциональное использование не наблюдается | ||||||||||||||
| Некоторые примеры использования лантаноидов[209] | |
|---|---|
| Металл | Применение |
| Eu, Tb | Люминесцентные лампы, светодиоды |
| Nd, Eu, Tb, Dy, Pr | Портативное беспроводное оборудование, смартфоны, мобильные телефоны и пр. |
| Eu, Tb, Er | Волоконная оптика |
| Eu, Tb, Gd, Pr, Ce | Плоскопанельные дисплеи |
| Nd, Tb, Pr, Dy | Медицинская визуализация (магнитно-резонансная томография), рентгенография |
| La | Электрические аккумуляторы |
| Nd, Pr, Dy, Tb | Гибридные автомобили, компьютерные диски, беспроводные электрические инструменты, ветрогенераторы и гидрогенераторы, система «старт-стоп» |
| La, Ce | Каталитический крекинг, системы очистки (например, очистка воды) |
Объём использования представителей семейства огромен: начиная от стекольной и заканчивая металлургической промышленностью; в качестве катализаторов на нефтеперерабатывающих заводах, люминесцентных активаторов, в электрокерамических соединениях, в высокотемпературных сверхпроводниках[220]. Несмотря на широкий спектр применения и обладание схожими химическими свойствами, некоторые металлы (Gd, Dy, Nd, Sm) имеют очень хорошие магнитные свойства, в то время как атомы Er и Tb обладают определёнными энергетическими состояниями, позволяющими использовать их в лазерах или световых приборах[5]. Современное использование металлов в высоких технологиях имеет под собой важное стратегическое значение[211].
Люминесцентные материалы[править | править код]
Как было описано выше, первое промышленное применение началось с добавления CeO2 в ThO2, что привело к более яркому свету при нагревании. В начале XX в. исследование Ж. Урбэном ионов EuIII, растворенных в различных матрицах, привело к открытию необычно яркого люминофора, излучающего оранжево-красный яркий свет (Y2O3:Eu [4—6 мол.%]). Этот люминофор использовался в люминесцентных лампах и электронно-лучевых трубках с начала 1960-х гг. и до сих пор используется для получения чистого красного цвета в светодиодах, дисплеях различных типов, включая плоскопанельные, несмотря на различные другие возможные и изученные (с ограниченным успехом) заместители[221].
Первое сообщение о получении лиганд-активированной (лиганд-сенсибилизированной) люминесценции лантаноидов в 1942 г. привело к последующим открытиям широкого спектра антенных лигандов, позволивших усилить эмиссию света[222][223]. С. Вайсмэном было доказано, что эмиссия комплексов Ln с органическими лигандами может быть осуществлена благодаря возбуждению электронных уровней в самом лиганде, после чего энергия собирается на возбуждённых состояниях ионов металла благодаря интрамолекулярной передаче энергии. Открытие получило название — антенный эффект[221].

Люминесцентные свойства ионов лантаноидов оказались важными для создания люминесцентных материалов, связанных с высокими технологиями[3]. Представители семейства применяются в плазменных панелях (например, допирование небольших количеств Eu3+ в Y2O3 — один из люминофоров, — позволяет достигнуть такой же интенсивности светоизлучения, что и у YBO3, Y1−xGdxBO3, но при меньшем давлении инертных газов в газонаполненных ячейках), FED-дисплеях (где полуторные оксиды люминофоров — более стабильные и экологичные, чем сульфидные, — допированы лантаноидами), в органических светодиодах (комплексные соединения Ln3+)[226].
Так же, их ионы нашли применение в высокоэнергетических детекторах радиации — сцинтилляторах; легированные с неорганическими кристаллами лантаноиды применяются в измерительных устройствах для регистрации γ-излучения и при рентгенографическом диагностировании. Быстрая эмиссия 5d → 4f у Ce3+ (продолжительностью 10—70 нс) делает его наилучшим кандидатом на использование в таких устройствах. Преимущество отдается соединениям с галогенидами, таких как LuI3:Ce3+, где световыход составляет 95 000 фотонов на 1 МэВ[226].
Магниты[править | править код]
История изучения постоянных магнитов на основе редкоземельных элементов берёт своё начало с 1959 г., в котором была опубликована работа по изучению сплава GdCo5. Впоследствии было опубликовано множество работ, касающихся способов получения, изучения, улучшения свойств YCo5, SmCo5 и примесей к нему[227][К 25]. К середине 1980-х гг. ученые получили три наиболее полезных сплава: SmCo5, Sm2Co17 и Nd2Fe14B. Каждый из них намного превосходит по своим полезным свойствам предыдущие типы магнитов, а лучшие — в десять раз сильнее альнико или ферритовых сплавов[228][229]. По максимальному показателю энергии продукта магниты можно расположить в следующем порядке: Nd2Fe14B (до 56,7 МГсЭ) > Sm2Co17 (22—32) > SmCo5 (22) > Альнико (до 11) > Ферриты (до 6)[230][К 26].
Магниты, состоящие из самария и кобальта (SmCo5), были разработаны в 1967 г.[227][231][К 27] и на протяжении долгого времени считались самыми сильными[232], однако в настоящее время используются реже неодимовых (в случаях, требующих устойчивость к коррозии или стойкость в эксплуатации при повышенных температурах[230]) из-за слабого магнитного поля и высокой стоимости его компонентов[233]: железо и неодим дешевле кобальта и самария соответственно, а сам сплав NdFeB содержит относительно меньшее количество лантаноида[228]. Самарий-кобальтовые магниты нашли своё применение в аэрокосмической и авиационной промышленности, требующих термической стабильности при 400—500 °C (предпочтение отдается Sm2Co17)[227].
Магнитные свойства неодима позволяют создавать мощнейшие постоянные магниты[234]. В 1984 г. был впервые получен сплав неодима, железа и бора (Nd2Fe14B)[228][235][236], широко используемый[К 28] в настоящее время во множестве технологий, требующих высокую коэрцитивную силу[233][237], и лучшая замена для которого до сих пор не найдена[238]. Неодим может быть замещен празеодимом и до 5 мас.% церием для увеличения конечной энергии продукта[239][240], а добавление тербия или диспрозия в сплав позволяет увеличить его коэрцитивность[227][241][242][243]. С другой стороны, из-за его термической демагнетизации, относительно низкая коэрцитивность[en] не может отвечать возрастающим к ней требованиям при работе высокотемпературных устройств, например, ветрогенераторов или некоторых элементов гибридных электромобилей[235][244][245][246].
Некоторые примеры использования магнитов: жесткие диски — 24,5 и 5,8 мас.% Nd и Pr соответственно (вес магнита 4,3 г; модель Seagate ST3500418AS, 2009 г.); 286 г Nd и 130 г Dy пришлось, в среднем, на каждый гибридный автомобиль (из 265 000 шт.), проданный в США и Германии в 2010 г.[118]; ветрогенераторы (приблизительно) — от 150 до 200 кг Nd и от 20 до 30 кг Dy на 1 МВт генерируемой мощности[247].

Гадолиний, его соли и сплавы играют заметную роль в магнитном охлаждении, в котором вещество нагревается, если его поместить во внешнее магнитное поле[9]. Первый эксперимент, благодаря которому удалось последовательно достичь снижения температуры до 0,25 K исследуемых образцов октагидрата сульфата гадолиния(III) (Gd2(SO4)3·8H2O) и результаты которого были предсказаны заранее, провели в 1933 г. У. Джиок и Д. МакДугалл[248]. (Позднее, в 1949 г. Джиоку была присуждена Нобелевская премия за изучение поведения веществ при сверхнизких температурах[249].) В настоящее время этот металл является одним из наиболее широко изученных охлаждающих магнитных материалов[250].
Промышленность[править | править код]
Изотопы гадолиния (155Gd, 157Gd) имеют необычно большое нейтронное сечение, которое позволяет использовать их в ядерной промышленности, например, в стержнях реактора[9]. Атомы гольмия, обладающие одним из наибольших магнитных моментов среди остальных элементов, позволяют создавать сильнейшие магнитные поля; данные сильные магниты, — одним из компонентов которых и является гольмий, — нашли своё применение в стержнях на АЭС[251][252][253].
Некоторые лантаноиды, например, церий из-за его экзотермической реакции с водородом (как и у остальных представителей) уже при комнатной температуре может быть использован в качестве газопоглотителя в электровакуумной промышленности и металлургии[50].
| Применение металлов в военных целях[254][255] | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Металл | Область применения | Технология | Пример | ||||||
| Nd, Pr, Sm, Dy, Tb | Системы управления и контроля | Сильные и компактные магниты | Ракеты Томагавк, высокоточные бомбы, JDAM, БПЛА | ||||||
| Большинство Ln | РЭБ | Накопление энергии, усиление плотности | Постановщики помех, электромагнитный рельсотрон, Система активного отбрасывания | ||||||
| Eu, Tb | Системы целенаведения | Усиление мощности и разрешающей способности | Лазерное наведение, лазеры воздушного базирования | ||||||
| Nd, Pr, Sm, Dy, Tb | Электромоторы | Сильные и компактные магниты | Интегрированный стартер-генератор, «Замволт» (DDG-1000), HMETD, JSF | ||||||
| Nd, La, Eu | Системы связи | Усиление и улучшение сигнала | Гидроакустические преобразователи, радары, MICAD | ||||||
Изготовленные на основе всех оксидов лантаноидов керамические пластинки обладают высокой гидрофобностью и прочностью, что позволяет использовать их там, где требуется соответствующие свойства, например: на лопастях турбин в электростанциях, через которые проходит пар, конденсируются капли воды (в диаметре несколько микрометров), что отрицательно сказывается на эффективности[256][257]. Данное свойство объясняется электронной структурой, которая препятствует образованию водородных связей с межфазными молекулами воды, и сохраняется даже после проверки в агрессивной среде (например, нагрев до высоких температур или обработка абразивными материалами). Более того, эти оксиды могут быть использованы для изготовления ультрагидрофобных поверхностей[258][259].
Отмечается эффективность (а также низкая токсичность при сравнении с хроматами[260][261]) применения лантана, церия и иттрия в качестве ингибиторов коррозии для алюминиевых и цинковых сплавов в водном растворе хлора[262][263][264][265][266], а также замедление коррозии железа и стали в газообразном растворе хлора[262][267][268][269][270][271]. Образование защитной плёнки, состоящей из комплекса гидратированных оксидов, происходит благодаря присутствию солей металлов в растворе, что подтверждается РФЭС[262][272]. Существует продолжающийся интерес исследователей к применению лантаноидов: свойства солей и их применение на ряде металлов было известно и изучалось на протяжении почти 30 лет, а основное внимание привлекали к себе церий и лантан. Большинство работ фокусировалось на алюминиевых сплавах; разработка конверсионных покрытий для других металлов происходила намного медленнее по различным причинам[273].

Металлы группы нашли своё применение в многослойных керамических конденсаторах (англ. Multilayer Ceramic Capacitor) — большинство лантаноидов (из которых выделяют Dy, Er и Ho) позволяет улучшить их свойства[164]: уменьшить тангенс угла потерь[274] и скорость старения[275][276][277], достичь стабильной ёмкости (±15 %) в широком промежутке температур (от −55 до +150 °C)[278]. Последний факт удовлетворяет требованиям EIA X8R и позволяет применять такие конденсаторы в высокотемпературных устройствах: наклонных скважинах (нефтеразведка), автомобилях, для военных нужд и в авиакосмической промышленности — все вышеперечисленные факты позволяют сделать вывод о высокой критичности лантаноидов (в виде примеси, допанта) при производстве конденсаторов с качественно хорошими характеристиками[164].
Современные электронные устройства содержат множество таких конденсаторов, ежегодный рост отгрузок с заводов которых составил 15 % в начале 2000-х гг.; в США их использовалось приблизительно 3 млрд/год[164][К 29]. Например, в мобильном телефоне содержится приблизительно 250 штук, 400 — в ноутбуке (лэптопе) и более 1000 в автомобильной электронике[279].
Медицина[править | править код]

Гадолиний в соединениях применяется в магнитно-резонансной томографии в качестве одного из лучших контрастирующих агентов, поскольку скапливается, например, в рубцовых тканях или опухолях, и «подсвечивает» такие ткани в МРТ[284]. А чтобы уменьшить негативное влияние на организм, ионы металла окружаются хелатирующими лигандами[9]. На территории Российской Федерации в продаже есть контрастные препараты под названиями «Гадовист», «Магневист»[285], содержащие ионы металла[281][286].
Сочетание инертных и биосовместимых наночастиц золота со стабильными ионами Ln3+, имеющими продолжительную люминесценцию или характерные магнитные характеристики, позволяет получить нанозонд, который бы подходил для применения в биомедицине или изучения биологических систем[287].
Длина волны гольмиевых лазеров составляет 2,08 мкм (излучение безопасно для зрения), что позволяет применять их в медицине, например, в виде гольмий-допированного алюмо-иттриевого граната (YAG) или иттрий-лантан-фторидных (YLF, LaYF4) лазеров[288]. Непрерывные эрбиевые и тулиевые импульсные лазеры, работающие на длине волны 3 мкм, подходят для применения в лазерной хирургии: рабочая длина волны совпадает с частотой колебаний атомов O—H в воде — достигается сильное поглощение луча биологическими тканями[289].
Поперечное сечение диспрозия позволяет использовать его для поглощения тепловых нейтронов, а высокая температура плавления позволяет применять в составе специальных сплавов нержавеющих сталей или в устройствах и деталях по ядерному контролю. При комбинировании металла с ванадием и другими редкоземельными элементами возможно использование в лазерных материалах. Халькогениды диспрозия-кадмия, являющиеся источниками инфракрасного излучения, нашли своё применение в изучении химических реакций[90].
Лантаноиды и лантан применяют как добавки к сталям, чугунам и другим сплавам для улучшения механической стойкости, коррозионной устойчивости и жаропрочности. Используют лантаноиды и лантан для получения специальных сортов стекла, в атомной технике. Соединения лантана, а также лантаноидов используют для изготовления лаков и красок, светящихся составов, в производстве кожи, в текстильной промышленности, в радиоэлектронике для изготовления катодов. Соединения лантаноидов применяются в лазерах.
Применение в будущем[править | править код]
Различные термодинамически устойчивые интерметаллиды состава LnxMy (где M = Mn, Fe, Co, Ni, Cu и нижестоящие под ними элементы в таблице) могут найти своё применение в виде наночастиц или тонких плёнок в области нанотехнологии, например: в фотокатодах, диэлектриках, сегнетоэлектриках, полупроводниках, выпрямителях (радиотехника и электроника), портативных компьютерах, стёклах (поглощающих УФ- и пропускающих ИК-излучение), постоянных магнитах (системы связи и компьютер), сверхпроводниках и композитных материалах, твердотельных лазерах (в особенности для военных нужд), люминофорах для цветных ТВ, катализаторах (регенерация выхлопных газов автомобилей) и водородных аккумуляторах. Более того, присутствие лантаноидов в металлических наночастицах увеличивает ударную вязкость, а также улучшает их структуру и пластичность[290].
Благодаря проведённым в Китае исследованиям были синтезированы ультратонкие нанокристаллы химически стабильных оксибромидов (OBr−3) европия, гадолиния, тербия и лантана, из которых последний, при допировании атомами Eu3+ (LaOBr:Eu3+), может быть использован для точного определения раковых клеток. Кристаллы могут приниматься этими больными (но не здоровыми) клетками, а благодаря люминесцентным свойствам и биосовместимости соединений, задаванию определённых длин волн отражающегося света (видного при подаче напряжения или под ультрафиолетом) и последующему подсвечиванию, их можно увидеть, например, через микроскоп. Все упомянутые свойства позволят онкологам определить мельчайшее количество больных клеток в пробах для биопсии[291][292].
Существует предположение об использовании оксибромидов лантаноидов в низкозатратных энергетических устройствах, использующих люминесцентные свойства, в качестве альтернативы, например, светодиодам[291].
Металлогели с изменяемым под УФ-излучением цветом, содержащие ионы Eu3+ и Tb3+ в различных определённых соотношениях, были разработаны в МТИ в 2015 г. Металлогели из ПЭГ, функционализированные терпиридиловыми лигандами, благодаря чувствительности к внешним взаимодействиям через проявление механо-, вапо-, термо- и хемохромизма, могут быть использованы в качестве тонкопленочных покрытий-индикаторов в растворе или газовой фазе вещества, например, для определения загрязнителей, токсинов, патогенов, изменения температуры и механического давления[293][294].
Существует предложение использовать лантаноиды в виде маркировочного материала (англ. taggant, от tag — бирка) для пометки исходного материала, идущего на создание конечного продукта, на каждой стадии его производства, чтобы контролировать и прослеживать поставщиков, продавцов и т. д. Отмечается его низкая стоимость по сравнению с обычными средствами борьбы с подделками (например, маркировка или чипование): достаточно нанести всего несколько частей на миллион такого вещества в ячейку матрицы для создания пометки[295].
См. также[править | править код]
Примечания[править | править код]
Комментарии
- ↑ По текущей рекомендации ИЮПАК, вместо термина лантаниды лучше использовать лантаноиды (подобные лантану, но не сам элемент), поскольку окончание -ид предпочтительно употреблять для обозначения отрицательных ионов, тогда как -оид указывает на сходство с одним из элементов химической группы или семейства
- ↑ В 1815 г., раньше открытия настоящего диоксида тория, была найдена «ториевая» земля, которая оказалась осно́вным фосфатом иттрия
- ↑ По другим данным: с 1843 по 1939 гг. было сделано более 70 заявлений об открытии различных представителей семейства (см. Biochemistry of the Lanthanides, 1990, p. 4)
- ↑ Символ точки с запятой («;») означает, что элемент был открыт независимо и отдельно одними исследователями от других
- ↑ Исследования К. Мосандера стали быстро известны благодаря нескольким сообщениям от Й. Берцелиуса своим коллегам. Об упоминании лантана в них см., например:
- Nouveau métal (фр.) // C.R. Hebd. Séances Acad. Sci. — 1839. — Vol. 8. — P. 356—357. — ISSN 00014036. Архивировано 9 марта 2016 года.
- Latanium — a New Metal (англ.) // The London and Edinburgh philosophical magazine and journal of science. — London, 1839. — Vol. XIV. — P. 390—391. — ISSN 1941-5966. Архивировано 1 апреля 2016 года.
- ↑ Термины иттриевая земля (yttria; оксид иттрия), цериевая земля (ceria; диоксид церия) и др. появились в ходе изучения и открытия оксидов новых элементов. В настоящее время они используются для указания их исторического происхождения
- ↑ Все известные земли, полученные после 1800 года, считались высшими оксидами соответствующих им элементов. См. Episodes from the History of the Rare Earth Elements, 1996, p. 40
- ↑ Данные цвета указаны для соединений с металлами, имеющими высшую степень окисления
- ↑ Позднее стало известным, что деципий по своим свойствам является гадолинием, открытым позже (см. Episodes from the History of the Rare Earth Elements, 1996, p. 59)
- ↑ Благодаря тому, что Жан Мариньяк подтвердил заявление М. Делафонтена о существовании тербия, был открыт иттербий. Название иттербию было дано исследователем благодаря нахождению (по его химическим свойствам) между иттрием и эрбием. (См. Handbook of the Physics and Chemistry of Rare Earths, 1988, p. 52 и Episodes from the History of the Rare Earth Elements, 1996, p. 60.) В том же году Делафонте нашел иттербий в сипилите (англ. sipylite) — минерале из Виргинии.
- ↑ В одной из работ ученого упоминается период времени, в котором производились исследования, касающиеся церия и иттрия: с января по март 1945 года. В ней же говорится о получении металлов «спектрографической чистоты». См. работу: Spedding F. H., Voigt A. F., Gladrow E. M., Sleight N. R. The Separation of Rare Earths by Ion Exchange.1,2I. Cerium and Yttrium // Journal of the American Chemical Society. — 1947. — Ноябрь (т. 69, № 11). — С. 2777—2781. — ISSN 0002-7863. — doi:10.1021/ja01203a058.
- ↑ Последнее значение дано без учёта падения цены на иттрий (в 64 раза); цены на скандий, лантан, церий, празеодим, неодим, прометий и самарий в источнике не указаны. Стоимость 1 грамма (более 99 % чистоты) Eu2O3 составила 1000 долл. США в 1949 г. и 12 — в 1957; Dy2O3 — 250 (1949) и 1,2 (1957); Ho2O3 — 900 и 2,2; Er2O3 — 900 и 1,35; Tm2O3 — 2800 и 13,35; Yb2O3 — 2000 и 13,35; Lu2O3 — 2000 и 13,35. См. источник: Spedding F. H. THE RARE-EARTH METALS // Metallurgical Reviews. — 1960. — Январь (т. 5, № 1). — С. 297—348. — ISSN 0076-6690. — doi:10.1179/mtlr.1960.5.1.297.
- ↑ Согласно источнику, поиск производился в Химической реферативной службе по словам scandium, yttrium, lanthanum и т. п. (на англ. языке), включая rare earth, lanthanide и lanthanoide, а также с использованием метода, позволяющего избежать пересечения данных при подсчётах.
- ↑ Прим. к карте: Мизери-Лейк и Хибины отмечены красной точкой, Маусе отмечен зелёной точкой, Стрендж-Лейк, Донгпао и Ловозеро — красно-зелёной.
Наиболее полный список всех известных месторождений, содержащих редкоземельные металлы, см. в:- The Rare Earths // Extractive Metallurgy of Rare Earths, Second Edition. — 2015. — 25 ноября. — С. 1—84. — ISBN 9781466576346. — doi:10.1201/b19055-2.;
- Greta J. Orris, Richard I. Grauch. Rare Earth Element Mines, Deposits, and Occurrences (англ.). Open-File Report 02-189. U.S. Department of the Interior, U.S. Geological Survey (2002). Дата обращения: 12 февраля 2016. Архивировано 18 июня 2015 года.;
- Weng Zhehan, Jowitt Simon M., Mudd Gavin M., Haque Nawshad. A Detailed Assessment of Global Rare Earth Element Resources: Opportunities and Challenges // Economic Geology. — 2015. — Vol. 110. — P. 1925-1952. — ISSN 0361-0128. — doi:10.2113/econgeo.110.8.1925. (помимо списка, выделяются и наиболее экономически привлекательные из них);
- Rare earth element mines, deposits, and occurrences (англ.). U.S. Department of the Interior, U.S. Geological Survey (24 сентября 2015). Дата обращения: 7 мая 2016. Архивировано 7 октября 2015 года.
- ↑ Согласно источнику, проценты вычислены из общемировых ресурсов оксидов РЗЭ (619 477 кт). В категорию «Другие» включены Афганистан, Аргентина, Финляндия, Перу, Швеция и т. д.
- ↑ 1 2 На горе Уэлд располагаются два соседних месторождения: Central Lanthanide Deposit (сокр. CLD, рус. Центральное месторождение лантаноидов) и Duncan
- ↑ Согласно источнику, возможность замены элементов приведена по шкале от 0 до 100, где 0 указывает на показательную заменимость элемента, существующую для всех основных видов применения, а 100 — отсутствие таковой для большинства видов даже с «адекватными характеристиками»: La — 75, Ce — 60, Pr — 41, Nd — 41, Sm — 38, Eu — 100, Gd, Tb, Ho, Er, Lu — 63, Tm и Yb — 88. Полные данные доступны как по web-ссылкам в источнике, так и по нижеследующим: http://www.pnas.org/content/suppl/2013/11/29/1312752110.DCSupplemental/pnas.201312752SI.pdf Архивная копия от 24 января 2019 на Wayback Machine и http://www.pnas.org/lookup/suppl/doi:10.1073/pnas.1312752110/-/DCSupplemental/st01.docx
- ↑ Согласно источнику, потребление металлов в стране значительно выросло с 2004 г. и составляет 70 % от общемирового. См.: Campbell Gary A. Rare earth metals: a strategic concern // Mineral Economics. — 2014. — 11 апреля (т. 27, № 1). — С. 21—31. — ISSN 2191-2203. — doi:10.1007/s13563-014-0043-y.
- ↑ Электронные конфигурации указаны в виде: [Xe] указанная конфигурация 6s2
- ↑ CAS-номер: 54375-47-2
- ↑ Согласно статье, первый вариант был выбран У. Дженсеном (doi:10.1007/s10698-015-9216-1) и Википедией; второй — Л. Ловелем (doi:10.1021/ed085p1482), Королевским химическим обществом и Американским химическим обществом; третий — ИЮПАК Архивная копия от 30 августа 2016 на Wayback Machine и самими авторами статьи: «Для нас основное состояние атома менее важно, чем химическая связь, в рассмотренных до сих пор системах»
- ↑ Согласно источнику, приведены усреднённые данные 5 здоровых человек (четверо мужчин и одна женщина), сдавших кровь. Относительное стандартное отклонение находится в пределах от 10,4 % (Ce) до 24,9 % (Tm). Исследования проведены благодаря применению ИСП-МС.
- ↑ Указаны массовые проценты, на которые пришлось 35 500 т. См. источник к диаграмме
- ↑ Проценты на круговой диаграмме указаны из расчёта годового потребления металлов (124 000 т) за 2009 г. См. источник к диаграмме
- ↑ Согласно другому источнику, история изучения постоянных магнитов на основе редкоземельных элементов берёт своё начало с 1966 г., в котором сотрудники Исследовательской лаборатории ВВС США получили сплав YCo5. См.: Cullity B. D., Graham C. D. Introduction to Magnetic Materials. — 2nd ed. — New Jersey: John Wiley & Sons, Inc., 2008. — 544 p. — ISBN 9780471477419, 9780470386323. — doi:10.1002/9780470386323.
- ↑ Согласно другому источнику, максимальная энергия продукта для неодимового магнита в 59,5 МГсЭ была достигнута в 2006 г. в компании Nippon Sumitomo. Коммерчески доступные неодимовые магниты имеют такое значение до 52 МГсЭ. См.: Pan Shuming. Rare Earth Permanent-Magnet Alloys’ High Temperature Phase Transformation. — 2013. — doi:10.1007/978-3-642-36388-7.
- ↑ По другим данным, сплав SmCo5 был разработан в 1970-х гг. (см. Manufacturing Methods for Samarium Cobalt Magnets. — Defense Technical Information Center, 1971. — 152 p. и Cullity B. D., Graham C. D. Introduction to Magnetic Materials. — 2nd ed. — New Jersey: John Wiley & Sons, Inc., 2008. — 544 p. — ISBN 9780471477419, 9780470386323. — doi:10.1002/9780470386323.), а попал под внимание ученых ещё в 1960 г. (см. Nassau K., Cherry L.V., Wallace W.E. Intermetallic compounds between lanthanons and transition metals of the first long period // Journal of Physics and Chemistry of Solids. — 1960. — Ноябрь (т. 16, № 1-2). — С. 131—137. — ISSN 0022-3697. — doi:10.1016/0022-3697(60)90083-4.)
- ↑ Выпуск NdFeB магнитов составил более 60000 т в 2008 г. Приблизительная общая стоимость проданных постоянных магнитов (из основных) в 2010 г. составила 9 млрд долл. США, из которых 62 % приходилось на NdFeB и 3 % на SmCo (на альнико и ферритовые магниты пришлось 1 % и 34 % соответственно). См.:
- Coey J.M.D. Permanent magnets: Plugging the gap // Scripta Materialia. — 2012. — Сентябрь (т. 67, № 6). — С. 524—529. — ISSN 1359-6462. — doi:10.1016/j.scriptamat.2012.04.036.;
- Gutfleisch Oliver, Willard Matthew A., Brück Ekkes, Chen Christina H., Sankar S. G., Liu J. Ping. Magnetic Materials and Devices for the 21st Century: Stronger, Lighter, and More Energy Efficient // Advanced Materials. — 2010. — 15 декабря (т. 23, № 7). — С. 821—842. — ISSN 0935-9648. — doi:10.1002/adma.201002180..
- ↑ Согласно источнику к предложению, информация по увеличению отгрузки с заводов приведена из данных, датируемых 2002 годом (см. дополнительно: Electrical Industry Alliance (EIA), World Capacitor Trade Statistics (WCTA), 2002), а данные по потреблению в США датируются 2011 годом (см. дополнительно: M.Kahn, Multilayer Ceramic Capacitors: Material and Manufacture, AVX technical Information, Myrtle Beach, SC, 2011)
Источники
- ↑ 1 2 Nomenclature of Inorganic Chemistry. IUPAC Recommendations / Eds.: Neil G. Connelly, Ture Damhus, Richard M. Hartshorn, Alan T. Hutton. — RSC Publishing, 2005. — P. 51, 52. — 366 p. — ISBN 0-85404-438-8. Архивировано 19 декабря 2019 года.
- ↑ CRC Handbook, 2009, p. 2—56.
- ↑ 1 2 3 4 The rare earth elements: fundamentals and applications, 2012, p. 112.
- ↑ The Elements, 2009, p. 135.
- ↑ 1 2 3 4 Zepf Volker. An Overview of the Usefulness and Strategic Value of Rare Earth Metals // Rare Earths Industry. — 2016. — P. 3-17. — ISBN 9780128023280. — doi:10.1016/B978-0-12-802328-0.00001-2.
- ↑ Biochemistry of the Lanthanides, 1990, p. 41.
- ↑ Bünzli Jean-Claude G. Lanthanides // Kirk-Othmer Encyclopedia of Chemical Technology. — 2013. — ISBN 0471238961. — doi:10.1002/0471238961.1201142019010215.a01.pub3.
- ↑ Lanthanoid (англ.). — статья из Encyclopædia Britannica Online. Дата обращения: 10 сентября 2015. Архивировано 5 сентября 2015 года.
- ↑ 1 2 3 4 5 6 Pyykkö Pekka. Magically magnetic gadolinium // Nature Chemistry. — 2015. — Август (т. 7, № 8). — С. 680—680. — ISSN 1755-4330. — doi:10.1038/nchem.2287.
- ↑ 1 2 Biochemistry of the Lanthanides, 1990, pp. 41—42.
- ↑ 1 2 3 Свойства элементов, 1985, с. 549.
- ↑ Hakala Reino W. Letters // Journal of Chemical Education. — 1952. — Ноябрь (т. 29, № 11). — С. 581. — ISSN 0021-9584. — doi:10.1021/ed029p581.2.
- ↑ Brian, M. Victor Moritz Goldschmidt: father of modern geochemistry. — San Antonio, Tex: Geochemical Society, 1992. — ISBN 0-941809-03X. Архивировано 7 декабря 2015 года.
- ↑ Goldschmidt V. M., Barth T., Lunde G. Geochemical distribution law of the elements. V. Isomorphy and polymorphy of the sesquioxides. The contraction of the «lanthanums» and its consequences // Skrifter Norske Videnskaps-Akademi i Oslo, I. Mat.-Naturv. Klasse. — 1925. — Т. 7. — С. 59.
- ↑ 1 2 3 Chemistry of the elements, 1997, p. 1227.
- ↑ 1 2 Levy, S.I. The Rare Earths: Their Occurrence, Chemistry, and Technology. — London: E. Arnold, 1915. — 345 p.
- ↑ Episodes from the History of the Rare Earth Elements, 1996, pp. 40—41.
- ↑ The Periodic Table of the Elements // Chemistry International -- Newsmagazine for IUPAC. — 2004. — Январь (т. 26, № 1). — ISSN 1365-2192. — doi:10.1515/ci.2004.26.1.8.
- ↑ 1 2 3 Biochemistry of the Lanthanides, 1990, p. 2.
- ↑ 1 2 3 4 5 6 Chemistry of the elements, 1997, p. 1228.
- ↑ Episodes from the History of the Rare Earth Elements, 1996, p. 70.
- ↑ 1 2 Handbook of the Physics and Chemistry of Rare Earths, 1988, p. 46.
- ↑ 1 2 Episodes from the History of the Rare Earth Elements, 1996, p. 49.
- ↑ Habashi F. Extractive metallurgy of rare earths // Canadian Metallurgical Quarterly. — 2013. — Июль (т. 52, № 3). — С. 224—233. — ISSN 0008-4433. — doi:10.1179/1879139513Y.0000000081.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 Episodes from the History of the Rare Earth Elements, 1996, p. xxii.
- ↑ 1 2 v. Welsbach Carl Auer. Die Zerlegung des Didyms in seine Elemente // Monatshefte für Chemie und verwandte Teile anderer Wissenschaften. — 1885. — Декабрь (т. 6, № 1). — С. 477—491. — ISSN 0343-7329. — doi:10.1007/BF01554643.
- ↑ Marinsky J. A., Glendenin L. E., Coryell C. D. The Chemical Identification of Radioisotopes of Neodymium and of Element 611 // Journal of the American Chemical Society. — 1947. — Ноябрь (т. 69, № 11). — С. 2781—2785. — ISSN 0002-7863. — doi:10.1021/ja01203a059.
- ↑ Lecoq de Boisbaudran, P. E. Nouvelles raies spectrales observées dans des substances extraites de la samaskite (фр.) // C.R. Hebd. Séances Acad. Sci. — 1879. — Vol. 88. — P. 322—323. — ISSN 00014036. Архивировано 9 марта 2016 года.
- ↑ Lecoq de Boisbaudran, P. E. Recherches sur le samarium, radical d'une terre nouvelle extraite de la samarskite (фр.) // C.R. Hebd. Séances Acad. Sci. — 1879. — Vol. 89. — P. 212—214. — ISSN 00014036. Архивировано 12 декабря 2018 года.
- ↑ Demarçay, E. Sur un nouvel élément contenu dans les terres rares voisines du samarium (фр.) // C.R. Hebd. Séances Acad. Sci. — 1896. — Vol. 122. — P. 728—730. — ISSN 00014036. Архивировано 13 декабря 2018 года.
- ↑ Demarçay, E. Sur un nouvel élément, l'europium (фр.) // C.R. Hebd. Séances Acad. Sci. — 1901. — Vol. 132. — P. 1484—1486. — ISSN 00014036. Архивировано 24 декабря 2013 года.
- ↑ Lecoq de Boisbaudran, P. E. Le Yα de M. de Marignac est définitivement nomme gadolinium (фр.) // C.R. Hebd. Séances Acad. Sci. — 1886. — Vol. 102. — P. 902. — ISSN 00014036. Архивировано 8 марта 2016 года.
- ↑ 1 2 3 Mosander C.G. XXX. On the new metals, lanthanium and didymium, which are associated with cerium; and on erbium and terbium, new metals associated with yttria // The London, Edinburgh, and Dublin Philosophical Magazine and Journal of Science. — 1843. — Октябрь (т. 23, № 152). — С. 241—254. — ISSN 1941-5966. — doi:10.1080/14786444308644728.
- ↑ Lecoq de Boisbaudran, P. E. L'holmine (ou terre X de M. Soret) contient au moins deux radicaux métalliques (фр.) // C.R. Hebd. Séances Acad. Sci. — 1886. — Vol. 102. — P. 1003. — ISSN 00014036. Архивировано 9 марта 2016 года.
- ↑ Lecoq de Boisbaudran, P. E. Sur le dysprosium (фр.) // C.R. Hebd. Séances Acad. Sci. — 1886. — Vol. 102. — P. 1005. — ISSN 00014036. Архивировано 10 марта 2016 года.
- ↑ 1 2 Soret, J.-L. Sur le spectre des terres faisant partie du groupe de l'yttria (фр.) // C.R. Hebd. Séances Acad. Sci. — 1879. — Vol. 89. — P. 521—523. — ISSN 00014036. Архивировано 20 ноября 2018 года.
- ↑ Marignac, J. C. Sur l'ytterbine, nouvelle terre contenue dans la gadolinite (фр.) // C.R. Hebd. Séances Acad. Sci. — 1878. — Vol. 87. — P. 578—581. — ISSN 00014036. Архивировано 9 марта 2016 года.
- ↑ Episodes from the History of the Rare Earth Elements, 1996, p. 73.
- ↑ Urbain, G. Un nouvel élément : le lutécium, résultant du dédoublement de l'ytterbium de Marignac (фр.) // C.R. Hebd. Séances Acad. Sci. — 1907. — Vol. 145. — P. 759—762. — ISSN 00014036. Архивировано 9 марта 2016 года.
- ↑ Голуб, 1971, с. 193.
- ↑ Выдающиеся химики мира, 1991, с. 541.
- ↑ 1 2 Episodes from the History of the Rare Earth Elements, 1996, p. xvii.
- ↑ 1 2 3 Lanthanides, Tantalum and Niobium, 1989, p. VI.
- ↑ 1 2 CRC Handbook, 2009, pp. 4—9.
- ↑ Выдающиеся химики мира, 1991, с. 542.
- ↑ 1 2 Голуб, 1971, с. 194.
- ↑ Популярная библиотека химических элементов, 1983, с. 109.
- ↑ 1 2 CRC Handbook, 2009, pp. 4—19.
- ↑ Episodes from the History of the Rare Earth Elements, 1996, p. 44.
- ↑ 1 2 Популярная библиотека химических элементов, 1983, с. 108.
- ↑ CRC Handbook, 2009, pp. 4—20.
- ↑ 1 2 3 Handbook of the Physics and Chemistry of Rare Earths, 1988, p. 44.
- ↑ Episodes from the History of the Rare Earth Elements, 1996, p. 45.
- ↑ Episodes from the History of the Rare Earth Elements, 1996, p. 45: «Dark brown on the surface, sometimes light brown in the fracture <…>».
- ↑ 1 2 3 Episodes from the History of the Rare Earth Elements, 1996, pp. 45—46.
- ↑ 1 2 Handbook of the Physics and Chemistry of Rare Earths, 1988, p. 43.
- ↑ Курилов В. В., Менделеев Д. И. Дидимий, химический элемент // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- ↑ Episodes from the History of the Rare Earth Elements, 1996, p. 46.
- ↑ Handbook of the Physics and Chemistry of Rare Earths, 1988, p. 45.
- ↑ 1 2 3 Популярная библиотека химических элементов, 1983, с. 149.
- ↑ Популярная библиотека химических элементов, 1983, с. 154.
- ↑ Выдающиеся химики мира, 1991, с. 552.
- ↑ 1 2 3 4 Episodes from the History of the Rare Earth Elements, 1996, p. 55.
- ↑ 1 2 Episodes from the History of the Rare Earth Elements, 1996, p. 59.
- ↑ CRC Handbook, 2009, p. 4—13.
- ↑ 1 2 3 Голуб, 1971, с. 195.
- ↑ Handbook of the Physics and Chemistry of Rare Earths, 1988, p. 47.
- ↑ Handbook of the Physics and Chemistry of Rare Earths, 1988, p. 49.
- ↑ 1 2 Handbook of the Physics and Chemistry of Rare Earths, 1988, pp. 49—50.
- ↑ Young C. A. Letter to the superintendent of the U. S. Coast Survey, containing a catalogue of bright lines in the spectrum of the solar atmosphere, observed at Sherman, Wyoming territory, USA, during July and August, 1872 // American Journal of Science. — 1872. — 1 ноября (т. s3-4, № 23). — С. 356—361. — ISSN 0002-9599. — doi:10.2475/ajs.s3-4.23.356.
- ↑ Popp O. Untersuchung über die Yttererde // Annalen der Chemie und Pharmacie. — 1864. — Т. 131, № 2. — С. 179—201. — ISSN 0075-4617. — doi:10.1002/jlac.18641310206.
- ↑ Handbook of the Physics and Chemistry of Rare Earths, 1988, p. 48.
- ↑ 1 2 3 Handbook of the Physics and Chemistry of Rare Earths, 1988, p. 52.
- ↑ Менделеев Д. И. Естественная система элементов и применение её к указанию свойств неоткрытых элементов // Журнал Русского химического общества. — 1871. — Т. III. — С. 25—56. Архивировано 17 марта 2014 года.
- ↑ 1 2 3 4 Episodes from the History of the Rare Earth Elements, 1996, p. 62.
- ↑ 1 2 Biochemistry of the Lanthanides, 1990, p. 5.
- ↑ Episodes from the History of the Rare Earth Elements, 1996, p. 69.
- ↑ Episodes from the History of the Rare Earth Elements, 1996, p. 37.
- ↑ 1 2 Biochemistry of the Lanthanides, 1990, p. 4.
- ↑ Episodes from the History of the Rare Earth Elements, 1996, p. 56.
- ↑ 1 2 Episodes from the History of the Rare Earth Elements, 1996, p. 68.
- ↑ Выдающиеся химики мира, 1991, с. 565.
- ↑ Handbook of the Physics and Chemistry of Rare Earths, 1988, pp. 55—56.
- ↑ 1 2 3 4 Handbook of the Physics and Chemistry of Rare Earths, 1988, p. 56.
- ↑ 1 2 3 Episodes from the History of the Rare Earth Elements, 1996, p. 60.
- ↑ Handbook of the Physics and Chemistry of Rare Earths, 1988, p. 61.
- ↑ 1 2 Episodes from the History of the Rare Earth Elements, 1996, p. 64.
- ↑ CRC Handbook, 2009, p. 4—23.
- ↑ CRC Handbook, 2009, p. 4—28.
- ↑ 1 2 CRC Handbook, 2009, p. 4—11.
- ↑ Episodes from the History of the Rare Earth Elements, 1996, pp. 68—69.
- ↑ 1 2 3 4 Голуб, 1971, с. 196.
- ↑ Лаврухина А.К., Поздняков А.А. Аналитическая химия технеция, прометия, астатина и франция. — М.: "Наука", 1966. — С. 108—109. — 307 с. — (Аналитическая химия элементов). — 3200 экз.
- ↑ Discovery of Promethium (англ.). Oak-Ridge National Laboratory. Дата обращения: 23 июля 2015. Архивировано из оригинала 5 марта 2016 года.
- ↑ Редкол.: Зефиров Н. С. (гл. ред.). Химическая энциклопедия: в 5 т. — М.: Большая Российская энциклопедия, 1995. — Т. 4. — С. 101. — 639 с. — 20 000 экз. — ISBN 5-85270-092-4.
- ↑ Популярная библиотека химических элементов, 1983, с. 137.
- ↑ 1 2 Spedding F. H. THE RARE-EARTH METALS // Metallurgical Reviews. — 1960. — Январь (т. 5, № 1). — С. 297—348. — ISSN 0076-6690. — doi:10.1179/mtlr.1960.5.1.297.
- ↑ Klemm W., Bommer H. Zur Kenntnis der Metalle der seltenen Erden // Zeitschrift f�r anorganische und allgemeine Chemie. — 1937. — 8 марта (т. 231, № 1-2). — С. 138—171. — ISSN 0863-1786. — doi:10.1002/zaac.19372310115.
- ↑ 1 2 Gschneidner Karl A. Systematics // Including Actinides. — 2016. — С. 1—18. — ISBN 9780444638519. — ISSN 0168-1273. — doi:10.1016/bs.hpcre.2016.07.001.
- ↑ Two-hundred-year impact of rare earths on science // Handbook of the Physics and Chemistry of Rare Earths / Ed.: Karl A. Gschneidner, Jr.; LeRoy Eyring. — Amsterdam: North-Holland, 1988. — Vol. 11. — P. 319. — 594 p. — ISBN 0444870806, 9780444870803.
- ↑ Hirano S., Suzuki K. T. Exposure, metabolism, and toxicity of rare earths and related compounds. (англ.) // Environmental health perspectives. — 1996. — Vol. 104 Suppl 1. — P. 85—95. — PMID 8722113.
- ↑ Nezu N., Asano M., Ouchi S. Cerium-144 in Food // Science. — 1962. — 12 января (т. 135, № 3498). — С. 102—103. — ISSN 0036-8075. — doi:10.1126/science.135.3498.102.
- ↑ LIEBSCHER K., SCHÖNFELD T., SCHALLER A. Concentration of Inhaled Cerium-144 in Pulmonary Lymph Nodes of Human Beings // Nature. — 1961. — Декабрь (т. 192, № 4809). — С. 1308—1308. — ISSN 0028-0836. — doi:10.1038/1921308a0.
- ↑ Hughes A.E., Mol J.M.C., Cole I.S. The cost and availability of rare earth-based corrosion inhibitors // Rare Earth-Based Corrosion Inhibitors. — 2014. — С. 291—305. — ISBN 9780857093479. — doi:10.1533/9780857093585.291.
- ↑ B.R.W. Hinton, D.R. Arnott; N.E. Ryan. The inhibition of aluminium alloy corrosion by cerous cations // Metals forum. — Pergamon Press, 1984. — С. 211—217. — ISSN 0160-7952. Архивировано 24 сентября 2016 года.
- ↑ Arnott D.R., Ryan N.E., Hinton B.R.W., Sexton B.A., Hughes A.E. Auger and XPS studies of cerium corrosion inhibition on 7075 aluminum alloy // Applications of Surface Science. — 1985. — Май (т. 22-23). — С. 236—251. — ISSN 0378-5963. — doi:10.1016/0378-5963(85)90056-X.
- ↑ 1 2 3 Adachi Gin-ya, Imanaka Nobuhito, Tamura Shinji. Research trends in rare earths: A preliminary analysis // Journal of Rare Earths. — 2010. — Декабрь (т. 28, № 6). — С. 843—846. — ISSN 1002-0721. — doi:10.1016/S1002-0721(09)60207-6.
- ↑ 1 2 Голуб, 1971, с. 197.
- ↑ 1 2 3 4 Goecke Franz, Jerez Celia G., Zachleder Vilém, Figueroa Félix L., BiÅ¡ová KateÅ™ina, Řezanka Tomáš, VÃtová Milada. Use of lanthanides to alleviate the effects of metal ion-deficiency in Desmodesmus quadricauda (Sphaeropleales, Chlorophyta) // Frontiers in Microbiology. — 2015. — 28 января (т. 6). — ISSN 1664-302X. — doi:10.3389/fmicb.2015.00002.
- ↑ Wind Energy Deployment and the Relevance of Rare Earths, 2014, p. 22.
- ↑ Wind Energy Deployment and the Relevance of Rare Earths, 2014, pp. 17—18.
- ↑ Voncken J. H. L. The Ore Minerals and Major Ore Deposits of the Rare Earths // SpringerBriefs in Earth Sciences. — 2015. — 25 декабря. — С. 15—52. — ISBN 9783319268071. — ISSN 2191-5369. — doi:10.1007/978-3-319-26809-5_2.
- ↑ Smith M.P., Moore K., Kavecsánszki D., Finch A.A., Kynicky J., Wall F. From mantle to critical zone: A review of large and giant sized deposits of the rare earth elements // Geoscience Frontiers. — 2016. — Май (т. 7, № 3). — С. 315—334. — ISSN 1674-9871. — doi:10.1016/j.gsf.2015.12.006.
- ↑ 1 2 Weng Zhehan, Jowitt Simon M., Mudd Gavin M., Haque Nawshad. A Detailed Assessment of Global Rare Earth Element Resources: Opportunities and Challenges // Economic Geology. — 2015. — 9 ноября (т. 110, № 8). — С. 1925—1952. — ISSN 0361-0128. — doi:10.2113/econgeo.110.8.1925.
- ↑ El Tan; Yuko Inoue (4 июля 2011). "Huge rare earth deposits found in Pacific: Japan experts" (англ.). Reuters. Архивировано из оригинала 24 сентября 2015. Дата обращения: 29 июля 2015.
{{cite news}}: Неизвестный параметр|coauthors=игнорируется (|author=предлагается) (справка)Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ 1 2 Jones Nicola. Sea holds treasure trove of rare-earth elements // Nature. — 2011. — 3 июля. — ISSN 1476-4687. — doi:10.1038/news.2011.393.
- ↑ 1 2 Kato Yasuhiro, Fujinaga Koichiro, Nakamura Kentaro, Takaya Yutaro, Kitamura Kenichi, Ohta Junichiro, Toda Ryuichi, Nakashima Takuya, Iwamori Hikaru. Deep-sea mud in the Pacific Ocean as a potential resource for rare-earth elements // Nature Geoscience. — 2011. — 3 июля (т. 4, № 8). — С. 535—539. — ISSN 1752-0894. — doi:10.1038/NGEO1185.
- ↑ 1 2 3 4 5 6 Zepf Volker. Rare Earth Elements // Springer Theses. — 2013. — ISBN 9783642354571. — ISSN 2190-5053. — doi:10.1007/978-3-642-35458-8.
- ↑ USGS, Hedrick J.B. Rare Earths (англ.) (Minerals yearbook) (2000). Дата обращения: 10 февраля 2016. Архивировано 8 марта 2016 года.
- ↑ Chen Zhanheng. Outline on the development and Policies of China Rare Earth industry (англ.) (7 апреля 2010). Дата обращения: 10 февраля 2016. Архивировано 9 июня 2011 года.
- ↑ C. Wu, Z. Yuan, G. Bai. Rare earth deposits in China // Rare Earth Minerals: Chemistry, origin and deposits / Eds.: Adrian P. Jones, Frances Wall, C. Terry Williams. — Chapman & Hall, 1996. — P. 281—310. — ISBN 0412610302. Архивировано 16 февраля 2016 года.
- ↑ Zhi Li L., Yang X. China’s rare earth ore deposits and beneficiation techniques. — Proceedings of ERES2014: 1st European rare earth resources conference, Milos, 2014. — С. 26—36. Архивировано 19 января 2020 года.
- ↑ Goodenough Kathryn M., Wall Frances. Critical Metal Mineralogy: Preface to the special issue of Mineralogical Magazine // Mineralogical Magazine. — 2016. — Февраль (т. 80, № 01). — С. 1—4. — ISSN 0026-461X. — doi:10.1180/minmag.2016.080.000.
- ↑ Kynicky J., Smith M. P., Xu C. Diversity of Rare Earth Deposits: The Key Example of China // Elements. — 2012. — 1 октября (т. 8, № 5). — С. 361—367. — ISSN 1811-5209. — doi:10.2113/gselements.8.5.361.
- ↑ YANG Ruidong, WANG Wei, ZHANG Xiaodong, LIU Ling, WEI Huairui, BAO Miao, WANG Jingxin. A new type of rare earth elements deposit in weathering crust of Permian basalt in western Guizhou, NW China // Journal of Rare Earths. — 2008. — Октябрь (т. 26, № 5). — С. 753—759. — ISSN 1002-0721. — doi:10.1016/S1002-0721(08)60177-5.
- ↑ 1 2 Eggert Roderick, Wadia Cyrus, Anderson Corby, Bauer Diana, Fields Fletcher, Meinert Lawrence, Taylor Patrick. Rare Earths: Market Disruption, Innovation, and Global Supply Chains // Annual Review of Environment and Resources. — 2016. — Ноябрь (т. 41, № 1). — С. 199—222. — ISSN 1543-5938. — doi:10.1146/annurev-environ-110615-085700.
- ↑ 2009 Minerals Yearbook (Rare Earths, Advance Release) (англ.) P. 6-10. U.S. Geological Survey; U.S. Department of the Interior (июль 2011). Дата обращения: 8 августа 2015. Архивировано 4 марта 2016 года.
- ↑ 2011 Minerals Yearbook (Rare Earths, Advance Release) (англ.) P. 6-7. U.S. Geological Survey; U.S. Department of the Interior (сентябрь 2013). Дата обращения: 8 августа 2015. Архивировано 22 марта 2015 года.
- ↑ 1 2 3 Klinger Julie Michelle. A historical geography of rare earth elements: From discovery to the atomic age // The Extractive Industries and Society. — 2015. — Июль. — ISSN 2214-790X. — doi:10.1016/j.exis.2015.05.006.
- ↑ Castilloux, R. Rare Earth Market Outlook: Supply, Demand, and Pricing from 2014 through 2020 (англ.). Ontario, Canada: Adamas Intelligence (2014). Дата обращения: 20 сентября 2015. Архивировано из оригинала 27 сентября 2015 года.
- ↑ 1 2 Mancheri Nabeel A. An Overview of Chinese Rare Earth Export Restrictions and Implications // Rare Earths Industry. — 2016. — P. 21-36. — ISBN 9780128023280. — doi:10.1016/B978-0-12-802328-0.00002-4.
- ↑ Campbell Gary A. Rare earth metals: a strategic concern // Mineral Economics. — 2014. — 11 апреля (т. 27, № 1). — С. 21—31. — ISSN 2191-2203. — doi:10.1007/s13563-014-0043-y.
- ↑ Jaireth Subhash, Hoatson Dean M., Miezitis Yanis. Geological setting and resources of the major rare-earth-element deposits in Australia // Ore Geology Reviews. — 2014. — Октябрь (т. 62). — С. 72—128. — ISSN 0169-1368. — doi:10.1016/j.oregeorev.2014.02.008.
- ↑ Goodenough K.M., Schilling J., Jonsson E., Kalvig P., Charles N., Tuduri J., Deady E.A., Sadeghi M., Schiellerup H., Müller A., Bertrand G., Arvanitidis N., Eliopoulos D.G., Shaw R.A., Thrane K., Keulen N. Europe's rare earth element resource potential: An overview of REE metallogenetic provinces and their geodynamic setting // Ore Geology Reviews. — 2016. — Январь (т. 72). — С. 838—856. — ISSN 0169-1368. — doi:10.1016/j.oregeorev.2015.09.019.
- ↑ Mariano A. N., Mariano A. Rare Earth Mining and Exploration in North America // Elements. — 2012. — 1 октября (т. 8, № 5). — С. 369—376. — ISSN 1811-5209. — doi:10.2113/gselements.8.5.369.
- ↑ Klyucharev Dmitry S., Volkova Nataliya M., Comyn Mikhail F. The problems associated with using non-conventional rare-earth minerals // Journal of Geochemical Exploration. — 2013. — Октябрь (т. 133). — С. 138—148. — ISSN 0375-6742. — doi:10.1016/j.gexplo.2013.03.006.
- ↑ Binnemans Koen, Jones Peter Tom. Rare Earths and the Balance Problem // Journal of Sustainable Metallurgy. — 2015. — Vol. 1. — P. 29-38. — ISSN 2199-3823. — doi:10.1007/s40831-014-0005-1.
- ↑ Jha Manis Kumar, Kumari Archana, Panda Rekha, Rajesh Kumar Jyothi, Yoo Kyoungkeun, Lee Jin Young. Review on hydrometallurgical recovery of rare earth metals // Hydrometallurgy. — 2016. — Май (т. 161). — С. 77. — ISSN 0304-386X. — doi:10.1016/j.hydromet.2016.01.003.
- ↑ Binnemans Koen, Jones Peter Tom, Blanpain Bart, Van Gerven Tom, Pontikes Yiannis. Towards zero-waste valorisation of rare-earth-containing industrial process residues: a critical review // Journal of Cleaner Production. — 2015. — Июль (т. 99). — С. 17—38. — ISSN 0959-6526. — doi:10.1016/j.jclepro.2015.02.089.
- ↑ Bandara H. M. Dhammika, Mantell Mark A., Darcy Julia W., Emmert Marion H. Rare Earth Recycling: Forecast of Recoverable Nd from Shredder Scrap and Influence of Recycling Rates on Price Volatility // Journal of Sustainable Metallurgy. — 2015. — 27 мая (т. 1, № 3). — С. 179—188. — ISSN 2199-3823. — doi:10.1007/s40831-015-0019-3.
- ↑ JIANG YUREN, SHIBAYAMA ATSUSHI, LIU KEJUN., FUJITA TOYOFISA. RECOVERY OF RARE EARTHS FROM THE SPENT OPTICAL GLASS BY HYDROMETALLURGICAL PROCESS // Canadian Metallurgical Quarterly. — 2004. — Январь (т. 43, № 4). — С. 431—438. — ISSN 0008-4433. — doi:10.1179/cmq.2004.43.4.431.
- ↑ Lyman J.W., Palmer G.R. Recycling of Rare Earths and Iron from NdFeB Magnet Scrap // High Temperature Materials and Processes. — 1993. — Январь (т. 11, № 1-4). — ISSN 2191-0324. — doi:10.1515/HTMP.1993.11.1-4.175.
- ↑ Anderson C D, Anderson C G, Taylor P R. Survey of recycled rare earths metallurgical processing // Canadian Metallurgical Quarterly. — 2013. — Июль (т. 52, № 3). — С. 249—256. — ISSN 0008-4433. — doi:10.1179/1879139513Y.0000000091.
- ↑ Abrahami S. T., Xiao Y., Yang Y. Rare-earth elements recovery from post-consumer hard-disc drives // Mineral Processing and Extractive Metallurgy. — 2014. — 8 декабря (т. 124, № 2). — С. 106—115. — ISSN 0371-9553. — doi:10.1179/1743285514Y.0000000084.
- ↑ Ueberschaar Maximilian, Rotter Vera Susanne. Enabling the recycling of rare earth elements through product design and trend analyses of hard disk drives // Journal of Material Cycles and Waste Management. — 2015. — 1 января (т. 17, № 2). — С. 266—281. — ISSN 1438-4957. — doi:10.1007/s10163-014-0347-6.
- ↑ Walton A., Yi Han, Rowson N.A., Speight J.D., Mann V.S.J., Sheridan R.S., Bradshaw A., Harris I.R., Williams A.J. The use of hydrogen to separate and recycle neodymium–iron–boron-type magnets from electronic waste // Journal of Cleaner Production. — 2015. — Октябрь (т. 104). — С. 236—241. — ISSN 0959-6526. — doi:10.1016/j.jclepro.2015.05.033.
- ↑ Zakotnik M., Tudor C.O. Commercial-scale recycling of NdFeB-type magnets with grain boundary modification yields products with ‘designer properties’ that exceed those of starting materials // Waste Management. — 2015. — Октябрь (т. 44). — С. 48—54. — ISSN 0956-053X. — doi:10.1016/j.wasman.2015.07.041.
- ↑ Binnemans K., Jones P.T. Perspectives for the recovery of rare earths from end-of-life fluorescent lamps // Journal of Rare Earths. — 2014. — Март (т. 32, № 3). — С. 195—200. — ISSN 1002-0721. — doi:10.1016/S1002-0721(14)60051-X.
- ↑ Machacek Erika, Richter Jessika Luth, Habib Komal, Klossek Polina. Recycling of rare earths from fluorescent lamps: Value analysis of closing-the-loop under demand and supply uncertainties // Resources, Conservation and Recycling. — 2015. — Ноябрь (т. 104). — С. 76—93. — ISSN 0921-3449. — doi:10.1016/j.resconrec.2015.09.005.
- ↑ Sommer P., Rotter V.S., Ueberschaar M. Battery related cobalt and REE flows in WEEE treatment // Waste Management. — 2015. — Ноябрь (т. 45). — С. 298—305. — ISSN 0956-053X. — doi:10.1016/j.wasman.2015.05.009.
- ↑ Yang Xiuli, Zhang Junwei, Fang Xihui. Rare earth element recycling from waste nickel-metal hydride batteries // Journal of Hazardous Materials. — 2014. — Август (т. 279). — С. 384—388. — ISSN 0304-3894. — doi:10.1016/j.jhazmat.2014.07.027.
- ↑ Bandara H. M. Dhammika, Field Kathleen D., Emmert Marion H. Rare earth recovery from end-of-life motors employing green chemistry design principles // Green Chemistry. — 2016. — Т. 18, № 3. — С. 753—759. — ISSN 1463-9262. — doi:10.1039/c5gc01255d.
- ↑ Riba Jordi-Roger, López-Torres Carlos, Romeral Luís, Garcia Antoni. Rare-earth-free propulsion motors for electric vehicles: A technology review // Renewable and Sustainable Energy Reviews. — 2016. — Май (т. 57). — С. 367—379. — ISSN 1364-0321. — doi:10.1016/j.rser.2015.12.121.
- ↑ Widmer James D., Martin Richard, Kimiabeigi Mohammed. Electric vehicle traction motors without rare earth magnets // Sustainable Materials and Technologies. — 2015. — Апрель (т. 3). — С. 7—13. — ISSN 2214-9937. — doi:10.1016/j.susmat.2015.02.001.
- ↑ Graedel T. E., Harper E. M., Nassar N. T., Reck Barbara K. On the materials basis of modern society // Proceedings of the National Academy of Sciences. — 2013. — 2 декабря (т. 112, № 20). — С. 6295—6300. — ISSN 0027-8424. — doi:10.1073/pnas.1312752110.
- ↑ Graedel T. E., Allwood Julian, Birat Jean-Pierre, Buchert Matthias, Hagelüken Christian, Reck Barbara K., Sibley Scott F., Sonnemann Guido. What Do We Know About Metal Recycling Rates? // Journal of Industrial Ecology. — 2011. — 9 мая (т. 15, № 3). — С. 355—366. — ISSN 1088-1980. — doi:10.1111/j.1530-9290.2011.00342.x.
- ↑ Reck B. K., Graedel T. E. Challenges in Metal Recycling // Science. — 2012. — 9 августа (т. 337, № 6095). — С. 690—695. — ISSN 0036-8075. — doi:10.1126/science.1217501.
- ↑ Lucas Jacques, Lucas Pierre, Le Mercier Thierry, Rollat Alain, Davenport William. Rare Earth Recycle // Rare Earths. — 2015. — С. 333—350. — ISBN 9780444627353. — doi:10.1016/B978-0-444-62735-3.00017-6.
- ↑ Binnemans Koen, Jones Peter Tom, Blanpain Bart, Van Gerven Tom, Yang Yongxiang, Walton Allan, Buchert Matthias. Recycling of rare earths: a critical review // Journal of Cleaner Production. — 2013. — Июль (т. 51). — С. 1—22. — ISSN 0959-6526. — doi:10.1016/j.jclepro.2012.12.037.
- ↑ Haxel G. B. et al. Rare Earth Elements—Critical Resources for High Technology (англ.). — 2002. — No. 087—02. Архивировано 19 июля 2020 года.
- ↑ European Commission. Critical raw materials for the EU (англ.). — Report of the Ad-hoc Working Group on defining critical raw materials, 2010.
- ↑ R.L.Moss, E.Tzimas, H.Kara, P.Willis, J.Kooroshy. Critical metals in strategic energy technologies. — Luxembourg: Publications Office of the European Union, 2011. — 162 p. — ISBN 978-92-79-20699-3. — doi:10.2790/35716.
- ↑ UNCTAD. Commodities at a Glance. Special issue on rare earths (англ.) (pdf) (2014). Дата обращения: 11 ноября 2015. Архивировано 16 декабря 2015 года.
- ↑ 1 2 3 4 Alam Mohammed A., Zuga Leonard, Pecht Michael G. Economics of rare earth elements in ceramic capacitors // Ceramics International. — 2012. — Декабрь (т. 38, № 8). — С. 6091—6098. — ISSN 0272-8842. — doi:10.1016/j.ceramint.2012.05.068.
- ↑ Golev Artem, Scott Margaretha, Erskine Peter D., Ali Saleem H., Ballantyne Grant R. Rare earths supply chains: Current status, constraints and opportunities // Resources Policy. — 2014. — Сентябрь (т. 41). — С. 52—59. — ISSN 0301-4207. — doi:10.1016/j.resourpol.2014.03.004.
- ↑ 1 2 Dent Peter C. Rare earth elements and permanent magnets (invited) // Journal of Applied Physics. — 2012. — Апрель (т. 111, № 7). — С. 07A721. — ISSN 0021-8979. — doi:10.1063/1.3676616.
- ↑ GU B. Mineral Export Restraints and Sustainable Development--Are Rare Earths Testing the WTO's Loopholes? // Journal of International Economic Law. — 2011. — 1 декабря (т. 14, № 4). — С. 765—805. — ISSN 1369-3034. — doi:10.1093/jiel/jgr034.
- ↑ Xiao Sheng-Xiong, Li Ai-Tao, Jiang Jian-Hong, Huang Shuang, Xu Xiao-Yan, Li Qiang-Guo. Thermochemical analysis on rare earth complex of gadolinium with salicylic acid and 8-hydroxyquinoline // Thermochimica Acta. — 2012. — Ноябрь (т. 548). — С. 33—37. — ISSN 0040-6031. — doi:10.1016/j.tca.2012.08.027.
- ↑ Shi Yaowu, Tian Jun, Hao Hu, Xia Zhidong, Lei Yongping, Guo Fu. Effects of small amount addition of rare earth Er on microstructure and property of SnAgCu solder // Journal of Alloys and Compounds. — 2008. — Апрель (т. 453, № 1-2). — С. 180—184. — ISSN 0925-8388. — doi:10.1016/j.jallcom.2006.11.165.
- ↑ 1 2 Mancheri Nabeel A. Chinese Monopoly in Rare Earth Elements: Supply–Demand and Industrial Applications // China Report. — 2012. — Ноябрь (т. 48, № 4). — С. 449—468. — ISSN 0009-4455. — doi:10.1177/0009445512466621.
- ↑ CHEN Zhanheng. Global rare earth resources and scenarios of future rare earth industry // Journal of Rare Earths. — 2011. — Январь (т. 29, № 1). — С. 1—6. — ISSN 1002-0721. — doi:10.1016/S1002-0721(10)60401-2.
- ↑ 1 2 Tang Jinkui, Zhang Peng. A Basis for Lanthanide Single-Molecule Magnets // Lanthanide Single Molecule Magnets. — 2015. — С. 1—39. — ISBN 9783662469989. — doi:10.1007/978-3-662-46999-6_1.
- ↑ 1 2 3 4 Голуб, 1971, с. 203.
- ↑ Lang Peter F., Smith Barry C. Ionization Energies of Lanthanides // Journal of Chemical Education. — 2010. — Август (т. 87, № 8). — С. 875—881. — ISSN 0021-9584. — doi:10.1021/ed100215q.
- ↑ Двухвалентными бывают, кроме Eu и Yb, Sm, Tm, а четырёхвалентым — Pr.
- ↑ 1 2 Голуб, 1971, с. 201.
- ↑ 1 2 Голуб, 1971, с. 202.
- ↑ [bse.sci-lib.com/article068666.html Лантаноиды: статья в БСЭ]
- ↑ Springer Handbook of Condensed Matter and Materials Data / Eds.: W. Martienssen; H. Warlimont. — Springer Berlin Heidelberg, 2005. — P. 84—88, 142—150. — 1121 p. — ISBN 3-540-44376-2.
- ↑ MacDonald Matthew R., Bates Jefferson E., Ziller Joseph W., Furche Filipp, Evans William J. Completing the Series of +2 Ions for the Lanthanide Elements: Synthesis of Molecular Complexes of Pr2+, Gd2+, Tb2+, and Lu2+ // Journal of the American Chemical Society. — 2013. — 22 мая (т. 135, № 26). — С. 9857—9868. — ISSN 0002-7863. — doi:10.1021/ja403753j.
- ↑ 1 2 Edelmann Frank T. Lanthanides and actinides: Annual survey of their organometallic chemistry covering the year 2013 // Coordination Chemistry Reviews. — 2015. — Февраль (т. 284). — С. 124—205. — ISSN 0010-8545. — doi:10.1016/j.ccr.2014.09.017.
- ↑ Fieser Megan E., MacDonald Matthew R., Krull Brandon T., Bates Jefferson E., Ziller Joseph W., Furche Filipp, Evans William J. Structural, Spectroscopic, and Theoretical Comparison of Traditional vs Recently Discovered Ln2+ Ions in the [K(2.2.2-cryptand)[(C5H4SiMe3)3Ln] Complexes: The Variable Nature of Dy2+ and Nd2+] // Journal of the American Chemical Society. — 2014. — 26 декабря (т. 137, № 1). — С. 369—382. — ISSN 0002-7863. — doi:10.1021/ja510831n.
- ↑ Sabnis R. W. Handbook of Biological Dyes and Stains. — 2010. — 23 февраля. — ISBN 9780470586242. — doi:10.1002/9780470586242.
- ↑ Brittain Harry G. Submicrogram determination of lanthanides through quenching of calcein blue fluorescence // Analytical Chemistry. — 1987. — 15 апреля (т. 59, № 8). — С. 1122—1125. — ISSN 0003-2700. — doi:10.1021/ac00135a012.
- ↑ Shafiq M., Arif Suneela, Ahmad Iftikhar, Asadabadi S. Jalali, Maqbool M., Rahnamaye Aliabad H.A. Elastic and mechanical properties of lanthanide monoxides // Journal of Alloys and Compounds. — 2015. — Январь (т. 618). — С. 292—298. — ISSN 0925-8388. — doi:10.1016/j.jallcom.2014.08.171.
- ↑ David J. Procter, Robert A. Flowers, Troels Skrydstrup. Organic Synthesis using Samarium Diiodide. — 2009. — ISBN 9781847551108. — doi:10.1039/9781849730754.
- ↑ Chemistry of the elements, 1997, p. 1240.
- ↑ Jantsch G., Skalla N. Zur Kenntnis der Halogenide der seltenen Erden. IV. Über Samarium(II)jodid und den thermischen Abbau des Samarium(III)jodids // Zeitschrift für anorganische und allgemeine Chemie. — 1930. — 4 ноября (т. 193, № 1). — С. 391—405. — ISSN 0863-1786. — doi:10.1002/zaac.19301930132.
- ↑ Jantsch G. Thermischer Abbau von seltenen Erd(III)halogeniden // Die Naturwissenschaften. — 1930. — Февраль (т. 18, № 7). — С. 155—155. — ISSN 0028-1042. — doi:10.1007/BF01501667.
- ↑ Girard P., Namy J. L., Kagan H. B. Divalent lanthanide derivatives in organic synthesis. 1. Mild preparation of samarium iodide and ytterbium iodide and their use as reducing or coupling agents // Journal of the American Chemical Society. — 1980. — Апрель (т. 102, № 8). — С. 2693—2698. — ISSN 0002-7863. — doi:10.1021/ja00528a029.
- ↑ Trzesowska Agata, Kruszynski Rafal, Bartczak Tadeusz J. Bond-valence parameters of lanthanides // Acta Crystallographica Section B Structural Science. — 2006. — 18 сентября (т. 62, № 5). — С. 745—753. — ISSN 0108-7681. — doi:10.1107/S0108768106016429.
- ↑ Fedushkin Igor L., Bochkarev Mikhail N., Dechert Sebastian, Schumann Herbert. A Chemical Definition of the Effective Reducing Power of Thulium(II) Diiodide by Its Reactions with Cyclic Unsaturated Hydrocarbons // Chemistry - A European Journal. — 2001. — Vol. 7. — P. 3558—3563. — ISSN 09476539. — doi:10.1002/1521-3765(20010817)7:16<3558::AID-CHEM3558>3.0.CO;2-H.
- ↑ Evans William J., Allen Nathan T. Ketone Coupling with Alkyl Iodides, Bromides, and Chlorides Using Thulium Diiodide: A More Powerful Version of SmI2(THF)x/HMPA // Journal of the American Chemical Society. — 2000. — Март (т. 122, № 9). — С. 2118—2119. — ISSN 0002-7863. — doi:10.1021/ja992951m.
- ↑ Evans William J., Allen Nathan T., Ziller Joseph W. The Availability of Dysprosium Diiodide as a Powerful Reducing Agent in Organic Synthesis: Reactivity Studies and Structural Analysis of DyI2((DME)3and Its Naphthalene Reduction Product1 // Journal of the American Chemical Society. — 2000. — Ноябрь (т. 122, № 47). — С. 11749—11750. — ISSN 0002-7863. — doi:10.1021/ja0034949.
- ↑ Ji Wen-Xin, Xu Wei, Xiao Yi, Wang Shu-Guang. Does the 4f-shell contribute to bonding in tetravalent lanthanide halides? // The Journal of Chemical Physics. — 2014. — 28 декабря (т. 141, № 24). — С. 244316. — ISSN 0021-9606. — doi:10.1063/1.4904722.
- ↑ Edelmann Frank T. Lanthanides and actinides: Annual survey of their organometallic chemistry covering the year 2010 // Coordination Chemistry Reviews. — 2012. — Декабрь (т. 256, № 23-24). — С. 2641—2740. — ISSN 0010-8545. — doi:10.1016/j.ccr.2012.07.027.
- ↑ Edelmann Frank T. Lanthanides and actinides: Annual survey of their organometallic chemistry covering the year 2011 // Coordination Chemistry Reviews. — 2013. — Апрель (т. 257, № 7-8). — С. 1122—1231. — ISSN 0010-8545. — doi:10.1016/j.ccr.2012.12.010.
- ↑ Edelmann Frank T. Lanthanides and actinides: Annual survey of their organometallic chemistry covering the year 2012 // Coordination Chemistry Reviews. — 2014. — Февраль (т. 261). — С. 73—155. — ISSN 0010-8545. — doi:10.1016/j.ccr.2013.11.008.
- ↑ Edelmann Frank T. Lanthanides and actinides: Annual survey of their organometallic chemistry covering the year 2014 // Coordination Chemistry Reviews. — 2016. — Январь (т. 306). — С. 346—419. — ISSN 0010-8545. — doi:10.1016/j.ccr.2015.07.017.
- ↑ 1 2 3 Muecke Gunter K., Möller Peter. The Not-So-Rare Earths // Scientific American. — 1988. — Январь (т. 258, № 1). — С. 72—77. — ISSN 0036-8733. — doi:10.1038/scientificamerican0188-72.
- ↑ 1 2 Bünzli Jean-Claude G., Eliseeva Svetlana V. Intriguing aspects of lanthanide luminescence // Chemical Science. — 2013. — Vol. 4. — P. 1939-1949. — ISSN 2041-6520. — doi:10.1039/C3SC22126A.
- ↑ The History and Use of Our Earth's Chemical Elements, 2006, p. 275.
- ↑ The constitution of group 3 of the periodic table. Дата обращения: 15 февраля 2019. Архивировано 5 июля 2016 года.
- ↑ Xu Wen-Hua, Pyykkö Pekka. Is the chemistry of lawrencium peculiar? // Physical Chemistry Chemical Physics. — 2016. — Т. 18, № 26. — С. 17351—17355. — ISSN 1463-9076. — doi:10.1039/c6cp02706g.
- ↑ Bünzli Jean-Claude G. Review: Lanthanide coordination chemistry: from old concepts to coordination polymers // Journal of Coordination Chemistry. — 2014. — 25 сентября (т. 67, № 23-24). — С. 3706—3733. — ISSN 0095-8972. — doi:10.1080/00958972.2014.957201.
- ↑ Handbook of the Physics and Chemistry of Rare Earths, 2011, pp. 1—94.
- ↑ Леенсон И.А. Карл Ауэр фон Вельсбах: редкие земли и яркий свет : журнал. — Химия и Жизнь, 2013. — № 10. — ISSN 0130-5972. Архивировано 5 октября 2018 года.
- ↑ Inagaki Kazumi, Haraguchi Hiroki. Determination of rare earth elements in human blood serum by inductively coupled plasma mass spectrometry after chelating resin preconcentration // The Analyst. — 2000. — Т. 125, № 1. — С. 191—196. — ISSN 0003-2654. — doi:10.1039/A907781B.
- ↑ 1 2 3 Rim Kyung Taek, Koo Kwon Ho, Park Jung Sun. Toxicological Evaluations of Rare Earths and Their Health Impacts to Workers: A Literature Review // Safety and Health at Work. — 2013. — Март (т. 4, № 1). — С. 12—26. — ISSN 2093-7911. — doi:10.5491/SHAW.2013.4.1.12.
- ↑ Biochemistry of the Lanthanides, 1990, p. 6.
- ↑ 1 2 The rare earth elements: fundamentals and applications, 2012, p. 2.
- ↑ 1 2 Niinistö Lauri. Industrial applications of the rare earths, an overview // Inorganica Chimica Acta. — 1987. — Декабрь (т. 140). — С. 339—343. — ISSN 0020-1693. — doi:10.1016/S0020-1693(00)81118-4.
- ↑ Falconnet Pierre. Rare earth industry update // Materials Chemistry and Physics. — 1992. — Март (т. 31, № 1-2). — С. 79—83. — ISSN 0254-0584. — doi:10.1016/0254-0584(92)90156-3.
- ↑ Eliseeva Svetlana V., Bünzli Jean-Claude G. Rare earths: jewels for functional materials of the future // New Journal of Chemistry. — 2011. — Т. 35, № 6. — С. 1165. — ISSN 1144-0546. — doi:10.1039/c0nj00969e.
- ↑ 1 2 3 Episodes from the History of the Rare Earth Elements, 1996, pp. 122—123.
- ↑ Handbook of the Physics and Chemistry of Rare Earths, 1988, p. 64.
- ↑ Levy S. I. The Rare Earths. Their Occurrence, Chemistry and Technology // Journal of the Röntgen Society. — 1915. — Апрель (т. 11, № 43). — С. 51—51. — ISSN 2053-132X. — doi:10.1259/jrs.1915.0030.
- ↑ Chegwidden J., Kingsnorth D.J. Rare Earths: facing the uncertainties of supply. 6th international rare Earths conference (2010). Дата обращения: 6 декабря 2015. Архивировано 4 марта 2016 года.
- ↑ ASX mid caps conference presentation (англ.). Lynas (2010). Дата обращения: 6 декабря 2015. Архивировано 3 июня 2014 года.
- ↑ Lanthanides, Tantalum and Niobium, 1989, p. VII.
- ↑ 1 2 Bünzli Jean-Claude G. On the design of highly luminescent lanthanide complexes // Coordination Chemistry Reviews. — 2015. — Vol. 293-294. — P. 19-47. — ISSN 00108545. — doi:10.1016/j.ccr.2014.10.013.
- ↑ Optimizing New Classes of Luminescent Lanthanide Complexes. — ProQuest, 2008. — P. 20. — 216 p. — ISBN 110909762X, 9781109097627. Архивированная копия. Дата обращения: 4 сентября 2015. Архивировано 27 сентября 2015 года.
- ↑ Weissman S. I. Intramolecular Energy Transfer The Fluorescence of Complexes of Europium // The Journal of Chemical Physics. — 1942. — Апрель (т. 10, № 4). — С. 214—217. — ISSN 0021-9606. — doi:10.1063/1.1723709.
- ↑ Уточникова Валентина. Люминесценция комплексов лантанидов: основные применения. Nanometer.ru (4 октября 2010). Дата обращения: 14 октября 2015. Архивировано 1 марта 2016 года.
- ↑ Wegh R. T., Donker H., Meijerink A., Lamminmäki R. J., Hölsä J. Vacuum-ultraviolet spectroscopy and quantum cutting forGd3+inLiYF4 // Physical Review B. — 1997. — 1 декабря (т. 56, № 21). — С. 13841—13848. — ISSN 0163-1829. — doi:10.1103/PhysRevB.56.13841.
- ↑ 1 2 Lanthanide Luminescence // Springer Series on Fluorescence. — 2011. — ISBN 9783642210228. — ISSN 1617-1306. — doi:10.1007/978-3-642-21023-5.. Страницы 219, 220, 222.
- ↑ 1 2 3 4 Pan Shuming. Rare Earth Permanent-Magnet Alloys’ High Temperature Phase Transformation. — 2013. — doi:10.1007/978-3-642-36388-7.
- ↑ 1 2 3 Cullity B. D., Graham C. D. Introduction to Magnetic Materials. — 2nd ed. — New Jersey: John Wiley & Sons, Inc., 2008. — 544 p. — ISBN 9780471477419, 9780470386323. — doi:10.1002/9780470386323.
- ↑ Strnat K. J., Hoffer G. I. YCo5 A Promising New Permanent Magnet Material (англ.). — Air Force Materials Lab Wright-Patterson AFB OH, 1966. Архивировано 4 марта 2016 года.
- ↑ 1 2 Joshi R.S., Kumar P.S.A. Magnetic Solid-State Materials // Comprehensive Inorganic Chemistry II. — 2013. — С. 271—316. — ISBN 9780080965291. — doi:10.1016/B978-0-08-097774-4.00413-7.
- ↑ Strnat K., Hoffer G., Olson J., Ostertag W., Becker J. J. A Family of New Cobalt‐Base Permanent Magnet Materials // Journal of Applied Physics. — 1967. — Март (т. 38, № 3). — С. 1001—1002. — ISSN 0021-8979. — doi:10.1063/1.1709459.
- ↑ Özgür Ümit, Alivov Yahya, Morkoç Hadis. Microwave ferrites, part 1: fundamental properties // Journal of Materials Science: Materials in Electronics. — 2009. — 25 июня (т. 20, № 9). — С. 789—834. — ISSN 0957-4522. — doi:10.1007/s10854-009-9923-2.
- ↑ 1 2 Xie Feng, Zhang Ting An, Dreisinger David, Doyle Fiona. A critical review on solvent extraction of rare earths from aqueous solutions // Minerals Engineering. — 2014. — Vol. 56. — P. 10-28. — ISSN 08926875. — doi:10.1016/j.mineng.2013.10.021.
- ↑ The Elements, 2009, p. 141.
- ↑ 1 2 Liang Liping, Ma Tianyu, Wu Chen, Zhang Pei, Liu Xiaolian, Yan Mi. Coercivity enhancement of Dy-free Nd–Fe–B sintered magnets by intergranular adding Ho63.4Fe36.6 alloy // Journal of Magnetism and Magnetic Materials. — 2016. — Январь (т. 397). — С. 139—144. — ISSN 0304-8853. — doi:10.1016/j.jmmm.2015.08.091.
- ↑ Sagawa M., Fujimura S., Togawa N., Yamamoto H., Matsuura Y. New material for permanent magnets on a base of Nd and Fe (invited) // Journal of Applied Physics. — 1984. — Vol. 55. — P. 2083. — ISSN 00218979. — doi:10.1063/1.333572.
- ↑ Brown David, Ma Bao-Min, Chen Zhongmin. Developments in the processing and properties of NdFeB-type permanent magnets // Journal of Magnetism and Magnetic Materials. — 2002. — Vol. 248. — P. 432-440. — ISSN 03048853. — doi:10.1016/S0304-8853(02)00334-7.
- ↑ Sugimoto S. Current status and recent topics of rare-earth permanent magnets // Journal of Physics D: Applied Physics. — 2011. — 28 января (т. 44, № 6). — С. 064001. — ISSN 0022-3727. — doi:10.1088/0022-3727/44/6/064001.
- ↑ Doyle F. M. Direct production of mixed, rare earth oxide feed for high energy-product magnets. — Rare Earths and Actinides: Science, Technology and Applications IV as held at the 2000 TMS Annual Meeting, 2000. — С. 31—44.
- ↑ Benz M. G. High-Energy-Product (Pr-Nd-Ce) FeB Magnets Produced Directly from Mixed-Rare-Earth-Oxide Feed for MRI Medical Imaging Applications // Rare-Earth Magnets and Their Applications, Sendai, Japan, September 2000. — The Japan Institute of Metals Proceedings, 2000. — Т. 14. — С. 99—108.
- ↑ Hu Z.H., Lian F.Z., Zhu M.G., Li W. Effect of Tb on the intrinsic coercivity and impact toughness of sintered Nd–Dy–Fe–B magnets // Journal of Magnetism and Magnetic Materials. — 2008. — Июнь (т. 320, № 11). — С. 1735—1738. — ISSN 0304-8853. — doi:10.1016/j.jmmm.2008.01.027.
- ↑ Xu Fang, Zhang Lanting, Dong Xianping, Liu Qiongzhen, Komuro Matahiro. Effect of DyF3 additions on the coercivity and grain boundary structure in sintered Nd–Fe–B magnets // Scripta Materialia. — 2011. — Vol. 64. — P. 1137-1140. — ISSN 13596462. — doi:10.1016/j.scriptamat.2011.03.011.
- ↑ Cao X.J., Chen L., Guo S., Li X.B., Yi P.P., Yan A.R., Yan G.L. Coercivity enhancement of sintered Nd–Fe–B magnets by efficiently diffusing DyF3 based on electrophoretic deposition // Journal of Alloys and Compounds. — 2015. — Май (т. 631). — С. 315—320. — ISSN 0925-8388. — doi:10.1016/j.jallcom.2015.01.078.
- ↑ Sepehri-Amin H., Une Y., Ohkubo T., Hono K., Sagawa M. Microstructure of fine-grained Nd–Fe–B sintered magnets with high coercivity // Scripta Materialia. — 2011. — Сентябрь (т. 65, № 5). — С. 396—399. — ISSN 1359-6462. — doi:10.1016/j.scriptamat.2011.05.006.
- ↑ Hu Bo-Ping, Niu E., Zhao Yu-Gang, Chen Guo-An, Chen Zhi-An, Jin Guo-Shun, Zhang Jin, Rao Xiao-Lei, Wang Zhen-Xi. Study of sintered Nd-Fe-B magnet with high performance of Hcj (kOe) + (BH)max (MGOe) > 75 // AIP Advances. — 2013. — Vol. 3. — P. 042136. — ISSN 21583226. — doi:10.1063/1.4803657.
- ↑ Zhang Pei, Ma Tianyu, Liang Liping, Yan Mi. Influence of Ta intergranular addition on microstructure and corrosion resistance of Nd–Dy–Fe–B sintered magnets // Journal of Alloys and Compounds. — 2014. — Апрель (т. 593). — С. 137—140. — ISSN 0925-8388. — doi:10.1016/j.jallcom.2014.01.055.
- ↑ Hatch G. P. Dynamics in the Global Market for Rare Earths // Elements. — 2012. — 1 октября (т. 8, № 5). — С. 341—346. — ISSN 1811-5209. — doi:10.2113/gselements.8.5.341.
- ↑ Giauque W. F., MacDougall D. P. Attainment of Temperatures Below 1° Absolute by Demagnetization ofGd2(SO4)3·8H2O // Physical Review. — 1933. — 1 мая (т. 43, № 9). — С. 768—768. — ISSN 0031-899X. — doi:10.1103/PhysRev.43.768.
- ↑ The Nobel Prize in Chemistry 1949 (англ.). Nobelprize.org. Дата обращения: 21 сентября 2015. Архивировано 28 марта 2014 года.
- ↑ Gschneidner K. A., Pecharsky V. K. Magnetocaloric Materials // Annual Review of Materials Science. — 2000. — Август (т. 30, № 1). — С. 387—429. — ISSN 0084-6600. — doi:10.1146/annurev.matsci.30.1.387.
- ↑ Behrsing T., Deacon G.B., Junk P.C. The chemistry of rare earth metals, compounds, and corrosion inhibitors // Rare Earth-Based Corrosion Inhibitors. — 2014. — С. 1—37. — doi:10.1533/9780857093585.1.
- ↑ Hoard R., Mance S., Leber R., Dalder E., Chaplin M., Blair K., Nelson D., Van Dyke D. Field enhancement of a 12.5-T magnet using holmium poles // IEEE Transactions on Magnetics. — 1985. — Март (т. 21, № 2). — С. 448—450. — ISSN 0018-9464. — doi:10.1109/TMAG.1985.1063692.
- ↑ Emsley, J. Nature's Building Blocks: An A-Z Guide to the Elements. — Oxford University Press, 2001. — P. 181–182. — 538 p. — (Oxford Pakistan Paperbacks Series). — ISBN 0-19-850341-5.
- ↑ The Rare Earths // Extractive Metallurgy of Rare Earths, Second Edition. — 2015. — 25 ноября. — С. 1—84. — ISBN 9781466576346. — doi:10.1201/b19055-2.
- ↑ Valerie Bailey Grasso. Rare Earth Elements in National Defense: Background, Oversight Issues, and Options for Congress (англ.). Congressional Research Service, R41744 (2013). Дата обращения: 11 февраля 2016. Архивировано 26 марта 2014 года.
- ↑ "Ни капель, ни царапин: Гидрофобная керамика". Популярная Механика. 21 января 2013. Архивировано из оригинала 24 сентября 2015. Дата обращения: 25 июля 2015.
- ↑ Peplow Mark. Ceramics surprise with durable dryness // Nature. — 2013. — 20 января. — ISSN 1476-4687. — doi:10.1038/nature.2013.12250.
- ↑ Azimi Gisele, Dhiman Rajeev, Kwon Hyuk-Min, Paxson Adam T., Varanasi Kripa K. Hydrophobicity of rare-earth oxide ceramics // Nature Materials. — 2013. — 20 января (т. 12, № 4). — С. 315—320. — ISSN 1476-1122. — doi:10.1038/nmat3545.
- ↑ Azimi Gisele, Kwon Hyuk-Min, Varanasi Kripa K. Superhydrophobic surfaces by laser ablation of rare-earth oxide ceramics // MRS Communications. — 2014. — 10 сентября. — С. 1—5. — ISSN 2159-6859. — doi:10.1557/mrc.2014.20.
- ↑ Hughes Anthony E., Ho Daniel, Forsyth Maria, Hinton Bruce R.W. TOWARDS REPLACEMENT OF CHROMATE INHIBITORS BY RARE EARTH SYSTEMS // Corrosion Reviews. — 2007. — Январь (т. 25, № 5-6). — ISSN 2191-0316. — doi:10.1515/CORRREV.2007.25.5-6.591.
- ↑ Forsyth Maria, Seter Marianne, Hinton Bruce, Deacon Glen, Junk Peter. New 'Green' Corrosion Inhibitors Based on Rare Earth Compounds // Australian Journal of Chemistry. — 2011. — Т. 64, № 6. — С. 812. — ISSN 0004-9425. — doi:10.1071/CH11092.
- ↑ 1 2 3 Mohammedi D., Ismail F., Rehamnia R., Bensalem R., Savadogo O. Corrosion behaviour of steel in the presence of rare earth salts: synergistic effect // Corrosion Engineering, Science and Technology. — 2015. — 4 июня (т. 50, № 8). — С. 633—638. — ISSN 1478-422X. — doi:10.1179/1743278215Y.0000000030.
- ↑ Zhang T., Li D.Y. The effect of YCl3 and LaCl3 additives on wear of 1045 and 304 steels in a dilute chloride solution // Materials Science and Engineering: A. — 2003. — Март (т. 345, № 1-2). — С. 179—189. — ISSN 0921-5093. — doi:10.1016/S0921-5093(02)00469-0.
- ↑ Aramaki Kunitsugu. The inhibition effects of chromate-free, anion inhibitors on corrosion of zinc in aerated 0.5 M NaCl // Corrosion Science. — 2001. — Март (т. 43, № 3). — С. 591—604. — ISSN 0010-938X. — doi:10.1016/S0010-938X(00)00085-8.
- ↑ Aramaki Kunitsugu. The inhibition effects of cation inhibitors on corrosion of zinc in aerated 0.5 M NaCl // Corrosion Science. — 2001. — Август (т. 43, № 8). — С. 1573—1588. — ISSN 0010-938X. — doi:10.1016/S0010-938X(00)00144-X.
- ↑ Gupta R.K., Sukiman N.L., Cavanaugh M.K., Hinton B.R.W., Hutchinson C.R., Birbilis N. Metastable pitting characteristics of aluminium alloys measured using current transients during potentiostatic polarisation // Electrochimica Acta. — 2012. — Апрель (т. 66). — С. 245—254. — ISSN 0013-4686. — doi:10.1016/j.electacta.2012.01.090.
- ↑ Catubig Rainier, Seter Marianne, Neil Wayne, Forsyth Maria, Hinton Bruce. Effects of Corrosion Inhibiting Pigment Lanthanum 4-Hydroxy Cinnamate on the Filiform Corrosion of Coated Steel // Journal of The Electrochemical Society. — 2011. — Т. 158, № 11. — С. C353. — ISSN 0013-4651. — doi:10.1149/2.012111jes.
- ↑ Bethencourt M, Botana F.J, Cauqui M.A, Marcos M, Rodrı́guez M.A, Rodrı́guez-Izquierdo J.M. Protection against corrosion in marine environments of AA5083 Al–Mg alloy by lanthanide chlorides // Journal of Alloys and Compounds. — 1997. — Март (т. 250, № 1-2). — С. 455—460. — ISSN 0925-8388. — doi:10.1016/S0925-8388(96)02826-5.
- ↑ Forsyth M., Wilson K., Behrsing T., Forsyth C., Deacon G. B., Phanasgoankar A. Effectiveness of Rare-Earth Metal Compounds as Corrosion Inhibitors for Steel // CORROSION. — 2002. — Ноябрь (т. 58, № 11). — С. 953—960. — ISSN 0010-9312. — doi:10.5006/1.3280785.
- ↑ Hinton B. R. W., Behrouzvaziri M., Forsyth M., Gupta R. K., Seter M., Bushell P. G. The Inhibition of Hydrogen Embrittlement in SAE 4340 Steel in an Aqueous Environment with the Rare Earth Compound Lanthanum 4 Hydroxy Cinnamate // Metallurgical and Materials Transactions A. — 2012. — 27 марта (т. 43, № 7). — С. 2251—2259. — ISSN 1073-5623. — doi:10.1007/s11661-012-1103-y.
- ↑ Montemor M.F, Simões A.M, Ferreira M.G.S. Composition and corrosion behaviour of galvanised steel treated with rare-earth salts: the effect of the cation // Progress in Organic Coatings. — 2002. — Апрель (т. 44, № 2). — С. 111—120. — ISSN 0300-9440. — doi:10.1016/S0300-9440(01)00250-8.
- ↑ Forsyth M., Seter M., Tan M. Y., Hinton B. Recent developments in corrosion inhibitors based on rare earth metal compounds // Corrosion Engineering, Science and Technology. — 2014. — 28 января (т. 49, № 2). — С. 130—135. — ISSN 1478-422X. — doi:10.1179/1743278214Y.0000000148.
- ↑ Hughes A.E., Harvey T.G., Birbilis N., Kumar A., Buchheit R.G. Coatings for corrosion prevention based on rare earths // Rare Earth-Based Corrosion Inhibitors. — 2014. — С. 186—232. — ISBN 9780857093479. — doi:10.1533/9780857093585.186.
- ↑ Mitic Vojislav V., Nikolic Zoran S., Pavlovic Vladimir B., Paunovic Vesna, Miljkovic Miroslav, Jordovic Branka, Zivkovic Ljiljana. Influence of Rare-Earth Dopants on Barium Titanate Ceramics Microstructure and Corresponding Electrical Properties // Journal of the American Ceramic Society. — 2010. — Январь (т. 93, № 1). — С. 132—137. — ISSN 0002-7820. — doi:10.1111/j.1551-2916.2009.03309.x.
- ↑ Kishi Hiroshi, Mizuno Youichi, Chazono Hirokazu. Base-Metal Electrode-Multilayer Ceramic Capacitors: Past, Present and Future Perspectives // Japanese Journal of Applied Physics. — 2003. — 15 января (т. 42, № Part 1, No. 1). — С. 1—15. — ISSN 0021-4922. — doi:10.1143/JJAP.42.1.
- ↑ Tsur Yoed, Hitomi Atsushi, Scrymgeour Ian, Randall Clive A. Site Occupancy of Rare-Earth Cations in BaTiO3 // Japanese Journal of Applied Physics. — 2001. — 15 января (т. 40, № Part 1, No. 1). — С. 255—258. — ISSN 0021-4922. — doi:10.1143/JJAP.40.255.
- ↑ Sakabe Yukio, Hamaji Yukio, Sano Harunobu, Wada Nobuyuki. Effects of Rare-Earth Oxides on the Reliability of X7R Dielectrics // Japanese Journal of Applied Physics. — 2002. — 15 сентября (т. 41, № Part 1, No. 9). — С. 5668—5673. — ISSN 0021-4922. — doi:10.1143/JJAP.41.5668.
- ↑ Jung Yun-Sung, Na Eun-Sang, Paik Ungyu, Lee Jinha, Kim Jonghee. A study on the phase transition and characteristics of rare earth elements doped BaTiO3 // Materials Research Bulletin. — 2002. — Август (т. 37, № 9). — С. 1633—1640. — ISSN 0025-5408. — doi:10.1016/S0025-5408(02)00813-9.
- ↑ Dang-Hyok Yoon. Tetragonality of barium titanate powder for a ceramic capacitor application // Journal of Ceramic Processing Research. — 2006. — Vol. 7. — P. 343—354. — ISSN 1229-9162. Архивировано 26 мая 2019 года.
- ↑ Prodi L., Rampazzo E., Rastrelli F., Speghini A., Zaccheroni N. Imaging agents based on lanthanide doped nanoparticles // Chem. Soc. Rev. — 2015. — Vol. 44. — P. 4922-4952. — ISSN 0306-0012. — doi:10.1039/C4CS00394B.
- ↑ 1 2 Магневист®. Регистр лекарственных средств России. — Инструкция по применению, противопоказания, состав и цена. Дата обращения: 21 сентября 2015. Архивировано 28 сентября 2015 года.
- ↑ Caravan Peter, Ellison Jeffrey J., McMurry Thomas J., Lauffer Randall B. Gadolinium(III) Chelates as MRI Contrast Agents: Structure, Dynamics, and Applications // Chemical Reviews. — 1999. — Сентябрь (т. 99, № 9). — С. 2293—2352. — ISSN 0009-2665. — doi:10.1021/cr980440x.
- ↑ Aime Silvio, Botta Mauro, Panero Maurizio, Grandi Maurizio, Uggeri Fulvio. Inclusion complexes between β-cyclodextrin and β-benzyloxy-α-propionic derivatives of paramagnetic DOTA- and DPTA-Gd(III) complexes // Magnetic Resonance in Chemistry. — 1991. — Сентябрь (т. 29, № 9). — С. 923—927. — ISSN 0749-1581. — doi:10.1002/mrc.1260290910.
- ↑ Medical imaging relaxes to brighten up (англ.). — Nature, 9 апреля 2002. — ISSN 1744-7933. — doi:10.1038/news020408-1. Архивировано 27 сентября 2015 года.
- ↑ Елена Большакова (16 июля 2015). "Bayer локализуется на «Полисане»". Коммерсантъ. Архивировано из оригинала 27 сентября 2015. Дата обращения: 21 сентября 2015.
- ↑ Гадовист®. Регистр лекарственных средств России. — Инструкция по применению, противопоказания, состав и цена. Дата обращения: 21 сентября 2015. Архивировано 28 сентября 2015 года.
- ↑ Lewis David J., Pikramenou Zoe. Lanthanide-coated gold nanoparticles for biomedical applications // Coordination Chemistry Reviews. — 2014. — Август (т. 273-274). — С. 213—225. — ISSN 0010-8545. — doi:10.1016/j.ccr.2014.03.019.
- ↑ Voncken J. H. L. Applications of the Rare Earths // SpringerBriefs in Earth Sciences. — 2015. — 25 декабря. — С. 89—106. — ISBN 9783319268071. — ISSN 2191-5369. — doi:10.1007/978-3-319-26809-5_5.
- ↑ Godard Antoine. Infrared (2–12 μm) solid-state laser sources: a review (англ.) // Comptes Rendus Physique. — 2007. — December (vol. 8, no. 10). — P. 1100—1128. — ISSN 1631-0705. — doi:10.1016/j.crhy.2007.09.010.
- ↑ Tsivadze A. Yu., Ionova G. V., Mikhalko V. K. Nanochemistry and supramolecular chemistry of actinides and lanthanides: Problems and prospects // Protection of Metals and Physical Chemistry of Surfaces. — 2010. — Март (т. 46, № 2). — С. 149—169. — ISSN 2070-2051. — doi:10.1134/S2070205110020012.
- ↑ 1 2 "Lighting up cancer cells to identify low concentrations of diseased cells" (англ.). ScienceDaily.com. 20 августа 2015. Архивировано из оригинала 5 сентября 2015. Дата обращения: 1 сентября 2015.
- ↑ Yan Dong, Lei Bo, Chen Bo, Wu Xue-Jun, Liu Zhengqing, Li Na, Ge Juan, Xue Yumeng, Du Yaping, Zheng Zhiping, Zhang Hua. Synthesis of high-quality lanthanide oxybromides nanocrystals with single-source precursor for promising applications in cancer cells imaging // Applied Materials Today. — 2015. — Ноябрь (т. 1, № 1). — С. 20—26. — ISSN 2352-9407. — doi:10.1016/j.apmt.2015.06.001.
- ↑ "Lanthanides Light Up" (англ.). ACS Publications. 07 сентября 2015. Архивировано из оригинала 17 августа 2016. Дата обращения: 27 октября 2015.
{{cite news}}: Проверьте значение даты:|date=(справка) - ↑ Chen Pangkuan, Li Qiaochu, Grindy Scott, Holten-Andersen Niels. White-Light-Emitting Lanthanide Metallogels with Tunable Luminescence and Reversible Stimuli-Responsive Properties // Journal of the American Chemical Society. — 2015. — 31 августа (т. 137, № 36). — С. 11590—11593. — ISSN 0002-7863. — doi:10.1021/jacs.5b07394.
- ↑ Guillou Olivier, Daiguebonne Carole, Calvez Guillaume, Bernot Kevin. A Long Journey in Lanthanide Chemistry: From Fundamental Crystallogenesis Studies to Commercial Anticounterfeiting Taggants // Accounts of Chemical Research. — 2016. — 15 апреля (т. 49, № 5). — С. 844—856. — ISSN 0001-4842. — doi:10.1021/acs.accounts.6b00058.
Литература[править | править код]
- На английском языке:
- CRC Handbook of Chemistry and Physics / Ed.: David R. Lide; William M. Haynes. — 90th ed. — London: CRC Press, 2009. — ISBN 9781420090840, 1420090844. (недоступная ссылка)
- Greenwood, N. N.; Earnshaw, A. Chemistry of the elements. — 2nd ed. — Oxford: Butterworth-Heinemann, 1997. — 1341 p. — ISBN 0750633654, 9780750633659.
- Episodes from the History of the Rare Earth Elements / Ed.: Evans, C. H. — Kluwer Academic Publishers, 1996. — Vol. 15. — P. 268. — ISBN 978-94-010-6614-3, 978-94-009-0287-9. — doi:10.1007/978-94-009-0287-9.
- Evans, C. H. Biochemistry of the Lanthanides. — Springer US, 1990. — Vol. 8. — P. 444. — ISBN 978-1-4684-8748-0; 978-1-4684-8750-3. — doi:10.1007/978-1-4684-8748-0.
- The rare earth elements: fundamentals and applications / Ed.: David A. Atwood. — Chichester, West Sussex: John Wiley & Sons, Ltd, 2012. — 606 p. — (Encyclopedia of inorganic and bioinorganic chemistry). — ISBN 9781119950974. Архивная копия от 21 декабря 2018 на Wayback Machine
- Lanthanides, Tantalum and Niobium / Ed.: Peter Möller; Petr Černý; Francis Saupé. — Springer Berlin Heidelberg, 1989. — Vol. 7. — ISBN 978-3-642-87264-8. — doi:10.1007/978-3-642-87262-4.
- Gray, T. The Elements: A Visual Exploration of Every Known Atom in the Universe. — New York: Black Dog & Leventhal Publishers, 2009. — 240 с. — ISBN 978-1-57912-814-2.
- Handbook of the Physics and Chemistry of Rare Earths / Ed.: Karl A. Gschneidner, Jr.; LeRoy Eyring. — Vol. 11. — Elsevier Science Publishers B.V., 1988. — 594 p. — ISBN 9780444870803.
- Handbook of the Physics and Chemistry of Rare Earths / Ed.: Karl A. Gschneidner, Jr., Jean-Claude G. Bünzli, Vitalij K. Pecharsky. — Vol. 41. — North Holland, 2011. — 560 p. — ISBN 978-0-444-53590-0.
- Brumme, A. Wind Energy Deployment and the Relevance of Rare Earths. — 1st ed. — Gabler Verlag, 2014. — 87 с. — ISBN 978-3-658-04912-6; 978-3-658-04913-3. — doi:10.1007/978-3-658-04913-3.
- Robert E. Krebs. The History and Use of Our Earth's Chemical Elements: A Reference Guide. — 2nd ed. — Greenwood Press, 2006. — 422 p. — ISBN 0-313-33438-2.
- На русском языке:
- В. А. Волков, Е. В. Вонский, Г. И. Кузнецова. Выдающиеся химики мира: Биографический справочник / Под ред.: В. И. Кузнецова. — М.: Высшая школа, 1991. — 656 с. — 100 000 экз. — ISBN 5-06-001568-8.
- Популярная библиотека химических элементов. Книга вторая / Петрянов-Соколов И. В. (отв. ред.). — М.: «Наука», 1983. — С. 137. — 573 с.
- Свойства элементов / Под ред.: М. Е. Дрица. — Справ. изд. — М.: Металлургия, 1985. — 672 с. — 6500 экз.
- На украинском языке:
- А. М. Голуб. Загальна та неорганична хімiя. — К.: Вища школа, 1971. — Т. 2. — 416 с. — 6700 экз.
Ссылки[править | править код]
- Статистические данные и информация по редкоземельным элементам от USGS
- Лантаноиды
- [bse.sci-lib.com/article068666.html Лантаноиды: статья в БСЭ]
Некоторые внешние ссылки в этой статье ведут на сайты, занесённые в спам-лист |





