Белки
Белки́ (протеи́ны, полипепти́ды[1]) — высокомолекулярные органические вещества, состоящие из альфа-аминокислот, соединённых в цепочку пептидной связью. В живых организмах аминокислотный состав белков определяется генетическим кодом, при синтезе в большинстве случаев используется 20 стандартных аминокислот[2]. Множество их комбинаций определяет большое разнообразие свойств молекул белков. Кроме того, аминокислотные остатки в составе белка часто подвергаются посттрансляционным модификациям, которые могут возникать и до того, как белок начинает выполнять свою функцию, и во время его «работы» в клетке. Часто в живых организмах несколько молекул разных белков образуют сложные комплексы, например фотосинтетический комплекс и другие комплексы.

Функции белков в клетках живых организмов более разнообразны, чем функции других биополимеров — полисахаридов и ДНК. Так, белки играют ключевую роль при иммунном ответе, они могут выполнять транспортную функцию (например, гемоглобин, переносящий газы в крови, и альбумины, транспортирующие жиры), запасающую (например, казеин молока), каталитическую (пищеварительные ферменты, ДНК-полимераза и РНК-полимераза участвуют в матричных реакциях), структурную (как примеры, из белка кератина состоят волосы и ногти, коллаген и эластин являются важными компонентами соединительной ткани, тубулин образует микротрубочки), рецепторную функцию в сигнальных системах клеток (одним из примеров является белок родопсин, необходимый для работы зрительных рецепторов и обеспечивающий формирование нервного импульса в ответ на действие фотонов света). Можно также выделить несколько не столь значительных функций, например, энергетическую (при истощении) и функцию ядов (белки-яды).
Белки — важная часть питания животных и человека (основные источники: мясо, птица, рыба, молоко, орехи, бобовые, зерновые; в меньшей степени: овощи, фрукты, ягоды и грибы), поскольку в их организмах не могут синтезироваться все незаменимые аминокислоты, и часть должна поступать с белковой пищей. В процессе пищеварения ферменты разрушают потреблённые белки до аминокислот, которые используются для биосинтеза собственных белков организма или подвергаются дальнейшему распаду для получения энергии.
За впервые проведённое определение аминокислотной последовательности белка — инсулина — методом секвенирования Фредерику Сенгеру была присвоена Нобелевская премия по химии в 1958 году.
Первые трёхмерные структуры белков гемоглобина и миоглобина были установлены методом дифракции рентгеновских лучей, соответственно, Максом Перуцем и Джоном Кендрю в конце 1950-х годов[3][4], за что в 1962 году они получили Нобелевскую премию по химии.
История изучения
[править | править код]
Впервые белок был получен (в виде клейковины) в 1728 г. итальянцем Якопо Бартоломео Беккари из пшеничной муки. Белки были выделены в отдельный класс биологических молекул в XVIII веке в результате работ французского химика Антуана де Фуркруа и других учёных, в которых было отмечено свойство белков коагулировать (денатурировать) под воздействием нагревания или кислот. В то время были исследованы такие белки, как альбумин («яичный белок»), фибрин (белок из крови) и глютен из зерна пшеницы.
В начале XIX века уже были получены некоторые сведения об элементарном составе белков, было известно, что при гидролизе белков образуются аминокислоты. Некоторые из этих аминокислот (например глицин и лейцин) уже были охарактеризованы. Голландский химик Геррит Мульдер на основе анализа химического состава белков выдвинул гипотезу, что практически все белки имеют сходную эмпирическую формулу. В 1836 году Мульдер предложил первую модель химического строения белков. Основываясь на теории радикалов, он после нескольких уточнений пришёл к выводу, что минимальная структурная единица белка обладает следующим составом: C40H62N10O12. Эту единицу он назвал «протеином» (Pr) (от др.-греч. протос — первый, первичный), а теорию — «теорией протеина»[5]. Сам термин «протеин» был предложен ещё шведским химиком Якобом Берцелиусом[6]. Согласно представлениям Мульдера, каждый белок состоит из нескольких протеинных единиц, серы и фосфора. Например, он предложил записывать формулу фибрина как 10PrSP. Мульдер также исследовал продукты разрушения белков — аминокислоты и для одной из них (лейцина) с малой долей погрешности определил молекулярную массу — 131 дальтон. По мере накопления новых данных о белках теория протеина стала подвергаться критике, но, несмотря на это, до конца 1850-х всё ещё считалась общепризнанной.
К концу XIX века было исследовано большинство аминокислот, которые входят в состав белков. В конце 1880-х гг. русский учёный А. Я. Данилевский отметил существование пептидных групп (CO—NH) в молекуле белка[7][8]. В 1894 году немецкий физиолог Альбрехт Коссель выдвинул теорию, согласно которой именно аминокислоты являются основными структурными элементами белков[9]. В начале XX века немецкий химик Эмиль Фишер экспериментально доказал, что белки состоят из аминокислотных остатков, соединённых пептидными связями. Он же осуществил первый анализ аминокислотной последовательности белка и объяснил явление протеолиза.
Однако центральная роль белков в организмах не была признана до 1926 года, когда американский химик Джеймс Самнер (впоследствии — лауреат Нобелевской премии по химии) показал, что фермент уреаза является белком[10].
Сложность выделения чистых белков затрудняла их изучение. Поэтому первые исследования проводились с использованием тех полипептидов, которые легко могли быть очищены в большом количестве, то есть белков крови, куриных яиц, различных токсинов, а также пищеварительных/метаболических ферментов, выделяемых после забоя скота. В конце 1950-х годов компания Armour Hot Dog Co. смогла очистить килограмм бычьей панкреатической рибонуклеазы А, которая стала экспериментальным объектом для многих исследований.
Идея о том, что вторичная структура белков — результат образования водородных связей между аминокислотными остатками, была высказана Уильямом Астбери в 1933 году, но Лайнус Полинг считается первым учёным, который смог успешно предсказать вторичную структуру белков. Позднее Уолтер Каузман, опираясь на работы Кая Линнерстрём-Ланга, внёс весомый вклад в понимание законов образования третичной структуры белков и роли в этом процессе гидрофобных взаимодействий. В конце 1940-х — начале 1950-х годов Фредерик Сенгер разработал метод секвенирования белков, с помощью которого он к 1955 году определил аминокислотную последовательность двух цепей инсулина[11][12][13], продемонстрировав, что белки — это линейные полимеры аминокислот, а не разветвлённые (как у некоторых сахаров) цепи, коллоиды или циклолы. Первым белком, аминокислотную последовательность которого установили советские/российские учёные, стала в 1972 году аспартатаминотрансфераза[14][15].
Первые пространственные структуры белков, полученные методом дифракции рентгеновских лучей (рентгеноструктурного анализа) стали известны в конце 1950-х — начале 1960-х годов, а структуры, открытые с помощью ядерного магнитного резонанса — в 1980-х годах. В 2012 году Банк данных о белках (Protein Data Bank) содержал около 87 000 структур белков[16].
В XXI веке исследование белков перешло на качественно новый уровень, когда исследуются не только индивидуальные очищенные белки, но и одновременное изменение количества и посттрансляционных модификаций большого числа белков отдельных клеток, тканей или целых организмов. Эта область биохимии называется протеомикой. С помощью методов биоинформатики стало возможно не только обработать данные рентгеноструктурного анализа, но и предсказать структуру белка, основываясь на его аминокислотной последовательности. В настоящее время криоэлектронная микроскопия крупных белковых комплексов и предсказание пространственных структур белковых доменов с помощью компьютерных программ приближаются к атомарной точности[17].
Свойства
[править | править код]Размер
[править | править код]
Размер белка может измеряться в числе аминокислотных остатков или в дальтонах (молекулярная масса), но из-за относительно большой величины молекулы масса белка выражается в производных единицах — килодальтонах (кДа). Белки дрожжей, в среднем, состоят из 466 аминокислотных остатков и имеют молекулярную массу 53 кДа. Самый большой из известных в настоящее время белков — титин — является компонентом саркомеров мускулов; молекулярная масса его различных вариантов (изоформ) варьирует в интервале от 3000 до 3700 кДа. Титин камбаловидной мышцы (лат. soleus) человека состоит из 38 138 аминокислот[18].
Для определения молекулярной массы белков применяют такие методы, как гель-фильтрация, электрофорез в полиакриламидном геле, масс-спектрометрический анализ, седиментационный анализ и другие[19].
Физико-химические свойства
[править | править код]Амфотерность
[править | править код]Белки обладают свойством амфотерности, то есть в зависимости от условий проявляют как кислотные, так и осно́вные свойства. В белках присутствуют несколько типов химических группировок, способных к ионизации в водном растворе: карбоксильные остатки боковых цепей кислых аминокислот (аспарагиновая и глутаминовая кислоты) и азотсодержащие группы боковых цепей основных аминокислот (в первую очередь, ε-аминогруппа лизина и амидиновый остаток CNH(NH2) аргинина, в несколько меньшей степени — имидазольный остаток гистидина). Каждый белок характеризуется изоэлектрической точкой (pI) — кислотностью среды (pH), при которой суммарный электрический заряд молекул данного белка равен нулю и, соответственно, они не перемещаются в электрическом поле (например при электрофорезе). В изоэлектрической точке гидратация и растворимость белка минимальны. Величина pI зависит от соотношения кислых и основных аминокислотных остатков в белке: у белков, содержащих много кислых аминокислотных остатков, изоэлектрические точки лежат в кислой области (такие белки называют кислыми), а у белков, содержащих больше основных остатков, — в щелочной (основные белки). Значение pI данного белка также может меняться в зависимости от ионной силы и типа буферного раствора, в котором он находится, так как нейтральные соли влияют на степень ионизации химических группировок белка. pI белка можно определить, например из кривой титрования или с помощью изоэлектрофокусирования[19].
В целом, pI белка зависит от выполняемой им функции: изоэлектрическая точка большинства белков тканей позвоночных лежит в пределах от 5,5 до 7,0, однако в некоторых случаях значения лежат в экстремальных областях: так, например, для пепсина — протеолитического фермента сильнокислого желудочного сока pI ~ 1[20], а для сальмина — белка-протамина молок лосося, особенностью которого является высокое содержание аргинина, — pI ~ 12. Белки, связывающиеся с нуклеиновыми кислотами за счёт электростатического взаимодействия с фосфатными группами, часто являются основными белками. Примером таких белков служат гистоны и протамины.
Растворимость
[править | править код]Белки различаются по степени растворимости в воде. Водорастворимые белки называются альбуминами, к ним относятся белки крови и молока. К нерастворимым, или склеропротеинам, относятся, например, кератин (белок, из которого состоят волосы, шерсть млекопитающих, перья птиц и т. п.) и фиброин, входящий в состав шёлка и паутины[21]. Растворимость белка определяется не только его структурой, но внешними факторами, такими как природа растворителя, ионная сила и pH раствора[19].
Белки также делятся на гидрофильные и гидрофобные. К гидрофильным относится большинство белков цитоплазмы, ядра и межклеточного вещества, в том числе нерастворимые кератин и фиброин. К гидрофобным относится большинство белков, входящих в состав биологических мембран, — интегральных мембранных белков, которые взаимодействуют с гидрофобными липидами мембраны[22] (у этих белков, как правило, есть и гидрофильные участки).
Денатурация
[править | править код]
Денатурацией белка называют любые изменения в его биологической активности и/или физико-химических свойствах, связанные с потерей четвертичной, третичной или вторичной структуры (см. раздел «Структура белка»). Как правило, белки достаточно стабильны в тех условиях (температура, pH, давление, инфракрасное излучение и др.), в которых они в норме функционируют в организме[10]. Резкое изменение этих условий приводит к денатурации белка. В зависимости от природы денатурирующего агента выделяют механическую (сильное перемешивание или встряхивание), физическую (нагревание, охлаждение, облучение, обработка ультразвуком) и химическую (кислоты и щёлочи, поверхностно-активные вещества, мочевина) денатурацию[19].
Денатурация белка может быть полной или частичной, обратимой или необратимой. Самый известный случай необратимой денатурации белка в быту — это приготовление куриного яйца, когда под воздействием высокой температуры растворимый в воде прозрачный белок овальбумин становится плотным, нерастворимым и непрозрачным. Денатурация в некоторых случаях обратима, как в случае осаждения водорастворимых белков с помощью солей аммония (метод высаливания), и этот метод используется как способ их очистки[23].
Структура
[править | править код]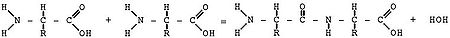
Молекулы белков представляют собой линейные полимеры, состоящие из остатков α-L-аминокислот (которые являются мономерами), также в состав белков могут входить модифицированные аминокислотные остатки и компоненты неаминокислотной природы. Для обозначения аминокислот в научной литературе используются одно- или трёхбуквенные сокращения на латинице, например, для валина: Val, V [24][25]. Хотя на первый взгляд может показаться, что использование в большинстве белков «всего» 20 аминокислот[2] ограничивает разнообразие белковых структур, на самом деле, количество их вариантов очень велико: для цепочки из 5 аминокислотных остатков оно составляет уже более 3 миллионов, а цепочка из 100 аминокислотных остатков (небольшой белок) может быть представлена более чем в 10130 вариантах. Цепочки длиной от 2 до нескольких десятков аминокислотных остатков часто называют пептидами, при большей степени полимеризации — белками, хотя это деление весьма условно.
При образовании белка в результате взаимодействия α-карбоксильной группы (–COOH) одной аминокислоты с α-аминогруппой (–NH2) другой аминокислоты образуются пептидные связи. Концы белка называют N- и C-концом, в зависимости от того, какая из групп концевого аминокислотного остатка свободна: –NH2 или –COOH, соответственно. При синтезе белка на рибосоме первым (N-концевым) аминокислотным остатком обычно является остаток метионина, а последующие остатки присоединяются к C-концу предыдущего.
Уровни организации
[править | править код]
К. Линдстрём-Ланг предложил выделять 4 уровня структурной организации белков: первичную, вторичную, третичную и четвертичную структуры. Хотя такое деление несколько устарело, им продолжают пользоваться[5]. Первичная структура (последовательность аминокислотных остатков) полипептида определяется структурой его гена и генетическим кодом, а структуры более высоких порядков формируются в процессе сворачивания белка[26]. Хотя пространственная структура белка в целом определяется его аминокислотной последовательностью, она является довольно лабильной и может зависеть от внешних условий, поэтому более правильно говорить о предпочтительной или наиболее энергетически выгодной конформации белка[5].
Первичная структура
[править | править код]
Первичная структура — последовательность аминокислотных остатков в полипептидной цепи. Первичную структуру белка, как правило, описывают, используя однобуквенные или трёхбуквенные обозначения для аминокислотных остатков.
Важными особенностями первичной структуры являются консервативные мотивы — устойчивые сочетания аминокислотных остатков, выполняющие определённую функцию и встречающиеся во многих белках. Консервативные мотивы сохраняются в процессе эволюции видов, по ним часто удаётся предсказать функцию неизвестного белка[27]. По степени гомологии (сходства) аминокислотных последовательностей белков разных организмов можно оценивать эволюционное расстояние между таксонами, к которым принадлежат эти организмы.
Первичную структуру белка можно определить методами секвенирования белков или по первичной структуре его мРНК, используя таблицу генетического кода.
Вторичная структура
[править | править код]Вторичная структура — локальное упорядочивание фрагмента полипептидной цепи, стабилизированное водородными связями. Ниже приведены самые распространённые типы вторичной структуры белков[26]:
- α-спирали — плотные витки вокруг длинной оси молекулы. Один виток составляет 3,6 аминокислотных остатка, шаг спирали равен 0,54 нм[28] (на один аминокислотный остаток приходится 0,15 нм). Спираль стабилизирована водородными связями между H и O пептидных групп, отстоящих друг от друга на 4 звена. Хотя α-спираль может быть как левозакрученной, так и правозакрученной, в белках преобладает правозакрученная. Спираль нарушают электростатические взаимодействия глутаминовой кислоты, лизина, аргинина. Расположенные близко друг к другу остатки аспарагина, серина, треонина и лейцина могут стерически мешать образованию спирали, остатки пролина вызывают изгиб цепи и тоже нарушают α-спирали;
- β-листы (складчатые слои) — несколько зигзагообразных полипептидных цепей, в которых водородные связи образуются между относительно удалёнными друг от друга (0,34 нм на аминокислотный остаток[29]) аминокислотами в первичной структуре или разными цепями белка (а не близко расположенными, как в α-спирали). Эти цепи обычно направлены N-концами в противоположные стороны (антипараллельная ориентация) или в одну сторону (параллельная β-структура). Также возможно существование смешанной β-структуры, состоящей из параллельной и антипараллельной β-структур[30]. Для образования β-листов важны небольшие размеры боковых групп аминокислот, преобладают обычно глицин и аланин;
- π-спирали;
- 310-спирали;
- неупорядоченные фрагменты.
Третичная структура
[править | править код]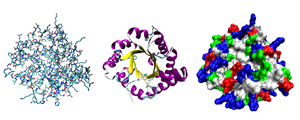
Третичная структура — пространственное строение полипептидной цепи. Структурно состоит из элементов вторичной структуры, стабилизированных различными типами взаимодействий, в которых гидрофобные взаимодействия играют важнейшую роль. В стабилизации третичной структуры принимают участие:
- ковалентные связи (между двумя остатками цистеина — дисульфидные мостики);
- ионные связи между противоположно заряженными боковыми группами аминокислотных остатков;
- водородные связи;
- гидрофобные взаимодействия. При взаимодействии с окружающими молекулами воды белковая молекула сворачивается так, чтобы неполярные боковые группы аминокислот оказались изолированы от водного раствора; на поверхности молекулы оказываются полярные гидрофильные боковые группы.
Исследования принципов укладки белков показали, что между уровнем вторичной структуры и атомарной пространственной структурой удобно выделять ещё один уровень — мотив укладки (архитектура, структурный мотив). Мотив укладки определяется взаимным расположением элементов вторичной структуры (α-спиралей и β-тяжей) в пределах белкового домена — компактной глобулы, которая может существовать или сама по себе или входить в состав более крупного белка наряду с другими доменами. Рассмотрим для примера один из характерных мотивов строения белков. Изображённый на рисунке справа глобулярный белок, триозофосфатизомераза, имеет мотив укладки, который называется α/β-цилиндр: 8 параллельных β-тяжей формируют β-цилиндр внутри ещё одного цилиндра, сложенного из 8 α-спиралей. Такой мотив обнаруживается примерно в 10 % белков[31].
Известно, что мотивы укладки являются довольно консервативными и встречаются в белках, которые не имеют ни функциональных, ни эволюционных связей. Определение мотивов укладки лежит в основе физической, или рациональной классификации белков (такой как CATH или SCOP)[31].
Для определения пространственной структуры белка применяют методы рентгеноструктурного анализа, ядерного магнитного резонанса и некоторые виды микроскопии.
Четвертичная структура
[править | править код]Четвертичная структура (или субъединичная, доменная) — взаимное расположение нескольких полипептидных цепей в составе единого белкового комплекса. Белковые молекулы, входящие в состав белка с четвертичной структурой, образуются на рибосомах по отдельности и лишь после окончания синтеза образуют общую надмолекулярную структуру. В состав белка с четвертичной структурой могут входить как идентичные, так и различающиеся полипептидные цепочки. В стабилизации четвертичной структуры принимают участие те же типы взаимодействий, что и в стабилизации третичной. Надмолекулярные белковые комплексы могут состоять из десятков молекул.
Классификация по типу строения
[править | править код]По общему типу строения белки можно разбить на три группы:
- Фибриллярные белки — образуют полимеры, их структура обычно высокорегулярна и поддерживается, в основном, взаимодействиями между разными цепями. Они образуют микрофиламенты, микротрубочки, фибриллы, поддерживают структуру клеток и тканей. К фибриллярным белкам относятся кератин и коллаген.
- Глобулярные белки — водорастворимы, общая форма молекулы более или менее сферическая.
- Мембранные белки — имеют пересекающие клеточную мембрану домены, но части их выступают из мембраны в межклеточное окружение и цитоплазму клетки. Мембранные белки выполняют функцию рецепторов, то есть осуществляют передачу сигналов, а также обеспечивают трансмембранный транспорт различных веществ. Белки-транспортёры специфичны, каждый из них пропускает через мембрану только определённые молекулы или определённый тип сигнала.
Простые и сложные белки
[править | править код]Помимо пептидных цепей, в состав многих белков входят и неаминокислотные группы, и по этому критерию белки делят на две большие группы — простые и сложные белки (протеиды). Простые белки состоят только из полипептидных цепей, сложные белки содержат также неаминокислотные, или простетические, группы. В зависимости от химической природы простетических групп среди сложных белков выделяют следующие классы[21]:
- Гликопротеины, содержащие в качестве простетической группы ковалентно связанные углеводные остатки; гликопротеины, содержащие остатки мукополисахаридов относятся к подклассу протеогликанов. В образовании связи с углеводными остатками обычно участвуют гидроксильные группы серина или треонина. Большая часть внеклеточных белков, в частности, иммуноглобулины относится к гликопротеинам. В протеогликанах углеводная часть составляет ~95 % от общей массы молекулы белка, они являются основным компонентом межклеточного матрикса;
- Липопротеины, содержащие в качестве простетической части нековалентно связанные липиды. Липопротеины, образованные белками-аполипопротеинами и связывающимися с ними липидами, используются для транспорта липидов в крови;
- Металлопротеиды, содержащие негемовые координационно связанные ионы металлов. Среди металлопротеидов есть белки, выполняющие депонирующие и транспортные функции (например железосодержащие ферритин и трансферрин) и ферменты (например, цинксодержащая карбоангидраза и различные супероксиддисмутазы, содержащие в активных центрах ионы меди, марганца, железа и других металлов);
- Нуклеопротеиды, содержащие нековалентно связанные ДНК или РНК. К нуклеопротеидам относится хроматин, из которого состоят хромосомы;
- Фосфопротеины, содержащие в качестве простетической группы ковалентно связанные остатки фосфорной кислоты. В образовании сложноэфирной связи с фосфатом участвуют гидроксильные группы серина, треонина и тирозина. Фосфопротеином, в частности, является казеин молока[32];
- Хромопротеиды, содержащие окрашенные простетические группы различной химической природы. К ним относится множество белков с металлсодержащей порфириновой простетической группой, выполняющие разнообразные функции: гемопротеины (белки, содержащие в качестве простетической группы гем, например гемоглобин и цитохромы), хлорофиллы, флавопротеиды с флавиновой группой и др.
Биофизика белка
[править | править код]Физические свойства белка в клетке с учётом водной оболочки и краудинга макромолекул[англ.] очень сложны. В пользу гипотезы о белке, как о упорядоченной «кристаллоподобной системе» — «апериодическом кристалле»[33][34] — свидетельствуют данные рентгеноструктурного анализа (вплоть до разрешения в 1 ангстрем)[35], высокая плотность упаковки[36], кооперативность процесса денатурации[37] и другие факты[38].
В пользу другой гипотезы, о жидкообразных свойствах белков в процессах внутриглобулярных движений (модель ограниченной прыжковой или непрерывной диффузии), свидетельствуют эксперименты по рассеянию нейтронов[39], мёссбауэровской спектроскопии[40][41].
Синтез
[править | править код]
Биосинтез
[править | править код]Универсальный способ: рибосомный синтез
[править | править код]Белки синтезируются живыми организмами из аминокислот на основе информации, закодированной в генах. Каждый белок состоит из уникальной последовательности аминокислотных остатков, которая определяется нуклеотидной последовательностью гена, кодирующего данный белок. Генетический код представляет собой способ перевода нуклеотидной последовательности ДНК (через РНК) в аминокислотную последовательность полипептидной цепи. Этот код определяет соответствие трёхнуклеотидных участков РНК, называемых кодонами, и определённых аминокислот, которые включаются в состав белка: последовательность нуклеотидов АУГ, например, соответствует метионину. Поскольку ДНК состоит из четырёх типов нуклеотидов, то общее число возможных кодонов равно 64; а так как в белках используется 20 аминокислот[2], то многие аминокислоты определяются более чем одним кодоном. Три кодона являются незначащими: они служат сигналами остановки синтеза полипептидной цепи и называются терминаторными кодонами, или стоп-кодонами[42].
Гены, кодирующие белки, сначала транскрибируются в последовательность нуклеотидов матричной РНК (мРНК) ферментами РНК-полимеразами. В подавляющем большинстве случаев белки живых организмов синтезируются на рибосомах — многокомпонентных молекулярных машинах, присутствующих в цитоплазме клеток. Процесс синтеза полипептидной цепи рибосомой на матрице мРНК называется трансляцией[42].
Рибосомный синтез белков принципиально одинаков у прокариот и эукариот, но различается в некоторых деталях. Так, мРНК прокариот может считываться рибосомами в аминокислотную последовательность белков сразу после транскрипции или даже до её завершения[43]. У эукариот же первичный транскрипт сначала должен пройти серию модификаций и переместиться в цитоплазму (к месту локализации рибосом), прежде чем может начаться трансляция. Скорость синтеза белков выше у прокариот и может достигать 20 аминокислот в секунду[44].

Ещё до начала трансляции ферменты аминоацил-тРНК-синтетазы специфично присоединяют аминокислоты к соответствующим им транспортным РНК (тРНК). Участок тРНК, который называется антикодоном, может комплементарно спариваться с кодоном мРНК, обеспечивая тем самым включение присоединённого к тРНК аминокислотного остатка в полипептидную цепь в соответствии с генетическим кодом.
Во время начальной стадии трансляции, инициации, инициаторный (обычно метиониновый) кодон узнаётся малой субъединицей рибосомы, к которой при помощи белковых факторов инициации присоединена аминоацилированная метиониновая тРНК. После узнавания стартового кодона к малой субъединице рибосомы присоединяется большая субъединица, и начинается вторая стадия трансляции — элонгация. При каждом шаге рибосомы от 5'- к 3'-концу мРНК считывается один кодон путём образования водородных связей между ним и комплементарным ему антикодоном транспортной РНК, к которой присоединён соответствующий аминокислотный остаток. Образование пептидной связи между последним аминокислотным остатком растущего пептида и аминокислотным остатком, присоединённым к тРНК, катализируется рибосомальной РНК (рРНК), образующей пептидилтрансферазный центр рибосомы. Этот центр позиционирует атомы азота и углерода в положении, благоприятном для прохождения реакции. Третья и последняя стадия трансляции, терминация, происходит при достижении рибосомой стоп-кодона, после чего белковые факторы терминации гидролизуют связь между последней тРНК и полипептидной цепью, прекращая её синтез. В рибосомах белки всегда синтезируются от N- к C-концу[42].
Нерибосомный синтез
[править | править код]У низших грибов и некоторых бактерий известен дополнительный (нерибосомный, или мультиферментный) способ биосинтеза пептидов, как правило, небольших и необычной структуры. Синтез этих пептидов, обычно вторичных метаболитов, осуществляется высокомолекулярным белковым комплексом, NRS-синтазой, без непосредственного участия рибосом. NRS-синтаза обычно состоит из нескольких доменов или отдельных белков, осуществляющих селекцию аминокислот, образование пептидной связи и высвобождение синтезированного пептида. Вместе эти домены составляют модуль. Каждый модуль обеспечивает включение одной аминокислоты в синтезируемый пептид. NRS-синтазы, таким образом, могут состоять из одного или более модулей. Иногда в состав этих комплексов входит домен, способный изомеризовать L-аминокислоты (нормальная форма) в D-форму[45][46].
Химический синтез
[править | править код]Короткие белки могут быть синтезированы химическим путём с использованием методов органического синтеза, например, химического лигирования[47]. Чаще всего химический синтез пептида происходит в направлении от C-конца к N-концу, в противоположность биосинтезу на рибосомах. Методом химического синтеза получают короткие иммуногенные пептиды (эпитопы), которые затем инъецируют животным с целью получения специфичных антител или гибридо́м. Кроме того, этот способ также используется для получения ингибиторов некоторых ферментов[48]. Химический синтез позволяет вводить в состав белков аминокислотные остатки, не встречающиеся в обычных белках, например такие, к боковым цепям которых присоединены флюоресцентные метки. Химические методы синтеза белков имеют ряд ограничений: они неэффективны при длине белка более 300 аминокислотных остатков, искусственно синтезированные белки могут иметь неправильную третичную структуру и у них отсутствую характерные посттрансляционные модификации (см. ниже).
Посттрансляционная модификация
[править | править код]
После завершения трансляции большинство белков подвергается дальнейшим химическим модификациям, которые называются посттрансляционными модификациями[49]. Известно более двухсот вариантов посттрансляционных модификаций белков[50].
Посттрансляционные модификации могут регулировать продолжительность существования белков в клетке, их ферментативную активность и взаимодействия с другими белками. В ряде случаев посттрансляционные модификации являются обязательным этапом созревания белка, в противном случае он оказывается функционально неактивным. Например при созревании инсулина и некоторых других гормонов необходим ограниченный протеолиз полипептидной цепи, а при созревании белков плазматической мембраны — гликозилирование.
Посттрансляционные модификации могут быть как широко распространёнными, так и редкими, вплоть до уникальных. Примером универсальной модификации служит убиквитинирование (присоединение к белку цепи из нескольких молекул короткого белка убиквитина), которое служит сигналом к расщеплению этого белка протеасомой[51]. Другой распространённой модификацией является гликозилирование — считается, что около половины белков человека гликозилировано[52]. К редким модификациям относят тирозинирование/детирозинирование и полиглицилирование тубулина[53].
Один и тот же белок может подвергаться многочисленным модификациям. Так, гистоны (белки, входящие в состав хроматина у эукариот) в разных условиях могут подвергаться более чем 150 различным модификациям[54].
Посттрансляционные модификации делят на:
- модификации главной цепи;
- отщепление N-концевого остатка метионина;
- ограниченный протеолиз — удаление фрагмента белка, которое может происходить с концов (отщепление сигнальных последовательностей) или, в отдельных случаях, в середине молекулы (созревание инсулина);
- присоединение различных химических групп к свободным амино- и карбоксильной группам (N-ацилирование, миристоилирование и др.);
- модификации боковых цепей аминокислот;
- присоединение или отщепление небольших химических групп (гликозилирование, фосфорилирование и др.);
- присоединение липидов и углеводородов;
- изменение стандартных аминокислотных остатков на нестандартные (образование цитруллина);
- образование дисульфидных мостиков между остатками цистеина;
- присоединение небольших белков (сумоилирование и убиквитинирование).
Жизненный цикл
[править | править код]Внутриклеточный транспорт и сортировка
[править | править код]Синтезируемые в цитоплазме эукариотической клетки белки должны транспортироваться в разные органоиды клетки: ядро, митохондрии, эндоплазматический ретикулум (ЭПР), аппарат Гольджи, лизосомы и др., а некоторые белки должны попасть во внеклеточную среду[55]. Для попадания в определённый отдел клетки белок должен обладать специфической меткой. В большинстве случаев такой меткой является часть аминокислотной последовательности самого белка (лидерный пептид, или сигнальная последовательность белка), но в некоторых случаях меткой служат посттрансляционно присоединённые к белку олигосахариды[56].
Транспорт белков в ЭПР осуществляется по мере их синтеза, так как рибосомы, синтезирующие белки с сигнальной последовательностью для ЭПР, «садятся» на специальные белки на его внешней мембране[57]. Из ЭПР в аппарат Гольджи, а оттуда в лизосомы и на внешнюю мембрану или во внеклеточную среду белки попадают путём везикулярного транспорта. В ядро белки, обладающие сигналом ядерной локализации, попадают через ядерные поры. В митохондрии и хлоропласты белки, обладающие соответствующими сигнальными последовательностями, попадают через специфические белковые поры-транслокаторы при участии шаперонов.
Поддержание структуры и деградация
[править | править код]Поддержание правильной пространственной структуры белков принципиально для их нормального функционирования. Неправильное сворачивание белков, приводящее к их агрегации, может быть вызвано мутациями, окислением, стрессовыми условиями или глобальными изменениями в физиологии клетки. Агрегация белков является характерным признаком старения организма. Считается, что неправильное сворачивание белков является причиной или усугубляет такие заболевания, как муковисцидоз, лизосомная болезнь накопления[англ.], а также нейродегенеративные расстройства (болезни Альцгеймера, Хантингтона и Паркинсона)[58].
В процессе эволюции клетками было выработано четыре основных механизма для противодействия агрегации белков. Первые два — повторное сворачивание (переукладка) с помощью шаперонов и расщепление протеазами — встречаются как у бактерий, так и у высших организмов. Аутофагия и накопление неправильно свёрнутых белков в особых немембранных органеллах характерны для эукариотов[29][59].
Шапероны
[править | править код]
Способность белков восстанавливать правильную трёхмерную структуру после денатурации позволила выдвинуть гипотезу о том, что вся информация о конечной структуре белка содержится в его аминокислотной последовательности. В настоящее время общепризнана теория о том, что стабильная конформация белка обладает минимальной свободной энергией по сравнению с другими возможными конформациями этого полипептида[60].
В клетках существует группа белков, функция которых — обеспечение правильного сворачивания других белков после их синтеза на рибосоме, восстановление структуры белков после их повреждения, а также создание и диссоциация белковых комплексов. Эти белки называются шаперонами. Концентрация многих шаперонов в клетке возрастает при резком повышении температуры окружающей среды, поэтому они относятся к группе Hsp (англ. heat shock proteins — белки теплового шока)[61]. Важность нормальной работы шаперонов для функционирования организма может быть проиллюстрирована на примере шаперона α-кристаллина, входящего в состав хрусталика глаза человека. Мутации в этом белке приводят к помутнению хрусталика из-за агрегирования белков и, как результат, к катаракте[62].
Протеолиз
[править | править код]Если третичная структура белков не может быть восстановлена, они разрушаются клеткой. Ферменты, осуществляющие деградацию белков, называются протеазами. По месту атаки молекулы субстрата протеолитические ферменты делятся на эндопептидазы и экзопептидазы:
- Эндопептидазы, или протеиназы, расщепляют пептидные связи внутри пептидной цепи. Они узнают и связывают короткие пептидные последовательности субстратов и относительно специфично гидролизуют связи между определёнными аминокислотными остатками.
- Экзопептидазы гидролизуют пептиды с концов цепи: аминопептидазы — с N-конца, карбоксипептидазы — с С-конца. Наконец, дипептидазы расщепляют только дипептиды.
По механизму катализа Международный союз по биохимии и молекулярной биологии выделяет несколько классов протеаз, среди них сериновые протеазы, аспарагиновые протеазы, цистеиновые протеазы и металлопротеазы[63].
Особый тип протеазы — протеасома, крупная мультисубъединичная протеаза, присутствующая в ядре и в цитоплазме эукариот, архей и некоторых бактерий[64][65].
Для того, чтобы белок-мишень расщепился протеасомой, он должен быть помечен путём присоединения к нему маленького белка убиквитина. Реакция присоединения убиквитина катализируется ферментами убиквитинлигазами. Присоединение первой молекулы убиквитина к белку служит для лигаз сигналом для дальнейшего присоединения молекул убиквитина. В результате к белку оказывается присоединена полиубиквитиновая цепь, которая связывается с протеасомой и обеспечивает расщепление белка-мишени[64][65]. В целом, эта система получила название убиквитин-зависимой деградации белка. Деградация 80—90 % внутриклеточных белков происходит при участии протеасомы.
Деградация белка в пероксисомах важна для протекания многих клеточных процессов, включая клеточный цикл, регуляцию экспрессии генов и ответ на окислительный стресс.
Аутофагия
[править | править код]
Аутофагия — это процесс деградации долгоживущих биомолекул, в частности, белков, а также органелл в лизосомах (у млекопитающих) или вакуолях (у дрожжей). Аутофагия сопровождает жизнедеятельность любой нормальной клетки, но стимулами к усилению процессов аутофагии в клетках могут служить нехватка питательных веществ, наличие в цитоплазме повреждённых органелл и, наконец, наличие в цитоплазме частично денатурированных белков и их агрегатов[66].
Различают три типа аутофагии: микроаутофагию, макроаутофагию и шаперон-зависимую аутофагию.
При микроаутофагии макромолекулы и обломки клеточных мембран захватываются лизосомой. Таким путём клетка может переваривать белки при нехватке энергии или строительного материала (например при голодании). Но процессы микроаутофагии происходят и при нормальных условиях и в целом неизбирательны. Иногда в ходе микроаутофагии перевариваются и органоиды; так, у дрожжей описана микроаутофагия пероксисом и частичная микроаутофагия ядер, при которой клетка сохраняет жизнеспособность[66].
При макроаутофагии участок цитоплазмы (часто содержащий какие-либо органоиды) окружается мембранным компартментом, похожим на цистерну эндоплазматического ретикулума. В результате этот участок отделяется от остальной цитоплазмы двумя мембранами. Такие двухмембранные органеллы называются аутофагосомами. Аутофагосомы сливаются с лизосомами, образуя аутофаголизосомы, в которых органеллы и остальное содержимое аутофагосом перевариваются. Видимо, макроаутофагия также неизбирательна, хотя часто подчёркивается, что с помощью неё клетка может избавляться от «отслуживших свой срок» органоидов (митохондрий, рибосом и др.)[66].
Третий тип аутофагии — шаперон-зависимая. При этом способе происходит направленный транспорт частично денатурированных белков из цитоплазмы сквозь мембрану лизосомы в её полость, где они перевариваются. Этот тип аутофагии, описанный только у млекопитающих, индуцируется стрессом[59].

JUNQ и IPOD
[править | править код]В условиях стресса, когда эукариотическая клетка не может справиться с накоплением большого числа денатурированных белков, они могут направляться в один из двух типов временных органелл — JUNQ и IPOD[англ.][67].
JUNQ (англ. JUxta Nuclear Quality control compartment — околоядерный компартмент контроля качества белков) ассоциирован со внешней стороной ядерной мембраны и содержит убиквитинированные белки, которые могут быстро переходить в цитоплазму, а также шапероны и протеасомы. Предполагаемая функция JUNQ состоит в переукладке и/или деградации белков[29].
IPOD (англ. Insoluble Protein Deposit — место отложения нерастворимых белков) расположен около центральной вакуоли и содержит неподвижные агрегаты формирующих амилоиды белков. Накопление этих белков в IPOD может предотвращать их взаимодействие с нормальными клеточными структурами, поэтому предполагают, что это включение имеет защитную функцию[29].
Функции белков в организме
[править | править код]Также как и другие биологические макромолекулы (полисахариды, липиды и нуклеиновые кислоты), белки являются необходимыми компонентами всех живых организмов и играют важную роль в жизнедеятельности клетки. Белки осуществляют процессы обмена веществ. Они входят в состав внутриклеточных структур — органелл и цитоскелета, секретируются во внеклеточное пространство, где могут выступать в качестве сигнала, передаваемого между клетками, участвовать в гидролизе пищи и образовании межклеточного вещества.
Классификация белков по их функциям является достаточно условной, так как один и тот же белок может выполнять несколько функций. Хорошо изученным примером такой многофункциональности служит лизил-тРНК-синтетаза — фермент из класса аминоацил-тРНК-синтетаз, которая не только присоединяет остаток лизина к тРНК, но и регулирует транскрипцию нескольких генов[68]. Многие функции белки выполняют благодаря своей ферментативной активности. Так, ферментами являются двигательный белок миозин, регуляторные белки протеинкиназы, транспортный белок натрий-калиевая аденозинтрифосфатаза и др.

Каталитическая функция
[править | править код]Наиболее хорошо известная функция белков в организме — катализ различных химических реакций. Ферменты — это белки, обладающие специфическими каталитическими свойствами, то есть каждый фермент катализирует одну или несколько сходных реакций. Ферменты катализируют реакции расщепления сложных молекул (катаболизм) и их синтеза (анаболизм), в том числе репликацию и репарацию ДНК и матричный синтез РНК. К 2013 году было описано более 5000 ферментов[69][70]. Ускорение реакции в результате ферментативного катализа может быть огромным: реакция, катализируемая ферментом оротидин-5'-фосфатдекарбоксилазой, например, протекает в 10¹⁷ раз быстрее некатализируемой (период полуреакции декарбоксилирования оротовой кислоты составляет 78 миллионов лет без фермента и 18 миллисекунд с участием фермента)[71]. Молекулы, которые присоединяются к ферменту и изменяются в результате реакции, называются субстратами.
Хотя ферменты обычно состоят из сотен аминокислотных остатков, только небольшая часть из них взаимодействует с субстратом, и ещё меньшее количество — в среднем 3—4 аминокислотных остатка, часто расположенные далеко друг от друга в первичной структуре — напрямую участвуют в катализе[72]. Часть молекулы фермента, которая обеспечивает связывание субстрата и катализ, называется активным центром.
Международный союз биохимии и молекулярной биологии в 1992 году предложил окончательный вариант иерархической номенклатуры ферментов, основанной на типе катализируемых ими реакций[73]. Согласно этой номенклатуре названия ферментов всегда должны иметь окончание -аза и образовываться от названий катализируемых реакций и их субстратов. Каждому ферменту приписывается индивидуальный код, по которому легко определить его положение в иерархии ферментов. По типу катализируемых реакций все ферменты делят на 6 классов:
- КФ 1: Оксидоредуктазы, катализирующие окислительно-восстановительные реакции;
- КФ 2: Трансферазы, катализирующие перенос химических групп с одной молекулы субстрата на другую;
- КФ 3: Гидролазы, катализирующие гидролиз химических связей;
- КФ 4: Лиазы, катализирующие разрыв химических связей без гидролиза с образованием двойной связи в одном из продуктов;
- КФ 5: Изомеразы, катализирующие структурные или геометрические изменения в молекуле субстрата;
- КФ 6: Лигазы, катализирующие образование химических связей между субстратами за счёт гидролиза дифосфатной связи АТФ или сходного трифосфата.
Структурная функция
[править | править код]Структурные белки цитоскелета, как своего рода арматура, придают форму клеткам и многим органоидам и участвуют в изменении формы клеток. Большинство структурных белков являются филаментозными: мономеры актина и тубулина это, например, глобулярные, растворимые белки, но после полимеризации они формируют длинные нити, из которых состоит цитоскелет, позволяющий клетке поддерживать форму[74]. Коллаген и эластин — основные компоненты межклеточного вещества соединительной ткани (например, хряща), а из другого структурного белка кератина состоят волосы, ногти, перья птиц и некоторые раковины.

Защитная функция
[править | править код]Существует несколько видов защитных функций белков:
- Физическая защита. Физическую защиту организма обеспечивают коллаген — белок, образующий основу межклеточного вещества соединительных тканей (в том числе костей, хряща, сухожилий и глубоких слоёв кожи (дермы)); кератин, составляющий основу роговых щитков, волос, перьев, рогов и др. производных эпидермиса. Обычно такие белки рассматривают как белки со структурной функцией. Примерами белков этой группы служат фибриногены и тромбины[75], участвующие в свёртывании крови.
- Химическая защита. Связывание токсинов белковыми молекулами может обеспечивать их детоксикацию. Особенно важную роль в детоксикации у человека играют ферменты печени, расщепляющие яды или переводящие их в растворимую форму, что способствует их быстрому выведению из организма[76].
- Иммунная защита. Белки, входящие в состав крови и других биологических жидкостей, участвуют в защитном ответе организма как на повреждение, так и на атаку патогенов. Белки системы комплемента и антитела (иммуноглобулины) относятся к белкам второй группы; они нейтрализуют бактерии, вирусы или чужеродные белки. Антитела, входящие в состав адаптивной иммунной системы, присоединяются к чужеродным для данного организма веществам, антигенам, и тем самым нейтрализуют их, направляя к местам уничтожения. Антитела могут секретироваться в межклеточное пространство или закрепляться в мембранах специализированных В-лимфоцитов, которые называются плазмоцитами[77].
Регуляторная функция
[править | править код]Многие процессы внутри клеток регулируются белковыми молекулами, которые не служат ни источником энергии, ни строительным материалом для клетки. Эти белки регулируют продвижение клетки по клеточному циклу, транскрипцию, трансляцию, сплайсинг, активность других белков и многие другие процессы. Регуляторную функцию белки осуществляют либо за счёт ферментативной активности (например, протеинкиназы), либо за счёт специфичного связывания с другими молекулами. Так, факторы транскрипции, белки-активаторы и белки-репрессоры, могут регулировать интенсивность транскрипции генов, связываясь с их регуляторными последовательностями. На уровне трансляции считывание многих мРНК также регулируется присоединением белковых факторов[78].
Важнейшую роль в регуляции внутриклеточных процессов играют протеинкиназы и протеинфосфатазы — ферменты, которые активируют или подавляют активность других белков путём присоединения к ним или отщепления фосфатных групп.

Сигнальная функция
[править | править код]Сигнальная функция белков — способность белков служить сигнальными веществами, передавая сигналы между клетками, тканями, о́рганами и организмами. Часто сигнальную функцию объединяют с регуляторной, так как многие внутриклеточные регуляторные белки тоже осуществляют передачу сигналов.
Сигнальную функцию выполняют белки-гормоны, цитокины, факторы роста и др.
Гормоны переносятся кровью. Большинство гормонов животных — это белки или пептиды. Связывание гормона с его рецептором является сигналом, запускающим ответную реакцию клетки. Гормоны регулируют концентрации веществ в крови и клетках, рост, размножение и другие процессы. Примером таких белков служит инсулин, который регулирует концентрацию глюкозы в крови.
Клетки взаимодействуют друг с другом с помощью сигнальных белков, передаваемых через межклеточное вещество. К таким белкам относятся, например, цитокины и факторы роста.
Цитокины — пептидные сигнальные молекулы. Они регулируют взаимодействия между клетками, определяют их выживаемость, стимулируют или подавляют рост, дифференцировку, функциональную активность и апоптоз, обеспечивают согласованность действий иммунной, эндокринной и нервной систем. Примером цитокинов может служить фактор некроза опухоли, который передаёт сигналы воспаления между клетками организма[79].
Транспортная функция
[править | править код]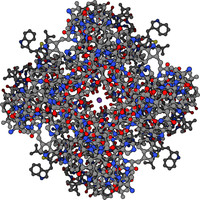
Растворимые белки, участвующие в транспорте малых молекул, должны иметь высокое сродство (аффинность) к субстрату, когда он присутствует в высокой концентрации, и легко его высвобождать в местах низкой концентрации субстрата. Примером транспортных белков можно назвать гемоглобин, который переносит кислород из лёгких к остальным тканям и углекислый газ от тканей к лёгким, а также гомологичные ему белки, найденные во всех царствах живых организмов[80].
Некоторые мембранные белки участвуют в транспорте малых молекул через мембрану клетки, изменяя её проницаемость. Липидный компонент мембраны водонепроницаем (гидрофобен), что предотвращает диффузию полярных или заряженных (ионы) молекул. Мембранные транспортные белки принято подразделять на белки-каналы и белки-переносчики. Белки-каналы содержат внутренние заполненные водой поры, которые позволяют ионам (через ионные каналы) или молекулам воды (через белки-аквапорины) перемещаться через мембрану. Многие ионные каналы специализируются на транспорте только одного иона; так, калиевые и натриевые каналы часто различают эти сходные ионы и пропускают только один из них[81]. Белки-переносчики связывают, подобно ферментам, каждую переносимую молекулу или ион и, в отличие от каналов, могут осуществлять активный транспорт с использованием энергии АТФ. «Электростанция клетки» — АТФ-синтаза, которая осуществляет синтез АТФ за счёт протонного градиента, также может быть отнесена к мембранным транспортным белкам[82].
Запасная (резервная) функция
[править | править код]К таким белкам относятся так называемые резервные белки, которые запасаются в качестве источника энергии и вещества в семенах растений (например, глобулины 7S и 11S) и яйцеклетках животных[83]. Ряд других белков используется в организме в качестве источника аминокислот, которые в свою очередь являются предшественниками биологически активных веществ, регулирующих процессы метаболизма.
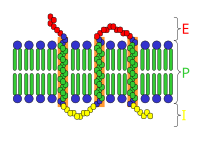
Рецепторная функция
[править | править код]Белковые рецепторы могут находиться как в цитоплазме, так и встраиваться в клеточную мембрану. Одна часть молекулы рецептора воспринимает сигнал, которым чаще всего служит химическое вещество, а в некоторых случаях — свет, механическое воздействие (например, растяжение) и другие стимулы. При воздействии сигнала на определённый участок молекулы — белок-рецептор — происходят её конформационные изменения. В результате меняется конформация другой части молекулы, осуществляющей передачу сигнала на другие клеточные компоненты. Существует несколько механизмов передачи сигнала. Некоторые рецепторы катализируют определённую химическую реакцию; другие служат ионными каналами, которые при действии сигнала открываются или закрываются; третьи специфически связывают внутриклеточные молекулы-посредники. У мембранных рецепторов часть молекулы, связывающаяся с сигнальной молекулой, находится на поверхности клетки, а домен, передающий сигнал, — внутри[84].
Моторная (двигательная) функция
[править | править код]
Целый класс моторных белков обеспечивает движения организма, например, сокращение мышц, в том числе локомоцию (миозин), перемещение клеток внутри организма (например, амёбоидное движение лейкоцитов), движение ресничек и жгутиков, а также активный и направленный внутриклеточный транспорт (кинезин, динеин). Динеины и кинезины проводят транспортировку молекул вдоль микротрубочек с использованием гидролиза АТФ в качестве источника энергии. Динеины переносят молекулы и органоиды из периферических частей клетки по направлению к центросоме, кинезины — в противоположном направлении[85][86]. Динеины также отвечают за движение ресничек и жгутиков эукариот. Цитоплазматические варианты миозина могут принимать участие в транспорте молекул и органоидов по микрофиламентам.
Белки в обмене веществ
[править | править код]Большинство микроорганизмов и растений могут синтезировать 20 стандартных аминокислот, а также дополнительные (нестандартные) аминокислоты, например, цитруллин. Но если аминокислоты есть в окружающей среде, даже микроорганизмы сохраняют энергию путём транспорта аминокислот внутрь клеток и выключения их биосинтетических путей[87].
Аминокислоты, которые не могут быть синтезированы животными, называются незаменимыми. Основные ферменты в биосинтетических путях, например, аспартаткиназа, которая катализирует первый этап в образовании лизина, метионина и треонина из аспартата, отсутствуют у животных.
Животные, в основном, получают аминокислоты из белков, содержащихся в пище. Белки разрушаются в процессе пищеварения, который обычно начинается с денатурации белка путём помещения его в кислотную среду и гидролиза с помощью ферментов, называемых протеазами. Некоторые аминокислоты, полученные в результате пищеварения, используются для синтеза белков организма, а остальные превращаются в глюкозу в процессе глюконеогенеза или используются в цикле Кребса. Использование белка в качестве источника энергии особенно важно в условиях голодания, когда собственные белки организма, в особенности мускулов, служат источником энергии[88]. Аминокислоты также являются важным источником азота в питании организма.
Единых норм потребления белков человеком нет. Микрофлора толстого кишечника синтезирует аминокислоты, которые не учитываются при составлении белковых норм.
Сладкие белки
[править | править код]Группа природных растительных белков, обладающих сладким вкусом. Выделяются преимущественно из семян и плодов тропических растений, произрастающих в Африке и Азии.
Сладкие белки в 100-3000 раз слаще обычного сахара (сахароза) в пересчете на массу, при этом отличаются небольшой калорийностью. На текущий момент идентифицированы семь белков сладкого вкуса, включая тауматин I и II (Ivengar, 1979), браззеин (Ming, D., Hellekant, G., 1994), мабинлин (Hu, Z., Min, H., 1983), монеллин (Inglett, G. E., May, J. F., 1969), куркулин (Yamashita H., 1990), пентадин (Morris JA, 1972), лизоцим (Maehashi, K., Udaka, S., 1998) и один белок, модифицирующий сладкий вкус — миракулин (Theerasilp S, Kurihara, 1988). За исключением лизоцима, который получают из яичного белка, остальные белки выделяют из тропических растений.
Сладкие белки используются в пищевой индустрии как безопасная альтернатива сахару и синтетическим подсластителям[89]. Они многократно (в несколько тысяч раз) слаще сахарозы[90], при этом отличаются низкой калорийностью (то есть, не провоцируют ожирение) и не влияют на выработку инсулина[91]. Кроме того, в отличие от сахара, сладкие белки не оказывают вредного воздействия на зубы и ротовую полость[89].
Подсластители на белковой основе используются для изготовления диетических продуктов, показанных при диабете и ожирении[89].
В качестве подсластителей и корректоров вкуса сладкие белки одобрены к применению в США[92], странах Евросоюза[93], Японии, России[94]. Они применяются как самостоятельно, так и в сочетании с другими натуральными и синтетическими сахарозаменителями[89].
Методы изучения
[править | править код]Структуру и функции белков изучают как на очищенных препаратах in vitro, так и в их естественном окружении в живом организме, in vivo. Исследования чистых белков в контролируемых условиях полезны для определения их функций: кинетических особенностей каталитической активности ферментов, относительного сродства к различным субстратам и т. п. Исследования белков in vivo в клетках или в целых организмах предоставляют дополнительную информацию о том, где они функционируют и как регулируется их активность[95].
Молекулярной и клеточной биологии
[править | править код]
Методы молекулярной и клеточной биологии обычно применяются для изучения синтеза и локализации белков в клетке. Широко применяется метод изучения локализации, основанный на синтезе в клетке химерного белка, состоящего из исследуемого белка, соединённого с «репортёром», например, зелёным флуоресцентным белком (GFP)[96]. Расположение такого белка в клетке можно увидеть с помощью флуоресцентного микроскопа[97]. Кроме того, белки можно визуализировать с помощью распознающих их антител, которые в свою очередь несут флуоресцентную метку. Часто одновременно с изучаемым белком визуализируют известные белки таких органелл, как эндоплазматический ретикулум, аппарат Гольджи, лизосомы и вакуоли, что позволяет более точно определить локализацию изучаемого белка[98].
Иммуногистохимические методы обычно используют антитела, которые конъюгированы с ферментами, катализирующими реакцию образования люминесцирующего или окрашенного продукта, что позволяет сравнить локализацию и количество изучаемого белка в образцах. Более редкой методикой определения расположения белков является равновесное ультрацентрифугирование клеточных фракций в градиенте сахарозы или хлорида цезия[99][100].
Наконец, один из классических методов — это иммуноэлектронная микроскопия, которая принципиально похожа на иммунофлуоресцентную микроскопию с тем отличием, что используется электронный микроскоп. Образец подготавливается для электронной микроскопии, а затем обрабатывается антителами к белку, которые соединены с электронно-плотным материалом, как правило, золотом[101].
С помощью сайт-направленного мутагенеза исследователи могут изменять аминокислотную последовательность белка и, следовательно, его пространственную структуру, расположение в клетке и регуляцию его активности. С помощью этого метода, используя модифицированные тРНК[102], можно также ввести в белок искусственные аминокислоты, и сконструировать белки с новыми свойствами[103].
Биохимические
[править | править код]Для выполнения анализа in vitro белок должен быть очищен от других клеточных компонентов. Этот процесс обычно начинается с разрушения клеток и получения так называемого клеточного экстракта. Далее методами центрифугирования и ультрацентрифугирования этот экстракт может быть разделён на: фракцию, содержащую растворимые белки; фракцию, содержащую мембранные липиды и белки; и фракцию, содержащую клеточные органеллы и нуклеиновые кислоты.

Осаждение белков методом высаливания применяется для разделения белковых смесей, а также позволяет сконцентрировать белки. Седиментационный анализ (центрифугирование) позволяет фракционировать белковые смеси по значению константы седиментации отдельных белков, измеряемой в сведбергах (S)[104]. Чтобы выделить необходимый белок или белки на основе таких свойств, как молекулярная масса, заряд и аффинность, затем используются различные виды хроматографии[105][106]. Кроме того, белки могут быть выделены в соответствии с их зарядом с использованием электрофокусирования[107].
Чтобы упростить процесс очистки белков, часто используется генетическая инженерия, которая позволяет создать производные белков, удобные для очистки, не затрагивая их структуры или активности. «Метки», представляющие собой небольшие аминокислотные последовательности, например, цепочку из 6 и более остатков гистидина, и прикрепляются к одному из концов белка. Когда экстракт клеток, синтезировавших «меченый» белок, пропускается через хроматографическую колонку, содержащую ионы никеля, гистидин связывается никелем и остаётся на колонке, в то время как остальные компоненты лизата беспрепятственно проходят сквозь колонку (никель-хелатная хроматография). Множество других меток было разработано, чтобы помочь исследователям выделить специфические белки из сложных смесей чаще всего методом аффинной хроматографии[108].
Степень очистки белка можно определить, если известны его молекулярная масса и изоэлектрическая точка — с помощью различных видов гель-электрофореза — или измерения ферментативной активности, если белок является ферментом. Масс-спектрометрия позволяет идентифицировать выделенный белок по его молекулярной массе и массе его фрагментов[109].
Для определения количества белка в образце используют ряд методов[110]: биуретовый метод, микробиуретовый метод, метод Бредфорда, метод Лоури, спектрофотометрический метод.
Протеомика
[править | править код]Совокупность белков клетки называется протеомом, его изучение — протеомикой, названной по аналогии с геномикой. Основные экспериментальные методы протеомики включают:
- 2D-электрофорез, который позволяет разделять многокомпонентные белковые смеси[111];
- масс-спектрометрию, которая позволяет идентифицировать белки по массе составляющих их пептидов с высокой пропускной способностью[112];
- белковые микрочипы, которые позволяют одновременно измерять содержание большого количества белков в клетке[113];
- дрожжевую двугибридную систему[англ.], которая позволяет систематически изучать белок-белковые взаимодействия[114].
Совокупность всех биологически значимых взаимодействий белков в клетке называется интерактомом[115]. Систематическое исследование структуры белков, представляющих все возможные типы третичных структур, называется структурной геномикой[116].
Предсказание структуры и моделирование
[править | править код]Предсказание пространственной структуры с помощью компьютерных программ (in silico) позволяется строить модели белков, структура которых ещё не определена экспериментально[117]. Самый успешный тип предсказания структур, известный как гомологическое моделирование, опирается на существующую «шаблонную» структуру, сходную по аминокислотной последовательности с моделируемым белком[118]. Методы предсказания пространственной структуры белков используются в развивающейся области генетической инженерии белков, с помощью которой уже получены новые третичные структуры белков[119]. Более сложной вычислительной задачей является прогнозирование межмолекулярных взаимодействий, таких как молекулярная стыковка и предсказание белок-белковых взаимодействий[120].
Укладка и межмолекулярные взаимодействия белков могут быть смоделированы с использованием молекулярной механики[англ.], в частности, молекулярной динамики и метода Монте-Карло, которые всё чаще используют преимущества параллельных и распределённых вычислений (например, проект Folding@home[121]). Укладка небольших α-спиральных белковых доменов, например, белка виллина[122] или одного из белков ВИЧ[123], были успешно смоделированы in silico. С помощью гибридных методов, сочетающих стандартную молекулярную динамику с квантовой механикой, были исследованы электронные состояния зрительного пигмента родопсина[124].
См. также
[править | править код]- Гиперпротеинемия
- Жиры
- Предсказание структуры белка
- Предсказание функции белка
- Прионы
- Сплайсинг белков
- Углеводы
Примечания
[править | править код]- ↑ С химической точки зрения все белки являются полипептидами. Однако короткие, меньше 30 аминокислотных остатков в длину полипептиды, особенно химически синтезированные, нельзя назвать белками.
- ↑ 1 2 3 Относительно недавно были найдены ещё 2 аминокислоты — селеноцистеин и пирролизин, которые входят в состав белков в клетках архей, однако их распространение в природе невелико. Таким образом, на сегодняшний известны уже́ 22 аминокислоты, которые входят в состав биосинтезируемых белков на основании наследственной информации, заложенной в природный геном живых организмов.
- ↑ Perutz M. F., Rossmann M. G., Cullis A. F., Muirhead H., Will G., North A. C. Structure of haemoglobin: a three-dimensional Fourier synthesis at 5.5-A. resolution, obtained by X-ray analysis (англ.) // Nature. — 1960. — Vol. 185, iss. 4711. — P. 416—422. — PMID 18990801.
- ↑ Kendrew J. C., Bodo G., Dintzis H. M., Parrish R. G., Wyckoff H., Phillips D. C. A three-dimensional model of the myoglobin molecule obtained by x-ray analysis (англ.) // Nature. — 1958. — Vol. 181, iss. 4610. — P. 662—666. — PMID 13517261.
- ↑ 1 2 3 Ю. А. Овчинников. Биоорганическая химия. — Москва: Просвещение, 1987. — С. 24—26.
- ↑ Henry Leicester. Berzelius, Jöns Jacob // Dictionary of Scientific Biography 2. — New York: Charles Scribner’s Sons, 1980. — С. 90—97. — ISBN 0-684-10114-9.
- ↑ Данилевский А.Я. Биолого-химические сообщения о белковых веществах (материалы для химической конституции и биогенеза их) // Физиологический сборник. — 1888. — Т. 1. — С. 289.
- ↑ Цветков Л. А. § 38. Белки // Органическая химия. Учебник для 10 класса. — 20-е изд. — М.: Просвещение, 1981. — С. 184—193. — 1 210 000 экз.
- ↑ Белки // Химическая энциклопедия. — Москва: Советская энциклопедия, 1988. Архивировано 3 февраля 2012 года.
- ↑ 1 2 N. H. Barton, D. E. G. Briggs, J. A. Eisen. Evolution. — Cold Spring Harbor Laboratory Press, 2007. — С. 38. — ISBN 978-0-87969-684-9.
- ↑ Нобелевская лекция Ф. Сэнгера. Дата обращения: 3 января 2013. Архивировано 5 января 2013 года.
- ↑ Sanger F., Tuppy H. The amino-acid sequence in the phenylalanyl chain of insulin. 2. The investigation of peptides from enzymic hydrolysates // Biochem J. — 1951. — Т. 49, вып. 4. — С. 481—490. — PMID 14886311. Архивировано 9 апреля 2022 года.
- ↑ Sanger F., Thompson E. O. The amino-acid sequence in the glycyl chain of insulin. II. The investigation of peptides from enzymic hydrolysates // Biochem J. — 1953. — Т. 53, вып. 3. — С. 366—374. — PMID 13032079.
- ↑ Овчинников Ю.А., Браунштейн А.Е., Егоров Ц.А., Поляновский О.Л., Алданова Н.А., Фейгина М.Ю., Липкин В.М., Абдулаев Н.Г., Гришин Е.В., Киселёв А.П., Модянов Н.Н., Носиков В.В. Полная первичная структура аспартатаминотрансферазы // Докл. АН СССР. — 1972. — Т. 207. — С. 728—731.
- ↑ Филиппович Ю.Б. Белки и их роль в процессах жизнедеятельности // Книга для чтения по органической химии. Пособие для учащихся. — М.: Просвещение, 1975. — С. 216—234.
- ↑ Protein Data Bank. Rutgers and UCSD. — Biological Macromolecular Resource. Дата обращения: 26 декабря 2012. Архивировано 27 декабря 2012 года.
- ↑ Yahav T., Maimon T., Grossman E., Dahan I., Medalia O. Cryo-electron tomography: gaining insight into cellular processes by structural approaches // Curr Opin Struct Biol. — 2011. — Т. 21, вып. 5. — С. 670—677. — PMID 21813274.
- ↑ Fulton A., Isaacs W. Titin, a huge, elastic sarcomeric protein with a probable role in morphogenesis // Bioessays. — 1991. — Т. 13, вып. 4. — С. 157—161. — PMID 1859393.
- ↑ 1 2 3 4 Х.-Д. Якубке, Х. Ешкайт. Глава 3.5 Физико-химические свойства // Аминокислоты, пептиды, белки. — Москва: Мир, 1985. — С. 356—363.
- ↑ EC 3.4.23.1 — pepsin A Пепсин А в информационной системе BRENDA. Дата обращения: 18 мая 2008. Архивировано 19 февраля 2020 года.
- ↑ 1 2 А. Н. Несмеянов, Н. А. Несмеянов. Начала органической химии. Книга вторая 221. Дата обращения: 26 декабря 2012. Архивировано 27 декабря 2012 года.
- ↑ Singer S. J. The structure and insertion of integral proteins in membranes // Annu Rev Cell Biol. — 1990. — Т. 6. — С. 247—296. — PMID 2275815.
- ↑ Страйер Л. Биохимия в 3 томах. — Москва: Мир, 1984.
- ↑ Nomenclature and symbolism for amino acids and peptides (Recommendations 1983) (англ.) // Pure and Applied Chemistry. — 1984-01-01. — Vol. 56, iss. 5. — P. 595–624. — ISSN 1365-3075. — doi:10.1351/pac198456050595. Архивировано 18 мая 2023 года.
- ↑ Аминокислоты // Химическая энциклопедия. — Москва: Советская энциклопедия, 1988. Архивировано 28 мая 2022 года.
- ↑ 1 2 Ленинджер А. Основы биохимии в 3 томах. — Москва: Мир, 1985.
- ↑ Koonin E. V., Tatusov R. L., Galperin M. Y. Beyond complete genomes: from sequence to structure and function // Curr Opin Struct Biol.. — 1998. — Т. 8, вып. 3. — С. 355—363. — PMID 9666332.
- ↑ David Whitford. Proteins: Structure and Function. — Wiley, 2005. — С. 41. — P. 542. — ISBN 978-0471498940.
- ↑ 1 2 3 4 David Whitford. Proteins: Structure and Function. — Wiley, 2005. — С. 45. — P. 542. — ISBN 978-0471498940.
- ↑ Финкельштейн А. В., Птицын О. Б. Вторичные структуры полипептидных цепей // Физика белка. — Москва: КДУ, 2005. — С. 86—95. — ISBN 5-98227-065-2.
- ↑ 1 2 Финкельштейн А. В., Птицын О. Б. Лекция 15 // Физика белка. — Москва: КДУ, 2005. — С. 189—205.
- ↑ А. Н. Несмеянов, Н. А. Несмеянов. Начала органической химии. Книга первая 331. Дата обращения: 26 декабря 2012. Архивировано 27 декабря 2012 года.
- ↑ Шрёдингер Э. Что такое жизнь с точки зрения физики? = пер. с англ. А.А. Малиновского. — Москва: РИМИС, 2009. — С. 176. — ISBN 978-5-9650-0057-9.
- ↑ Волькенштейн М.В. Биофизика. — Москва: Наука, 1988.
- ↑ Huber R. Conformational flexibility in protein molecules (англ.) // Nature. — 1979. — Vol. 280, iss. 5723. — P. 538—539. — PMID 460436.
- ↑ Richards F. M. Areas, volumes, packing and protein structure // Annu Rev Biophys Bioeng. — 1977. — Т. 6. — С. 151—176. — PMID 326146.
- ↑ Привалов П.Л. Стабильность белков и гидрофобные взаимодействия // Биофизика. — 1987. — Т. 32, вып. 5. — С. 742—760. — PMID 3318936.
- ↑ Морозов В. Н., Морозова Т. Я. Механические свойства глобулярных белков // Молекулярная биология. — 1983. — Т. 17, вып. 3. — С. 577—586. — PMID 6877232.
- ↑ Doster W., Cusack S., Petry W. Dynamical transition of myoglobin revealed by inelastic neutron scattering (англ.) // Nature. — 1989. — Vol. 337, iss. 6209. — P. 754—756. — PMID 2918910.
- ↑ Parak F., Frolov E. N., Mössbauer R. L., Goldanskii V. I. Dynamics of metmyoglobin crystals investigated by nuclear gamma resonance absorption // J Mol Biol. — 1981. — Т. 145, вып. 4. — С. 825—833. — PMID 7265223.
- ↑ Шайтан К.В., Рубин А.Б. Стохастическая динамика и электронно-конформационные взаимодействия в белках // Биофизика. — 1985. — Т. 30, вып. 3. — С. 517—526. — PMID 3896324.
- ↑ 1 2 3 Спирин А. С. Глава II. Информационная РНК и генетический код // Молекулярная биология. Структура рибосомы и биосинтез белка. — Москва: Высшая школа, 1986. — С. 9—16.
- ↑ Benjamin Lewin. Genes VIII. — Upper Saddle River, NJ: Pearson Prentice Hall, 2004. — ISBN 0131439812.
- ↑ Dobson C. M. The nature and significance of protein folding // Mechanisms of Protein Folding (англ.) / Pain R. H.. — 2nd. — New York, NY: Oxford University Press, 2000.
- ↑ Stack D., Neville C., Doyle S. Nonribosomal peptide synthesis in Aspergillus fumigatus and other fungi // Microbiology. — 2007. — Т. 153, вып. Pt 5. — С. 1297—1306. — PMID 17464044. (недоступная ссылка)
- ↑ Welker M., von Döhren H. Cyanobacterial peptides — nature's own combinatorial biosynthesis // FEMS Microbiol Rev. — 2006. — Т. 30, вып. 4. — С. 530—563. — PMID 16774586.
- ↑ Wilken J., Kent S. B. Chemical protein synthesis // Curr Opin Biotechnol. — 1998. — Т. 9, вып. 4. — С. 412—426. — PMID 9720266.
- ↑ Dawson P. E., Kent S. B. Synthesis of native proteins by chemical ligation // Annu Rev Biochem. — 2000. — Т. 69. — С. 923—960. — PMID 10966479.
- ↑ Jones D. T. Protein secondary structure prediction based on position-specific scoring matrices // J Mol Biol. — 1999. — Т. 292, вып. 2. — С. 195—202. — PMID 10493868.
- ↑ Jensen O. N. Interpreting the protein language using proteomics // Nat Rev Mol Cell Biol. — 2006. — Т. 7, вып. 6. — С. 391—403. — PMID 16723975.
- ↑ Demartino G. N., Gillette T. G. Proteasomes: machines for all reasons (англ.) // Cell. — Cell Press, 2007. — Vol. 129, iss. 4. — P. 659—662. — PMID 17512401. Архивировано 18 марта 2021 года.
- ↑ Walsh G., Jefferis R. Post-translational modifications in the context of therapeutic proteins (англ.) // Nature Biotechnology. — Nature Publishing Group, 2006. — Vol. 24, iss. 10. — P. 1241—1252. — PMID 17033665.
- ↑ Rosenbaum, J. Cytoskeleton: functions for tubulin modifications at last (англ.) // Curr Biol : journal. — 2000. — Vol. 10. — P. 801—803. — ISSN 0960-9822. — doi:10.1016/S0960-9822(00)00767-3. — PMID 11084355.
- ↑ Bronner C., Chataigneau T., Schini-Kerth V. B., Landry Y. The "Epigenetic Code Replication Machinery", ECREM: a promising drugable target of the epigenetic cell memory // Curr Med Chem. — 2007. — Т. 14, вып. 25. — С. 2629—2641. — PMID 17979715.
- ↑ Alberts B., Johnson A., Lewis J., et al. Chapter 12. Intracellular Compartments and Protein Sorting // Molecular Biology of the Cell. 4th edition. — New York: Garland Science, 2002. Архивировано 21 июня 2022 года.
- ↑ Hegde R. S., Bernstein H. D. The surprising complexity of signal sequences // Trends Biochem Sci. — 2006. — Т. 31, вып. 10. — С. 563—571. — PMID 16919958.
- ↑ Saraogi I., Shan S. O. Molecular mechanism of co-translational protein targeting by the signal recognition particle // Traffic. — Т. 12, вып. 5. — С. 535—542.
- ↑ Alberti S. Molecular mechanisms of spatial protein quality control // Prion. — 2012. — Т. 6, вып. 5. — С. 437—442. — doi:10.4161/pri.22470. — PMID 23051707.
- ↑ 1 2 Shintani T., Klionsky D. J. Autophagy in health and disease: a double-edged sword (англ.) // Science. — 2004. — Vol. 306, iss. 5698. — P. 990—995. — PMID 15528435. Архивировано 12 июня 2020 года.
- ↑ Anfinsen C. B. Principles that Govern the Folding of Protein Chains (англ.) // Science. — 1973. — Vol. 181, iss. 4096. — P. 223—230. — PMID 4124164. Нобелевская лекция. Автор, совместно со Стэнфордом Муром и Уильямом Стейном, получил Нобелевскую премию по химии за «изучение рибонуклеазы, в особенности взаимоотношений между аминокислотной последовательностью фермента и его биологически активной конформацией».
- ↑ Ellis R. J., van der Vies S. M. Molecular chaperones // Annu Rev Biochem. — 1991. — Т. 60. — С. 321—347. — doi:10.1146/annurev.bi.60.070191.001541. — PMID 1679318.
- ↑ Sun Y., MacRae T. H. The small heat shock proteins and their role in human disease // FEBS J. — 2005. — Т. 272, вып. 11. — С. 2613—2627. — PMID 15943797. Архивировано 22 июля 2014 года.
- ↑ Union of Biochemistry and Molecular Biology (NC-IUBMB). Nomenclature Committee of the International Union of Biochemistry and Molecular Biology (NC-IUBMB). Дата обращения: 29 декабря 2012. Архивировано 5 января 2013 года.
- ↑ 1 2 Lodish H, Berk A, Matsudaira P., Kaiser C. A., Krieger M., Scott M. P., Zipursky S. L., Darnell J. Chapter 3 // Molecular cell biology. — 5th. — New York: W.H. Freeman and CO, 2004. — С. 66—72. — ISBN 0-7167-4366-3.
- ↑ 1 2 Сорокин А. В., Ким Е. Р., Овчинников Л. П. Протеасомная система деградации и процессинга белков // Успехи биологической химии. — 2009. — Т. 49. — С. 3—76. Архивировано 7 октября 2013 года.
- ↑ 1 2 3 Farrugia G., Balzan R. Oxidative stress and programmed cell death in yeast // Front Oncol. — 2012. — Т. 2, вып. 64. — doi:10.3389/fonc.2012.00064. — PMID 22737670.
- ↑ Kaganovich D., Kopito R., Frydman J. Misfolded proteins partition between two distinct quality control compartments (англ.) // Nature. — 2008. — Vol. 454, iss. 7208. — P. 1088—1095. — doi:10.1038/nature07195. — PMID 18756251. Архивировано 15 декабря 2019 года.
- ↑ Yannay-Cohen N., Razin E. Translation and transcription: the dual functionality of LysRS in mast cells // Mol Cells. — 2006. — Т. 22, вып. 2. — С. 127—132. — PMID 17085962.
- ↑ База данных номенклатуры ферментов ENZYME. Дата обращения: 25 апреля 2013. Архивировано 28 апреля 2013 года.
- ↑ Bairoch A. The ENZYME database in 2000 // Nucleic Acids Res. — 2000. — Т. 28, вып. 1. — С. 304—305. — PMID 10592255. Архивировано 3 февраля 2022 года.
- ↑ Radzicka A., Wolfenden R. A proficient enzyme (англ.) // Science. — 1995. — Vol. 267, iss. 5194. — P. 90—93. — PMID 7809611.
- ↑ The Catalytic Site Atlas at The European Bioinformatics Institute. Дата обращения: 28 сентября 2007. Архивировано 20 июня 2013 года.
- ↑ Номенклатура ферментов на сайте Международного союза биохимии и молекулярной биологии. Дата обращения: 25 апреля 2013. Архивировано 28 апреля 2013 года.
- ↑ Erickson H. P. Evolution of the cytoskeleton // Bioessays. — 2007. — Т. 29, вып. 7. — С. 668—677. — PMID 17563102. Архивировано 26 апреля 2021 года.
- ↑ Wolberg A. S. Thrombin generation and fibrin clot structure // Blood Rev. — 2007. — Т. 21, вып. 3. — С. 131—142. — PMID 17208341.
- ↑ Я. Кольман, К.-Г. Рем. Наглядная биохимия. — Москва: Мир, 2000. — С. 308—309.
- ↑ Li J., Barreda D. R., Zhang Y. A., Boshra H., Gelman A. E., Lapatra S., Tort L., Sunyer J. O. B lymphocytes from early vertebrates have potent phagocytic and microbicidal abilities // Nat Immunol. — 2006. — Т. 7, вып. 10. — С. 1116—1124. — PMID 16980980.
- ↑ Hinnebusch A. G. Translational regulation of GCN4 and the general amino acid control of yeast // Annu Rev Microbiol. — 2005. — Т. 59. — С. 407—450. — PMID 16153175.
- ↑ Повещенко А. Ф., Абрамов В. В., Козлов В. В. Цитокины — факторы нейроэндокринной регуляции // Успехи физиологических наук. — 2007. — Т. 38, вып. 3. — С. 40—46.
- ↑ Wittenberg JB. On optima: the case of myoglobin-facilitated oxygen diffusion. Gene. 2007 Aug 15. 398(1—2):156—161.
- ↑ Driessen AJ, Nouwen N. Protein Translocation Across the Bacterial Cytoplasmic Membrane. Annu Rev Biochem. 2007 Dec 13 [Epub ahead of print]
- ↑ Drory O., Nelson N. The emerging structure of vacuolar ATPases (англ.) // Physiology (Bethesda).. — 2006. — Vol. 21. — P. 317—325. Архивировано 21 ноября 2008 года.
- ↑ Eliot M. Hermana and Brian A. Larkins. Protein Storage Bodies and Vacuoles // The Plant Cell. — 1999. — Т. 11. — С. 601—613.
- ↑ Dupré DJ, Hébert TE. Biosynthesis and trafficking of seven transmembrane receptor signalling complexes. Cell Signal. 2006;18(10):1549—1559
- ↑ Karp G. Cell and Molecular Biology: Concepts and Experiments, Fourth ed, pp. 346—358. John Wiley and Sons, Hoboken, NJ. 2005.
- ↑ Schroer, Trina A. Dynactin. Annual Review of Cell and Developmental Biology. 2004 20, 759—779. PMID 15473859
- ↑ Voet D, Voet JG. Biochemistry Vol 1 3rd ed., Hoboken, NJ (2004).
- ↑ Brosnan J. Interorgan amino acid transport and its regulation (англ.) // J Nutr[англ.] : journal. — 2003. — Vol. 133, no. 6 Suppl 1. — P. 2068S—72S. — PMID 12771367. Архивировано 26 июля 2006 года.
- ↑ 1 2 3 4 Fawibe O.O. Ogunyale O.G. Ajiboye A.A. Agboola D.A. Botanical and Protein Sweeteners (англ.) // Journal of Advanced Laboratory Research in Biology : journal. — 2014. — 1 October (vol. 5, no. 4). — P. 169-187. — ISSN 0976-7614. Архивировано 26 апреля 2023 года.
- ↑ Henrik Wel, Kees Loeve. Isolation and Characterization of Thaumatin I and II, the Sweet-Tasting Proteins from Thaumatococcus daniellii Benth (англ.) // European Journal of Biochemistry. — 1972-12. — Vol. 31, iss. 2. — P. 221–225. — ISSN 1432-1033 0014-2956, 1432-1033. — doi:10.1111/j.1432-1033.1972.tb02522.x.
- ↑ I. Faus. Recent developments in the characterization and biotechnological production of sweet-tasting proteins (англ.) // Applied Microbiology and Biotechnology. — 2000-02-01. — Vol. 53, iss. 2. — P. 145–151. — ISSN 1432-0614. — doi:10.1007/s002530050001.
- ↑ DEPARTMENT OF HEALTH AND HUMAN SERVICES Food and Drug Administration GENERALLY RECOGNIZED AS SAFE (GRAS) NOTICE (англ.). www.fda.gov. USA DEPARTMENT OF HEALTH AND HUMAN SERVICES (29 февраля 2016). Дата обращения: 21 июня 2023. Архивировано 28 декабря 2022 года.
- ↑ EFSA Panel on Food Additives and Nutrient Sources added to Food (ANS). Scientific Opinion on the safety of the extension of use of thaumatin (E 957) // EFSA Journal. — 2015-11. — Т. 13, вып. 11. — doi:10.2903/j.efsa.2015.4290.
- ↑ ТР ТС 029/2012 Технический регламент Таможенного союза "Требования безопасности пищевых добавок, ароматизаторов и технологических вспомогательных средств" от 20 июля 2012 - docs.cntd.ru. docs.cntd.ru. Дата обращения: 21 июня 2023. Архивировано 9 июня 2022 года.
- ↑ David Whitford. Proteins: Structure and Function. — Wiley, 2005. — С. 313. — P. 542. — ISBN 978-0471498940.
- ↑ Stepanenko O. V., Verkhusha V. V., Kuznetsova I. M., Uversky V. N., Turoverov K. K. Fluorescent proteins as biomarkers and biosensors: throwing color lights on molecular and cellular processes (англ.) // Current Protein & Peptide Science : journal. — 2008. — Vol. 9, no. 4. — P. 338—369. — doi:10.2174/138920308785132668. — PMID 18691124. — PMC 2904242.
- ↑ Yuste R. Fluorescence microscopy today (англ.) // Nature Methods : journal. — 2005. — Vol. 2, no. 12. — P. 902—904. — doi:10.1038/nmeth1205-902. — PMID 16299474.
- ↑ Margolin W. Green fluorescent protein as a reporter for macromolecular localization in bacterial cells (англ.) // Methods (San Diego, Calif.)[англ.] : journal. — 2000. — Vol. 20, no. 1. — P. 62—72. — doi:10.1006/meth.1999.0906. — PMID 10610805. Архивировано 9 июня 2019 года.
- ↑ Walker J. H., Wilson K. Principles and Techniques of Practical Biochemistry (англ.). — Cambridge, UK: Cambridge University Press, 2000. — P. 287—289. — ISBN 0-521-65873-X.
- ↑ Остерман Л. А. Методы исследования белков и нуклеиновых кислот: Электрофорез и ультрацентрифугирование (практическое пособие). — М.: «Наука», 1981. — С. 240—263. — 288 с.
- ↑ Mayhew T. M., Lucocq J. M. Developments in cell biology for quantitative immunoelectron microscopy based on thin sections: a review (англ.) // Histochemistry and Cell Biology[англ.] : journal. — 2008. — Vol. 130, no. 2. — P. 299—313. — doi:10.1007/s00418-008-0451-6. — PMID 18553098. — PMC 2491712.
- ↑ Hohsaka T., Sisido M. Incorporation of non-natural amino acids into proteins (англ.) // Current Opinion in Chemical Biology. — Elsevier, 2002. — Vol. 6, no. 6. — P. 809—815. — doi:10.1016/S1367-5931(02)00376-9. — PMID 12470735.
- ↑ Cedrone F., Ménez A., Quéméneur E. Tailoring new enzyme functions by rational redesign (англ.) // Current Opinion in Structural Biology : journal. — Elsevier, 2000. — Vol. 10, no. 4. — P. 405—410. — doi:10.1016/S0959-440X(00)00106-8. — PMID 10981626.
- ↑ Colea J. L., Hansenb J. C. «Analytical Ultracentrifugation as a Contemporary Biomolecular Research Tool» // J. Biomol. Techn. V 10. 1999. P. 163—176
- ↑ Murray R. F., Harper H. W., Granner D. K., Mayes P. A., Rodwell V. W. Harper's Illustrated Biochemistry (англ.). — New York: Lange Medical Books/McGraw-Hill, 2006. — ISBN 0-07-146197-3.
- ↑ Остерман Л. А. Хроматография белков и нуклеиновых кислот. — Москва, 1985.
- ↑ Hey J., Posch A., Cohen A., Liu N., Harbers A. Fractionation of complex protein mixtures by liquid-phase isoelectric focusing (англ.) // Methods in Molecular Biology[англ.] : journal. — 2008. — Vol. 424. — P. 225—239. — ISBN 978-1-58829-722-8. — doi:10.1007/978-1-60327-064-9_19. — PMID 18369866.
- ↑ Terpe K. Overview of tag protein fusions: from molecular and biochemical fundamentals to commercial systems (англ.) // Applied Microbiology and Biotechnology[англ.] : journal. — Springer, 2003. — Vol. 60, no. 5. — P. 523—533. — doi:10.1007/s00253-002-1158-6. — PMID 12536251.
- ↑ Н. А. Понькин. Что в имени твоём, масс-спектрометрия? Архивная копия от 4 марта 2016 на Wayback Machine сайт Всероссийского масс-спектрометрического общества
- ↑ Editor: John M. Walker. The Protein Protocols Handbook. — 3. — Springer. — С. 3—69. — 1985 с. — (Springer Protocols Handbooks). — ISBN 978-1-60327-474-6. Архивировано 18 августа 2016 года. Архивированная копия. Дата обращения: 29 сентября 2017. Архивировано 18 августа 2016 года.
- ↑ Görg A., Weiss W., Dunn M. J. Current two-dimensional electrophoresis technology for proteomics (англ.) // Proteomics : journal. — 2004. — Vol. 4, no. 12. — P. 3665—3685. — doi:10.1002/pmic.200401031. — PMID 15543535.
- ↑ Conrotto P, Souchelnytskyi S. Proteomic approaches in biological and medical sciences: principles and applications // Exp Oncol.. — Т. 30, вып. 3. — С. 171—180. — PMID 18806738.
- ↑ Joos T., Bachmann J. Protein microarrays: potentials and limitations (англ.) // Frontiers in Bioscience[англ.] : journal. — Frontiers in Bioscience[англ.], 2009. — Vol. 14, no. 14. — P. 4376—4385. — doi:10.2741/3534. — PMID 19273356. Архивировано 28 ноября 2012 года.
- ↑ Koegl M., Uetz P. Improving yeast two-hybrid screening systems (англ.) // Briefings in Functional Genomics & Proteomics. — 2007. — Vol. 6, no. 4. — P. 302—312. — doi:10.1093/bfgp/elm035. — PMID 18218650. Архивировано 15 апреля 2013 года. Архивированная копия. Дата обращения: 1 января 2013. Архивировано из оригинала 15 апреля 2013 года.
- ↑ Plewczyński D., Ginalski K. The interactome: predicting the protein–protein interactions in cells (англ.) // Cellular & Molecular Biology Letters : journal. — 2009. — Vol. 14, no. 1. — P. 1—22. — doi:10.2478/s11658-008-0024-7. — PMID 18839074.
- ↑ Zhang C., Kim S. H. Overview of structural genomics: from structure to function (англ.) // Current Opinion in Chemical Biology : journal. — Elsevier, 2003. — Vol. 7, no. 1. — P. 28—32. — doi:10.1016/S1367-5931(02)00015-7. — PMID 12547423.
- ↑ Zhang Y. Progress and challenges in protein structure prediction (англ.) // Current Opinions in Structural Biology : journal. — 2008. — Vol. 18, no. 3. — P. 342—348. — doi:10.1016/j.sbi.2008.02.004. — PMID 18436442. — PMC 2680823.
- ↑ Xiang Z. Advances in homology protein structure modeling (англ.) // Current Protein and Peptide Science. — 2006. — Vol. 7, no. 3. — P. 217—227. — doi:10.2174/138920306777452312. — PMID 16787261. — PMC 1839925.
- ↑ Kuhlman B., Dantas G., Ireton G. C., Varani G., Stoddard B. L., Baker D. Design of a novel globular protein fold with atomic-level accuracy (англ.) // Science : journal. — 2003. — Vol. 302, no. 5649. — P. 1364—1368. — doi:10.1126/science.1089427. — . — PMID 14631033. Архивировано 8 марта 2020 года.
- ↑ Ritchie D. W. Recent progress and future directions in protein–protein docking (англ.) // Current Protein and Peptide Science : journal. — 2008. — Vol. 9, no. 1. — P. 1—15. — doi:10.2174/138920308783565741. — PMID 18336319.
- ↑ Scheraga H. A., Khalili M., Liwo A. Protein-folding dynamics: overview of molecular simulation techniques (англ.) // Annual Review of Physical Chemistry[англ.] : journal. — 2007. — Vol. 58. — P. 57—83. — doi:10.1146/annurev.physchem.58.032806.104614. — . — PMID 17034338.
- ↑ Zagrovic B., Snow C. D., Shirts M. R., Pande V. S. Simulation of folding of a small alpha-helical protein in atomistic detail using worldwide-distributed computing (англ.) // Journal of Molecular Biology[англ.] : journal. — 2002. — Vol. 323, no. 5. — P. 927—937. — doi:10.1016/S0022-2836(02)00997-X. — PMID 12417204.
- ↑ Herges T., Wenzel W. In silico folding of a three helix protein and characterization of its free-energy landscape in an all-atom force field (англ.) // Physical Review Letters : journal. — 2005. — Vol. 94, no. 1. — P. 018101. — doi:10.1103/PhysRevLett.94.018101. — . — PMID 15698135.
- ↑ Hoffmann M., Wanko M., Strodel P., König P. H., Frauenheim T., Schulten K., Thiel W., Tajkhorshid E., Elstner M. Color tuning in rhodopsins: the mechanism for the spectral shift between bacteriorhodopsin and sensory rhodopsin II (англ.) // Journal of the American Chemical Society[англ.] : journal. — 2006. — Vol. 128, no. 33. — P. 10808—10818. — doi:10.1021/ja062082i. — PMID 16910676.
Литература
[править | править код]- Альбертс Б., Брей Д., Льюис Дж. и др. Молекулярная биология клетки. В 3 томах. — М.: Мир, 1994. — ISBN 5-03-001986-3.
- Ленинджер А. Основы биохимии. В 3 томах. — М.: Мир, 1985.
- Страйер Л. Биохимия. В 3 томах. — М.: Мир, 1984.
Ссылки
[править | править код]- Свойства аминокислот и белков
- PDB — Protein Data Bank
- Обзоры статей о фолдинге белков на русском
- Хаос и порядок дискретных систем в свете синергетической теории информации (В статье проводится количественный анализ первичной структуры белков со стороны соотношения хаоса и порядка)
- Научно-популярный фильм «Белок»
Эта статья входит в число избранных статей русскоязычного раздела Википедии. |