Дофамин
| Дофамин | |||
|---|---|---|---|
 | |||
| Общие | |||
| Систематическое наименование |
2-(3,4-дигидроксифенил)-этиламин | ||
| Хим. формула | C8H11NO2 | ||
| Физические свойства | |||
| Состояние | твёрдое, белое порошкообразное с характерным запахом | ||
| Молярная масса | 153,1784 ± 0,008 г/моль | ||
| Плотность | 1,26 г/см³ | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 128 °C | ||
| Химические свойства | |||
| Константа диссоциации кислоты | 8,93 | ||
| Растворимость | |||
| • в воде | 60 г/100 мл воды | ||
| Классификация | |||
| Рег. номер CAS | 51-61-6 | ||
| PubChem | 681 | ||
| Рег. номер EINECS | 2 EC | ||
| SMILES | |||
| InChI | |||
| ChEBI | 18243 | ||
| ChemSpider | 661 | ||
| Безопасность | |||
| ЛД50 | 1780 мг/кг (крысы, перорально)[1] | ||
| Токсичность | слабо токсичен, ирритант | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Дофами́н (допами́н[2], DA) — гормон и нейромедиатор. Синтезируется из L-ДОФА. В дальнейшем из дофамина может синтезироваться норадреналин.
В мозге дофамин участвует в регуляции поведения и моторики. В кровеносных сосудах вызывает их расширение, в почках увеличивает выделение мочи, в поджелудочной железе снижает выработку инсулина, в пищеварительной системе снижает перистальтику желудочно-кишечного тракта и защищает слизистую кишечника, в иммунной системе снижает активность лимфоцитов. За исключением кровеносных сосудов, дофамин в каждой из этих периферических систем синтезируется локально и оказывает свое действие вблизи клеток, которые его выделяют.
Дофамин используется как лекарственный препарат для внутривенных инъекций при сердечной недостаточности или кардиогенном шоке.
Нейромедиатор[править | править код]
Чувство удовлетворения[править | править код]
Считается, что дофамин является одним из химических факторов внутреннего подкрепления (ФВП) и служит важной частью «системы вознаграждения» мозга, поскольку вызывает чувство удовольствия (или удовлетворения), чем влияет на процессы мотивации и обучения[3][4]. Однако, это мнение, продвигаемое популярной культурой и средствами массовой информации, ошибочно. Последние исследования показывают[5][6][7], что дофамин не вызывает чувства удовольствия или удовлетворения, а создаёт сильное ощущение предвкушения от получения результата или нежелания его получения, подобное тому, которое испытывают люди перед оргазмом или при сильном отвращении. Дофамин естественным образом вырабатывается в больших количествах во время положительного, по субъективному представлению человека, опыта — к примеру: секса, приёма вкусной пищи, приятных телесных ощущений[8], таким образом, придавая этим событиям мотивационную важность. Нейробиологические эксперименты показали, что даже воспоминания о поощрении могут увеличить уровень дофамина[9][3][4][10], поэтому данный нейромедиатор используется мозгом для оценки и мотивации, закрепляя важные для выживания и продолжения рода действия[11].
Чувство любви и привязанности[править | править код]
Дофамин (а также окситоцин) имеет важное значение и для формирования чувства любви, в том числе материнской[12]:136—138. В экспериментах на серых полёвках вида Microtus ochrogaster, для которого характерны моногамные семьи, было показано, что дофамин (в частности, D2-рецепторы) лежит в основе чувства привязанности к партнёру и супружеской верности у этих грызунов. По-видимому, сходную роль дофамин играет и у человека[12]:197—198.
Когнитивные функции[править | править код]
Дофамин играет немаловажную роль в обеспечении когнитивной деятельности. Активация дофаминергической передачи необходима при процессах переключения внимания человека с одного этапа когнитивной деятельности на другой. Таким образом, недостаточность дофаминергической передачи приводит к повышенной инертности больного, которая клинически проявляется замедленностью когнитивных процессов (брадифрения) и персеверациями. Данные нарушения являются наиболее типичными когнитивными симптомами болезней с дофаминергической недостаточностью — например, болезни Паркинсона[13]. Дофамин участвует в процессах обучения; как показали немецкие нейробиологи (Klein и др., 2007) в эксперименте на людях, дофамин обеспечивает возможность эффективно учиться на своих ошибках, и нехватка дофамина может приводить к игнорированию негативного опыта[12]:208—209.
Синтетические аналоги. Влияние наркотиков на уровень дофамина[править | править код]
Как и у большинства нейромедиаторов, у дофамина существуют синтетические аналоги, а также стимуляторы его выделения в мозге. В частности, многие наркотики увеличивают выработку и высвобождение дофамина в мозге в 5—10 раз, что позволяет людям, которые их употребляют, получать чувство удовольствия искусственным образом[14][15]. Так, амфетамин напрямую стимулирует выброс дофамина, воздействуя на механизм его транспортировки[16]. Другие наркотики, например кокаин и некоторые иные психостимуляторы, блокируют естественные механизмы обратного захвата дофамина, увеличивая его концентрацию в синаптическом пространстве[17]. Морфий и никотин имитируют действие натуральных нейромедиаторов[17]. Введение антагонистов опиоидных рецепторов предотвращает вызванное этанолом увеличение дофамина в отделах мозга крыс, тем самым означая, что алкоголь увеличивает дофамин в мозге посредством опиоидной системы[18]. Если пациент продолжает чрезмерно стимулировать свою «систему поощрения», постепенно мозг адаптируется к искусственно повышаемому уровню дофамина, производя меньше гормона и снижая количество рецепторов в «системе поощрения»[19]. Это один из факторов, побуждающих человека, принимающего наркотики, увеличивать дозу для получения прежнего эффекта. Дальнейшее развитие химической толерантности может постепенно привести к метаболическим нарушениям в головном мозге, а в долговременной перспективе потенциально нанести серьёзный ущерб здоровью мозга[20].
Биосинтез[править | править код]
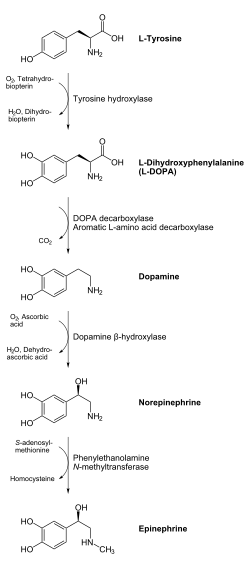
Предшественником дофамина является L-тирозин (он синтезируется из фенилаланина), который гидроксилируется ферментом тирозингидроксилазой с образованием L-ДОФА, которая, в свою очередь, декарбоксилируется с помощью фермента L-ДОФА-декарбоксилазы и превращается в дофамин. Этот процесс происходит в цитоплазме нейрона.
Рецепторы[править | править код]
Постсинаптические дофаминовые рецепторы относятся к семейству GPCR. Существует по меньшей мере пять различных подтипов дофаминовых рецепторов — D1—5. Рецепторы D1 и D5 обладают довольно значительной гомологией и сопряжены с белком GS, который стимулирует аденилатциклазу, вследствие чего их обычно рассматривают совместно как D1-подобные рецепторы. Остальные рецепторы подсемейства подобны D2 и сопряжены с Gi-белком, который ингибирует аденилатциклазу, вследствие чего их объединяют под общим названием D-2-подобные рецепторы. Таким образом, дофаминовые рецепторы играют роль модуляторов долговременной потенциации[21].
Участие во «внутреннем подкреплении» принимают D2 и D4 рецепторы.
В больших концентрациях дофамин также стимулирует α- и β-адренорецепторы. Влияние на адренорецепторы связано не столько с прямой стимуляцией адренорецепторов, сколько со способностью дофамина высвобождать норадреналин из гранулярных пресинаптических депо, то есть оказывать непрямое адреномиметическое действие.
«Круговорот» дофамина[править | править код]

Синтезированный нейроном дофамин накапливается в дофаминовых везикулах (т. н. «синаптическом пузырьке»). Этот процесс является протон-сопряжённым транспортом. В везикулу с помощью протон-зависимой АТФ-азы закачиваются ионы H+. При выходе протонов по градиенту концентрации, в везикулу поступают молекулы дофамина.
Далее дофамин выводится в синаптическую щель. Часть его участвует в передаче нервного импульса, воздействуя на клеточные D-рецепторы постсинаптической мембраны, а часть возвращается в пресинаптический нейрон с помощью обратного захвата. Ауторегуляция выхода дофамина обеспечивается D2 и D3 рецепторами на мембране пресинаптического нейрона. Обратный захват производится транспортёром дофамина. Вернувшийся в клетку медиатор расщепляется с помощью моноаминооксидазы (МАО) и, далее, альдегиддегидрогеназы и катехол-О-метил-трансферазы до гомованилиновой кислоты.
Участие в системе поощрения[править | править код]

Исследование Олдса и Милнера на крысах[править | править код]
В фундаментальном исследовании 1954 года канадские учёные Джеймс Олдс и его коллега Питер Милнер обнаружили, что если имплантировать электроды в определённые участки мозга, особенно в средний узел переднего мозга, то крысу можно приучить нажимать рычаг в клетке, включающий стимуляцию низковольтными разрядами электричества[22]. Когда крысы научились стимулировать этот участок, они нажимали рычаг до тысячи раз в час[22]. Это дало основание предположить, что стимулируется центр наслаждения. Один из главных путей передачи нервных импульсов в этом участке мозга — дофаминовый, поэтому исследователи выдвинули версию, что главное химическое вещество, связанное с удовольствием, — это дофамин. В дальнейшем это предположение было подтверждено радионуклидными томографическими сканерами и открытием антипсихотиков (лекарственных средств, подавляющих продуктивные симптомы шизофрении)[23].
Эксперимент Шульца на обезьяне[править | править код]
Однако в 1997 году было показано, что дофамин играет более тонкую роль. В эксперименте Шульца у обезьяны создавали условный рефлекс по классической схеме Павлова: после светового сигнала в рот обезьяне впрыскивали сок[24]. Было установлено, что:
- Когда сок впрыскивали неожиданно (не предваряя его сигналом), активность дофаминовых нейронов увеличивалась.
- На этапе обучения активность дофаминовых нейронов увеличивалась по-прежнему в ответ на впрыскивание сока.
- Когда условный рефлекс был сформирован, активность дофаминовых нейронов увеличивалась после подачи сигнала (до впрыскивания сока). Само впрыскивание сока на активности этих нейронов больше не отражалось (что противоречит гипотезе, согласно которой дофамин связан просто с получением удовольствия).
- Если в момент, когда ожидалось получение сока, сок не впрыскивали, активность дофаминовых нейронов снижалась.
Это позволило предположить, что дофамин участвует в формировании и закреплении условных рефлексов при положительном подкреплении и в гашении их, если подкрепление прекращается. Другими словами, если наше ожидание награды оправдывается, мозг сообщает нам об этом выработкой дофамина. Если же награда не последовала, снижение уровня дофамина сигнализирует, что модель разошлась с реальностью. В дальнейших работах показано, что активность дофаминовых нейронов хорошо описывается известной моделью обучения автоматов: действиям, быстрее приводящим к получению награды, приписывается большая ценность. Таким образом происходит обучение методом проб и ошибок[25].
Дофаминергическая система[править | править код]


Как часть системы регулирования чувства удовольствия дофамин производится в телах нейронов, расположенных в ВОП, и высвобождается в прилежащее ядро и префронтальную кору. Его моторные функции связаны с другим путём: производящие гормон клеточные тела расположены в чёрной субстанции, а высвобождение гормона происходит в полосатое тело
Известно несколько дофаминовых ядер, расположенных в мозге. Это дугообразное ядро (лат. nucleus arcuatus), дающее свои отростки в срединное возвышение гипоталамуса. Дофаминовые нейроны чёрной субстанции посылают аксоны в стриатум (хвостатое и чечевицеобразное ядро). Нейроны, находящиеся в области вентральной покрышки, дают проекции к лимбическим структурам и коре.
Основными дофаминовыми путями являются:
- мезокортикальный путь (процессы мотивации и эмоциональные реакции)
- мезолимбический путь (продуцирование чувств удовольствия, ощущения награды и желания)
- нигростриарный путь (двигательная активность, экстрапирамидная система)
Тела нейронов нигростриарного, мезокортикального и мезолимбического трактов образуют комплекс нейронов чёрной субстанции и вентрального поля покрышки. Аксоны этих нейронов идут вначале в составе одного крупного тракта (медиального пучка переднего мозга), а далее расходятся в различные мозговые структуры. Некоторые авторы объединяют мезокортикальную и мезолимбическую подсистемы в единую систему, однако более обоснованно выделение мезокортикальной и мезолимбической подсистем соответственно проекциям в лобную кору и лимбические структуры мозга[26].
В экстрапирамидной системе дофамин играет роль стимулирующего нейромедиатора, способствующего повышению двигательной активности, уменьшению двигательной заторможенности и скованности, снижению гипертонуса мышц. Физиологическими антагонистами дофамина в экстрапирамидной системе являются ацетилхолин и ГАМК.
Отдел мозга, называемый чёрной субстанцией (чёрным веществом), является важнейшей составной частью дофаминергической системы награды. Кроме того, он имеет ключевое значение для мотивации и эмоциональной регуляции материнского поведения[12]:141. Вентральная часть покрышки среднего мозга, вентромедиальная часть префронтальной коры и миндалина, также относящиеся к дофаминергическим областям мозга, тоже играют очень важную роль в системе вознаграждения[12]:143—144.
Другие подсистемы[править | править код]
Выделяют также тубероинфундибулярный путь (лимбическая система — гипоталамус — гипофиз), инцертогипоталамический, диенцефалоспинальный и ретинальный[26] (иногда, вдобавок к этому, перивентрикулярную и ольфакторную системы[27]). Данная дифференциация не является абсолютной, поскольку проекции дофаминергических нейронов разных трактов «перекрываются»; кроме того, в мозге отмечается и диффузное распределение дофаминергических элементов (отдельных клеток с отростками)[26].
В гипоталамусе и гипофизе дофамин играет роль естественного тормозного нейромедиатора, угнетающего секрецию ряда гормонов. При этом угнетающее действие на секрецию разных гормонов реализуется при разных концентрациях дофамина, что обеспечивает высокую специфичность регуляции. Наиболее чувствительна к тормозящему действию дофаминергических сигналов секреция пролактина, в меньшей степени — секреция соматолиберина и соматотропина, в ещё меньшей — секреция кортиколиберина и кортикотропина и в совсем малой степени — секреция тиролиберина и тиротропина. Секреция гонадотропинов и гонадолиберина не угнетается дофаминергическими сигналами[источник не указан 474 дня].
Ввиду чувствительности некоторых гормональных подсистем к уровню дофамина препараты-дофаминомиметики, усиливающие его синтез, могут применяться в качестве терапии при гормональных заболеваниях. Например, дофаминомиметики назначают при гиперпролактинемии и при болезни Паркинсона.
Дофамин и другие нейромедиаторы[править | править код]
Дофаминергические подсистемы находятся под контролем или сами контролируют норадренергические, серотонинергические, ГАМК-ергические, холинергические, мелатонинергические, глутаматергические, пептидергические системы. ГАМК-ергические и серотонинергические системы находятся в антагонистических отношениях с дофаминергической системой, а норадренергическая и дофаминергическая системы в различных функциональных состояниях функционируют однонаправленно: как в период бодрствования, так и в период сна. Взаимодействия дофаминергической и холинергической систем сложны, в условиях патологических процессов активность этих систем неоднозначна[27].
Гормон[править | править код]
Дофамин обладает рядом физиологических свойств, характерных для адренергических веществ.
Влияние на сердце, сосуды[править | править код]
Дофамин вызывает повышение сопротивления периферических сосудов (менее сильное, чем под влиянием норадреналина). Он повышает систолическое артериальное давление в результате стимуляции α-адренорецепторов. Также дофамин увеличивает силу сердечных сокращений в результате стимуляции β-адренорецепторов. Увеличивается сердечный выброс. Частота сердечных сокращений увеличивается, но не так сильно, как под влиянием адреналина.
Потребность миокарда в кислороде под влиянием дофамина повышается, однако в результате увеличения коронарного кровотока обеспечивается повышенная доставка кислорода.
Влияние на почки[править | править код]
В результате специфического связывания с дофаминовыми рецепторами почек дофамин уменьшает сопротивление почечных сосудов, увеличивает в них кровоток и почечную фильтрацию. Наряду с этим повышается натрийурез. Происходит также расширение мезентериальных сосудов. Этим действием на почечные и мезентериальные сосуды дофамин отличается от других катехоламинов (норадреналина, адреналина и др.). Однако в больших концентрациях дофамин может вызывать сужение почечных сосудов.
Дофамин ингибирует также синтез альдостерона в коре надпочечников, понижает секрецию ренина почками, повышает секрецию простагландинов тканью почек.
Влияние на пищеварение[править | править код]
Дофамин тормозит перистальтику желудка и кишечника, вызывает расслабление нижнего пищеводного сфинктера и усиливает желудочно-пищеводный и дуодено-желудочный рефлюкс. В ЦНС дофамин стимулирует хеморецепторы триггерной зоны и рвотного центра и тем самым принимает участие в осуществлении акта рвоты.
Влияние на нервную систему[править | править код]
Через гематоэнцефалический барьер дофамин мало проникает, и повышение уровня дофамина в плазме крови оказывает малое влияние на функции ЦНС, за исключением действия на находящиеся вне гематоэнцефалического барьера участки, такие как триггерная зона.
Повышение уровня дофамина[править | править код]
Повышение уровня дофамина в плазме крови происходит при шоке, травмах, ожогах, кровопотере, стрессовых состояниях, при различных болевых синдромах, тревоге, страхе. Дофамин играет роль в адаптации организма к стрессовым ситуациям, травмам, кровопотере и др.
Также уровень дофамина в крови повышается при ухудшении кровоснабжения почек или при повышенном содержании ионов натрия, а также ангиотензина или альдостерона в плазме крови. По-видимому, это происходит вследствие повышения синтеза дофамина из ДОФА в ткани почек при их ишемии или при воздействии ангиотензина и альдостерона. Вероятно, этот физиологический механизм служит для коррекции ишемии почек и для противодействия гиперальдостеронемии и гипернатриемии.
Патологии[править | править код]
Наиболее известными патологиями, связанными с дофамином, являются шизофрения и паркинсонизм, а также обсессивно-компульсивное расстройство. Различные независимые исследования показали, что многие лица, страдающие шизофренией, имеют повышенную дофаминергическую активность в некоторых структурах мозга[28][29][30], пониженную дофаминергическую активность в мезокортикальном пути[31][32][33][34] и префронтальной коре[31][32][28]. Для лечения шизофрении применяются антипсихотики — препараты, которые блокируют рецепторы дофамина преимущественно D2-типа и варьируются в степени аффинности к другим значимым нейромедиаторным рецепторам[35]. Типичные высокопотентные антипсихотики (такие, как галоперидол, трифтазин) в основном подавляют рецепторы D2, а большинство атипичных антипсихотиков (например, клозапин, оланзапин) и типичные низкопотентные (такие, как аминазин) воздействуют одновременно на целый ряд нейромедиаторных рецепторов: дофамина, серотонина, гистамина, ацетилхолина и других[35].
Предполагается, что снижение уровня дофамина в мезокортикальном пути связано с негативными симптомами шизофрении[31] (сглаживание аффекта, апатия, бедность речи, ангедония, уход из общества[32]), а также с когнитивными расстройствами[31] (дефициты внимания, рабочей памяти, исполнительных функций[32]). Антипсихотическое действие нейролептиков, то есть их способность редуцировать продуктивные нарушения — бред, галлюцинации, психомоторное возбуждение — связывают с угнетением дофаминергической передачи в мезолимбическом пути[34]. Нейролептики также угнетают дофаминергическую передачу и в мезокортикальном пути[36], что при длительной терапии часто приводит к усилению негативных нарушений[37] (см. Нейролептический дефицитарный синдром).
Длительная блокада нейролептиками дофаминовых рецепторов приводит к компенсаторным процессам; в связи с этим дофаминовая гипотеза шизофрении подвергается критике: утверждается, что чрезмерная активность в дофаминовой системе (увеличение концентрации дофамина, повышение чувствительности дофаминовых рецепторов или увеличение их плотности) может быть обусловлена не самой болезнью, а длительным применением нейролептиков[38]:89—90.
Паркинсонизм связан с пониженным содержанием дофамина в нигростриарном пути. Наблюдается при разрушении чёрной субстанции, патологии D1-подобных рецепторов. С угнетением дофаминергической передачи в нигростриарной системе связывают и развитие экстрапирамидных побочных эффектов при приёме антипсихотиков[34]: лекарственного паркинсонизма, дистонии, акатизии, поздней дискинезии и др. Для лечения болезни Паркинсона часто используют агонисты дофаминовых рецепторов (то есть аналоги дофамина: прамипексол, бромокриптин, перголид и др.): на сегодняшний день это самая многочисленная группа противопаркинсонических средств[39]. Некоторые из антидепрессантов также обладают дофаминергической активностью[40].
С нарушением дофаминергической системы связывают и такие расстройства, как ангедония, депрессия, деменция, патологическая агрессивность, фиксация патологических влечений, синдром персистирующей лактореи-аменореи, импотенция, акромегалия, синдром беспокойных ног и периодических движений в конечностях[27].
Снижение в результате мутаций количества дофаминовых рецепторов второго типа (D2) в некоторых участках мозга повышает риск импульсивного поведения, алкогольной и наркотической зависимостей. Для людей с пониженным количеством D2-рецепторов характерен также повышенный риск ожирения (поскольку эти люди нередко склонны к обжорству), других вредных привычек — в частности, страсти к азартным играм. Причиной того, что люди с пониженным количеством D2-рецепторов склонны к поиску экстремальных способов получения удовольствия от жизни, является, по всей видимости, нехватка положительных эмоций у этих людей; кроме того, причиной может являться сниженная способность этих людей учиться на собственных ошибках, делать правильные выводы из отрицательного опыта[12]:207—208.
Процесс старения[править | править код]
Со снижением уровня дофамина в подкорковых образованиях и передних отделах головного мозга связывают также процесс нормального старения[41]. По данным исследований, процесс старения проявляется уменьшением объёма и массы головного мозга и уменьшением числа синаптических связей; кроме уменьшения числа церебральных рецепторов, имеет место и медиаторная церебральная недостаточность. С возрастом уменьшается количество и плотность дофаминовых D2-рецепторов стриатума, снижается концентрация дофамина в подкорковых образованиях головного мозга. Клиническими проявлениями этих изменений являются обеднение мимики, некоторая общая замедленность, сгорбленная, старческая поза, укорочение длины шага.
«Дофамин-чувствительные» изменения отмечаются также в когнитивной сфере: с возрастом снижается быстрота реакции, становится труднее усваивать и реализовывать новую программу действия, снижается уровень внимания, объём оперативной памяти. При отсутствии органической патологии возрастные когнитивные изменения не приводят к дезадаптации пожилых людей и позволяют поддерживать привычный ритм социальной активности[41].
См. также[править | править код]
Примечания[править | править код]
- ↑ Dopamine (англ.). DrugBank. Дата обращения: 8 января 2023. Архивировано 8 января 2023 года.
- ↑ В русской терминологии принято название «дофамин». Вариант «допамин» представляет собой прямую транслитерацию принятого в англоязычной литературе термина dopamine и отсутствует в русских словарях. Различие объясняется разницей в сокращениях, возникшей из-за соответствия ph = ф: dihydroxyphenylalanine = DOPA, дигидроксифенилаланин = ДОФА.
- ↑ 1 2 It's all about dopamine. Дата обращения: 22 сентября 2011. Архивировано из оригинала 22 августа 2011 года.
- ↑ 1 2 Biology of Happiness. Дата обращения: 22 сентября 2011. Архивировано из оригинала 22 августа 2011 года.
- ↑ Nestler, Eric J. (Eric Jonathan), 1954-. Molecular neuropharmacology : a foundation for clinical neuroscience. — 2nd ed. — New York: McGraw-Hill Medical, 2009. — 1 online resource с. — ISBN 978-0-07-164119-7, 0-07-164119-X, 0-07-148127-3, 978-0-07-148127-4, 978-1-281-79174-0, 1-281-79174-1.
- ↑ M. N. Baliki, A. Mansour, A. T. Baria, L. Huang, S. E. Berger. Parceling Human Accumbens into Putative Core and Shell Dissociates Encoding of Values for Reward and Pain (англ.) // Journal of Neuroscience. — 2013-10-09. — Vol. 33, iss. 41. — P. 16383–16393. — ISSN 1529-2401 0270-6474, 1529-2401. — doi:10.1523/JNEUROSCI.1731-13.2013.
- ↑ Jennifer M. Wenzel, Noah A. Rauscher, Joseph F. Cheer, Erik B. Oleson. A Role for Phasic Dopamine Release within the Nucleus Accumbens in Encoding Aversion: A Review of the Neurochemical Literature (англ.) // ACS Chemical Neuroscience. — 2015-01-21. — Vol. 6, iss. 1. — P. 16–26. — ISSN 1948-7193 1948-7193, 1948-7193. — doi:10.1021/cn500255p. Архивировано 23 ноября 2021 года.
- ↑ Ваш мозг во время секса. Дата обращения: 22 сентября 2011. Архивировано 22 августа 2011 года.
- ↑ Удовольствие: дофамин. Дата обращения: 12 октября 2011. Архивировано 8 мая 2013 года.
- ↑ Кокаиновые наркоманы могут получать удовольствие только от одного ожидания этого удовольствия. Дата обращения: 12 октября 2011. Архивировано 26 марта 2013 года.
- ↑ Dopamine and desire. Дата обращения: 22 сентября 2011. Архивировано 22 августа 2011 года.
- ↑ 1 2 3 4 5 6 Марков А. Эволюция человека. Книга 2. Обезьяны, нейроны и душа. — Corpus, 2011. — Т. 2. — 512 с. — (Династия). — 5000 экз. — ISBN 978-5-271-36294-1. — ISBN 978-5-17-078089-1.
- ↑ Захаров В. В., Яхно Н. Н. Когнитивные расстройства в пожилом и старческом возрасте: Методическое пособие для врачей. — Москва, 2005. Архивировано 23 декабря 2012 года.
- ↑ Your Brain on Drugs: Dopamine and Addiction. Дата обращения: 22 сентября 2011. Архивировано 22 августа 2011 года.
- ↑ Dopamine — A Sample Neurotransmitter. Дата обращения: 22 сентября 2011. Архивировано из оригинала 22 августа 2011 года.
- ↑ A Mechanism for Amphetamine-Induced Dopamine Overload.
- ↑ 1 2 HOW DRUGS AFFECT NEUROTRANSMITTERS. Дата обращения: 22 сентября 2011. Архивировано 22 августа 2011 года.
- ↑ Участие опиоидной и дофаминовой систем мозга в реализации аддиктивных свойств этанола. cyberleninka.ru. Дата обращения: 20 февраля 2020. Архивировано 20 февраля 2020 года.
- ↑ Addiction and Dopamine (D2) Receptor Levels (2006). Дата обращения: 22 сентября 2011. Архивировано 22 августа 2011 года.
- ↑ The Science Behind Drug Use and Addiction. Дата обращения: 22 сентября 2011. Архивировано из оригинала 22 августа 2011 года.
- ↑ Mehta M.A., Riedel W.J. Dopaminergic Enhancement of Cognitive Function. // Curr. Pharm. Des. 2006. v. 12. pp. 2487—2500.
- ↑ 1 2 Британская энциклопедия, см. раздел "Reward and punishment". Дата обращения: 15 октября 2011. Архивировано 3 февраля 2012 года.
- ↑ The Functional Neuroanatomy of Pleasure and Happiness. Дата обращения: 15 октября 2011. Архивировано 3 февраля 2012 года.
- ↑ Wolfram Schultz. Дата обращения: 28 августа 2021. Архивировано 28 августа 2021 года.
- ↑ К. Фрит, Мозг и душа. М.: Астрель: Corpus, 2012. C. 148—153
- ↑ 1 2 3 Орловская Д. Д. Нейрохимические системы мозга // Общая психиатрия / Под ред. А. С. Тиганова. — Москва, 2006. Архивировано 29 сентября 2013 года.
- ↑ 1 2 3 Левин Я.И. Нейрохимическая медицина. Часть 1. Церебральные дофаминергические системы // Современная терапия психических расстройств. — 2008. — № 1. Архивировано 14 апреля 2021 года.
- ↑ 1 2 The Dopamine Hypothesis of Schizophrenia: Version III—The Final Common Pathway. Дата обращения: 22 сентября 2011. Архивировано 23 августа 2011 года.
- ↑ Increased Striatal Dopamine Transmission in Schizophrenia: Confirmation in a Second Cohort. Архивировано 23 августа 2011 года.
- ↑ Dysconnection in Schizophrenia: From Abnormal Synaptic Plasticity to Failures of Self-monitoring. Дата обращения: 22 сентября 2011. Архивировано 23 августа 2011 года.
- ↑ 1 2 3 4 Abi-Dargham A., Moore H. Prefrontal DA transmission at D1 receptors and the pathology of schizophrenia (англ.) // Neuroscientist : journal. — 2003. — October (vol. 9, no. 5). — P. 404—416. — doi:10.1177/1073858403252674. — PMID 14580124.
- ↑ 1 2 3 4 Abi-Dargham A. The Dopamine Hypothesis of Schizophrenia. Schizophrenia Research Forum (5 декабря 2005). Дата обращения: 26 сентября 2011. Архивировано 3 февраля 2012 года. Перевод: Дофаминовая гипотеза шизофрении (15 августа 2008). Дата обращения: 26 сентября 2011. Архивировано из оригинала 3 февраля 2012 года.
- ↑ Lieberman J.A. Dopamine partial agonists: a new class of antipsychotic (англ.) // CNS Drugs : journal. — 2004. — Vol. 18, no. 4. — P. 251—267. — PMID 15015905. (недоступная ссылка)
- ↑ 1 2 3 Справочное руководство по психофармакологическим и противоэпилептическим препаратам, разрешенным к применению в России / Под ред. С. Н. Мосолова. — 2-е, перераб. — М.: «Издательство БИНОМ», 2004. — С. 17. — 304 с. — 7000 экз. — ISBN 5-9518-0093-5.
- ↑ 1 2 A Roadmap to Key Pharmacologic Principles in Using Antipsychotics. PubMed (USA).
- ↑ Basu D., Marudkar M., Khurana H. Abuse of neuroleptic drug by psychiatric patients (неопр.). — 2000. — Т. 54, № 2. — С. 59—62. — PMID 11271726. — PMC 1324958. Архивировано 29 ноября 2011 года.
- ↑ Бородин В. И. Сперидан (рисперидон) при терапии шизофренических психозов // Психиатрия и психофармакотерапия. — 2006. — Вып. 8 (4). Архивировано 19 ноября 2012 года.
- ↑ Models of Madness: Psychological, Social and Biological Approaches to Schizophrenia / Edited by J.Read, L.R.Mosher and R.P.Bentall. — Basingstoke: Brunner Routledge, 2004. Перевод: Модели безумия: Психологические, социальные и биологические подходы к пониманию шизофрении / Редакторы: Дж.Рид, Л.Р.Мошер, Р.П.Бенталл. — Ставрополь: Изд-во Возрождение, 2008.
- ↑ Катунина Е. А. Агонисты дофаминовых рецепторов и проблема эквивалентности доз // Неврология. — 2010. — № 2. Архивировано 14 апреля 2021 года.
- ↑ Shelton RC, Tomarken AJ. Can Recovery From Depression Be Achieved? // American Psychiatric Association Psychiatr Serv. — November 2001. — № 52. — С. 1469—1478. Архивировано 14 сентября 2011 года. Перевод: Можно ли достичь выздоровления при депрессии? // Обзор современной психиатрии. — November 2004. — Вып. 21. Архивировано 19 января 2012 года.
- ↑ 1 2 Преображенская И. С. Умеренные когнитивные расстройства: диагностика и лечение // Неврология. — 2008. — № 1. Архивировано 24 марта 2012 года.
Литература[править | править код]
- Ашмарин И. П., Ещенко Н. Д., Каразеева Е. П. Нейрохимия в таблицах и схемах. — М.: Экзамен, 2007.
- Васильев В. Н. Диагностика и терапия инкурабельных нервных и психических заболеваний допаминовой этиологии. Биокоррекция Васильева. — М.: Медиакит, 2009. — 247 с. — ISBN 978-5-9901746-1-0.
Ссылки[править | править код]
- Schizophrenia Research Forum
- Methylphenidate facilitates learning-induced amygdala plasticity — результаты исследования, связанного с механизмами D1 и D2 — рецепторов дофамина (англ. яз.).
- Окислительный стресс — на стыке NMDA- и ГАМК-гипотез шизофрении?
- Дубынин В. Дофамин. ИД «ПостНаука» (31 октября 2016). — лекция о болезни Паркинсона, связи дофамина с шизофренией и истории нейролептиков. Дата обращения: 21 ноября 2016.

