DDR1
DDR1 (англ. discoidin domain receptor tyrosine kinase 1; CD167a , КФ 2.7.10.1) — мембранный белок, фермент из надсемейства рецепторных тирозинкиназ, продукт гена DDR1.
DDR1 входит в группу рецепторов, которые содержат домен, гомологичный белку дискоидин 1 из Dictyostelium discoideum.
Функции[править | править код]
Рецептор DDR1 играет роль в межклеточных взаимодействиях и распознавании.[1] Взаимодействие между лейкоцитарным DDR1 и коллагеном облегчает адгезию, миграцию, дифференцировку/созревание лейкоцитов и продукцию ими цитокинов и хемокинов. [2]
Структура[править | править код]
DDR1 — крупный белок, состоит из 895 аминокислот, молекулярная масса белковой части — 101,1 кДа. N-концевой участок (398 аминокислот) является внеклеточным, далее расположен единственный трансмембранный фрагмент и внутриклеточный фрагмент (470 аминокислот). Внеклеточный фрагмент включает 4 участка N-гликозилирования. Цитозольный участок включает протеинкиназный домен, участок связывания с АТФ, 4 аутофосфорилируемых тирозинов и PPxY-мотив.
Рецептор взаимодействует с WWC1 (посредством WW доменов), входит в тримолекулярный комплекс с белками WWC1 и PRKCZ (как правило в несвязанном с коллагеном состоянии).
В результате альтернативного сплайсинга образуются 5 изоформ белка.
Каталитическая активность[править | править код]
Внутриклеточный протеинкиназный домен фосфорилирует собственные остатки тирозина, перенося фосфатную группу с АТФ на гидроксильную группу аминокислоты. Аутофосфорилирование происходит при взаимодействии DDR1 с коллагенами типов I—VI.
Тканевая специфичность[править | править код]
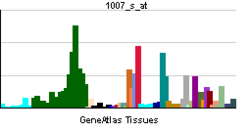
Белок в небольшой степени экспрессирован на эпителиальных клетках большинства тканей, максимальная экспрессия наблюдается в мозге, лёгких, плаценте и почках. Высокая степень экспрессии найдена во многих линиях клеток карциномы, особенно в клетках рака молочной железы. Отсутствует в соединительной ткани, на эндотелиальных клетках, в жировой и мышечной тканях и на гематопоэтических клетах.
См.также[править | править код]
Примечания[править | править код]
- ↑ Uniprot database entry for CD11a (accession number Q08345). Дата обращения: 17 апреля 2012. Архивировано 28 августа 2017 года.
- ↑ Yoshimura T., Matsuyama W., Kamohara H. Discoidin domain receptor 1: a new class of receptor regulating leukocyte-collagen interaction (англ.) // Immunol. Res. : journal. — 2005. — Vol. 31, no. 3. — P. 219—230. — doi:10.1385/IR:31:3:219. — PMID 15888913.
Библиография[править | править код]
- Yoshimura T., Matsuyama W., Kamohara H. Discoidin domain receptor 1: a new class of receptor regulating leukocyte-collagen interaction (англ.) // Immunol. Res. : journal. — 2005. — Vol. 31, no. 3. — P. 219—230. — doi:10.1385/IR:31:3:219. — PMID 15888913.
- Edelhoff S., Sweetser D.A., Disteche C.M. Mapping of the NEP receptor tyrosine kinase gene to human chromosome 6p21.3 and mouse chromosome 17C (англ.) // Genomics : journal. — Academic Press, 1995. — Vol. 25, no. 1. — P. 309—311. — doi:10.1016/0888-7543(95)80144-B. — PMID 7774938.
- Shelling AN; Butler R; Jones T; Laval, S.; Boyle, J.M.; Ganesan, T.S. Localization of an epithelial-specific receptor kinase (EDDR1) to chromosome 6q16 (англ.) // Genomics : journal. — Academic Press, 1995. — Vol. 25, no. 2. — P. 584—587. — doi:10.1016/0888-7543(95)80065-T. — PMID 7789998.
- Weiner T.M., Liu E.T., Craven R.J., Cance W.G. Expression of growth factor receptors, the focal adhesion kinase, and other tyrosine kinases in human soft tissue tumors (англ.) // Ann. Surg. Oncol. : journal. — 1995. — Vol. 1, no. 1. — P. 18—27. — doi:10.1007/BF02303537. — PMID 7834423.
- Laval S; Butler R; Shelling AN; Hanby, AM; Poulsom, R; Ganesan, T.S. Isolation and characterization of an epithelial-specific receptor tyrosine kinase from an ovarian cancer cell line (англ.) // Cell Growth Differ. : journal. — 1995. — Vol. 5, no. 11. — P. 1173—1183. — PMID 7848919.
- Kato J.Y., Matsuoka M., Strom D.K., Sherr C.J. Regulation of cyclin D-dependent kinase 4 (cdk4) by cdk4-activating kinase (англ.) // Mol. Cell. Biol. : journal. — 1994. — Vol. 14, no. 4. — P. 2713—2721. — PMID 8139570. — PMC 358637.
- Di Marco E; Cutuli N; Guerra L; Cancedda, R; De Luca, M. Molecular cloning of trkE, a novel trk-related putative tyrosine kinase receptor isolated from normal human keratinocytes and widely expressed by normal human tissues (англ.) // J. Biol. Chem. : journal. — 1993. — Vol. 268, no. 32. — P. 24290—24295. — PMID 8226977.
- Perez JL; Shen X; Finkernagel S; Sciorra, L; Jenkins, NA; Gilbert, DJ; Copeland, NG; Wong, T.W. Identification and chromosomal mapping of a receptor tyrosine kinase with a putative phospholipid binding sequence in its ectodomain (англ.) // Oncogene : journal. — 1994. — Vol. 9, no. 1. — P. 211—219. — PMID 8302582.
- Johnson J.D., Edman J.C., Rutter W.J. A receptor tyrosine kinase found in breast carcinoma cells has an extracellular discoidin I-like domain (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 1993. — Vol. 90, no. 12. — P. 5677—5681. — doi:10.1073/pnas.90.12.5677. — PMID 8390675. — PMC 46784.
- Perez J.L., Jing S.Q., Wong T.W. Identification of two isoforms of the Cak receptor kinase that are coexpressed in breast tumor cell lines (англ.) // Oncogene : journal. — 1996. — Vol. 12, no. 7. — P. 1469—1477. — PMID 8622863.
- Valent A; Meddeb M; Danglot G; Duverger, A.; Nguyen, V. C.; Bernheim, A. Assignment of the NTRK4 (trkE) gene to chromosome 6p21 (англ.) // Hum. Genet. : journal. — 1996. — Vol. 98, no. 1. — P. 12—5. — doi:10.1007/s004390050152. — PMID 8682498.
- Playford MP; Butler RJ; Wang XC; Katso, R M; Cooke, I E; Ganesan, T S. The genomic structure of discoidin receptor tyrosine kinase (англ.) // Genome Res. : journal. — 1996. — Vol. 6, no. 7. — P. 620—627. — doi:10.1101/gr.6.7.620. — PMID 8796349.
- Sakuma S; Saya H; Tada M; Nakao, M; Fujiwara, T; Roth, JA; Sawamura, Y; Shinohe, Y; Abe, H. Receptor protein tyrosine kinase DDR is up-regulated by p53 protein (англ.) // FEBS Lett. : journal. — 1997. — Vol. 398, no. 2—3. — P. 165—169. — doi:10.1016/S0014-5793(96)01234-3. — PMID 8977099.
- Nemoto T; Ohashi K; Akashi T; Johnson, Jeffrey D.; Hirokawa, Katsuiku. Overexpression of protein tyrosine kinases in human esophageal cancer (англ.) // Pathobiology : journal. — 1998. — Vol. 65, no. 4. — P. 195—203. — doi:10.1159/000164123. — PMID 9396043.
- Tanaka K; Nagayama Y; Nakano T; Takamura, N; Namba, H; Fukada, S; Kuma, K; Yamashita, S; Niwa, M. Expression profile of receptor-type protein tyrosine kinase genes in the human thyroid (англ.) // Endocrinology : journal. — 1998. — Vol. 139, no. 3. — P. 852—858. — doi:10.1210/en.139.3.852. — PMID 9492013.
- Vogel W., Gish G.D., Alves F., Pawson T. The discoidin domain receptor tyrosine kinases are activated by collagen (англ.) // Mol. Cell : journal. — 1998. — Vol. 1, no. 1. — P. 13—23. — doi:10.1016/S1097-2765(00)80003-9. — PMID 9659899.
- Shrivastava A; Radziejewski C; Campbell E; Kovac, Lubomir; McGlynn, Marion; Ryan, Terence E; Davis, Sam; Goldfarb, Mitchell P; Glass, David J. An orphan receptor tyrosine kinase family whose members serve as nonintegrin collagen receptors (англ.) // Mol. Cell : journal. — 1998. — Vol. 1, no. 1. — P. 25—34. — doi:10.1016/S1097-2765(00)80004-0. — PMID 9659900.
- Vogel W; Brakebusch C; Fässler R; Alves, F; Ruggiero, F; Pawson, T. Discoidin domain receptor 1 is activated independently of beta(1) integrin (англ.) // J. Biol. Chem. : journal. — 2000. — Vol. 275, no. 8. — P. 5779—5784. — doi:10.1074/jbc.275.8.5779. — PMID 10681566.
- Foehr ED; Tatavos A; Tanabe E; Raffioni, S; Goetz, S; Dimarco, E; De Luca, M; Bradshaw, R.A. Discoidin domain receptor 1 (DDR1) signaling in PC12 cells: activation of juxtamembrane domains in PDGFR/DDR/TrkA chimeric receptors (англ.) // The FASEB Journal : journal. — Federation of American Societies for Experimental Biology, 2000. — Vol. 14, no. 7. — P. 973—981. — PMID 10783152.
- Weiner HL; Huang H; Zagzag D; Boyce, Hayden; Lichtenbaum, Roger; Ziff, Edward B. Consistent and selective expression of the discoidin domain receptor-1 tyrosine kinase in human brain tumors (англ.) // Neurosurgery : journal. — 2001. — Vol. 47, no. 6. — P. 1400—1409. — doi:10.1097/00006123-200012000-00028. — PMID 11126911.
- Mohan R.R., Mohan R.R., Wilson S.E. Discoidin domain receptor (DDR) 1 and 2: collagen-activated tyrosine kinase receptors in the cornea (англ.) // Exp. Eye Res. : journal. — 2001. — Vol. 72, no. 1. — P. 87—92. — doi:10.1006/exer.2000.0932. — PMID 11133186.